Hay un debate permanente respecto al uso sistemático de la trombectomía por aspiración en los pacientes con infarto agudo de miocardio con elevación del segmento ST. El objetivo de este estudio es comparar los resultados de la intervención y los resultados clínicos en pacientes tratados con intervención coronaria percutánea primaria asistida mediante trombectomía por aspiración con los de una intervención coronaria percutánea primaria convencional en el contexto de infarto agudo de miocardio con elevación del segmento ST.
MétodosSe realizó un metanálisis de 26 ensayos controlados y aleatorizados con un total de 11.943 pacientes. Los resultados clínicos se extrajeron durante el periodo máximo de seguimiento y se utilizaron modelos de efectos aleatorios para evaluar las diferencias de los resultados.
ResultadosNo se observaron diferencias en el riesgo de muerte por cualquier causa (razón de riesgos combinada = 0,88; intervalo de confianza del 95%, 0,74-1,04; p = 0,124), reinfarto (razón de riesgos combinada = 0,85; intervalo de confianza del 95%, 0,67-1,08; p = 0,176), revascularización de vaso diana (razón de riesgos combinada = 0,86; intervalo de confianza del 95%, 0,73-1,00; p = 0,052) o trombosis de stent definitiva (razón de riesgos combinada = 0,76; intervalo de confianza del 95%, 0,49-1,16; p = 0,202) entre los dos grupos tras una media ponderada de tiempo de seguimiento de 10,4 meses. Se produjeron reducciones significativas de no lograr flujo Thrombolysis In Myocardial Infarction 3 (razón de riesgos combinada = 0,70; intervalo de confianza del 95%, 0,60-0,81; p < 0,001), el grado 3 de opacificación (blush) miocárdica (razón de riesgos combinada = 0,76; intervalo de confianza del 95%, 0,65-0,89; p = 0,001), resoluciones del segmento ST incompletas (razón de riesgos combinada = 0,72; intervalo de confianza del 95%, 0,62-0,84; p < 0,001) y los signos de embolización distal (razón de riesgos combinada = 0,61; intervalo de confianza del 95%, 0,46-0,81; p = 0,001) con la trombectomía por aspiración, pero las estimaciones fueron heterogéneas entre los ensayos.
ConclusionesEn pacientes con infarto agudo de miocardio con elevación del segmento ST no seleccionados, la intervención coronaria percutánea primaria asistida mediante trombectomía por aspiración no mejora los resultados clínicos pese a la mejora de los parámetros de reperfusión epicárdicos y miocárdicos.
Palabras clave
La intervención coronaria percutánea primaria (ICPP) es el tratamiento estándar para los pacientes con infarto agudo de miocardio con elevación del segmento ST (IAMCEST)1,2. En comparación con la fibrinolisis, la ICPP se asocia a una mejora de la permeabilidad de la arteria relacionada con el infarto, menor riesgo de reoclusión y reinfarto, una resolución más rápida y más completa de la elevación del segmento ST y una mejora de la reperfusión epicárdica (flujo Thrombolysis In Myocardial Infarction [TIMI] 3) y miocárdica (grado de opacificación o blush miocárdica [MBG] 3)3. Considerados conjuntamente, estos efectos favorables se traducen en una reducción del tamaño del infarto y una mejora de la supervivencia4.
No obstante, hasta una cuarta parte de las arterias coronarias con reperfusión muestran signos de deterioro del flujo a nivel del miocardio (MBG < 2) después de la ICPP5, lo que con frecuencia se denomina fenómeno de no-reflujo y se asocia a un aumento del tamaño del infarto y una reducción de la supervivencia6. Entre otras causas, la embolización de material trombótico y restos de placas hacia la microcirculación durante el implante del stent es un presunto mecanismo importante de la lesión por reperfusión7, que ha conducido al desarrollo de dispositivos específicos destinados a mejorar en mayor medida los resultados8.
Aunque los dispositivos de protección distal no lograron mejorar la reperfusión epicárdica y miocárdica ni el tamaño del infarto, la trombectomía por aspiración (TA) ha producido algunos resultados positivos9. La intervención es técnicamente sencilla, no requiere mucha dedicación de tiempo y puede llevarse a cabo con facilidad en casi todas las anatomías10. En varios estudios y revisiones sistemáticas, se ha descrito una mejora de los parámetros de reperfusión después de la TA10–14. Sin embargo, no se ha observado de manera uniforme un efecto beneficioso en cuanto a la supervivencia8,15–17. Teniendo en cuenta los resultados a 1 año, recientemente presentados, del amplio ensayo Thrombus Aspiration in ST-Elevation myocardial infarction in Scandinavia (TASTE), se ha realizado un metanálisis para valorar la utilidad clínica de la TA en el tratamiento del IAMCEST.
MÉTODOSEstrategia de búsquedaSe realizó una búsqueda bibliográfica en las bases de datos de MEDLINE y EMBASE a través de OvidSp, PubMed y Cochrane Central Register of Controlled Trials (CENTRAL), utilizando una combinación de palabras y términos clave relacionados con «thrombectomy», «thrombus» y «myocardial infarction», sin aplicar restricciones respecto al idioma. Se examinaron los metanálisis publicados y las listas de bibliografía de los ensayos finalmente elegibles. Se presentó la lista de ensayos clínicos aleatorizados identificados a expertos en la materia, y se les solicitó que indicaran otras referencias a ensayos clínicos aleatorizados aún no identificadas. Las búsquedas se realizaron el 5 de septiembre de 2014 (tablas 1 y 2 del material suplementario).
Criterios de elegibilidadLos ensayos incluidos cumplieron los siguientes criterios: a) estudiaron la ICPP asistida mediante TA en el contexto del IAMCEST, y b) asignaron a los pacientes aleatoriamente a una ICPP con o sin TA en un plazo de 24h tras el inicio de los síntomas. La TA incluyó todos los dispositivos de trombectomía manual y los dispositivos de aspiración por vacío. Se incluyeron los ensayos en que se asignó aleatoriamente una ICP de rescate, pero no los que evaluaron la ICP facilitada con fibrinolisis. Se excluyeron los estudios que no aportaban ninguna evaluación de parámetros de valoración preespecificados, los que utilizaban dispositivos de trombectomía mecánicos, los de injertos de vena safena, los que comparaban distintos dispositivos de trombectomía entre sí y las estrategias combinadas (es decir, con el empleo adicional de tratamiento antitrombótico o dispositivos de protección). Dos investigadores (Ernest Spitzer and Stefan Stortecky) realizaron de manera independiente el examen de selección, revisaron los artículos y determinaron si eran aptos para el análisis con el programa EROS (Early Revision Organizing Software) a través de internet. Las discrepancias se resolvieron por consenso.
Extracción de los datos y parámetros de valoración preespecificadosSe extrajeron las características de los ensayos, los pacientes y las intervenciones, incluido el diseño del estudio, la duración del seguimiento, información sobre la calidad metodológica, el origen de la financiación, el momento de la aleatorización, edad, sexo, diabetes mellitus, tiempo de isquemia (tabla 3 del material suplementario), uso de fármacos antitrombóticos por vía oral y parenteral, enfermedad multivaso, infarto de miocardio con territorio de la arteria descendente anterior izquierda afectado y visualización de un trombo como requisito para la aleatorización.
Los resultados de la intervención evaluados incluyeron un marcador indirecto de la reperfusión epicárdica, consistente en no alcanzar un flujo de grado TIMI 318, marcadores indirectos de la reperfusión miocárdica, consistentes en no alcanzar un MBG de grado 319 y la resolución incompleta de la elevación del segmento ST (RSTi) (resolución menor que el 70% de la suma de la elevación inicial del segmento ST)20, así como ausencia de implante directo de stents21 y signos de embolización distal7.
Los objetivos clínicos preespecificados fueron muerte por cualquier causa, reinfarto, revascularización de vaso diana, trombosis de stent definitiva e ictus. No se dispuso de los datos relativos a la muerte por cualquier causa de 8 ensayos; en 5 de dichos ensayos, se utilizó la muerte cardiaca como parámetro de valoración sustituto. El reinfarto incluyó los infartos de miocardio con o sin onda Q en todos los estudios. La revascularización del vaso diana se definió como una nueva intervención percutánea o una operación de bypass arterial coronario del vaso diana o de las ramas de este. Si no se presentaba información sobre la revascularización del vaso diana, se utilizó como parámetro sustituto la revascularización de la lesión diana. La trombosis de stent definitiva se definió como una trombosis en el segmento en que se había implantado el stent, confirmada mediante angiografía o anatomía patológica, según los criterios del Academic Research Consortium22. Se registraron por separado el número de pacientes que presentaron un acontecimiento adverso y el número total de pacientes en riesgo. En todos los ensayos, se utilizaron los resultados del seguimiento a 1 mes y el seguimiento más largo disponible. La extracción de los datos la realizaron dos de los autores (Ernest Spitzer y Giulio G. Stefanini) de manera independiente, y las discrepancias se resolvieron por consenso.
Evaluación de la calidadLa calidad metodológica se evaluó mediante la extracción de la información relativa a la ocultación de la asignación aleatoria, la ocultación de la asignación del tratamiento a los investigadores que validaban los eventos clínicos, la independencia de los investigadores que evaluaban las variables de valoración angiográficas y electrocardiográficas y la inclusión de todos los individuos aleatorizados en el análisis según el principio de intención de tratar23. La ocultación de la asignación del tratamiento se consideró adecuada si los investigadores encargados de la selección de los pacientes no conocían antes de la asignación cuál era el siguiente tratamiento que correspondía aplicar. Se consideró que el análisis se atenía al principio de intención de tratar si todos los pacientes aleatorizados eran analizados en el grupo al que habían sido asignados inicialmente, con independencia del tratamiento real recibido.
Análisis estadísticoLas razones de riesgo se calcularon mediante el número de pacientes por grupo que presentaron acontecimientos adversos (y en el denominador el número de pacientes aleatorizados por grupo por lo que respecta a los resultados clínicos y el número de pacientes analizados por grupo por lo que se refiere a los resultados de la intervención) como medidas del efecto del tratamiento, y se usaron modelos de efectos aleatorios de DerSimonian y Laird para combinar las estimaciones de los diversos ensayos. Se realizó un metanálisis global de todos los resultados clínicos utilizando la duración máxima del seguimiento disponible en cada ensayo. También se analizaron los resultados de la intervención, pero se excluyeron del análisis de la RST el estudio EXPORT y el de Lelek et al, ya que ambos presentaron la RST > 50% como completa, lo que no era comparable a lo realizado en otros ensayos. Se excluyeron del análisis de implante directo de stents el Thrombus Aspiration during Percutaneous Coronary Intervention in Acute Myocardial Infarction Study (TAPAS) y el Polish-Italian-Hungarian Randomized ThrombEctomy Trial (PIHRATE), ya que los grupos de control se habían asignado aleatoriamente a una predilatación con balón. Se determinó la heterogeneidad existente entre los distintos ensayos empleando el parámetro estadístico I2, se elaboraron gráficos de embudo para evaluar la asimetría y se utilizó la prueba de Egger para valorar los efectos de los estudios pequeños. Se hicieron análisis estratificados de todos los objetivos, utilizando las siguientes características de los ensayos: ocultación adecuada de la asignación, validación con diseño ciego de los resultados clínicos o evaluación independiente de los resultados de la intervención, análisis adecuados según el principio de intención de tratar, tamaño del ensayo, estudio unicéntrico o multicéntrico, financiación dependiente de la industria y año de publicación (2010-2014 o anterior). Se evaluó la presencia de interacción para los resultados clínicos en un plazo ≤ 30 días y ≥ 1 año de seguimiento cuando se dispuso de ello. Se realizaron análisis de sensibilidad según los siguientes criterios: con la exclusión de los ensayos en los que se utilizaron dispositivos de aspiración por vacío, con la exclusión del ensayo TASTE, y con la exclusión de los ensayos TASTE y TAPAS. Se utilizó un análisis por intención de tratar para todos los resultados clínicos.
Se siguió lo establecido en la declaración Preferred Reporting Items for Systematic Reviews and Meta-Analyses (PRISMA) para realizar este metanálisis. Todos los valores de p fueron bilaterales y se utilizó un valor de p<0,05 para establecer la significación estadística; se calcularon los intervalos de confianza del 95% (IC95%). Todos los análisis se realizaron con el programa Stata 13 (Stata Corporation; College Station, Texas, Estados Unidos).
RESULTADOSSe identificaron 831 referencias bibliográficas y se consideró que 87 de ellas eran potencialmente elegibles para el análisis (figura 1 del material suplementario). Un total de 38 publicaciones que describían 26 ensayos cumplieron los criterios de inclusión y se incluyeron en el metanálisis, 13 resúmenes y 25 artículos completos (tabla 3 del material suplementario). En estos ensayos se había incluido en la aleatorización a 11.943 pacientes tratados con una ICPP en el contexto de un IAMCEST, asignándoles un tratamiento adyuvante con TA (n=5.969) o una ICPP sola (n=5.974). En 20 ensayos, se asignó a los pacientes a dispositivos de TA manuales, incluidos los dispositivos Diver (Invatec; Brescia, Italia) (cuatro con 531 pacientes), Pronto (Vascular Solutions; Minneapolis, Minnesota, Estados Unidos) (uno con 148 pacientes), Export (Medtronic; Minneapolis, Minnesota, Estados Unidos) (11 con 2.557 pacientes), Eliminate (Terumo Clinical Supply; Gifu, Japón) (dos con 269 pacientes) y Thrombuster II (Kaneka Medical Products; Osaka, Japón) (uno con 86 pacientes). Un ensayo no indicaba el catéter manual utilizado (71 pacientes). En cuatro ensayos se asignó a los pacientes a una TA asistida con bomba de vacío, incluidos los dispositivos TVAC (Nipro; Osaka, Japón) (uno con 355 pacientes) y Rescue (BSC; Maple Grove, Minnesota, Estados Unidos) (tres con 545 pacientes). En dos ensayos se combinaron catéteres, uno que empleó el Diver y el Rescue en 137 pacientes y otro que usó el Eliminate, el Export y el Pronto en 7.244 pacientes. En siete ensayos con 691 pacientes, se exigió evidencia de trombo para la inclusión en la aleatorización.
Las características basales clínicas, angiográficas y de la intervención se resumen en la tabla 3 del material suplementario. Las características metodológicas de los ensayos clínicos aleatorizados incluidos se resumen en la tabla 4 del material suplementario. La ocultación de la asignación fue adecuada en siete ensayos y no se aportó información al respecto en 19. La validación con diseño ciego de los eventos clínicos por un comité de eventos clínicos independiente se describió en dos ensayos, la evaluación independiente de las variables de valoración angiográficas en seis ensayos y la evaluación independiente de las variables de valoración electrocardiográficas en cuatro. En 17 ensayos se analizaron los datos según el principio de intención de tratar. La duración máxima del seguimiento osciló entre el periodo de hospitalización y 2 años, con una duración del seguimiento mayor de 1 mes en 15 ensayos. Ocho ensayos mencionaban que la financiación recibida era independiente de la industria.
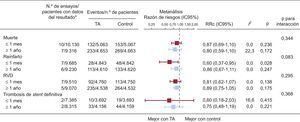
Resultados clínicosLas razones de riesgo combinadas (RRc) de los metanálisis de efectos aleatorios se presentan en la figura 1. Con una duración máxima del seguimiento ponderada de 10,4 meses, no hubo diferencias significativas en el riesgo de muerte por cualquier causa (RRc=0,88; IC95%, 0,74-1,04; p=0,124), reinfarto (RRc=0,85; IC95%, 0,67-1,08; p=0,176), revascularización de vaso diana (RRc=0,86; IC95%, 0,73-1,00; p=0,052) o TS definitiva (RRc=0,76; IC95%, 0,49-1,16; p=0,202) entre los grupos. El riesgo de ictus fue similar en ambos grupos, pero los intervalos de confianza fueron amplios (RRc=1,03; IC95%, 0,57-1,86; p=0,922).
Metanálisis de los resultados clínicos en el seguimiento máximo. IC95%: intervalo de confianza del 95%; RRc: razón de riesgos combinada de metanálisis de efectos aleatorios; RVD: revascularización de vaso diana; TA: trombectomía por aspiración. I2 = 0 en cada uno de los cinco metanálisis. aObsérvese que los ensayos con cero eventos en ambos grupos fueron excluidos de los metanálisis. bTodos los ictus se registraron dentro de los primeros 30 días de seguimiento.
No se observó evidencia alguna de heterogeneidad entre los ensayos respecto a ninguno de los objetivos analizadas (I2=0% para todos los objetivos) (figura 2 del material suplementario). Los gráficos de embudo no indicaron efectos de los estudios pequeños y los análisis estratificados no mostraron evidencia alguna de interacción de los efectos del tratamiento con las características del ensayo respecto a ninguno de los resultados clínicos, excepto por las tendencias estadísticas que indicaban efectos beneficiosos de la ICPP asistida mediante TA en los ensayos unicéntricos por lo que respecta a muerte por cualquier causa y reinfarto. Se observó una tendencia similar que indicaba efectos favorables en cuanto a muerte por cualquier causa en los ensayos iniciales (figura 3 y tabla 5 del material suplementario). Los análisis estratificados de comparación de los resultados a corto plazo con los resultados a largo plazo no mostraron interacciones significativas (figura 2). Los resultados de los análisis de sensibilidad se resumen en la tabla 6 del material suplementario, e indican que los resultados fueron uniformes tras la exclusión de los ensayos en que se utilizaron dispositivos de aspiración por vacío.
Metanálisis de los resultados clínicos estratificados respecto al tiempo de seguimiento. IC95%: intervalo de confianza del 95%; RRc: razón de riesgos combinada de metanálisis de efectos aleatorios; RVD: revascularización de vaso diana; TA: trombectomía por aspiración. Todos los ictus se registraron dentro de los primeros 30 días de seguimiento, por lo que no se realizó una estratificación. *Se excluyen los resultados con cero eventos de ambos grupos.
Las RRc de los metanálisis de efectos aleatorios para los resultados de la intervención se presentan en la figura 3. El uso de TA se asoció a una reducción significativa del flujo TIMI < 3 tras la intervención (RRc=0,70; IC95%, 0,60-0,81; p<0,001), el MBG < 3 (RRc=0,76; IC95%, 0,65-0,89; p=0,001) y la RSTi (RRc=0,72; IC95%, 0,62-0,84; p<0,001). La TA se asoció también a menor frecuencia de ausencia de implante directo de stents (RRc=0,42; IC95%, 0,30-0,57; p<0,001) y de embolización distal (RRc=0,61; IC95%, 0,46-0,81; p=0,001) en comparación con la ICPP sola (figura 4 del material suplementario).
Metanálisis de los resultados de la intervención. IC95%: intervalo de confianza del 95%; MBG: grado de opacificación (blush) miocárdica; RRc: razón de riesgos combinada de metanálisis de efectos aleatorios; RST: resolución de la elevación del segmento ST; TA: trombectomía por aspiración; TIMI: Thrombolysis In Myocardial Infarction. Obsérvese que los ensayos con cero eventos en ambos grupos fueron excluidos de los metanálisis. *Véase en «Métodos» la descripción de los ensayos excluidos de los análisis de la resolución de la elevación del segmento ST incompleta y la ausencia de implante directo de stents.
La heterogeneidad entre los ensayos fue baja por lo que respecta al flujo TIMI < 3 tras la intervención (I2=0%) y la embolización distal (I2=12,3%). Sin embargo, hubo evidencia de gran heterogeneidad en el MBG < 3 (I2=73,3%), la RSTi (I2=74,4%) y la ausencia de implante directo de stents (I2=92%). Los gráficos de embudo revelaron mayor efecto beneficioso de la TA en los ensayos de menor tamaño en RSTi y ausencia de implante directo de stents, con una prueba de Egger positiva para la asimetría (figura 5 del material suplementario). En los análisis estratificados se observó que generalmente los ensayos con adecuado enmascaramiento de la asignación del tratamiento mostraban menor efecto beneficioso en los resultados de la intervención, con interacciones formalmente positivas para la RSTi y la ausencia de implante directo de stents (p<0,003 en ambos casos), así como una tendencia estadística por lo que respecta al flujo TIMI < 3 (p=0,07). También hubo interacciones positivas con la evaluación independiente de los resultados en cuanto a la RSTi (p<0,001), con el tamaño muestral en cuanto a la RSTi y la ausencia de implante directo de stents (p<0,01 en ambos casos), con el diseño unicéntrico frente al multicéntrico en cuanto a la RSTi y la ausencia de implante directo de stents (p<0,002 en ambos casos) y con el año de publicación en cuanto a la RSTi (p<0,001). En general, los ensayos mostraron un efecto beneficioso inferior en los resultados de la intervención si eran más recientes, de mayor calidad y de mayor tamaño muestral (tabla 7 del material suplementario). La estratificación según el uso selectivo de la TA basado en la presencia basal de signos de un trombo no reveló una interacción significativa. Es de destacar que se trató selectivamente y con criterios no uniformes a menos del 6% de los pacientes (tabla 8 y figura 6 del material suplementario).
DISCUSIÓNLos resultados de este metanálisis de 26 ensayos aleatorizados, realizados en 11.943 pacientes y con una duración máxima del seguimiento ponderada de 10,4 meses, en el contexto de una ICPP realizada por un IAMCEST con o sin TA adyuvante, pueden resumirse de la siguiente forma:
- •
El uso de la TA adyuvante en pacientes con IAMCEST no seleccionados, en el contexto de una ICPP, no reduce significativamente la mortalidad por cualquier causa, el reinfarto, la revascularización del vaso diana ni la trombosis de stent definitiva.
- •
Aunque la TA da lugar a una mejora de los parámetros de reperfusión epicárdica y miocárdica, hay evidencias de un sesgo, de tal manera que los ensayos más recientes, los de mayor calidad y los de mayor tamaño muestral muestran una mejora inferior a la indicada por los demás.
- •
El riesgo de ictus no se ve afectado por el empleo de la TA.
La aspiración directa del material trombótico en el contexto de un IAMCEST mediante dispositivos de TA es una intervención sencilla, que intenta reducir la carga de trombo con objeto de mejorar los resultados de la intervención y los resultados clínicos en los pacientes con IAMCEST. Basándose en los resultados alentadores obtenidos en los ensayos de un tamaño relativamente pequeño, el uso de la TA se ha extendido rápidamente en la práctica clínica. No obstante, no se ha demostrado un efecto favorable de la TA en los resultados clínicos de isquemia mediante ensayos clínicos aleatorizados con la potencia estadística adecuada. Recientemente, el ensayo TASTE no mostró superioridad de la TA frente a la ICPP convencional en la variable de valoración principal, consistente en muerte por cualquier causa a los 30 días y a 1 año, en pacientes con IAMCEST no seleccionados24,25. En el presente metanálisis, se ha resumido toda la evidencia disponible, basada en estudios aleatorizados, y ello constituye la base de evidencia global más amplia existente hasta ahora sobre la TA.
Contrariamente a lo indicado por varios metanálisis previos, estos resultados indican ausencia de beneficio en cuanto a los resultados clínicos en el momento de máximo seguimiento11,13,15,16,26. Recientemente se ha señalado que, a pesar de que no se observó efecto beneficioso en el seguimiento a corto plazo, la mortalidad tardía puede reducirse con la TA26. Esto llevó a que se planteara la pregunta de si la igualdad existente en la mortalidad temprana estaba relacionada con una falta de precisión estadística o si había un mecanismo real que explicara una posible reducción de la mortalidad tardía. En un análisis estratificado, no se observaron interacciones formales en cuanto al momento de evaluación de los resultados (30 días o 1 año). Estos resultados se veían influidos de manera importante por el ensayo TASTE, puesto que tras su exclusión los resultados concordaron con los de los metanálisis previos en el análisis de sensibilidad realizado. No obstante, se exploraron las estimaciones combinadas después de la exclusión de los ensayos TASTE y TAPAS, y nuevamente hubo ausencia de efectos beneficiosos favorables a la TA.
Diversos informes indican que el uso sin restricciones de la trombectomía puede no aportar un efecto beneficioso a todos los pacientes con IAMCEST27–30. Aun en el caso de una trombectomía efectiva, hay otros factores determinantes del pronóstico, como el tiempo de isquemia, la amplitud del área en riesgo, la presencia de un flujo colateral antes de la intervención y la calidad de la reperfusión al final de la intervención, así como el tipo de stent, que es preciso tener en cuenta31–33. La interrelación entre esos factores puede reducir de manera importante la influencia de la TA en la mortalidad global de pacientes con IAMCEST no seleccionados. Es de destacar que al menos un 35% de los pacientes incluidos en el ensayo TASTE no presentaron inicialmente un trombo identificable angiográficamente (trombo de grado TIMI > 1), lo cual oculta los posibles efectos beneficiosos en los pacientes con gran carga trombótica.
Kumbhani et al26 observaron una reducción significativa del reinfarto y la trombosis de stent durante una media ponderada de seguimiento de 2,7 meses. Los resultados del presente estudio a los 10,4 meses mostraron ausencia de diferencias entre los grupos para las dos variables de valoración; sin embargo, después de estratificar los resultados extraídos en función de que el seguimiento fuera de corta (30 días) o larga duración (1 año), se observaron unas tasas de reinfarto significativamente inferiores a los 30 días, y este efecto favorable desapareció en el análisis realizado a 1 año. Esta observación se debía a una incidencia numéricamente inferior de los reinfartos a 1 mes en los pacientes asignados aleatoriamente a la TA de los ensayos TAPAS y TASTE24,25,34. No obstante, los resultados del TASTE a 1 año mostraron la práctica ausencia de diferencias entre los grupos (el 2,7 frente al 2,7%; hazard ratio [HR]=0,97; IC95%, 0,73-1,28; p=0,81).
Los efectos inmediatos de la TA en la reperfusión se han puesto de manifiesto de manera uniforme en los ensayos aleatorizados y metanálisis previos, que han mostrado una mejora del flujo TIMI y el MBG después de la intervención. Estos resultados confirman una mejora significativa respecto a la perfusión tanto epicárdica como miocárdica en los pacientes tratados con TA. Sin embargo, los gráficos de embudo asimétricos y los análisis estratificados indican que los metanálisis previos pueden haber sobrevalorado el efecto beneficioso si no tuvieron en cuenta la calidad metodológica y el tamaño muestral como posibles explicaciones de la heterogeneidad existente entre los ensayos. La estratificación según el año de publicación mostró también una interacción significativa en cuanto a un marcador de la reperfusión miocárdica (es decir, la RSTi), que podría ser consecuencia de la selección de los pacientes, la mejora de los tratamientos periintervención (es decir, las pautas de medicación antitrombótica) o, nuevamente, la calidad metodológica. No obstante, teniendo en cuenta el bajo grado de heterogeneidad y las pruebas de interacción negativas, las estimaciones globales parecen válidas para el flujo TIMI < 3, el MBG < 3 y la embolización distal. Por el contrario, la ausencia de implante directo de stents y la RSTi deben interpretarse con precaución.
En un reciente metanálisis de la TA en pacientes con IAMCEST14, se ha descrito una tendencia a un riesgo de ictus superior con la TA. Sin embargo, el análisis tuvo limitaciones, al menos en parte, debido a la notificación poco uniforme de los ictus en los diversos ensayos incluidos, así como al bajo número de pacientes incluidos en el cálculo de las estimaciones. En el presente metanálisis, no hubo diferencias en el riesgo de ictus entre los pacientes tratados con o sin TA, lo cual indica ausencia de problemas de seguridad en relación con la TA y el riesgo de episodios cerebrovasculares.
LimitacionesLos resultados de este metanálisis deben interpretarse teniendo en cuenta las siguientes limitaciones. En primer lugar, en ausencia de datos de pacientes individuales, los resultados deben interpretarse como efectos medios, y no se puede descartar una diferencia de la magnitud de los efectos en subgrupos específicos. En segundo lugar, no se pudo analizar los datos sobre la influencia de la TA en el tamaño del infarto, debido a la notificación poco uniforme en los ensayos incluidos. En tercer lugar, los resultados de la intervención mostraron heterogeneidad, efecto de los estudios pequeños, y el análisis estratificado mostró evidencia de menor efecto beneficioso cuanto mayor calidad metodológica. Sin embargo, las RRc de las variables de valoración clínicas no mostraron heterogeneidad entre los diversos ensayos y no se asociaron al tamaño o la calidad del ensayo, lo cual respalda la robustez de los resultados en cuanto a los parámetros clínicos. En cuarto lugar, este análisis tiene la limitación de una media ponderada de seguimiento de 10,4 meses, y no se puede descartar un efecto beneficioso a más largo plazo. Por último, los resultados de próxima aparición del ensayo A Randomized Trial of Routine Aspiration ThrOmbecTomy With PCI Versus PCI ALone in Patients With STEMI Undergoing Primary PCI (TOTAL) (NCT01149044) aportarán nueva luz sobre los efectos de la TA en los pacientes con IAMCEST a los que se trata con una ICPP, junto con un metanálisis a nivel de pacientes que se ha previsto realizar combinando los datos de los ensayos TASTE y TOTAL.
CONCLUSIONESEn pacientes con IAMCEST no seleccionados, la ICPP asistida mediante TA no mejora los resultados clínicos a pesar de la mejora de los parámetros de reperfusión epicárdicos y miocárdicos.
FINANCIACIÓNLa financiación para el presente análisis proviene en parte de una subvención de la Swiss National Science Foundation concedida a los Prof. S. Windecker y P. Jüni (subvención 33CM30-140336). El Dr. E. Spitzer ha recibido una beca de investigación de la European Association of Percutaneous Cardiovascular Interventions (EAPCI) de la Sociedad Europea de Cardiología y una subvención de investigación de la Sociedad Española de Cardiología. El Dr. G.G. Stefanini ha recibido una beca de investigación (SPUM [Special Programme University Medicine]) de la Swiss National Science Foundation.
CONFLICTO DE INTERESESEl Prof. P. Jüni formó parte, sin recibir remuneración, del comité directivo o el comité ejecutivo estadístico de ensayos financiados por Abbott Vascular, Biosensors, Medtronic y Johnson & Johnson. La CTU (Clinical Trials Unit) Bern, la unidad de ensayos clínicos de la University of Bern, tiene una política de no aceptar honorarios ni pagos por consultoría. Sin embargo, la CTU Bern participa en el diseño, la realización o el análisis de estudios clínicos financiados por Abbott Vascular, Ablynx, Amgen, AstraZeneca, Biosensors, Biotronik, Boehringer Ingelheim, Eisai, Eli Lilly, Exelixis, Geron, Gilead Sciences, Nestlé, Novartis, Novo Nordisk, Padma, Roche, Schering-Plough, St. Jude Medical y Swiss Cardio Technologies. El Prof. S. Windecker ha tenido contratos de investigación con la institución de Biotronik y St. Jude. Todos las demás autores han indicado que no tienen relaciones que declarar.
Queremos dar las gracias a Jingying Wang, estudiante de doctorado en el Institute of Social and Preventive Medicine de Berna, por su ayuda en la traducción del chino al inglés.