Todavía no se conoce la eficacia a largo plazo de la ablación con criobalón de la fibrilación auricular paroxística aislada. Se presentan los resultados de un seguimiento a largo plazo de la intervención de ablación con un solo criobalón.
MétodosSe llevó a cabo el aislamiento de la vena pulmonar en 103 pacientes (72 varones; mediana de edad, 52 años) con fibrilación auricular paroxística aislada sintomática. El objetivo de este estudio observacional de cohorte era la primera recurrencia de la arritmia (fibrilación auricular, taquicardia auricular o aleteo auricular) documentada mediante electrocardiograma en un seguimiento de 5 años, en ausencia de tratamiento antiarrítmico.
ResultadosSe estableció aislamiento completo agudo de la vena pulmonar en el 86% de los pacientes con un solo criobalón. Las tasas de éxito a los 6 meses, 1 año y 5 años tras una sola intervención fueron del 94, el 91 y el 77% respectivamente. Se observó recurrencia de la arritmia en 24 casos, tras una mediana de 14,8 [intervalo, 8,0-16,8] meses. Se controló bien solo con bloqueadores beta a 13 pacientes sintomáticos; 7 pacientes sintomáticos recibieron tratamiento antiarrítmico (de clase IC en 5 pacientes; dronedarona en 2) que se introdujo durante el periodo de aclaramiento. Dos de ellos presentaron una recurrencia temprana de la arritmia solamente durante el periodo de aclaramiento; se mantuvieron sin arritmia en el seguimiento posterior durante el tratamiento con dronedarona. La tasa de complicaciones fue relativamente baja e incluyó una incidencia del 4,8% de parálisis transitoria del nervio frénico.
ConclusionesUna intervención de ablación con un solo criobalón para la fibrilación auricular paroxística aislada produjo tasas altas de eficacia aguda y a medio y largo plazo. La tasa de complicaciones fue relativamente baja e incluyó una incidencia del 4,8% de parálisis transitoria del nervio frénico.
Palabras clave
La escasa eficacia del tratamiento farmacológico para los pacientes con fibrilación auricular (FA) es bien conocida1. La ablación de la FA por catéter es una modalidad terapéutica importante para estos pacientes y la piedra angular de la mayoría de las intervenciones de aislamiento de la vena pulmonar (AVP)2.
En los últimos años, los avances tecnológicos han conducido a la aplicación de métodos de AVP de orientación anatómica «directos», que son más rápidos y pueden resultar más seguros. Se ha demostrado la superioridad de la ablación con criobalón (ACB) respecto a los fármacos antiarrítmicos (FAA)3, con unas tasas de éxito comparables a las de las intervenciones de AVP realizadas mediante radiofrecuencia, en los pacientes con FA paroxística4,5. Recientemente, ha demostrado la alta eficacia de la ACB como tratamiento de primera línea en una cohorte seleccionada de pacientes con seguimiento a medio plazo6.
La prevalencia general de la FA es del 0,4 al 1% de la población general7,8. En ese grupo, la FA paroxística aislada (FAPA)9,10 se da en un 1% del total de casos de FA11. Aunque esta población tiene un riesgo de mortalidad, insuficiencia cardiaca y complicaciones tromboembólicas relativamente bajo, el riesgo de progresión a una FA persistente o permanente se ha estimado en un 47%11,12. Además, recientemente se han descrito los efectos beneficiosos de la abolición temprana de la FA en cuanto a la prevención del remodelado auricular y la evolución a FA persistente/permanente13.
Las guías más recientes14,15 recomiendan claramente centrarse en los pacientes jóvenes (edad<65 años) de «bajo riesgo» con FA. El consenso más reciente subraya la necesidad de presentar los resultados de éxito a largo plazo, definido como «ausencia de recurrencias de FA, aleteo auricular, taquicardia auricular (FLATA) tras un periodo de aclaramiento de 3 meses durante un mínimo de 36 meses de seguimiento a partir de la fecha de la ablación, en ausencia de tratamiento con FAA de clases I y III», sobre todo para las «tecnologías de ablación más recientes» como las técnicas con balón, y en poblaciones específicas de pacientes, como pacientes con FA aislada2. Siguiendo lo indicado en esas recomendaciones2,14, presentamos el primer examen de resultados y seguridad a muy largo plazo de la ACB en pacientes con FAPA.
MÉTODOSPacientesSe definió a los pacientes con FA aislada como individuos jóvenes (edad<65 años) sin signos clínicos ni ecocardiográficos de enfermedad cardiorrespiratoria, incluida la hipertensión9,10,16. Entre el 1 de enero de 2005 y el 31 de diciembre de 2008, se incluyó en el estudio a 103 pacientes consecutivos con FAPA refractaria a la medicación y recurrente. En todos los pacientes, la FA paroxística se documentó mediante electrocardiograma (ECG) al menos en una ocasión durante los 3 meses previos a la ablación. Los criterios de exclusión fueron la fibrilación no paroxística, cualquier cardiopatía estructural, hipertensión, enfermedad pulmonar obstructiva crónica tratada con simpaticomiméticos beta, insuficiencia respiratoria grave, diátesis hemorrágica o intolerancia a la heparina o a la anticoagulación oral, intento previo de ablación de FA, trombo en la aurícula izquierda (AI), embarazo y comorbilidad grave.
Este estudio unicéntrico se llevó a cabo en Kerckoff Klinik, Bad Nauheim, Alemania.
PreablaciónSe obtuvo la historia clínica de los pacientes durante las visitas ambulatorias, con un examen detallado de los registros médicos, incluidos los ECG y los ECG-Holter que mostraban episodios de FA. Todos los pacientes dieron su consentimiento informado por escrito. El estudio recibió la aprobación del comité de ética interno del centro. Se suspendió la anticoagulación oral 3 días antes de la intervención y se sustituyó por heparina de bajo peso molecular subcutánea. Se suspendieron los FAA al menos 3 días antes ablación. Se autorizó el uso de bloqueadores beta según lo establecido en el protocolo.
Se realizó una ecocardiografía a todos los pacientes para determinar el diámetro de la AI y descartar la presencia de un trombo en la AI. Se evaluó el tamaño de la AI midiendo el eje corto y el eje largo en la proyección apical de cuatro cámaras17.
IntervenciónLa intervención ya se ha descrito anteriormente18,19. Tras realizar las punciones transeptales, se introdujo la heparina para mantener un tiempo de coagulación activado >300 s durante toda la intervención. En resumen, se utilizó un criobalón de 23 y/o 28mm (Arctic FrontalTM, Medtronic Cryocath). El tiempo de aplicación fue de 240-300 s. Durante la ACB de las venas pulmonares del lado derecho, se evaluó el movimiento frénico no afectado mediante la estimulación continua del nervio frénico y monitorización continua de la respiración espontánea. Tras el aislamiento inicial, se verificó la posible recurrencia de la conducción venosa pulmonares (VP) durante un periodo de observación de 30min. Si no se podía alcanzar un AVP con el tamaño de criobalón de primera elección, se utilizaba un tamaño diferente en un nuevo intento. Si no se podía confirmar el AVP tras cinco aplicaciones consecutivas por VP con ninguno de los balones utilizados, se aplicaba un catéter de crioablación con punta de 8mm (FreezorMAXTM, Medtronic Cryocath) para la ablación por contacto para completar el AVP, que se verificaba después de que hubiera producido una eliminación completa de todas las señales de la VP a nivel del antro o del ostium. Además, se confirmó el bloqueo de salida y de entrada de todas las VP mediante maniobras de marcapasos, según un método descrito anteriormente18,19.
Tratamiento tras la ablaciónDespués de la intervención, se continuó la administración de heparina intravenosa para alcanzar un tiempo de tromboplastina parcial de 60–80 s, seguida de anticoagulación oral con warfarina sódica durante al menos 3 meses, con un objetivo de razón internacional normalizada 2–3. Se suspendió el tratamiento antiarrítmico. Se permitió el empleo de bloqueadores beta durante el periodo de seguimiento.
SeguimientoEl estricto protocolo de seguimiento de este estudio se atiene a lo establecido en las recomendaciones más recientes2. Después del alta hospitalaria, se programaron visitas trimestrales de seguimiento de los pacientes. El seguimiento más tardío (> 1 año después de la intervención) se llevó a cabo una vez al año durante 5 años. Se obtuvieron registros de ECG-Holter de 7 días en cada visita de seguimiento. Se indicó a todos los pacientes que, en caso de sentir palpitaciones de cualquier tipo, debían realizarse un ECG para confirmar o descartar FLATA.
Análisis estadísticoEl estudio utilizó un diseño de cohorte observacional. El objetivo del estudio se definió como la primera recurrencia de FLATA después del periodo de aclaramiento de 3 meses durante un seguimiento de 5 años en ausencia de FAA. Se utilizó un análisis univariable de Kaplan-Meier para estimar la supervivencia sin FLATA. Los datos de las variables de tipo continuo se describen mediante mediana [intervalo intercuartílico]. Las variables de tipo discreto se presentan como número y porcentaje. Se consideraron significativas las diferencias con valor de p<0,05.
RESULTADOSCaracterísticas de los pacientes y de la intervenciónEn total, participaron en el estudio 103 pacientes consecutivos. Las características clínicas de los pacientes y las características de la intervención se presentan en las tablas 1 y 2 respectivamente. Se observó anatomía atípica de la VP en 10 pacientes (9,7%): VP derechas accesorias en 2 (1,9%) y ostium de la VP izquierda común en 8 (7,8%). Se obtuvo un aislamiento agudo de todas las VP con un criobalón de un solo tamaño en 85 pacientes (82%). Se aplicó una combinación de balones de 23 y 28mm en 14 pacientes (14%) y se usó el FreezorMaxTM en 4 (4%). Por lo tanto, se alcanzó el AVP con una sola intervención en todos los pacientes.
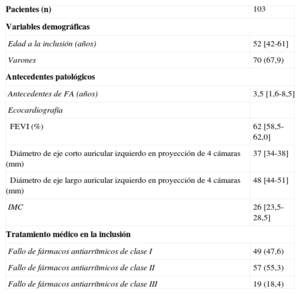
Características basales
| Pacientes (n) | 103 |
| Variables demográficas | |
| Edad a la inclusión (años) | 52 [42-61] |
| Varones | 70 (67,9) |
| Antecedentes patológicos | |
| Antecedentes de FA (años) | 3,5 [1,6-8,5] |
| Ecocardiografía | |
| FEVI (%) | 62 [58,5-62,0] |
| Diámetro de eje corto auricular izquierdo en proyección de 4 cámaras (mm) | 37 [34-38] |
| Diámetro de eje largo auricular izquierdo en proyección de 4 cámaras (mm) | 48 [44-51] |
| IMC | 26 [23,5-28,5] |
| Tratamiento médico en la inclusión | |
| Fallo de fármacos antiarrítmicos de clase I | 49 (47,6) |
| Fallo de fármacos antiarrítmicos de clase II | 57 (55,3) |
| Fallo de fármacos antiarrítmicos de clase III | 19 (18,4) |
FA: fibrilación auricular; FEVI: fracción de eyección del ventrículo izquierdo; IMC: índice de masa corporal.
Los datos expresan n (%) o mediana [intervalo intercuartílico].
Características de la intervención
| Pacientes (n) | 103 |
| Datos básicos | |
| Tiempo de fluoroscopia (min) | 33 [24-45] |
| Tiempo de intervención acumulado (h) | 3,5 [3,0-4,0] |
| Tipo de crioablación o FreezorMAXTM | |
| Pacientes tratados con criobalón de 23 mm | 14 (13,6) |
| Pacientes tratados con criobalón de 28 mm | 75 (72,8) |
| Pacientes tratados con criobalón de 23 y 28 mm | 14 (13,6) |
| VPSD tratadas | 1 (1,0) |
| VPID tratadas | 5 (4,8) |
| VPSI tratadas | 10 (9,7) |
| VPII tratadas | 7 (6,8) |
| Pacientes tratados con FreezorMax | 4 (3,9) |
| VPSD tratadas | 2 (1,9) |
| VPID tratadas | 2 (1,9) |
| VPSI tratadas | 1 (1,0) |
| VPII tratadas | 1 (1,0) |
| Aplicaciones de criobalón | |
| VPSD | 2,6±0,9 |
| VPID | 2,7±1,2 |
| VPSI | 2,9±1,2 |
| VPII | 2,9±1,1 |
| Temperatura alcanzada durante las aplicaciones de criobalón (°C) | |
| VPSD | –52 [–56 a –47] |
| VPID | –47 [–54 a –42] |
| VPSI | –51 [–60 a –47] |
| VPII | –45 [–53 a –42] |
| Tiempo acumulado de aplicaciones de criobalón por paciente (s) | 3.300 [2.400-3.950] |
| VPSD | 727 [600-1.000] |
| VPID | 720 [600-1.000] |
| VPSI | 869 [600-1.080] |
| VPII | 800 [600-1.000] |
VPID: vena pulmonar inferior derecha; VPII: vena pulmonar inferior izquierda; VPSD: vena pulmonar superior derecha; VPSI: vena pulmonar superior izquierda.
Los datos expresan n (%), media ± desviación estándar o mediana [intervalo intercuartílico].
Se produjeron complicaciones perintervención, con necesidad de intervención, en 6 pacientes. Hubo un taponamiento cardiaco que se trató con drenaje pericárdico. En 5 casos, se observó parálisis del nervio frénico durante la ablación correspondiente a la VP superior derecha. Se observó un derrame pericárdico que no requirió intervención. No se identificó ninguna otra complicación.
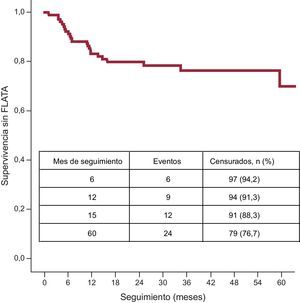
SeguimientoNo se perdió del seguimiento a ningún paciente. Por lo que respecta al objetivo principal, la tasa de éxito a 5 años tras una única intervención de ACB fue del 77% (figura).
Resultados a 5 años en pacientes con fibrilación auricular paroxística aislada. Curva de Kaplan-Meier de supervivencia libre de eventos tras una sola intervención de ablación con criobalón en pacientes jóvenes con fibrilación auricular paroxística aislada. Grupo de estudio (n = 103). FLATA: fibrilación auricular, aleteo auricular, taquicardia auricular.
No influyeron en los resultados usar FAA antes de la ACB ni usar un criobalón de mayor tamaño o FreezorMaxTM durante la intervención. Se utilizaron bloqueadores beta en 60 pacientes (58%); 57 de ellos ya recibían tratamiento con bloqueadores beta antes la intervención de ACB; en 3 casos, se introdujeron durante el seguimiento. Se observó recurrencia de FLATA en 24 pacientes tras una mediana de 14,8 [8,0-16,8] meses. A 13 pacientes sintomáticos se los controló bien con solo bloqueadores beta; 7 pacientes sintomáticos recibieron tratamiento con FAA (de clase IC en 5 pacientes; dronedarona en 2) que comenzó durante el periodo de aclaramiento, incluido 1 paciente que ya estaba en tratamiento con bloqueadores beta; 2 de estos pacientes sufrieron recurrencia temprana de FLATA solo durante el periodo de aclaramiento; se mantuvieron sin FLATA en el seguimiento posterior durante el tratamiento con dronedarona. Finalmente, 7 pacientes con recurrencia de FLATA requirieron reintervención.
DISCUSIÓNTanto las guías más recientes14 como una declaración de consenso2 subrayan la necesidad de presentar datos sobre la eficacia a largo plazo del uso de las nuevas técnicas de ablación en poblaciones de pacientes específicas. Este artículo presenta un seguimiento a muy largo plazo de la ACB en pacientes con FAPA.
En general, durante el seguimiento se observó ausencia de FLATA tras una sola intervención de ACB y sin tratamiento con FAA (excepto por los bloqueadores beta) en el 88% de los pacientes a los 15 meses y el 77% a los 5 años. La tasa de complicaciones fue aceptablemente baja.
Justificación de la selección de los pacientesLa FA se asocia a un aumento de 5 veces en el riesgo de ictus14. El diagnóstico de FA antes de que se produzcan las primeras complicaciones es crucial para la prevención del ictus. Se recomienda un examen de detección sistemática oportunista de la FA para los pacientes de ≥ 65 años14. Las guías recientes han resaltado la conveniencia de utilizar el enfoque de factores de riesgo para estratificar el riesgo de ictus de los pacientes. Se ha recomendado modificar la práctica clínica para centrarse más en identificar a los pacientes con FA de «bajo riesgo real» (es decir, edad <65 años y FA aislada)14. Además, la puntuación de riesgo CHA2DS2-VASc (insuficiencia cardiaca congestiva, hipertensión, edad ≥ 75 [doble], diabetes, ictus [doble], enfermedad vascular y categoría de sexo [mujeres])recientemente adoptada ha identificado la edad > 65 años como uno de los factores de riesgo14.
En un reciente consenso internacional sobre nomenclatura y clasificación de la FA, se mencionó que solamente la FA en ausencia de cardiopatía debe denominarse aislada (lone)20,21. El diagnóstico de la FA aislada es básicamente un diagnóstico de exclusión y le debe preceder una evaluación cuidadosa, que incluya la obtención detallada de antecedentes del paciente, exploración física, determinación de la presión arterial, análisis de laboratorio, ECG, ecocardiografía y, según algunos expertos, radiografía de tórax y prueba de esfuerzo con ejercicio15,20. Clínicamente, se han diferenciado cinco tipos de FA basados en la duración de la arritmia: FA de primer diagnóstico, paroxística, persistente, persistente de larga duración y permanente22.
En consecuencia, el estudio se centró en los pacientes con FAPA jóvenes y de bajo riesgo real. El predominio del sexo masculino característico en esta cohorte, en relación varones:mujeres de 3:1, ya se ha descrito23.
Éxito agudo de la intervenciónUna revisión sistemática previa ha puesto de manifiesto que el éxito agudo de la intervención se pudo alcanzar en 99% (intervalo, 92-100%) de un total de 924 pacientes24. La ablación con el catéter de criobalón por sí sola alcanzó el AVP en el 78% de los pacientes, mientras que un enfoque híbrido, con ablación focal concomitante logró AVP completo en el 99% de los pacientes24. En el presente estudio, se logró el aislamiento completo en el 96% (99 de 103) de los casos con la técnica de criobalón sola. No obstante, hubo que cambiar el tamaño del balón en 14 intervenciones en pacientes con diversas características anatómicas. La aplicación adicional de lesiones producidas con el FreezorMaxTM, que se llevó a cabo en 4 pacientes, produjo el AVP completo en el 100%. Recientemente se han descrito resultados comparables en un estudio de Namdar et al6 en una pequeña cohorte de 18 pacientes con FAPA. En 2 pacientes, fueron necesarias también lesiones adicionales producidas mediante contacto con radiofrecuencia6.
Resultados clínicosNo hay datos sobre los resultados clínicos a largo plazo tras la intervención de ACB en pacientes jóvenes con FAPA. El único estudio publicado, que describe los resultados a 1 año en pacientes con FAPA, indicó una tasa de éxito del 82%6. No obstante, la principal limitación de ese estudio es el bajo número de pacientes: solo 11 llegaron a los 12 meses de seguimiento.
Nuestros resultados parecen prometedores. Después de una sola intervención de ACB, se observó una supervivencia total libre de FLATA sin tratamiento con FAA muy alta: el 91% a los 12 meses, el 88% a los 15 meses y el 77% a los 5 años de seguimiento. Además, el resultado clínico general, tras la inclusión de 17 pacientes con buen control del ritmo con FAA, fue del 93% a los 5 años de seguimiento. Tan solo 7 pacientes requirieron reintervención para aliviar los síntomas de FA. No se observó progresión a FA persistente en ninguno de los pacientes.
Muchos son los posibles motivos de que la cohorte de pacientes jóvenes con FAPA estudiada haya tenido tan favorable evolución clínica. Estos pacientes no presentan agrandamiento auricular y tienen FA paroxística. En este contexto, la probabilidad de un proceso de remodelado profundo es baja y la aparición de la FA depende de un desencadenante más que de un sustrato. La mayor parte de los desencadenantes tienen su origen en la unión AI-VP25. La ACB centrada en el AVP, que elimina los desencadenantes y en parte el sustrato, situados cerca de la unión AI-VP, proporciona un porcentaje elevado de éxitos en esos pacientes. El fracaso terapéutico del AVP en este grupo es consecuencia de un aislamiento incompleto de los desencadenantes de AI-VP o de la existencia de desencadenantes que no tengan su origen en la unión de AI-VP. Además, la combinación de una AI de tamaño normal y un balón relativamente grande puede conducir no solo a un AVP circular en el ostium, sino también al AVP mediante ablación en bloque en el antro homolateral, lo cual podría proporcionar una mejora adicional de los resultados clínicos26.
En la toma de decisiones ante un paciente joven en cuanto al uso de FAA o tratamiento ablativo, se debe tener en cuenta factores como la posible duración de la exposición a los FAA27. El efecto proarrítmico de los FAA, como arritmias ventriculares mortales, se ha descrito claramente28. El tiempo que se emplea determinada medicación, en especial en el caso de la amiodarona, se asocia con otras complicaciones bien conocidas28. No obstante, el tratamiento médico tiene escasa eficacia en cuanto a la preservación del ritmo sinusal29. El ensayo STOP AF, recientemente publicado, ha demostrado que la ACB resulta más eficaz que los FAA en el tratamiento de los pacientes con FA paroxística sintomática3. Sin embargo, los resultados del ensayo STOP AF no pueden extrapolarse directamente a nuestra cohorte de pacientes.
Además, teniendo en cuenta el riesgo de isquemia cerebral silente perintervención, la tecnología de criobalón parecía ser la más segura para el tratamiento de los pacientes con FA. La incidencia de signos de microembolias cerebrales durante la ablación percutánea de la FA en los pacientes tratados con ACB fue la más baja observada, en comparación con el catéter de radiofrecuencia30. Por otro lado, la incidencia de episodios embólicos intracraneales subclínicos fue inferior después de la ACB (4%) que tras las intervenciones de radiofrecuencia (7%) y de radiofrecuencia en fase con multielectrodos (37%)30. Por consiguiente, la población de individuos jóvenes con FAPA estudiada parece ser la más apropiada para una estrategia de tratamiento con balón en la que el objetivo de la intervención es únicamente el AVP.
SeguridadLa complicación más frecuente de la intervención de ACB es la parálisis del nervio frénico, que tiene una incidencia total del 6%24. La incidencia previamente descrita de parálisis del nervio frénico persistente tras la ablación era del 5% (67 de 1.349), con recuperación completa en 1 año en la mayoría de los pacientes (62 de 1.349)24.
Se observaron 5 casos (4,8%) de parálisis del nervio frénico durante la ACB en la VP superior derecha y ninguno en las otras VP. En 4 de estos pacientes, se utilizó un criobalón de 28mm. A pesar de la interrupción inmediata del ciclo de congelación al producirse pérdida de captura del nervio frénico, la parálisis del nervio frénico persistió después de la intervención, pero a los 12 meses se observó plena recuperación en los 5 pacientes.
Un estudio reciente ha puesto de manifiesto que el uso sistemático de estimulación del nervio frénico conjuntamente con un catéter con criobalón de 28mm no logró eliminar el problema de la parálisis del nervio frénico31. Se ha propuesto que la relación anatómica entre la VP superior derecha y la vena cava superior puede tener valor predictivo respecto al desarrollo de parálisis del nervio frénico durante la ACB con un catéter de criobalón de 28mm: los factores predictivos, la prevención y la temperatura baja del criobalón al inicio del ciclo de congelación proporcionaron una señal de alarma sensible respecto a la inminencia de parálisis del nervio frénico32. La exploración con técnicas de imagen para evaluar antes de la intervención la relación entre VP superior derecha y vena cava superior, evitando la posición del catéter antral en la VP superior derecha, la estrecha supervisión de la temperatura y el cese súbito del aporte de energía32 o deshinchar inmediatamente el balón33 pueden mejorar en mayor medida la seguridad de la intervención. Recientemente se ha propuesto monitorizar la amplitud de los potenciales de acción motores compuestos diafragmáticos para detectar la inminencia de parálisis hemidiafragmática34.
Limitaciones del estudioEste estudio tiene las siguientes posibles limitaciones: a) es un estudio prospectivo de un solo centro y no aleatorizado, con las limitaciones inherentes a este tipo de diseño de investigación. Sin embargo, no hubo sesgo de selección en la inclusión en el estudio, ya que se incluyó en el análisis a todos los pacientes consecutivos sometidos a ACB por FAPA en nuestro centro; b) según lo establecido en el consenso más reciente2, se presentan los resultados del seguimiento sin tener en cuenta las recurrencias aparecidas durante el periodo de aclaramiento, lo que podría conducir a sobrestimar la tasa de éxito real, y c) los datos más recientes35,36, no conocidos en el momento de realizar este estudio, indican que la monitorización intermitente del ritmo es significativamente inferior a la monitorización continua con dispositivos implantados. El seguimiento se basó en la evaluación clínica y en registros de ECG-Holter de 7 días. Aunque la inmensa mayoría de los pacientes tenían formas persistentes de FLATA, es posible que no se hayan detectado algunos episodios no sostenidos asintomáticos. Cualquier arritmia asintomática no detectada debería haberse producido por igual en todos los subgrupos, y no es probable que hubiera modificado las conclusiones de este estudio4. No se realizaron exploraciones esofágicas para descartar posibles lesiones después de la intervención. Recientemente se ha descrito alta incidencia de lesiones esofágicas con los nuevos dispositivos de ACB37–39. No obstante, no se conocía estos datos en el momento de realizar el presente estudio, en el que solamente se usaron criobalones de primera generación.
Consecuencias clínicasLas consecuencias clínicas de los resultados de este estudio son notables por lo que respecta a la asistencia prestada a los pacientes jóvenes con FAPA. En primer lugar, hay que presentar datos de seguimiento a largo plazo. Los pacientes con FAPA parecen ser los candidatos de primera línea para ACB. No obstante, deben conocer las posibles complicaciones asociadas a la intervención, incluida la parálisis del nervio frénico. El uso de otras técnicas de imagen adicionales antes de la intervención y una vigilancia más intensiva de la función del nervio frénico podrían reducir al mínimo el riesgo de parálisis del nervio frénico. En segundo lugar, está justificada la monitorización continua, aun cuando inicialmente se haya considerado que la ACB se ha realizado con éxito. La incidencia de recurrencias tardías puede estar relacionada con la amplitud de monitorización electrocardiográfica y una recurrencia más temprana puede no pasar inadvertida en algunos pacientes con síntomas mínimos o sin síntomas2,36.
CONCLUSIONESEste estudio muestra que una sola intervención de ACB para la FAPA da lugar a altas tasas de eficacia aguda y a medio y largo plazo. La tasa de complicaciones fue relativamente baja e incluyó una incidencia del 4,8% de parálisis transitoria del nervio frénico.
CONFLICTO DE INTERESESEl Dr. Maciej Wójcik ha contado con el apoyo de la European Heart Rhythm Association (beca de formación en electrofisiología clínica durante 2 años, 2007-2009); el Prof. Thomas Neumann ha recibido honorarios por conferencias de Medtronic Cryocath; los Dres. Malte Kuniss y Heinz-Friedrich Pitschner recibieron honorarios por conferencias y por participación en reuniones de consejos asesores de Medtronic Cryocath.