Los síndromes coronarios agudos tienen un amplio espectro de formas de presentación clínica y de riesgo de evolución adversa. Debe establecerse una distinción entre el riesgo tratable (grado de isquemia, gravedad de la enfermedad coronaria y deterioro hemodinámico agudo) y riesgo no tratable (edad avanzada, lesión miocárdica previa, enfermedad renal crónica, otras comorbilidades). Se ha excluido de los ensayos clínicos «generadores de guías» a la mayoría de los pacientes con riesgo «no tratable». En los últimos años, a pesar de la escasez de ensayos aleatorizados específicos, se han realizado avances importantes en el tratamiento de los pacientes ancianos y los pacientes con comorbilidades: se ha pasado del nihilismo terapéutico a un ajuste cuidadoso de las dosis de fármacos antitrombóticos, tendencia al abordaje radial de las intervenciones coronarias percutáneas y también una cirugía cardiaca menos invasiva. Son de esperar nuevos avances como consecuencia del desarrollo de pautas de medicación apropiadas para ancianos y pacientes con disfunción renal, el abordaje sistemáticamente multidisciplinario del tratamiento de los pacientes con diabetes mellitus y anemia y la decisión de realizar ensayos aleatorizados en estas poblaciones de alto riesgo.
Palabras clave
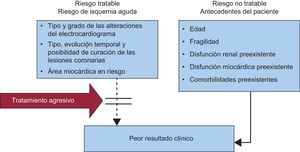
Los síndromes coronarios agudos (SCA) tienen un amplio espectro de formas de presentación clínica y de riesgo de evolución adversa. Como regla general, en medicina, cuanto mayor es el riesgo basal, mayor es el beneficio que aporta un abordaje agresivo y temprano. Sin embargo, en el SCA debe hacerse una distinción entre el riesgo atribuible al evento isquémico agudo, que se puede tratar con una intervención adecuada, y el riesgo derivado de las características basales del paciente, las comorbilidades y la fragilidad, que puede no ser tratable y hacer al paciente más vulnerable al daño iatrogénico (figura 1).
Estratificación del riesgo en el síndrome coronario agudo. Se debe distinguir entre el riesgo tratable y el no tratable. Una intervención farmacoinvasiva agresiva puede reducir el impacto pronóstico de la carga isquémica aguda, mientras que las variables de riesgo no tratables aumentan el riesgo de daños iatrogénicos.
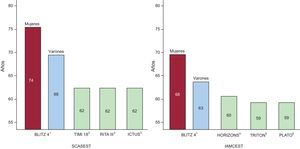
La identificación de los pacientes de alto riesgo es fácil; se han desarrollado diversos instrumentos de estratificación del riesgo, basados en los datos obtenidos en decenas de miles de pacientes incluidos en ensayos clínicos aleatorizados (ECA) y en registros. Por otro lado, decidir la forma de tratar a los pacientes de alto riesgo y la forma de minimizar el riesgo del tratamiento farmacológico y la intervención coronaria exige un juicio clínico sólido, la adopción de medidas específicas y, en la mayoría de los casos, un abordaje multidisciplinario. Es frecuente que no esté respaldado por las guías de práctica clínica, puesto que se basan principalmente en la evidencia generada por los ECA, de los que a menudo se excluye a los pacientes con comorbilidades significativas y en los que los pacientes ancianos suelen estar infrarrepresentados1–7 (figura 2).
Comparación de la media de edad poblacional en el registro actual BLITZ 4 de síndrome coronario agudo en las unidades coronarias italianas y los ensayos generadores de guías para el infarto agudo de miocardio con elevación del segmento ST y el síndrome coronario agudo sin elevación del segmento ST. Los ensayos aleatorizados han incluido poblaciones de pacientes mucho más jóvenes que los de la práctica clínica habitual. IAMCEST: infarto agudo de miocardio con elevación del segmento ST; SCASEST: síndrome coronario agudo sin elevación del segmento ST. Reproducido con permiso de Savonitto7.
En este artículo se examina la evidencia actual relativa al tratamiento del SCA de los pacientes ancianos y los pacientes con diabetes mellitus (DM), enfermedad renal crónica (ERC) o anomalías hematológicas, que pueden introducir una confusión en el abordaje invasivo y temprano del SCA.
ANCIANOSLos pacientes ancianos son una gran porción de los pacientes hospitalizados por SCA, porcentaje que aumentará aún más en las próximas décadas8. No hay una definición uniformemente aceptada de «anciano» mediante valores de corte de la edad. Los únicos dos estudios específicos y prospectivos que han abordado estrategias de tratamiento para pacientes ancianos con SCA han utilizado como valor de corte la edad ≥ 75 años9,10. Dicho umbral es el más comúnmente utilizado en la literatura médica actual11, mientras que en artículos más antiguos se utilizaron valores de corte inferiores, como los de 60 a 65 años. Esta cuestión es importante al interpretar la bibliografía, puesto que la relación entre la edad y la evolución clínica (en especial la mortalidad, pero también la hemorragia) muestra un agravamiento drástico alrededor de los 75 años11. Además, la edad creciente no implica tan solo más años, sino también un cambio de las características generales de la población con SCA. Las mujeres presentan un aumento de < 30% cuando la población en estudio tiene una media de edad de 60-63 años (como ocurre en la mayoría de los ECA) a un 50% en las poblaciones de estudio con una media de 80 años9,10. Las poblaciones ancianas incluyen, además, > 70% de pacientes hipertensos, un 35% de diabéticos, un 20% con una tasa de filtrado glomerular estimado (TFGe)<60ml/min, así como un mayor número de pacientes con antecedentes de infarto de miocardio (IM) o ictus o con fibrilación auricular y enfermedad arterial periférica2,3,9–13. Todos estos trastornos implican problemas específicos a la hora de decidir las estrategias de tratamiento. Por último, la mayor parte de los ECA y las guías sobre SCA no tienen en cuenta la fragilidad de los pacientes (y se ha demostrado que esta afecta profundamente a la evolución clínica de los ancianos14) entre las variables que hay que evaluar y analizar para orientar las estrategias de tratamiento.
En 2007, dos declaraciones científicas del American Heart Association Council on Clinical Cardiology revisaron la literatura médica existente sobre el tratamiento del SCA sin elevación del segmento ST (SCASEST)15 y el infarto agudo de miocardio con elevación del ST (IAMCEST)16 en los ancianos: estos documentos resaltaron el hecho de que los ancianos están en gran parte infrarrepresentados en las poblaciones de los ECA que son la base de las guías de práctica clínica.
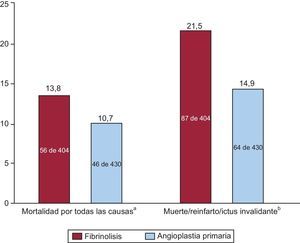
Tratamiento del infarto de miocardio con elevación del segmento STLa angioplastia primaria (intervencionismo coronario percutáneo primario [ICPp]) se ha establecido como la estrategia de reperfusión más efectiva y segura para los pacientes ancianos con IAMCEST. El ensayo TRIANA se inició en 2005 para comparar la eficacia y la seguridad del ICPp y la fibrinolisis en los pacientes muy ancianos con IAMCEST9. Ese estudio, para el que se planificó la inclusión de 570 pacientes, se interrumpió tras la incorporación de 266 pacientes en un periodo de 33 meses y mostró una tendencia a la reducción de la variable de valoración principal, consistente en los episodios observados en 30 días de muerte, nuevo IM o ictus invalidante con el ICPp (el 18,9 frente al 25,4%; odds ratio [OR]=0,69; intervalo de confianza del 95% [IC95%], 0,38-1,23). La incidencia de cada uno de los componentes de la variable de valoración principal fue inferior con el ICPp. Un análisis combinado de este ECA y dos ECA previos en los que se comparó el ICPp con el tratamiento lítico, publicado en ese mismo artículo9, mostró una tendencia a la reducción de la mortalidad y una reducción significativa de los episodios de muerte, nuevo IM e ictus en 30 días (figura 3). La relevancia de los datos de este ECA respecto a la práctica clínica se ha confirmado en el análisis del registro prospectivo multicéntrico de la Reseau de Cardiologie de Franche Comte, con una comparación de dos periodos, en 2001 y 200617. De 2001 a 2006, el ICPp pasó a ser la modalidad preferente de terapia de reperfusión frente a la fibrinolisis (OR ajustada=6,9; IC95%, 3,1-15), y este cambio en la estrategia se asoció a una cifra significativamente inferior de mortalidad a 30 días en 2006 (el 9,2 frente al 23,3%; p<0,001).
Resumen del metanálisis de ensayos aleatorizados de comparación del tratamiento fibrinolítico con la angioplastia primaria en pacientes con infarto de miocardio con elevación del ST de edad ≥ 75 años. aOdds ratio = 0,74 (intervalo de confianza del 95%, 0,49-1,13; p = 0,16). bOdds ratio = 0,64 (intervalo de confianza del 95%, 0,45-0,91; p = 0,13). Datos tomados de Bueno et al9.
Un reciente metanálisis, con la inclusión de 6.298 pacientes tratados con ICPp e implante de stents de la base de datos de la DESERT Cooperation12 confirmó que, a pesar de la tasa de mortalidad esperada en el seguimiento a largo plazo de los pacientes ancianos mayor que la de los de menor edad (hazard ratio [HR]=2,17; IC95%, 1,97-2,39; p<0,0001), no se observó influencia de la edad en el riesgo de nuevo IM, trombosis de stent o revascularización del vaso diana.
Se observó un resultado favorable en 199 pacientes de edad ≥80 años tratados en el marco del sistema de IAMCEST regional de Minneapolis18. La mediana de duración de la hospitalización fue 4 días; la mortalidad intrahospitalaria, el 11,6% y la mortalidad a 1 año, el 25,6%. De los 166 pacientes de edad ≥80 años que vivían de manera independiente o con asistencia antes del ingreso en el hospital y sobrevivieron, a 150 (90,4%) se les dio el alta para pasar a una situación de vida similar o tenían prevista esta situación tras una permanencia temporal en una residencia.
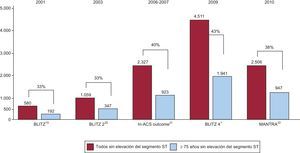
Tratamiento invasivo del síndrome coronario agudo sin elevación del segmento STLos pacientes con SCASEST son de más edad que los pacientes con IAMCEST e incluyen un mayor porcentaje de mujeres1. Tal como se indica en la figura 4, en recientes registros italianos de SCA, los pacientes de edad ≥ 75 años representan aproximadamente un 40% de los casos de SCASEST1,19–22. En los últimos años, los análisis inferenciales basados en registros23 y los análisis de subgrupos de ECA2,3 han indicado que un abordaje invasivo en los pacientes ancianos se asocia a mejor resultado clínico que con el tratamiento conservador. En el registro multicéntrico ROSAI–223, De Servi et al. compararon los resultados clínicos a 30 días en 564 pacientes de edad ≥ 75 años con los de 1.017 pacientes de menos edad: los ancianos tenían unas características basales más desfavorables y recibieron menos tratamientos farmacológicos basados en la evidencia. Se adoptó una estrategia agresiva temprana en el 39% de los pacientes ancianos y el 56% de los más jóvenes (p<0,001). Se aplicó un enfoque intervencionista en un plazo de 30 días en el 30 y el 48% de los casos (p<0,001). A los 30 días, los ancianos presentaban mayores tasas de muerte (el 6,4 frente al 1,7%), IM (el 7,1 frente al 5%) e ictus (el 1,3 frente al 0,5%). El análisis multivariable del grupo de pacientes ancianos identificó que la estrategia conservadora (OR=2,31; IC95%, 1,20-4,48) y el diagnóstico de IM sin onda Q (OR=2,27; IC95%, 1,32-3,93) eran factores independientes predictivos de eventos clínicos en un plazo de 30 días. Por otro lado, el citado registro Reseau Franche Compte no observó entre 2001 y 2006 mejora alguna en los resultados clínicos a 30 días de los pacientes ancianos con SCASEST, a pesar de cuadruplicarse el uso de la estrategia invasiva17. Sin embargo, es preciso tener en cuenta que una variable de valoración basada en un periodo de 30 días puede no reflejar ventajas del abordaje invasivo de los SCASEST que podrían evidenciarse en una evaluación muy posterior, y tal seguimiento se ha aplicado en ECA.
En los pacientes de edad ≥ 75 años incluidos en el ensayo TACTICS–TIMI 182, la estrategia invasiva temprana aportó una reducción absoluta de 10,8 puntos porcentuales (el 10,8 frente al 21,6%; p=0,016) y una reducción relativa del 56% en la variable de muerte o IM a los 6 meses, lo cual es un efecto beneficioso muy superior al observado en los grupos de menos edad. En este estudio, las tasas de hemorragia mayor TIMI (Thrombolysis In Myocardial Infarction) fueron casi prohibitivas con la estrategia agresiva temprana en los de edad ≥ 75 años (el 16,6 frente al 6,5%; p=0,009), muy probablemente debido al tratamiento inicial sistemático con tirofibán y heparina no fraccionada y el uso universal del abordaje femoral para el cateterismo.
En un análisis conjunto de los datos individuales de los ensayos FRISC II, ICTUS y RITA-3 (FIR)3, todos los cuales compararon la estrategia invasiva ordinaria frente a una estrategia selectiva en el SCASEST, se evaluaron los resultados clínicos hasta 5 años después de la hospitalización índice. La variable de valoración combinada de muerte cardiovascular e IM fue significativamente inferior con la estrategia invasiva ordinaria en los pacientes de 65–74 años (HR=0,72; IC95%, 0,58-0,90) y ≥ 75 años (HR=0,71; IC95%, 0,55-0,91), pero no en los pacientes < 65 (HR=1,11; IC95%, 0,90-1,38; p<0,001 para la interacción entre estrategia de tratamiento y edad). La interacción se debía a un exceso de casos de IM temprano en los pacientes > 65 años, mientras que no hubo heterogeneidad entre los grupos de edad en lo relativo a la muerte cardiovascular. Los efectos beneficiosos fueron menores en las mujeres que en los varones (p<0,009 para la interacción).
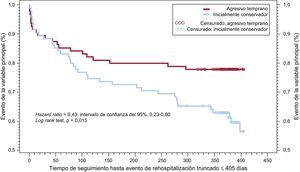
El estudio italiano del SCA en el anciano10 fue el primer ECA en que se incluyó exclusivamente a pacientes de edad ≥ 75 años con SCASEST: se asignó aleatoriamente a los pacientes a una estrategia invasiva temprana (angiografía coronaria y, si estaba indicado, revascularización en un plazo de 72h) o una estrategia inicialmente conservadora (angiografía y revascularización solo en casos de isquemia recurrente). El estudio se programó inicialmente para la inclusión de 504 pacientes y se estableció una variable de valoración principal correspondiente al seguimiento a los 6 meses, que posteriormente se modificó para pasar a la valoración principal a los 12 meses, con un tamaño muestral de 313 pacientes; a otros 332 pacientes excluidos del ensayo por cualquier razón se los incluyó en un registro paralelo. La media de edad de los participantes era 82 años y el 50% eran mujeres. La variable de valoración principal (un beneficio clínico neto en cuanto a mortalidad por todas las causas, IM, ictus invalidante y nueva hospitalización por causas cardiovasculares o hemorragia grave) mostró una reducción significativa con el enfoque invasivo temprano en los pacientes con elevación de troponinas al ingreso (el 61% de los casos) (figura 5), si bien el efecto beneficioso no fue significativo para el conjunto de la población en estudio (el 27,9 frente al 34,6%; HR=0,80; IC95%, 0,53-1,19), con una interacción significativa entre el tratamiento y el estado troponínico (p=0,03). Todos los componentes de la variable de valoración principal mostraron una tendencia al beneficio con la estrategia invasiva temprana. Es de destacar que, incluso en esa población de mayores, el 80% de las causas de muerte en el plazo de 1 año fueron de tipo cardiovascular y la mayoría, de origen isquémico24, lo cual apunta a un tratamiento agresivo tanto en la fase aguda como para la prevención secundaria. En este estudio contemporáneo, solo se registró 1 caso validado (0,6%) de hemorragia mayor durante el ingreso inicial y hubo 3 hospitalizaciones posteriores debidas a hemorragia grave (1,9%)10. Estos notables resultados de seguridad pueden deberse también a una elevada (75%) tasa de uso del abordaje radial para intervencionismo coronario primario (ICP) y el poco empleo (el 20% de los pacientes tratados con ICP) de inhibidores de la glucoproteína IIb/IIIa.
Curvas de supervivencia de Kaplan-Meier de la variable de valoración principal (mortalidad por todas las causas, reinfarto, ictus invalidante y rehospitalización por causa cardiovascular o hemorragia) en pacientes con infarto agudo de miocardio sin elevación del segmento ST (elevación de troponina al ingreso) asignados aleatoriamente a una estrategia invasiva temprana o selectiva. Datos tomados de Savonitto et al10, reproducido con permiso de Savonitto7.
Por último, en un reciente análisis de metarregresión que incluyó todos los ECA que han comparado estrategias de tratamiento en el SCASEST, se ha confirmado que la estrategia invasiva temprana ordinaria reduce los episodios de la variable de valoración combinada de muerte e IM (para la interacción, p=0,044) y nuevas hospitalizaciones (para la interacción, p<0,0001), en mayor medida en los ancianos que en los pacientes de menos edad, sin diferencias significativas entre varones y mujeres25.
Shock cardiogénico y parada cardiaca extrahospitalariaA los pacientes ancianos con shock cardiogénico y los reanimados de una parada cardiaca presentada fuera del hospital, tradicionalmente se los ha considerado no candidatos a ICP en el contexto de un SCA. Un análisis de subgrupos del ensayo SHOCK mostró una tendencia no significativa al aumento de la mortalidad a 30 días (el 75 frente al 53%) tras tratar a un total de 56 pacientes ancianos con IM agudo y shock cardiogénico con revascularización de urgencia en comparación con la estabilización médica inicial26. Un reciente metanálisis de estudios no aleatorizados27 ha englobado a un total de 1.935 pacientes ≥ 75 años con IM y shock cardiogénico, 468 de ellos tratados con revascularización de urgencia y 1.467 con estabilización médica inicial. A pesar de una tasa de éxito de la revascularización en los pacientes ancianos menor que la de los más jóvenes (n=7 estudios; el 88 frente al 95%; p<0,0001), los pacientes tratados con revascularización de urgencia presentaron menos mortalidad a corto plazo (el 55 frente al 72%; OR=0,48; IC95%, 0,33-0,69) y a medio plazo (el 60 frente al 80%; OR=0,47; IC95%, 0,27-0,83). Sin embargo, este tipo de análisis no permite concluir que el mejor resultado clínico sea atribuible a la selección de los pacientes en vez de al efecto positivo de la revascularización de urgencia.
En el registro de ICPp de la región de Lombardía de Italia28, la edad avanzada no está entre los factores predictivos de la mortalidad intrahospitalaria de los pacientes tratados con ICPp de urgencia después de sufrir una parada cardiaca fuera del hospital: en dicho estudio, los factores predictivos independientes significativos fueron el tiempo transcurrido entre la parada y la llamada al servicio de urgencias médicas, la presencia de shock cardiogénico al ingreso, la asistolia como ritmo inicial y una puntuación de 3 en la escala de coma de Glasgow. Un reciente análisis de 6.972 pacientes de edad ≥ 65 (media, 75,8±7,0) años supervivientes a parada cardiaca fuera del hospital y dados de alta con vida29, de los que una cuarta parte había sufrido un IM agudo, puso de manifiesto que la supervivencia a largo plazo tenía una notable dependencia del déficit neurológico existente al alta y, en general, no difería de la mortalidad observada tras un episodio de insuficiencia cardiaca. Considerando conjuntamente toda esta información, parece razonable realizar una angiografía de urgencia con vistas a posible ICP a los pacientes ancianos reanimados de una parada cardiaca fuera del hospital, a menos que se haya reanimado al paciente a partir de una asistolia y siempre que al ingreso no presente shock cardiogénico o 3 puntos en la escala de coma de Glasgow.
Tratamiento antitrombóticoEl tratamiento antitrombótico es la piedra angular del tratamiento del SCA, tanto para los pacientes a los que se aplica una estrategia invasiva como en los tratados de manera conservadora. El uso de anticoagulantes y antiagregantes plaquetarios en los pacientes ancianos requiere un cuidadoso ajuste individualizado de la posología y una evaluación prudente del riesgo de hemorragia. Hay diversas variables fisiopatológicas y farmacológicas que influyen en el metabolismo y la distribución de los fármacos en los pacientes que es diferente entre los ancianos y los de menos edad30, y un comentario detallado de estas especificidades queda fuera del ámbito del presente artículo. Sin embargo, es preciso retener como mínimo los siguientes apuntes:
- •
El riesgo de hemorragia gastrointestinal con el ácido acetilsalicílico incluso a dosis bajas aumenta con la edad y con el antecedente de úlcera péptica31; en consecuencia, se recomienda administrar a estos pacientes un inhibidor de la bomba de protones32.
- •
Para los pacientes ancianos candidatos a tratamiento fibrinolítico, se recomienda usar la mitad de dosis de tenecteplasa, ajustada según el peso33, en combinación con enoxaparina en dosis de 0,75mg/kg y sin el bolo intravenoso inicial34, seguido de clopidogrel (75 mg) sin dosis de carga.
- •
Para los pacientes sometidos a ICPp, parece razonable utilizar bivalirudina en vez de heparina no fraccionada y un inhibidor de la glucoproteína IIb/IIIa, dado que el riesgo de hemorragia es muy inferior4.
- •
En la fase aguda del SCASEST, fondaparinux (2,5mg una vez al día) debe ser el anticoagulante de elección para los pacientes tratados de manera conservadora35, mientras que las dosis de enoxaparina deben determinarse meticulosamente en función de la TFGe. El uso de bivalirudina durante la intervención se ha asciado a una reducción de las hemorragias en los ancianos y menor mortalidad a 1 año36.
- •
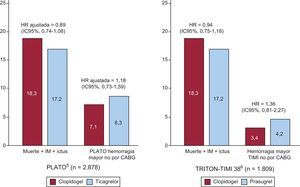
Clopidogrel continúa siendo el antagonista de los receptores de adenosindifosfato de elección para la mayoría de los pacientes ancianos. En comparación con clopidogrel, los dos inhibidores más potentes, prasugrel y ticagrelor, presentaron unos resultados notablemente similares, con una leve reducción de la variable de valoración isquémica a costa de un aumento del riesgo de hemorragia mayor (figura 6)5,6. En consecuencia, cuando está indicado un antagonista de los receptores de adenosindifosfato como adyuvante del ácido acetilsalicílico, el empleo de estos nuevos fármacos debería restringirse a pacientes con alergia a clopidogrel o tras una evaluación individualizada y cuidadosa de la relación beneficio-riesgo. El ensayo Elderly ACS-2 (NCT01777503) está comparando específicamente el prasugrel en dosis reducidas (5mg una vez al día) con clopidogrel en 2.000 pacientes ≥ 75 años, con SCA y sometidos a ICP precoz.
Figura 6.Tasas de muerte cardiovascular, reinfarto de miocardio no mortal, ictus no mortal y hemorragia mayor durante el periodo de seguimiento de pacientes de edad ≥ 75 años incluidos en los ensayos PLATO5 y TRITON-TIMI 386. Obsérvese que: a) la duración media del seguimiento fue de 9,2 meses en el ensayo PLATO, en comparación con 14,5 meses en el TRITON-TIMI 38, y b) las definiciones de hemorragia fueron diferentes. La comparación de las tasas de riesgo de los tratamientos se expresa en forma de hazard ratio en el TRITON y hazard ratio ajustada en el PLATO. CABG: cirugía de revascularización aortocoronaria; HR: hazard ratio; IC95%: intervalo de confianza del 95%; IM: infarto de miocardio; TIMI: Thrombolysis In Myocardial Infarction. Reproducido con permiso de Savonitto7.
(0.16MB).
Según la encuesta Euro Heart Survey, el 21% de los pacientes con IAMCEST y el 27% de los que tuvieron un SCASEST tenían DM conocida o de nuevo diagnóstico al ingreso37. En comparación con los pacientes sin DM, los que presentan este trastorno tienen peores resultados durante la hospitalización y a largo plazo38, sin que ello se explique por completo por las comorbilidades asociadas a la DM, que continúa siendo un predictor potente de peor evolución clínica tras la introducción de un ajuste respecto a los factores de confusión de mayor relevancia. Una excepción a esta regla pueden ser los ancianos, pues el exceso de mortalidad observado entre los ancianos diabéticos es atribuible en su mayor parte a la ERC preexistente y al daño miocárdico39. Los pacientes con DM no se han visto beneficiados por la reciente reducción de la mortalidad observada en los pacientes sin DM40. Esto podría reflejar la existencia de una mayor carga de factores de riesgo, pero también el uso de un tratamiento menos agresivo41. Los datos obtenidos de registros han mostrado de manera uniforme que los pacientes con SCA y DM reciben un tratamiento subóptimo, en comparación con los pacientes no diabéticos, tanto en las revascularizaciones como en la pauta de medicación antiagregante plaquetaria42,43. Esta última cuestión puede ser de especial importancia, teniendo en cuenta las aberraciones específicas de la función plaquetaria que dan lugar a un aumento de la reactividad plaquetaria durante el tratamiento43.
Una cuestión relacionada con el metabolismo de la glucemia en el SCA es el papel pronóstico de la hiperglucemia, cuya prevalencia oscila entre el 25 y el 50% de los pacientes ingresados por un SCA44. La glucemia al ingreso mantuvo un efecto potente e independiente en la mortalidad hasta 1 año después del IM y más45. La intensidad de la asociación entre la hiperglucemia al ingreso y el riesgo de mortalidad después de un IM agudo se mantiene con independencia del estado diabético46 y puede reducir el efecto de la DM en la mortalidad cuando se ajusta por los valores de glucemia al ingreso42. La hiperglucemia al ingreso puede ser tanto un marcador de respuesta de estrés aguda (p. ej., en pacientes con inestabilidad hemodinámica) como un indicador de resistencia subyacente a la insulina44. Un estudio prospectivo de Suecia y otros varios informes han señalado que la mayoría de esos pacientes pueden, de hecho, tener una DM no diagnosticada47–49. Esto puede explicar que la determinación de glucemia en ayunas durante las primeras 24h de hospitalización y otros parámetros de glucometría a más largo plazo hayan mejorado la capacidad de predecir la mortalidad a 30 días50. En consecuencia, las guías actuales proponen que la determinación de la glucemia debe formar parte de los análisis de laboratorio iniciales de todos los pacientes con un SCA confirmado o sospechado, y debe ser objeto de supervisión frecuente en los pacientes con DM conocida o hiperglucemia al ingreso51,52. Además, las guías antes mencionadas incluyen el siguiente conjunto de recomendaciones:
- •
Es preciso evitar tanto la hiperglucemia excesiva (> 180-200mg/dl) como la hipoglucemia (< 90mg/dl). A pesar del creciente conjunto de conocimientos acerca de la capacidad de discriminación que tiene la elevación de la glucosa respecto a la predicción de la mortalidad en los pacientes con SCA, y de algunas evidencias que indican que se obtiene un mejor resultado clínico con un control estricto de la glucosa en otras poblaciones de pacientes en estado crítico53, los estudios realizados en las unidades de cuidados intensivos médicas y quirúrgicas han atenuado el entusiasmo inicial por el control estricto de la glucemia54–56. De hecho, el riesgo asociado a la glucemia al ingreso presenta una curva en U, con aumento de la tasa de eventos asociados tanto a la hiperglucemia como a la hipoglucemia57.
- •
Se recomienda una estrategia invasiva temprana para los pacientes diabéticos con SCASEST. El enfoque óptimo para la revascularización coronaria debe basarse en una evaluación multidisciplinaria (heart team), y a la hora de optar entre cirugía de revascularización aortocoronaria o ICP, se debe tener en cuenta la complejidad de la enfermedad coronaria antes que el estado de la DM. De hecho, los datos procedentes de los registros y los ECA indican que la cirugía de revascularización aortocoronaria permite una mejor supervivencia a largo plazo de los pacientes diabéticos con enfermedad multivaso58.
- •
Si se considera factible y apropiada la estrategia basada en ICP, se debe preferir los stents liberadores de fármacos a los metálicos sin recubrimiento. Los registros prospectivos grandes han confirmado el efecto beneficioso de los stents liberadores de fármacos en la DM, con una reducción ajustada del riesgo absoluto a 3 años del 3% de mortalidad por todas las causas e IM, en comparación con los stents metálicos sin recubrimiento59. La comparación directa de diferentes stents liberadores de fármacos no aportó evidencias concluyentes de la superioridad de un tipo sobre otro60.
- •
El tratamiento antitrombótico está indicado igual que para los pacientes no diabéticos, teniendo en cuenta la ya mencionada hiperreactividad plaquetaria de los pacientes diabéticos43. Se ha descrito resistencia a ácido acetilsalicílico en la DM y en la hiperglucemia, y se ha observado un aumento del recambio plaquetario en la DM de manera asociada a un aumento de la síntesis de tromboxano A260. Los datos preliminares indican que una pauta de tratamiento con ácido acetilsalicílico 2 veces al día puede mejorar la inhibición plaquetaria en la DM, pero esos datos requerirán una evaluación más detallada en estudios clínicos60. Los intentos de mejorar los resultados clínicos aumentando la dosis diaria de clopidogrel no han dado resultado61. En cambio, los antagonistas de los receptores de adenosindifosfato de tercera generación prasugrel y ticagrelor aportan efectos antiagregantes plaquetarios más potentes y predecibles. En un análisis de subgrupo definido a priori de la cohorte de pacientes con DM, la reducción de la variable de valoración isquémica principal coincidió con los resultados generales obtenidos con ticagrelor62 y fue aún más profunda con prasugrel63, sin que hubiera un aumento de las hemorragias en comparación con clopidogrel.
- •
A los pacientes con SCA e hiperglucemia pero sin antecedentes de DM, se los debe evaluar en más detalle para determinar la gravedad de sus alteraciones metabólicas. Esta evaluación puede incluir determinaciones de glucosa en ayunas y glucohemoglobina y una prueba de sobrecarga oral de glucosa posterior al alta52.
La tasa de filtrado glomerular (TFG) se reduce progresivamente con la edad, a un ritmo aproximado de 8ml/min/1,73 m2 cada década, y un alto porcentaje de los ancianos tienen una TFG < 60 ml/min/1,73 m2. A partir de los 30 años se inicia un proceso de sustitución de los glomérulos por tejido fibroso, denominado glomerulosclerosis, que afecta a un número creciente de glomérulos a medida que avanza la edad64. El envejecimiento se acompaña también de una disminución de la producción de creatinina (sarcopenia senil) y, en consecuencia, la concentración sérica de creatinina no aumenta de manera proporcional a la disminución progresiva de la TFG. Así, una creatinina sérica de 1mg/dl corresponde a una TFG de 120ml/min a la edad de 20 años, pero de solo 60ml/min en un sujeto de 80 años. Dada la complejidad que representa la determinación directa de la TFG mediante la infusión de sustancias exógenas, se han propuesto fórmulas para estimar la FG a partir de las concentraciones séricas de marcadores endógenos que los glomérulos filtran. Las ecuaciones basadas en la creatinina, como las fórmulas Modification of Diet in Renal Disease y CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration) incluyen la edad y el sexo como variables, mientras que solo la fórmula de Cockcroft-Gault tiene en cuenta también el peso corporal. Todas esas ecuaciones subestiman la TFG determinada directamente en un 20–25%, y la razón más probable es que esas ecuaciones se desarrollaron en pacientes con una disminución de la masa muscular, en comparación con adultos sanos65. En consecuencia, los pacientes de más edad con con TFGe de 45–59ml/min/1,73 m2 tienen menor probabilidad que los pacientes más jóvenes de progresión a enfermedad renal terminal, y cuando esta progresión se produce es más lenta que en los pacientes de menos edad66. Además, los pacientes ancianos tienen un riesgo de muerte ajustado por edad menor que el de los más jóvenes con TFGe similar.
Aunque la ERC es un factor de riesgo bien conocido en el SCASEST67, su papel en la determinación del pronóstico de los pacientes ancianos con SCASEST no se ha determinado por el momento. En el estudio Italian Elderly ACS, alrededor del 60% de los pacientes tenían TFGe<60ml/min/1,73 m2 al utilizar las fórmulas CKD-EPI o Modification of Diet in Renal Disease, en comparación con el 80% al aplicar la ecuación de Cockcroft-Gault68. Al analizarlo como una variable continua, la TFGe fue uno de los factores independientes predictivos de la mortalidad24, y a este respecto la fórmula de Cockroft-Gault fue significativamente mejor que las otras dos ecuaciones68.
Las manifestaciones clínicas del SCA con frecuencia son atípicas en los pacientes con ERC, y la dificultad diagnóstica puede verse incrementada por el hecho de que las concentraciones séricas de troponinas a menudo estén elevadas en los ancianos con ERC.
Los pacientes con ERC son más propensos a presentar complicaciones hemorrágicas que los pacientes con función renal preservada. Se han descrito defectos de la adhesión y la agregación de las plaquetas que conducen a la tendencia hemorrágica de los pacientes con ERC69. En consecuencia, estos pacientes deben ser tratados con precaución al utilizar fármacos antitrombóticos que se eliminan exclusiva o sustancialmente a través de los riñones, como los inhibidores de la glucoproteína IIb/IIIa de molécula pequeña y enoxaparina, y es preciso aplicar un ajuste de reducción de dosis de estos fármacos en función de la TFGe. Los errores de dosis en los pacientes con ERC, principalmente por lo que respecta a la prescripción, son la causa de una parte sustancial de las reacciones adversas a medicamentos que se producen en los pacientes con SCA. En la ERC grave, enoxaparina y fondaparinux están contraindicados: en esos pacientes debe usarse heparina no fraccionada, la cual tiene, además, la ventaja de que su actividad anticoagulante puede supervisarse fácilmente mediante el tiempo de tromboplastina parcial activado y que se puede neutralizarla rápidamente en caso de hemorragia. La dosis de bivalirudina debe reducirse también en los pacientes con ERC grave.
De entre los antagonistas del receptor P2Y12, ticagrelor ha mostrado unos resultados notablemente favorables en comparación con clopidogrel en el ensayo PLATO, con una reducción significativa de las variables de valoración isquémicas y de la mortalidad entre los pacientes con ERC70. Aunque las hemorragias mayores y mortales no aumentaron de manera significativa con ticagrelor, fueron numéricamente superiores entre los pacientes asignados a ticagrelor en comparación con lo observado en los pacientes asignados a clopidogrel, en especial los pacientes con ERC grave (el 23,6 frente al 14,1%).
A la gran mayoría de los ancianos con ERC, no se los trata con técnicas invasivas, ya que muchos médicos son reacios a utilizar la angiografía coronaria en este contexto, debido al riesgo de mayor deterioro en la TFG. Esta infrautilización lleva a infradiagnóstico de la enfermedad coronaria significativa y a menores tasas de revascularizaciones posteriores. Además, no se puede evaluar adecuadamente los posibles efectos beneficiosos de una estrategia invasiva, ya que se ha incluido solo a unos pocos pacientes con ERC grave en los ECA que comparan estrategia invasiva frente a conservadora. Los pocos datos existentes proceden de los registros publicados: entre ellos, el registro SWEDEHEART aportó datos sobre 5.689 pacientes con infarto agudo de miocardio sin elevación del segmento ST y ERC en estadio>371. Los pacientes con valores de TFGe inferiores tuvieron menor probabilidad de que se les practicara angiografía coronaria y revascularización en los 14 días siguientes al ingreso. En los pacientes sometidos a angiografía coronaria, la menor función renal se asoció a mayor gravedad de la enfermedad coronaria. La mortalidad a 1 año ajustada fue un 36% inferior con una estrategia invasiva, si bien la diferencia de mortalidad observada con el tratamiento invasivo se reducía con la disminución de la función renal, sin que hubiera diferencias de mortalidad en los pacientes con TFGe<15ml/min/1,73 m2. Sin embargo, debe observarse que se excluyó del análisis a los pacientes > 80 años. El «nihilismo terapéutico» adoptado con los pacientes con ERC se extiende también a las medidas de prevención secundaria, como las recomendaciones de dejar de fumar, reducción del peso, ejercicio y rehabilitación cardiaca. Además, fármacos como las estatinas, los bloqueadores beta y los antiagregantes plaquetarios se prescriben al alta a los pacientes con ERC con menos frecuencia que a los pacientes sin ERC72.
ANEMIALa anemia, definida según los criterios de la Organización Mundial de la Salud (hemoglobina<13g/dl en los varones o<12g/dl en las mujeres)73, se observó en un 15–20% de los pacientes con SCA74. La guía de 2011 de la European Society of Cardiology para el tratamiento del SCASEST identifica la anemia como un importante factor de riesgo de complicaciones tanto isquémicas como hemorrágicas51. La actualización de 2012 de la guía de la European Society of Cardiology para el IAMCEST menciona la anemia como factor de riesgo de un peor resultado clínico, y ello indica que el tratamiento antiagregante plaquetario combinado doble debe usarse con precaución75. Los autores proponen que se determine con exactitud la hemoglobina para la estratificación del riesgo y que se preste atención al tratamiento antitrombótico, el tipo de stent y la vía de acceso vascular (con preferencia por el abordaje radial); también proponen emplear un umbral restrictivo para las transfusiones, reservando los productos hemoderivados para la inestabilidad hemodinámica o pacientes con hematocrito<25% o hemoglobina<7g/dl. Sin embargo, señalan que el tratamiento de este tipo de pacientes se basa en datos empíricos.
La evidencia aportada por la literatura médica reciente añade los siguientes resultados y propuestas:
- •
La revisión sistemática de los análisis ajustados señala a un aumento del riesgo de muerte por todas las causas en los pacientes anémicos (HR ajustada a 1 año=1,63; IC95%, 1,10-2,40), con efecto dependiente de la dosis76.
- •
La anemia puede afectar a los resultados clínicos como consecuencia de que se combinen la disminución del aporte de oxígeno al miocardio en las zonas distales a las estenosis coronarias y el aumento de la demanda miocárdica de oxígeno, y esto constituye la primera causa de IM de tipo II, definido por un desequilibrio en el aporte de oxígeno77.
- •
La anemia, tanto basal como producida durante la hospitalización, aporta una información independiente pronóstica del riesgo de hemorragia y predictiva de la mortalidad o la recurrencia de IM, que se añade a la de los instrumentos pronósticos isquémicos tradicionales. La adición de la anemia al ingreso a las puntuaciones tradicionales del riesgo isquémico puede llevar a que casi un 50% de los pacientes con SCA sean reclasificados a una categoría de riesgo inferior78.
- •
La anemia es muy frecuente en los pacientes ancianos con enfermedades cardiovasculares agudas, hasta un 43% de este grupo de pacientes79. En este contexto, la anemia se asocia a mayor prevalencia de comorbilidades como DM tipo 2 ERC, insuficiencia cardiaca crónica y enfermedad cerebrovascular. Sin embargo, su valor pronóstico independiente continúa siendo válido aun después de introducir un ajuste por edad, sexo, las covariables de mayor relevancia clínica y el estado de fragilidad24,80.
- •
Las intervenciones destinadas a corregir la anemia, como la transfusión de concentrados de hematíes, pueden asociarse a una peor evolución clínica. De hecho, en el contexto del IM, el empleo liberal de transfusiones de sangre se ha asociado a un aumento del riesgo absoluto ponderado de un 12%, con un número de pacientes que es necesario tratar de 8 (IC95%, 6-17)81. Sin embargo, la mayor parte de la literatura médica centrada en las estrategias de transfusión consiste en ECA de tipo piloto o estudios observacionales y puede verse afectada por un perfil de mayor riesgo de los pacientes anémicos que sea un factor de confusión82.
- •
El empleo de hierro carboximaltosa por vía intravenosa es útil para aliviar los síntomas de los pacientes con insuficiencia cardiaca y ferropenia, mejora la tolerancia al ejercicio y la calidad de vida y reduce los eventos cardiovasculares. Sin embargo, las consecuencias para la salud a largo plazo no están claras y serán necesarios nuevos estudios al respecto83.
- •
Los agentes estimuladores de la eritropoyesis no parecen garantizar un efecto beneficioso en cuanto a la mortalidad, los eventos cardiovasculares y las hospitalizaciones de los pacientes con anemia de leve a moderada y cardiopatía, y pueden asociarse a efectos nocivos graves. En un ECA grande se estudió a 2.278 pacientes con insuficiencia cardiaca sistólica y hemoglobina en 9–12g/dl a asignados a tratamiento con darbepoetina con ajuste de dosis para alcanzar un objetivo de hemoglobina de 13g/dl o placebo; no hubo diferencias en cuanto a los resultados de salud ni en los episodios tromboembólicos en el grupo de intervención tras una mediana de 28 meses de seguimiento84. Sin embargo, no se han realizado ensayos que hayan evaluado en pacientes con cardiopatías los efectos de un objetivo de hemoglobina más moderado (10–12g/dl) en comparación con un objetivo inferior.
Así pues, los pacientes con SCA y anemia presentan un aumento de la prevalencia de múltiples comorbilidades, un perfil de riesgo cardiovascular elevado y un peor resultado clínico general. La compleja condición de esta cohorte supone un verdadero reto para la toma de decisiones terapéuticas; son necesarias guías específicas con recomendaciones de tratamiento médico y estrategias invasivas adaptadas a las diversas situaciones clínicas. Los clínicos deben reducir al mínimo el riesgo hemorrágico empleando los modelos de riesgo existentes y deben ajustar el tipo y la dosis de fármacos antitrombóticos. Debe usarse el acceso radial para el cateterismo cardiaco y el ICP siempre que sea posible. Hay que hacer todo lo posible, empezando ya en la fase aguda, por identificar la causa de la anemia, ya que la detección de una pérdida hemática gastrointestinal tiene importantes repercusiones para el tratamiento antitrombótico posterior.
CONCLUSIONESEn los últimos años, a pesar de la escasez de ECA específicos, se han realizado avances importantes en el tratamiento de los pacientes ancianos y los pacientes con comorbilidades: se ha pasado del nihilismo terapéutico a un ajuste cuidadoso de las dosis de fármacos antitrombóticos, a una tendencia al abordaje radial de las intervenciones coronarias percutáneas y también a una cirugía cardiaca menos invasiva. Son de prever nuevos avances como consecuencia del desarrollo de pautas de medicación apropiadas para ancianos y pacientes con disfunción renal, así como del abordaje sistemáticamente multidisciplinario para el tratamiento de pacientes con DM y anemia, y de la decisión de realizar ensayos aleatorizados en estas poblaciones de alto riesgo.
CONFLICTO DE INTERESESNinguno.
Sección patrocinada por AstraZeneca