Sra. Editora:
El síndrome de la vena cava superior (VCS) es una afección que comprende los síntomas derivados de la disminución u obstrucción del flujo sanguíneo a través de la VCS.
En función de la gravedad de los síntomas y la etiología, el tratamiento puede comprender cirugía, en ocasiones con construcción de un puente venovenoso. Como alternativa a la cirugía convencional, se ha desarrollado la angioplastia simple o con stent.
Desde enero de 1993 hasta diciembre de 2011, en nuestro centro 5 pacientes presentaron este síndrome y todos ellos fueron tratados percutáneamente sin complicaciones: 1 con angioplastia simple1, 1 con stent convencional y 3 con stent recubierto de politetrafluoroetileno. En la Tabla se resumen sus principales características y el tratamiento realizado.
Características clínicas basales y datos angiográficos de los pacientes
| Paciente 1 | Paciente 2 | Paciente 3 | Paciente 4 | Paciente 5 | |
| Sexo | Varón | Varón | Varón | Varón | Mujer |
| Edad | 12 | 47 | 68 | 74 | 10 |
| Clínica | Congestión yugular y circulación torácica superficial severa | BAV; edema en esclavina y circulación venosa colateral | BAV; congestión facial y circulación venosa colateral | Brugada; imposibilidad de implantación de nuevo electrodo | Edema en esclavina y circulación venosa colateral |
| Obstrucción | Subtotal | Total larga (3 cm) | Total corta (2 cm) | Subtotal | Subtotal |
| Gradiente VCS/AD | 17 | 7 | 11 | 3 | 7 |
| Etiología | DVPPA | DVPPA; electrodo de MP | Electrodo de MP | Electrodo de DAI | DVPPA |
| Tiempo desde intervención hasta tratamiento percutáneo | 6 meses | Desde cirugía 6 años y desde MP 4 meses | 9 años y 1 mes | 6 años y 10 meses | 8 años |
| Tipo de cirugía/MP | Apertura de tabique interauricular y tunelización con parche | Ampliación de VCS con parche y drenaje de venas anómalas a través de una CIA; MP DDD | MP VDD | DAI | Ampliación de VCS con parche y apertura de tabique interauricular y tunelización con parche |
| Balón | Match® 7 × 40 | Balt® 20 × 50 | BiB® 18 × 50/9 × 40 | Maxi® LD 14 × 30 | Optapro® 12 × 30 |
| Stent | No | Covered Stent™ Numed 8Z 45 mm | Covered Stent™ Numed 8Z 35 mm | Covered Stent™ Numed 8Z 45 mm | Palmaz® XD 29 |
| Balón de posdilatación | Monofoil 15 × 40 | Mullins 18 × 30 | No | Mullins 16 × 30 y 18 × 30 | No |
AD: aurícula derecha; BAV: bloqueo auriculoventricular; CIA: comunicación interauricular; DAI: desfibrilador automático implantable; DVPPA: drenaje venoso pulmonar parcial anómalo; MP: marcapasos; VCS: vena cava superior.
En cuanto a la técnica empleada, en los casos con paso anterógrado se procedió vía yugular con catéteres multipropósito de 5 o 6 Fr (Cordis), por el cual se introdujo una guía recta de 0,035” de 260 cm (Boston), que a su vez se capturó en aurícula derecha (AD) mediante catéter lazo Goose Neck® (ev3) de 15 mm, y se estableció un circuito venovenoso para luego proseguir por vía femoral.
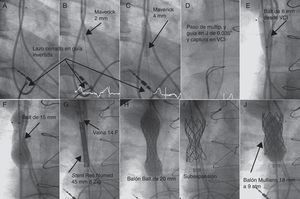
En los 2 casos con obstrucción completa, por vía femoral posicionamos un catéter lazo Goose Neck® de 15 mm en la base de AD y, a través del catéter multipropósito, avanzamos una guía coronaria PT Graphix® de 0,014” (Boston) invertida. La guía se progresa, con control angiográfico en dos proyecciones, paralela al electrodo del marcapasos. Una vez atravesada la obstrucción, fijamos el extremo rígido de la guía con el lazo y lo descendemos a AD (Figura). Seguidamente se dilata con balones coronarios Maverick® (Boston) de 2, 3 y 4 mm (Figura) para después avanzar el multipropósito por el túnel creado y sustituir la guía coronaria por una guía de 0,035” que se extrae por vena femoral estableciendo el «raíl yugulofemoral» (Figura).
Figura. Imágenes angiográficas del procedimiento de desobstrucción de vena cava superior del paciente. VCI: vena cava inferior.
En el caso de la angioplastia simple, utilizamos balones de 7 y 15 mm Balt™ introducidos vía femoral. En los procedimientos con stent, accedimos también por vía femoral y en todos ellos predilatamos con balones de 8 a 15 mm (Figura) para introducir la vaina de Mullins (Cook) de 9 a 14 Fr hasta la VCS (Figura). Se utilizaron tres stents recubiertos de politetrafluoroetileno de 45 mm y 8 Zig® (Numed) y un stent Palmaz® XD 29 (Cordis), que se montaron en diferentes balones propios con relación balón/VCS = 1 (Figura; Tabla). En dos casos, el stent infraexpandido se redilató a alta presión (9 atm) con balón de Mullins (Figura).
En todos los casos se desobstruyó completamente, y a las 24 h se dio el alta hospitalaria a todos los pacientes, con tratamiento antiagregante en los casos 1, 2, 4 y 5 y anticoagulante en el caso 3.
Todos los pacientes han permanecido asintomáticos desde el procedimiento, con un seguimiento medio de 46,6 (9-120) meses; al año se confirmó la permeabilidad del stent recubierto mediante resonancia magnética en el caso 1 y tomografía computarizada torácica en los casos 2 y 3. Los marcapasos de los pacientes 2 y 3 se comprobaron en la unidad de arritmias, que confirmó su buen funcionamiento.
La experiencia existente en el tratamiento de la obstrucción de VCS es escasa, con resultado hemodinámico inicial del 100% en los pacientes tratados con stent y del 78% en los tratados con angioplastia con balón, sin diferencias a largo plazo entre ambas opciones percutáneas2.
En los pacientes que además son portadores de un electrodo de estimulación cardiaca, se plantean tres estrategias: angioplastia simple con balón, con el riesgo de reestenosis por recoil; otra opción es la retirada inicial del cable seguida de la desobstrucción mediante implantación de stent recubierto o no y colocación de un nuevo marcapasos3, 4. De este modo disminuimos el riesgo de reestenosis y de daño del electrodo, pero obliga a implantar un nuevo marcapasos.
Una última medida consiste en implantar un stent sin retirar el cable, que queda atrapado entre la pared venosa y el stent5. Con esta estrategia existe el riesgo de disfunción inmediata del marcapasos debido a la plataforma metálica, aunque ya hay experiencia al respecto que muestra la normofunción de los marcapasos inmediatamente después del procedimiento. Sin embargo, aún se desconocen los posibles efectos a largo plazo producidos porque el electrodo interfiere reiteradamente contra el extremo del stent, ya que el propio movimiento cardiaco podría generar un punto de fatiga porque el cable queda fijado por el stent, además de la dificultad para la extracción en caso de infección/trombosis del cable6. Esta última estrategia puede ser de interés en pacientes en los que la retirada del electrodo sea imposible o muy dificultosa y/o en pacientes muy ancianos o con expectativa de vida corta.
Nuestro grupo propone el empleo de stents recubiertos con el fin de evitar el posible deterioro agudo y crónico del electrodo, dado que el propio recubrimiento podría amortiguar la compresión del cable hasta que se generase la neoendotelización.
Autor para correspondencia: koldobika.garciasanroman@osakidetza.net