La septostomía auricular (SA) electiva en adultos con hipertensión arterial pulmonar (HAP) grave y triple tratamiento específico (antagonistas de los receptores de la endotelina, inhibidores de la fosfodiesterasa 5 y prostanoides) puede proporcionar un beneficio clínico adicional como puente al trasplante pulmonar cuando fracasa el tratamiento médico o como tratamiento de destino si el trasplante pulmonar no es factible. Está indicada, según las guías de práctica clínica1, en pacientes con HAP en clase funcional III-IV con insuficiencia cardiaca derecha refractaria o con síncopes de esfuerzo, bien como puente al trasplante pulmonar o cuando otras opciones terapéuticas no están disponibles. Sin embargo, la realidad es que ha sido poco practicada en nuestro medio.
Presentamos la experiencia con esta técnica en pacientes adultos con HAP bajo tratamiento específico en una unidad de referencia. Esta es, en nuestro conocimiento, la serie más larga en España que describe los resultados con esta técnica en el contexto del tratamiento contemporáneo de la HAP.
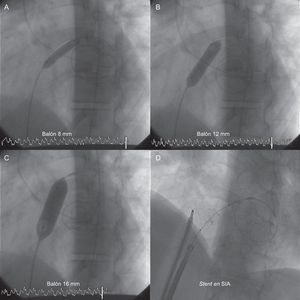
Desde 2005 hemos realizado 11 procedimientos de SA y una fenestración del tabique interauricular con stent en 10 pacientes (ocho mujeres, edad media 43,5 años). La tabla recoge los datos de los pacientes y los procedimientos. Todos estaban en clase funcional III-IV y todos recibían epoprostenol, siete de ellos en triple tratamiento específico con antagonistas de los receptores de la endotelina e inhibidores de la fosfodiesterasa 5, y tres en doble tratamiento con inhibidores de la fosfodiesterasa 5. Se trataron con inotrópicos, diuréticos intravenosos y transfusiones para alcanzar las condiciones idóneas para realizar la SA. No se realizó SA como procedimiento de rescate en situación terminal. Se realizó con punción transeptal con aguja de Brockenbrough y según el protocolo de dilatación gradual con balón descrito por Sandoval et al2, sin sedación, para valorar adecuadamente los cambios en la saturación arterial periférica de oxígeno. Según la técnica de Sandoval et al2, tras realizar la punción transeptal se procedió a una dilatación gradual del orificio, comenzando con un diámetro de 4mm y siguiendo con dilataciones con balones de 8, 12 y 16mm. Entre cada paso y el siguiente se esperó 3 minutos, y tras este tiempo se determinaron la presión telediastólica del ventrículo izquierdo y la saturación arterial de oxígeno. El tamaño final del defecto se individualizó en cada paciente, en función de que ocurriera alguna de las siguientes situaciones: elevación de la presión telediastólica del ventrículo izquierdo > 18mmHg, reducción de la saturación arterial periférica de oxígeno < 80% o reducción de esta > 10% respecto a la basal, o bien que se alcanzara el tamaño máximo de dilatación del tabique (16mm). En dos pacientes se utilizó ecografía intracardiaca, y el resto de los procedimientos se guiaron solo por fluoroscopia. La fenestración del tabique interauricular con stent se realizó según la técnica de stent en diábolo descrita por Stümper et al3, sin sedación, monitorizada por fluoroscopia y ecografía intracardiaca. Después de realizar la punción transeptal con aguja de Brockenbrough se avanzó la guía de Inoue a la aurícula izquierda y se procedió a dilatar el tabique interauricular con el dilatador y la vaina de Mullins. Posteriormente se cambió por una vaina de 12 Fr manteniendo la guía de Inoue en la aurícula izquierda. Se montó un stent Palmaz® GenesisTM (Johnson & Johnson) de 19mm sobre un balón de 16×40mm, al cual se le hizo un lazo central de 5mm de diámetro con una derivación de marcapasos epicárdico. Se procedió a avanzar todo el sistema a través de la vaina sobre la guía de Inoue, y guiado por escopia y por ecografía intracardiaca se procedió a colocar el stent centrado en el tabique interauricular y a inflar el balón. Así queda liberado el stent con forma de diábolo centrado en el tabique interauricular, al tener un lazo rodeando el balón que limita la expansión central de este. El diámetro de la fenestración será el predeterminado por el diámetro del lazo que rodea el balón. Tras la SA se resolvió la insuficiencia cardiaca derecha refractaria y desaparecieron los síncopes de esfuerzo en todos los pacientes. El primer paciente presentó bloqueo auriculoventricular completo. No hubo otras complicaciones asociadas a la técnica. El seguimiento medio fue de 24 meses (rango: 1-67) y durante este tiempo se produjo, en tres pacientes (33%), un cierre espontáneo de la SA; la saturación arterial periférica de oxígeno contraindicó nueva SA en un caso, en otro realizamos una fenestración del tabique interauricular con stent (figura) y en el tercero realizamos una nueva SA a los 18 meses. La supervivencia fue del 90% a 30 días, del 75% a 6 meses y del 57% al año. Un paciente falleció 1 semana después de la SA durante la inducción anestésica para la implantación de un catéter de Hickman, tres fallecieron por progresión de la enfermedad, tres recibieron un trasplante con éxito y los tres restantes siguen vivos (dos en lista de trasplante y la paciente con fenestración del tabique interauricular con stent sin reoclusión ni migración del dispositivo 44 meses después).
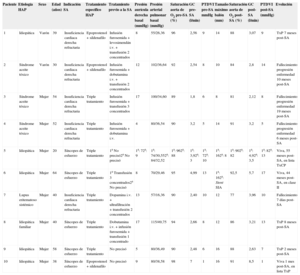
Datos de los pacientes y procedimientos de septostomía auricular
| Paciente | Etiología HAP | Sexo | Edad (años) | Indicación SA | Tratamiento específico HAP | Tratamiento previo a la SA | Presión aurícula derecha basal (mmHg) | Presión arterial pulmonar basal (mmHg) | Saturación aorta de O2 pre-SA (%) | GC pre-SA (l/min) | PTDVI pre-SA mmHg | Tamaño máximo balón (mm) | Saturación aorta de O2 post-SA (%) | GC post-SA (l/min) | PTDVI post-SA (mmHg) | Evolución |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | Idiopática | Varón | 39 | Insuficiencia cardiaca derecha refractaria | Epoprostenol + sildenafilo | Infusión furosemida + levosimendán i.v. + transfusión 2 concentrados | 8 | 55/26,36 | 96 | 2,56 | 9 | 14 | 88 | 3,07 | 9 | TxP 7 meses post-SA |
| 2 | Síndrome aceite tóxico | Varón | 30 | Insuficiencia cardiaca derecha refractaria | Epoprostenol + sildenafilo | Infusión furosemida + dobutamina i.v. + transfusión 2 concentrados | 12 | 102/36,64 | 92 | 2,54 | 8 | 10 | 84 | 2,8 | 14 | Fallecimiento progresión enfermedad 10 meses post-SA |
| 3 | Síndrome aceite tóxico | Mujer | 54 | Insuficiencia cardiaca derecha refractaria | Triple tratamiento | Infusión furosemida + transfusión 3 concentrados | 17 | 100/34,60 | 89 | 1,8 | 6 | 8 | 81 | 2,12 | 8 | Fallecimiento progresión enfermedad 19 meses post-SA |
| 4 | Síndrome aceite tóxico | Mujer | 52 | Insuficiencia cardiaca derecha refractaria | Triple tratamiento | Infusión furosemida + dobutamina i.v. | 4 | 80/36,54 | 90 | 3,2 | 5 | 14 | 91 | 3,2 | 5 | Fallecimiento progresión enfermedad 6 meses post-SA |
| 5 | Idiopática | Mujer | 20 | Síncopes de esfuerzo | Triple tratamiento | 1a No precisó2a No precisó | 1a: 72a: 9 | 1a: 74/30,552a: 84/32,52 | 1a: 962a: 88 | 1a: 3,92a: 3 | 1a: 72a: 10 | 1a: 162a: 8 | 1a: 902a: 82 | 1a: 4,92a: 3,5 | 1a: 82a: 13 | Viva, 55 meses post-SA, en lista TxCP |
| 6 | Idiopática | Mujer | 64 | Síncopes de esfuerzo | Triple tratamiento | 1a Transfusión 3 concentrados2a No precisó | 8 | 70/29,46 | 95 | 4,99 | 13 | 1a: 162a: Stent SIA | 92,5 | 5,7 | 17 | Viva, 44 meses post-SA, en clase II |
| 7 | Lupus eritematoso sistémico | Mujer | 40 | Insuficiencia cardiaca derecha refractaria | Triple tratamiento | Dopamina i.v. + ultrafiltración + transfusión 2 concentrados | 13 | 57/16,36 | 90 | 2,40 | 10 | 12 | 77 | 3,96 | 10 | Fallecimiento 7 días post-SA |
| 8 | Idiopática familiar | Mujer | 40 | Síncopes de esfuerzo | Triple tratamiento | Dobutamina i.v. + infusión furosemida + transfusión 1 concentrado | 17 | 115/49,75 | 94 | 2,66 | 8 | 12 | 86 | 3,21 | 13 | TxP 8 meses post-SA |
| 9 | Idiopática | Mujer | 58 | Síncopes de esfuerzo | Triple tratamiento | No precisó | 5 | 80/36,49 | 90 | 2,48 | 6 | 16 | 88 | 2,63 | 7 | TxP 2 meses post-SA |
| 10 | Idiopática | Mujer | 38 | Síncopes de esfuerzo | Epoprostenol + sildenafilo | No precisó | 9 | 80/38,58 | 98 | 7 | 1 | 16 | 91 | 8,5 | 1 | Viva 1 mes post-SA, en lista TxP |
GC: gasto cardiaco; HAP: hipertensión arterial pulmonar; i.v: intravenoso; PTDVI: presión telediastólica del ventrículo izquierdo; SA: septostomía auricular; SIA: septo interauricular; TxCP: trasplante cardiopulmonar; TxP: trasplante pulmonar.
La utilidad de la SA bajo triple tratamiento específico para la HAP no ha sido evaluada. El porcentaje de pacientes que recibe triple tratamiento específico es escaso en la mayoría de las series publicadas4,5. En la nuestra, todos los pacientes recibían epoprostenol, siete de ellos en triple tratamiento específico y tres en doble tratamiento con inhibidores de la fosfodiesterasa 5. A pesar de tratamiento optimizado, la SA proporcionó un beneficio clínico adicional en todos, con mejoría de la clase funcional y resolución de la clínica de insuficiencia cardiaca derecha refractaria y síncopes, tanto en los que se realizó como puente al trasplante pulmonar como en los que se llevó a cabo por fracaso del tratamiento médico sin otras alternativas terapéuticas. Es probable que el uso generalizado de la SA se haya visto limitado por las tasas relativamente altas de mortalidad del procedimiento y periprocedimiento (5% y 16%, respectivamente)5, y porque el momento más adecuado para obtener el máximo beneficio con esta técnica es incierto. Por ello, aunque alguna serie propone su realización en fases precoces de la enfermedad, en la mayoría de los países con acceso a medicamentos de elevado coste económico y trasplante pulmonar se realiza en fases tardías, cuando el tratamiento médico fracasa o como último recurso antes del trasplante. No obstante, realizada en fases terminales de la enfermedad la mortalidad es alta, por lo que se recomienda evitar realizarla como rescate en dichas situaciones4,5. En nuestra serie, la SA se indicó en fases avanzadas de la enfermedad ante el fracaso del tratamiento médico, pero no como procedimiento de rescate en pacientes en situación terminal. Posiblemente se apuró la indicación en la paciente que falleció a la semana de la SA, ya que precisó ultrafiltración e inotrópicos para poder realizar la SA. Ningún paciente falleció como consecuencia del procedimiento. La supervivencia a 30 días en nuestra serie es del 90%. A medio plazo está en la línea de lo publicado: 75% a 6 meses y 57% al año1,4,5 en relación con progresión de la enfermedad.
En nuestra experiencia, la SA en pacientes bajo tratamiento médico optimizado para la HAP, realizada de manera electiva ante el fracaso de este, es una opción terapéutica que se asocia a una baja morbimortalidad periprocedimiento y que es efectiva en cuanto a proporcionar una mejoría funcional en la mayoría de los pacientes con HAP grave con insuficiencia cardiaca derecha refractaria o en situación de bajo gasto, ya sea como puente al trasplante pulmonar o como coadyuvante al tratamiento médico.