Es bien sabido que ocasionalmente una lesión coronaria angiográficamente aparentemente significativa podría no causar isquemia y viceversa. Por eso las decisiones terapéuticas basadas en un conocimiento de la fisiología coronaria son cada vez más importantes. El uso de la reserva fraccional de flujo (RFF), una herramienta útil para determinar en el laboratorio de hemodinámica las lesiones que se pueden beneficiar de revascularización, ha conseguido una indicación de clase IA en las guías de la Sociedad Europea de Cardiología. Recientemente, el índice diastólico instantáneo sin ondas, de más facilidad de uso que la RFF, se considera equivalente a ella. En esta revisión se repasan y se profundiza en los conceptos de RFF e índice diastólico instantáneo sin ondas y se revisan las evidencias que justifican su uso, así como sus perspectivas futuras.
Palabras clave
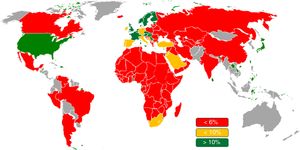
La fisiología coronaria tiene un papel establecido en el campo de la intervención coronaria. La reserva fraccional de flujo (RFF) ha permitido tratar a los pacientes con enfermedad coronaria (EC) de un modo más exacto y seguro que con la estimación visual angiográfica. Actualmente la RFF se utiliza mucho en todo el mundo (figura 1). Dada la evidencia acumulada durante los últimos 20 años, que incluye 3 grandes ensayos aleatorizados (DEFER, FAME y FAME 21–3), el uso de la RFF para la EC estable se recomienda en las guías de ESC/EACTS (European Society of Cardiology/European Association for Cardio-Thoracic Surgery) y ACC/AATS/AHA/ASE/ASNC/SCAI/SCCT/STS (American College of Cardiology/American Association for Thoracic Surgery/American Heart Association/American Society of Echocardiography/American Society of Nuclear Cardiology/Society for Cardiovascular Angiography and Interventions/Society of Cardiovascular Computed Tomography/Society of Thoracic Surgeons)4–6. Recientemente se ha introducido el cociente diastólico instantáneo sin ondas (iFR), que no requiere hiperemia7, como alternativa a la RFF. Cinco años después de su presentación inicial, 2 grandes ensayos aleatorizados, el DEFINE-FLAIR y el iFR–SWEDEHEART, han mostrado simultáneamente la no inferioridad del iFR en comparación con la RFF8,9. Hoy el iFR se considera equivalente como modalidad diagnóstica para la cardiopatía isquémica en las versiones más recientes de las guías6. En este artículo de revisión se resume la evidencia existente sobre la fisiología coronaria, en especial respecto a estas 2 modalidades, y se comentan también las perspectivas futuras en este campo.
Uso de la reserva fraccional de flujo en diferentes partes del mundo en 2016. La reserva fraccional de flujo se utiliza actualmente en todo el mundo en la toma de decisiones; sin embargo, su frecuencia de uso en el laboratorio de cateterismo no es alta, a pesar de las recomendaciones de las guías clínicas. Reproducido con permiso de Philips Volcano, informe de investigación de mercado del Decision Resources Group.
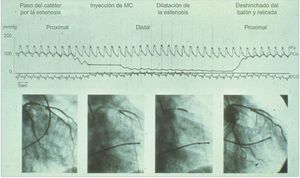
Hace 40 años, Andreas Grüntzig llevó a cabo la primera intervención coronaria percutánea (ICP) del mundo10. Es más, también entonces se realizó el primer registro de la presión coronaria a través de la estenosis antes y después de la ICP (figura 2). Grüntzig midió el gradiente de presión transestenótico con un catéter guía lleno de líquido. A pesar de la introducción temprana en el campo de la ICP, el uso práctico de la fisiología coronaria en el laboratorio de cateterismo no se inició hasta finales de la década de los noventa, debido a cuestiones tecnológicas y teóricas. Dado que no se disponía de las guías de presión bien desarrolladas que se utilizan hoy, la presión coronaria se determinó durante años con el propio catéter, que no resultaba muy fiable debido al deterioro del flujo anterógrado inducido por el uso del catéter11. La relación entre la presión coronaria y el flujo coronario fue objeto de una activa investigación tras la introducción del concepto de hiperemia12. Finalmente, los avances tecnológicos y teóricos permitieron el desarrollo del concepto de RFF.
Primer caso de intervención coronaria percutánea. En 1979, se registró la presión coronaria a través de la estenosis antes y después de la angioplastia con balón en el primer caso de intervención coronaria. MC: medio de contraste; Pa: presión aórtica; PCo: presión coronaria. Reproducido con permiso de Grüntzig et al.10.
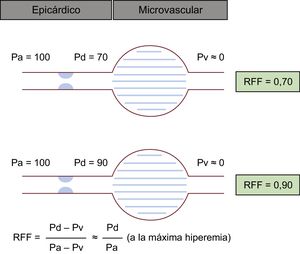
Pijls et al. describieron la RFF por primera vez en 199313. El concepto de RFF se basa en la idea de que la hiperemia máxima podría alcanzar una correlación lineal entre el flujo coronario y la presión coronaria, ya que la resistencia coronaria es estable y mínima durante la dilatación arterial máxima. La RFF se define como el cociente entre la presión distal (Pd) media y la presión aórtica (Pa) media durante la hiperemia máxima inducida por fármacos vasodilatadores. Por ejemplo, una RFF de 0,70 indica que el flujo coronario se reduce en un 30% respecto al normal, y una RFF de 0,90, que el flujo coronario solo se reduce en un 10% respecto al normal, debido a la existencia de estenosis (figura 3). Teniendo en cuenta la gravedad de la estenosis, el territorio y la viabilidad del miocardio y la perfusión colateral, la RFF permite determinar la trascendencia funcional de la EC. En un estudio relativamente pequeño, se propuso que el valor umbral para la detección de una isquemia significativa era 0,75, y se demostró un alto rendimiento diagnóstico de la RFF, con una sensibilidad del 88%, una especificidad del 100% y una exactitud del 93% en comparación con la ecocardiografía de estrés con dobutamina, la gammagrafía de perfusión miocárdica de estrés y el electrocardiograma de esfuerzo14. Posteriormente se realizaron numerosos estudios para comparar la RFF con las pruebas funcionales no invasivas, y se observó una correlación general aceptable15–28 (tabla 1). Actualmente se considera que el mejor valor de corte para diferir la ICP en la práctica clínica es 0,80 tras la validación en múltiples ensayos aleatorizados prospectivos realizados con ese umbral2,3.
Esquema del concepto de RFF. Durante la hiperemia máxima, cabe presumir una relación directa entre la presión y el flujo coronarios, ya que se puede soslayar el efecto de la microcirculación. Pese a que en la estimación visual se da el mismo grado de estenosis, los casos ilustrados muestran unos valores de RFF totalmente diferentes. Pa: presión aórtica; Pd: presión distal; Pv: presión venosa central; RFF: reserva fraccional de flujo.
Estudios de la reserva fraccional de flujo comparada con pruebas funcionales no invasivas
| Publicación | Comparación con pruebas no invasivas | Pacientes (n) | Mejor valor de corte | Exactitud (%) |
|---|---|---|---|---|
| Pijls et al.15, 1995 | X-ECG | 60 | 0,74 | 97 |
| De Bruyne et al.16, 1995 | MPS, X-ECG | 60 | 0,66 | 87 |
| Pijls et al.14, 1996 | DSE, MPS, X-ECG | 45 | 0,75 | 93 |
| Bartunek et al.17, 1997 | DSE | 75 | 0,75 | 81 |
| Caymaz et al.18, 2000 | MPS | 30 | 0,75 | 95 |
| Abe et al.19, 2000 | MPS | 46 | 0,75 | 91 |
| Chamuleau et al.20, 2001 | MPS | 127 | 0,74 | 77 |
| Yanagisawa et al.21, 2002 | MPS | 165 | 0,75 | 76 |
| Seo et al.22, 2002 | MPS | 25 | 0,75 | 60 |
| Morishima et al.23, 2004 | MPS | 20 | 0,75 | 85 |
| Kobori et al.24, 2005 | MPS | 147 | 0,75 | 70 |
| Hacker et al.25, 2005 | MPS | 50 | 0,75 | 86 |
| Krüger et al.26, 2005 | MPS | 42 | 0,75 | 88 |
| Samady et al.27, 2006 | DSE, MPS | 48 | 0,78 | 92 |
| Van de Hoef et al.28, 2012 | MPS | 232 | 0,76 | 74 |
DSE: ecocardiografía de estrés con dobutamina; MPS: gammagrafía de perfusión miocárdica; X–ECG: electrocardiograma de esfuerzo.
Se resumen los 3 grandes ensayos aleatorizados que desempeñaron un papel muy importante en el establecimiento de la RFF:
Estudio DEFEREl estudio aleatorizado DEFER inicial se llevó a cabo para evaluar la seguridad de diferir la ICP guiándose por la RFF1. En ese estudio se incluyeron pacientes con angina estable y una estenosis intermedia, pero con RFF > 0,75, y se les asignó aleatoriamente diferir (grupo de aplazamiento) o realizar (grupo de realización) la intervención. Después de esta publicación inicial, hoy se dispone de seguimientos a largo plazo y a más largo plazo de la cohorte del estudio DEFER a 5 años29 y a 15 años30. En la supervivencia sin eventos no hubo diferencias entre el grupo de aplazamiento y el grupo de realización. Los autores llegaron a la conclusión de que los pacientes con una RFF > 0,75 se encontraban en una situación estable y segura y que, en estos casos, el implante de un stent no reduce el riesgo de eventos cardiacos en la EC sin una isquemia significativa.
Estudio FAMEEl segundo ensayo controlado y aleatorizado fue mayor que el DEFER. El estudio FAME se realizó para evaluar la efectividad de la ICP guiada por la RFF en comparación con la ICP con bajo guía angiográfica en pacientes con EC multivaso2. En dicho ensayo, se aleatorizó a un total de 1.005 pacientes con estenosis ≥ 50% del diámetro del vaso en al menos 2 de las 3 arterias coronarias epicárdicas principales a ICP con stents farmacoactivos (SFA) guiada por las determinaciones de la RFF o solo con guía angiográfica. El valor de corte utilizado para la toma de decisiones fue 0,80. Los autores llegaron a la conclusión de que la ICP guiada por la RFF redujo significativamente la tasa de eventos del objetivo combinado formado de muerte, infarto de miocardio no mortal y nueva revascularización a 1 año (el 13,2 frente al 18,3%; riesgo relativo = 0,72; intervalo de confianza del 95%, 0,54-0,96; p = 0,02). Después de este estudio, el valor de corte de RFF = 0,80 se ha utilizado a menudo para decidir entre realizar o diferir una ICP en la práctica clínica, aun cuando la RFF = 0,75 es el valor de corte definitivo para determinar si hay isquemia significativa o no, lo que ha generado luego el problema de la «zona gris de la RFF».
Estudio FAME 2El tercer ensayo fue el estudio FAME 2, realizado para examinar si la ICP guiada por la RFF junto con un tratamiento médico óptimo (TMO) era superior al TMO solo o no3. Se planificó un seguimiento clínico a los 2 años para un total de 1.220 pacientes. Sin embargo, en el grupo de TMO, el evento adverso revascularización urgente se produjo con una frecuencia superior a la esperada, y el estudio se interrumpió prematuramente (seguimiento medio, 7 meses). Los autores llegaron a la conclusión de que la ICP guiada por la RFF junto con el TMO, en comparación con el TMO solo, redujo la necesidad de revascularización urgente a los pacientes con una EC estable e isquemia demostrada. Dado que el estudio se interrumpió antes de lo previsto, los investigadores no pudieron extraer ninguna conclusión respecto al objetivo clínico «duro» de los eventos muerte o infarto de miocardio.
SITUACIÓN ACTUALCon más de 20 años de investigaciones y experiencia clínica, la fisiología coronaria tiene ya un lugar establecido en el campo de las intervenciones percutáneas. Los resultados clínicos durante el seguimiento de 15 años del estudio DEFER y el de 5 años del estudio FAME han reforzado la idea de que la toma de decisiones basada en la RFF es segura y lógica29,30. Durante este periodo, los conocimientos y la evidencia relativa a la RFF se han enfrentado a más problemas específicos en diversas situaciones clínicas. Algunos de ellos se comentan en la primera parte de este apartado.
Utilidad de la RFF en la práctica clínica realEnfermedad multivasoTras el inicio de la era de los SFA y la introducción de los SFA de nueva generación, hoy la ICP se realiza a menudo para la enfermedad multivaso. Sin embargo, los resultados clínicos a largo plazo de la ICP en la enfermedad de 3 vasos son menos satisfactorios de lo esperado pese a usarse los SFA más recientes cuando se utiliza la angiografía como guía para la revascularización31,32. Por otro lado, en el estudio FAME, la ICP guiada por la RFF para la enfermedad multivaso alcanzó mejores resultados clínicos y, además, mostró que el número de stents utilizados por paciente era significativamente menor en el grupo en tratamiento guiado por la RFF (1,9 ± 1,3 frente a 2,7 ± 1,2; p < 0,001)2.
Aunque la gammagrafía de perfusión miocárdica se considera el patrón de referencia para la detección de la isquemia, varios estudios indicaron que había una discrepancia en los resultados en comparación con los de la RFF en la enfermedad multivaso33,34. Esta discrepancia podría explicarse por el fenómeno de la isquemia equilibrada, en el que la prueba de estrés con gammagrafía muestra un resultado aparentemente normal como consecuencia de la reducción de la perfusión miocárdica en todos los territorios coronarios de los pacientes con una enfermedad multivaso. En consecuencia, se considera lógico evaluar la enfermedad multivaso con la RFF para la toma de decisiones respecto a la revascularización.
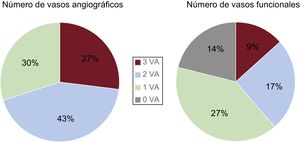
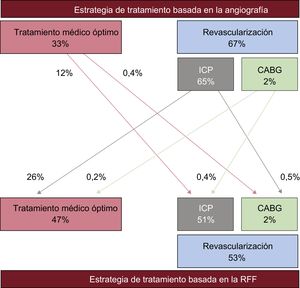
Es bien sabido que la evaluación fisiológica con la RFF reduce el número de vasos con enfermedad funcional y podría modificar también el tratamiento del paciente35,36 (figura 4). Recientemente, un registro multicéntrico de Japón ha indicado que se observó una reclasificación de la estrategia de tratamiento en alrededor del 40% de los pacientes con EC mediante la determinación de la RFF37,38 (figura 5).
Número de vasos evaluados mediante angiografía y mediante reserva fraccional de flujo. El número de vasos afectados funcionalmente puede cambiar de manera notable respecto a la evaluación angiográfica inicial. VA: vaso afectado. Reproducido con permiso de Sant’Anna et al.35.
Resultados del registro CVIT-DEFER. La estrategia de tratamiento puede cambiar drásticamente con la evaluación funcional. CABG: cirugía de revascularización aortoconaria; ICP: intervención coronaria percutánea; RFF: reserva fraccional de flujo. Reproducido con permiso de Nakamura et al.37,38.
Se ha evaluado también la relación entre la RFF y las modalidades de diagnóstico por imagen intracoronaria39–47. Al comienzo de esta investigación, la ecografía intravascular (IVUS) mostró una buena correlación con la RFF39. Sin embargo, estudios recientes indican que la exactitud en la predicción de una RFF significativa mediante el área luminal mínima (ALM) en la IVUS fue de aproximadamente un 60–70%, lo cual no se considera satisfactorio en la práctica clínica (tabla 2). Esta discrepancia podría explicarse por el hecho de que las evaluaciones con el ALM sola no tienen en cuenta el diámetro del vaso diana, la longitud de las lesiones y el flujo colateral44,45. La tomografía de coherencia óptica ha surgido como nueva modalidad invasiva de diagnóstico por la imagen que aporta una resolución mejor que la de la IVUS y una evaluación más precisa de la luz del vaso y el borde del stent48. Sin embargo, su correlación con una RFF significativa también ha sido escasa y los valores de corte del ALM que predecían mejor una RFF significativa tendieron a ser menores que los de la IVUS46,47 (tabla 2). Así pues, la IVUS y la tomografía de coherencia óptica no podían ser una alternativa a la RFF y actualmente debe optarse por el uso complementario de técnicas de imagen intracoronaria y evaluación funcional.
Correlación en los estudios de la reserva fraccional de flujo y las modalidades de diagnóstico por imagen
| Publicación | Número de lesiones | Valor de corte de la RFF | Modalidad | AML (mm2) | Exactitud (%) |
|---|---|---|---|---|---|
| Takagi et al.39, 1999 | 51 | 0,75 | IVUS | 3,0 | 84 |
| Briguori et al.40, 2001 | 53 | 0,75 | IVUS | 4,0 | 64 |
| Kang et al.41, 2011 | 236 | 0,80 | IVUS | 3,4 | 68 |
| Koo et al.42, 2011 | 267 | 0,80 | IVUS | 2,75 | 67 |
| Ben-Dor et al.43, 2012 | 205 | 0,80 | IVUS | 3,09 | 70 |
| Kang et al.44, 2012 | 784 | 0,80 | IVUS | 2,4 | 69 |
| Waksman et al.45, 2013 | 367 | 0,80 | IVUS | 3,07 | 64 |
| Gonzalo et al.46, 2012 | 61 | 0,80 | OCT | 2,36 | 66 |
| Shiono et al.47, 2012 | 62 | 0,75 | OCT | 1,91 | 85 |
AML: área luminal mínima; IVUS: ecografía intravascular; OCT: tomografía de coherencia óptica; RFF: reserva de flujo fraccional.
La ICP de una lesión en bifurcación sigue planteando un verdadero reto, pero la RFF ha aportado un conocimiento útil en estos casos. Koo et al.49,50 utilizaron la RFF para evaluar la rama lateral enjaulada tras el implante de un stent a través de las lesiones en bifurcación. Aunque se observó estenosis angiográfica en muchos de los casos, menos de una tercera parte de estas lesiones del ostium con estenosis > 75% del diámetro presentaron una RFF < 0,75. Los autores señalaron que no era necesaria una intervención adicional para la rama lateral enjaulada si el flujo sanguíneo coronario estaba conservado. Hoy este conocimiento se ha ampliado a las lesiones en bifurcación de la principal izquierda, que son una de las cuestiones más difíciles en la ICP y respalda la viabilidad del implante de stents a través de la principal izquierda51.
Agentes hiperémicosSe dispone de varios agentes hiperémicos. La inyección intravenosa (i.v.) de adenosina, en especial a través de una vía venosa central, es el patrón de referencia, y el fármaco actúa en un plazo de 1–2min, crea un grado estable de hiperemia máxima y es relativamente seguro como forma de estrés farmacológico52,53. Durante la inyección de adenosina, los pacientes perciben a menudo una molestia en el tórax o en la garganta. La inyección intracoronaria (i.c.) de adenosina puede aplicarse con seguridad y se dispone también de otros agentes hiperémicos, como el adenosina 5’-trifosfato (i.v. o i.c.), la papaverina (i.c.) y el nicorandil (i.c.)54–56. La diferencia entre los diversos agentes hiperémicos se resume en la tabla 3.
Propiedades de varios agentes hiperémicos
| Agentes hiperémicos | Tipo de inyección | Dosis | Tiempo transcurrido hasta alcanzar la hiperemia máxima | Duración | Ventajas | Efectos adversos y otros inconvenientes* |
|---|---|---|---|---|---|---|
| Adenosina/ATP | i.v. | 140-150 μg/kg/min | 2-3 min | 1-2 min | Seguro | Molestias en el pecho y rubefacción facial (30–70%), caída de la presión arterial, BAV (muy raro), contraindicación en el asma |
| Adenosina/ATP | i.c. | ACI: ≥ 80 μg ACD: ≥ 4 μg | 5-10 s | 5 s | Respuesta rápida | BAV (raro) No permite la retirada debido a la corta duración* |
| Papaverina | i.c. | ACI: 12-20 mg ACD: 8-12 mg | 15 s | 30-60 s | Respuesta rápida | Prolongación del intervalo QT, torsade des pointes (0,5%) |
| Nicorandil | i.c. | 2 mg | 15 s | 20-30 s | Respuesta segura y rápida | FV (excepcionalmente rara) Coste elevado* |
ACD: arteria coronaria derecha; ACI: arteria coronaria izquierda; ATP: adenosina 5’-trifosfato; BAV: bloqueo auriculoventricular; FV: fibrilación ventricular; i.c.: inyección intracoronaria; i.v.: inyección intravenosa.
También es sabido que la introducción de la RFF en la práctica clínica tiene sentido económico, ya que el estudio FAME demostró que la ICP guiada por la RFF permitía un ahorro de 675 dólares por paciente en tiempo de intervención y un ahorro > 2.000 dólares por paciente y año, al tiempo que alcanzaban unos resultados clínicos preferibles57. Muy recientemente, se ha demostrado la favorable relación coste-efectividad de la ICP guiada por la RFF en el seguimiento de 3 años del ensayo FAME 2, en el que se puso de manifiesto que la ICP en pacientes con una EC estable y una RFF reducida era ventajosa en comparación con el TMO solo, ya que proporcionaba una mejora de los resultados clínicos y de la calidad de vida, sin que hubiera un aumento de los costes58.
Limitaciones de la RFFAunque, como se ha indicado, el uso de la RFF en la práctica clínica tiene muchas ventajas, implica también algunos problemas.
Baja tasa de aplicaciónA pesar de las recomendaciones claras de las guías clínicas, la RFF no se utiliza con la frecuencia esperada (figura 1). Entre las posibles razones de la baja tasa de aplicación, estarían el tiempo necesario para realizar las mediciones de la RFF, el carácter invasivo adicional de la guía en la angiografía coronaria, los efectos adversos de los agentes hiperémicos, los costes asociados con la adenosina, la molestia sufrida por el paciente, las contraindicaciones y la falta de reembolso59.
Diferencia en la respuesta a los fármacosAunque la adenosina (i.v.) es el patrón de referencia para obtener la hiperemia, en estudios previos se han observado diversos tipos de respuesta a la adenosina (i.v.), lo cual puede dificultar la determinación de la RFF real, aparte del valor mínimo de Pd/Pa60,61, y se sabe también que algunos pacientes no responden bien a la adenosina.
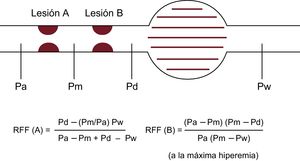
Lesiones en tándemLas lesiones en tándem se definen por la presencia de 2 lesiones, cada una con estenosis > 50%, en la misma arteria coronaria y separadas por un segmento angiográficamente normal. En las lesiones en tándem, la RFF resulta con frecuencia engañosa para el cardiólogo intervencionista, ya que cada estenosis influye en el flujo sanguíneo hiperémico y, por consiguiente, no puede conocerse el gradiente de presión exacto de cada estenosis antes de tratarla62. Aunque se han propuesto ecuaciones para predecir la RFF de cada lesión por separado63, su uso no resulta práctico porque la determinación de la presión enclavada requiere el hinchado de un balón en el vaso distal (figura 6). La intervención práctica debe basarse en una estrategia en etapas: después de haber implantado un stent en la estenosis de mayor gradiente, debe repetirse el registro de retirada para determinar si debe desplegarse un segundo stent y dónde hacerlo64, y esto resulta laborioso y pesado a la mayoría de los cardiólogos intervencionistas.
Esquema del concepto de RFF en las lesiones en tándem. Existen ecuaciones para la predicción de la RFF de cada lesión por separado, pero son complicadas. Pa: presión aórtica; Pd: presión distal; Pm: presión coronaria entre 2 lesiones; Pw: presión coronaria enclavada; RFF: reserva fraccional de flujo.
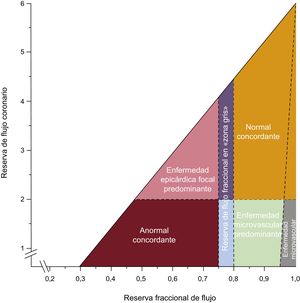
Aunque se sabe que la exactitud diagnóstica de la RFF y de la reserva de flujo coronario (RFC) para la EC es equivalente, los resultados de la RFF y de la RFC no concuerdan en un 30–40% de los casos de EC65: se ha propuesto que este fenómeno tiene su origen en la diferente distribución de la afección epicárdica y microvascular66 (figura 7). Se demostraron las consecuencias adversas de la discrepancia entre la RFF y la RFC en comparación con los casos en que la RFF y la RFC eran normales, y se observó que ello era atribuible principalmente a los casos con RFF normal y RFC anormal, mientras que la discrepancia con RFF anormal y RFC normal se asociaban predominantemente con un resultado clínico equivalente en comparación con los casos de RFF y RFC concordantes67.
Diagrama conceptual de la relación entre la reserva fraccional de flujo y la reserva de flujo coronario. Hay una discrepancia entre ellas. Reproducido con permiso de Van de Hoef et al.67.
No se sabe cuál es la mejor forma de abordar el tratamiento de las lesiones con una RFF en la zona gris, definida como la RFF entre 0,75 y 0,80, ya que en estudios anteriores se han obtenido resultados contradictorios en estos pacientes68,69. Sería lógico tomar las decisiones basándose en un criterio clínico multilateral para cada paciente concreto con la RFF situada en la zona gris, utilizando otras modalidades de imagen de perfusión, teniendo en cuenta las características anatómicas, los antecedentes del paciente y la relación riesgo-beneficio de la ICP.
La era del iFR está a la vuelta de la esquinaMás recientemente, ha surgido un gran interés por los gradientes en reposo, dadas las muchas limitaciones de la RFF que se han comentado. Es de destacar que el iFR se introdujo como alternativa a la RFF en 20127 y ha mostrado un rendimiento diagnóstico equivalente al de la RFF en varios estudios realizados con técnicas invasivas y no invasivas en un corto tiempo70–74. Además, la ICP guiada por el iFR fue no inferior a la ICP guiada por la RFF por lo que respecta a los eventos adversos cardiovasculares en un seguimiento de 1 año en 2 grandes ensayos multicéntricos aleatorizados distintos8,9, que condujeron a la inclusión del iFR en las guías clínicas como un método equivalente al de la RFF en Estados Unidos6.
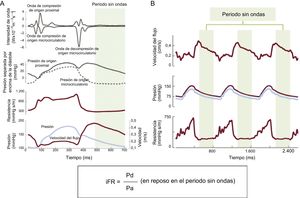
ConceptoEl iFR se mide en la parte media o tardía del periodo diastólico, de resistencia coronaria baja y constante, denominada periodo sin ondas, y la presión media durante ese periodo se obtiene en una posición distal a la lesión y se indexa respecto a la Pa simultánea7. En este periodo, la presión y la velocidad del flujo tienen una relación lineal entre ellas, lo cual permite utilizar el índice basado solo en la presión para evaluar la gravedad de la lesión coronaria. Además, el aislamiento de la determinación de la presión en el periodo sin ondas elimina la interacción entre el miocardio y la microcirculación coronaria en la sístole y al comienzo de la diástole, durante las cuales la compresión de la microcirculación aumenta la resistencia intracoronaria75,76 (figura 8).
Esquema del concepto del periodo sin ondas y el iFR. A: el sombreado verde resalta el periodo sin ondas de la diástole, ya que las múltiples ondas diferentes que se propagan a partir de los extremos proximal y distal del vaso están inactivas. B: los registros de la velocidad del flujo (línea superior), la presión proximal (azul claro) y la presión distal (púrpura) y la resistencia instantánea (línea inferior) muestran la estabilidad del periodo sin ondas de un latido a otro. iFR: cociente diastólico instantáneo sin ondas; Pa: presión aórtica; Pd: presión distal. Reproducido con permiso de Nijjer et al.76. Esta figura se muestra a todo color solo en la versión electrónica del artículo. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
Tras la introducción del iFR, varios estudios llegaron a la conclusión de que se observaba concordancia con la RFF en aproximadamente un 80% de los casos, y también mostraron que la detección del periodo sin ondas era necesaria para realizar la medición77–79. Tras estas comparaciones del iFR con la RFF, se realizaron una serie de estudios adicionales de comparación del iFR, la RFF y otros parámetros de referencia de la isquemia (tabla 4). En estos estudios se observó no solo un rendimiento diagnóstico equivalente del iFR70–74, sino también la posibilidad de una correlación mayor entre el iFR y la función microvascular en comparación con la observada con la RFF71,72.
Comparación del cociente diastólico instantáneo sin ondas y la reserva fraccional de flujo en la evaluación de la isquemia
| Publicación | Modalidad | N | Exactitud diagnóstica del AUC para la RFF (%) | Exactitud diagnóstica del AUC para el iFR (%) | p |
|---|---|---|---|---|---|
| Sen et al.70, 2013 | REH | 51 | 92 | 92 | NS |
| Sen et al.71 2013 | REH | 120 | 82 | 89 | < 0,01 |
| Petraco et al.72,, 2014 | RFC | 216 | 67 | 74 | < 0,01 |
| Van de Hoef et al.73, 2015 | MPS | 85 | 63 | 62 | NS |
| Hwang et al.74, 2017 | PET | 115 | 70 | 74 | NS |
AUC: área bajo la curva; iFR: cociente diastólico instantáneo sin ondas; MPS: gammagrafía de perfusión miocárdica; NS: no significativo; PET: tomografía por emisión de positrones; REH: resistencia de la estenosis en hiperemia; RFC: reserva de flujo coronario; RFF: reserva fraccional de flujo.
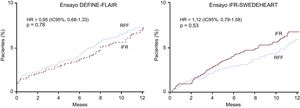
Muy recientemente se ha descrito la efectividad del iFR como guía para la ICP en comparación con la RFF en el estudio DEFINE-FLAIR y el estudio iFR-SWEDEHEART, que hasta la fecha son los mayores ensayos clínicos aleatorizados realizados en el campo de la fisiología coronaria8,9. Se aleatorizó en relación 1:1 a más de 4.500 pacientes de 2 estudios diferentes a ICP guiada por el iFR o ICP guiada por la RFF, tomando como valores de corte para la revascularización un iFR ≤ 0,89 y una RFF ≤ 0,80. El objetivo principal, que fue la combinación de muerte por cualquier causa, infarto de miocardio no mortal y revascularización no programada en 1 año, se produjo en los estudios DEFINE-FLAIR e iFR-SWEDEHEART en el 6,8 y el 6,7% de los pacientes de los grupos de iFR y el 7,0 y el 6,1% de los de los grupos de RFF. Los investigadores llegaron a la conclusión de que la ICP guiada por iFR era no inferior a la ICP guiada por la RFF por lo que respecta al riesgo de eventos cardiovasculares a 1 año (figura 9). Además, en los grupos de iFR, el número de estenosis funcionalmente significativas y las tasas de revascularización fueron inferiores, la duración de la intervención fue menor y hubo un porcentaje más bajo de pacientes que sufrieron síntomas adversos asociados con la intervención.
Resultados de los estudios DEFINE-FLAIR e iFR-SWEDEHEART. Las curvas de Kaplan-Meier de ambos ensayos muestran la no inferioridad del iFR respecto a la RFF en los acontecimientos adversos cardiacos mayores a los 12 meses. IC95%: intervalo de confianza del 95%; iFR: cociente diastólico instantáneo sin ondas; RFF: reserva fraccional de flujo. Reproducido con permiso de Davies et al.8 y Götberg et al.9.
En la práctica clínica actual, se prefiere la RFF debido a la evidencia que se ha generado respecto a ella a lo largo de años, mientras que el iFR tiende a preferirse por las ventajas adicionales y por la emergencia de nuevas pruebas. Las guías clínicas las han considerado equivalentes6. Los datos del estudio SYNTAX II, recientemente publicado, indican que la aplicación de la fisiología coronaria a la técnica de la ICP, tanto si se usa la RFF como si se emplea el iFR, podrán mejorar los resultados clínicos en los pacientes con enfermedad de 3 vasos80.
PERSPECTIVAS FUTURASFisiología coronaria en el SCAUna de las cuestiones de interés actual en este campo es el de la interrogación fisiológica de las lesiones no culpables en el síndrome coronario agudo (SCA). Dos ensayos recientes respaldan el empleo de la revascularización de arterias no relacionadas con el infarto guiada por la RFF. El ensayo DANAMI-3-PRIMULTI demostró que la revascularización completa en etapas guiada por la RFF antes del alta hospitalaria conduce a una reducción significativa de las futuras revascularizaciones en el seguimiento a 1 año, en comparación con la ICP solo de la arteria relacionada con el infarto81. De manera análoga, los investigadores del ensayo Compare-Acute examinaron si el tratamiento guiado por la RFF mejoraba los resultados en los pacientes con infarto agudo de miocardio con elevación del segmento ST y enfermedad multivaso, con objeto de evaluar los beneficios aportados por la revascularización en el contexto del tratamiento agudo de lesiones no relacionadas con el infarto82. Las revascularizaciones guiadas por la RFF en el momento de la ICP primaria produjeron una tasa menor de eventos cardiovasculares de la variable de valoración combinada a 1 año, principalmente por la reducción de las revascularizaciones posteriores. Sin embargo, dada la falta de un grupo de comparación fisiológico, no pudo determinarse el potencial pleno de la fisiología coronaria aplicada al SCA, y esto es algo que deberá evaluarse en futuros estudios. Además, es importante señalar que la evaluación fisiológica invasiva de la arteria no relacionada con el infarto en el SCA no es un proceso benigno. Se produjeron eventos adversos graves en un 0,2% de la población del ensayo Compare-Acute, como disección de la arteria coronaria con oclusión vascular posterior, infarto de miocardio y muerte. La relación riesgo-beneficio de la introducción adicional de una guía en lesiones no culpables o de la inducción de hiperemia en un SCA no está clara y requiere más estudio.
Como guía para la CABGNo se dispone de datos objetivos respecto al uso de la fisiología coronaria como guía para la cirugía de revascularización aortocoronaria (CABG). Solo un estudio ha mostrado que la tasa de oclusión fue significativamente mayor en la angiografía a 1 año cuando la derivación se aplicó a estenosis que no eran funcionalmente significativas, lo que indica que la fisiología coronaria podría aportar mejores resultados en la CABG, al igual que en el campo de la ICP83. Serán necesarios ensayos prospectivos aleatorizados que se centren en los objetivos clínicos «duros» para investigar las ventajas de la CABG guiada por RFF/iFR.
Potencial del iFRPor lo que respecta a la frecuencia de uso, el iFR se utilizará de manera más amplia cuando se presenten los resultados clínicos a más largo plazo de los estudios DEFINE-FLAIR e iFR-SWEDEHEART.
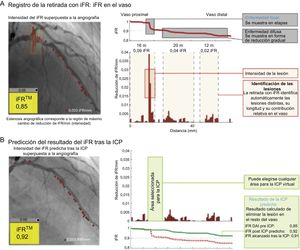
Como consecuencia de la aplicación del índice en reposo, un estudio reciente ha señalado que el iFR podría resolver una de las limitaciones de la RFF: la interrelación hemodinámica entre las estenosis de las lesiones en tándem durante la hiperemia63. La utilidad de la cartografía de la presión intracoronaria, que permite identificar los segmentos que contribuyen en mayor medida a producir el deterioro hemodinámico causado por las lesiones difusas o en tándem, y la predicción del iFR después de un implante de stent virtual, se demostró en el estudio de retirada con iFR84 (figura 10). Esta tecnología está más avanzada y deberá validarse en un futuro próximo. Sin embargo, para utilizar al máximo esta tecnología, es imprescindible una mejora en las propiedades de la guía de presión, de manera que dicha guía pueda usarse como guía de ICP en las intervenciones realizadas en la práctica clínica real.
Caso representativo del estudio de retirada con iFR. A: el registro conjunto de la línea de retirada con iFR junto con la coronariografía permite identificar una pérdida de presión a lo largo de todo el trayecto del vaso y diferencia la enfermedad focal de la difusa. B: la intervención coronaria percutánea (ICP) virtual calcula el resultado del iFR esperado tras la ICP para el área elegida para esta. DAI: arteria coronaria descendente anterior izquierda; iFR: cociente diastólico instantáneo sin ondas. Reproducido con permiso de Nijjer et al.84.
Recientemente se ha introducido el concepto de la dinámica de fluidos computarizada para combinar las técnicas de imagen coronarias con la fisiología coronaria, y se han desarrollado varias modalidades prometedoras. La RFF basada en la tomografía computarizada cardiaca ha alcanzado un alto rendimiento diagnóstico en varios estudios multicéntricos prospectivos, en comparación con la angiografía por tomografía computarizada85–87, y se han señalado ventajas en cuanto a calidad de vida y resultados económicos, en comparación con la práctica clínica convencional88. El cociente de flujo cuantitativo, que es una RFF basada en la angiografía coronaria cuantitativa tridimensional, permitiría determinar la lesión hemodinámicamente significativa sin utilizar una guía de presión ni hiperemia89. La RFF virtual derivada de la tomografía de coherencia óptica permitiría determinar la relación entre la morfología y la fisiología coronarias90. Estas tecnologías tienen como objetivo indicar el valor simulado de la RFF a partir solo de las imágenes coronarias, aprovechando las ventajas que aportan las propiedades específicas de cada modalidad.
CONCLUSIONESLa fisiología coronaria está adquiriendo cada vez más importancia para los actuales cardiólogos intervencionistas, gracias a una abundante evidencia y un prometedor futuro en desarrollo. La evidencia acumulada hasta la fecha parece indicar que «debe usarse RFF/iFR para una mejor ICP». Las nuevas tecnologías que se están desarrollando en este campo están generando también mucho interés.
CONFLICTO DE INTERESEST. Warisawa y C.M. Cook han recibido pagos por consultoría de Philips. J.E. Davies ha recibido subvenciones de investigación de Philips y AstraZeneca y pagos por consultoría de Medtronic, Philips y ReCor Medical y posee patentes relativas a la tecnología de iFR, que se han licenciado a Philips.