La guía de insuficiencia cardiaca de la Sociedad Europea de Cardiología define un nuevo grupo de pacientes con fracción de eyección del ventrículo izquierdo intermedia (40-49%) (ICFEi) cuyas características y pronóstico no están bien definidos. Nuestro objetivo es analizar este grupo en pacientes hospitalizados por insuficiencia cardiaca (Registro REDINSCOR II).
MétodosEstudio observacional prospectivo de 1.420 pacientes clasificados según la fracción de eyección: deprimida (ICFEd), < 40%; intermedia (ICFEi), 40-49% y conservada (ICFEc), ≥ 50%. Se comparan entre los 3 grupos las características clínicas, la mortalidad y sus causas y los ingresos por insuficiencia cardiaca al mes, a los 6 meses y al año. Se obtuvo la puntuación de propensión emparejando según grupo de fracción de eyección.
ResultadosLa distribución de pacientes fue: 583 (41%) con ICFEd, 227 (16%) con ICFEi y 610 (43%) con ICFEc. El grupo con ICFEi se parece más al de ICFEc en cuanto a edad, prevalencia de hipertensión arterial y fibrilación auricular, aunque comparte con la ICFEd el predominio de varones, la etiología isquémica y el mayor uso de fármacos clase I para ICFEd. Las demás características fueron intermedias. No se detectaron diferencias entre los 3 grupos en la mortalidad total, las causas de muerte y los reingresos por insufiencia cardiaca. Esta similitud en el pronóstico se confirmó en el análisis ajustado por puntuación de propensión.
ConclusionesEl grupo de pacientes con ICFEi comparte características con los de ICFEc e ICFEd, aunque está más próximo al de ICFEc. La mortalidad total, las causas de muerte o las rehospitalizaciones por insuficiencia cardiaca eran similares en los 3 grupos.
Palabras clave
La terminología empleada más frecuentemente para describir la insuficiencia cardiaca (IC) se basa en la fracción de eyección del ventrículo izquierdo (FEVI), que abarca un amplio espectro de pacientes, desde la FEVI normal (≥ 50%), clásicamente denominada IC con FEVI conservada (ICFEc), a la FEVI reducida (< 50%), denominada IC con FEVI deprimida (ICFEd).
La diferenciación de la IC por la FEVI es importante tanto por su significado pronóstico como porque la mayoría de los ensayos clínicos han utilizado este parámetro para la selección de pacientes. Los principales ensayos en ICFEd incluyeron a pacientes con FEVI ≤ 35-40%, y por el momento el beneficio terapéutico se limita a este grupo1,2. Sin embargo, los registros y ensayos clínicos en ICFEc han utilizado diferentes puntos de corte (FEVI > 40%, FEVI > 45%, FEVI > 50%), y por este motivo se considera que la FEVI entre el 40 y el 49% es una «zona gris» que requiere una mejor caracterización. Así, la nueva guía de IC de la Sociedad Europea de Cardiología (ESC)1 establece una nueva categoría de pacientes con IC y FEVI intermedia (ICFEi) para valores de FEVI del 40-49%, y destacan la necesidad de estimular la investigación clínica y terapéutica en este particular grupo de pacientes.
La Red de Investigación Cardiovascular del Instituto de Salud Carlos III (RIC) dispone de una base de datos sobre pacientes hospitalizados por IC aguda (registro REDINSCOR II) que incluye datos clínico-epidemiológicos y pronósticos. El objetivo de nuestro estudio es analizar y comparar las características clínicas, terapéuticas y pronósticas de los pacientes con ICFEd, ICFEi e ICFEc incluidos en el registro REDINSCOR II.
MÉTODOSPoblación de estudioLos datos parten de un registro nacional (REDINSCOR II), multicéntrico y prospectivo, que aglutina hasta 20 hospitales españoles de distinta complejidad e incluye a pacientes de edad ≥ 18 años hospitalizados en el servicio de cardiología al menos 24 h cuyo motivo de ingreso principal fue la presentación de signos o síntomas compatibles con IC aguda, tanto de novo como descompensada, y con una radiografía de tórax con datos de congestión pulmonar. En ningún caso se trata de una continuación de la Red REDINSCOR previa, que incluía a pacientes con IC crónica reclutados en las consultas de cardiología3.
Se excluyó a los pacientes con IC y síndrome coronario agudo con elevación del ST, pacientes con una enfermedad terminal cuyo pronóstico vital fuera < 1 año y aquellos con alguna condición que limitase el seguimiento posterior. Estableció el diagnóstico de IC el cardiólogo responsable del paciente de acuerdo con los criterios establecidos en la guía de IC.
El registro se llevó entre octubre de 2013 y diciembre de 2014 e incluyó un total de 1.831 pacientes consecutivos ingresados por IC aguda, de los que se incluyó en el análisis solo a los que tenían determinación ecocardiográfica de la FEVI durante el ingreso (1.084) o en los 6 meses previos (336), en total 1.420 pacientes (el 77,6% del total).
Las características basales de los pacientes excluidos por ausencia de determinación ecocardiográfica de FEVI (411 pacientes [22%]) se muestran en la tabla 1 del material suplementario.
Se realizaron controles telefónicos del estado vital y de la presencia de eventos al mes, a los 3, a los 6 meses y al año de su inclusión en el registro. Las pérdidas en el seguimiento fueron mínimas (30 pacientes [1,6%]) y se censuraron para el análisis. El estudio contó con la aprobación de los comités de ética de los hospitales participantes y se dispone del consentimiento informado firmado por cada paciente incluido.
Se establecieron 3 grupos de IC según la FEVI: IC con FEVI deprimida (ICFEd) si la FEVI es < 40%, IC con FEVI intermedia (ICFEi) si la FEVI es del 40-49% e ICFEc si la FEVI es ≥ 50%.
El objetivo de nuestro estudio es analizar en REDINSCOR II las características clínicas, terapéuticas y pronósticas de los pacientes con ICFEi y compararlas con los 2 patrones clásicos de IC (ICFEd e ICFEc).
Análisis estadísticoLas variables cuantitativas se expresan como media ± desviación estándar y las cualitativas, como frecuencia (porcentaje). Se utilizó el test de la χ2 o el exacto de Fisher para comparar las variables cualitativas y la ANOVA o t de Student para comparar las variables cuantitativas.
Se realizó un análisis mediante puntuación de propensión emparejada para equilibrar los grupos y minimizar el sesgo que supone estudiar el efecto de los grupos de FEVI a partir de un estudio observacional. La puntuación de propensión emparejada iguala las características basales de los grupos por unas variables definidas, lo que permite analizar el efecto de una intervención o factor. Para la puntuación de propensión emparejada se usó el protocolo 1:1 sin reemplazo, con caliper 0,2 desviaciones estándar de la puntuación de propensión, con el método de emparejamiento nearest neighbour. Para diagnosticar el equilibrio entre grupos, se utilizó la «diferencia estandarizada»4 para comparar la media de las variables continuas y binarias, que no se influye por el tamaño de la muestra y permite la comparación del equilibrio relativo de variables con diferentes unidades. En nuestro caso, se esperaban diferencias estandarizadas < 0,2.
La puntuación de propensión emparejada se obtuvo mediante el paquete estadístico MatchIt del proyecto R. Las variables independientes fueron: sexo, edad, IC previa, diabetes mellitus, hipertensión, enfermedad pulmonar obstructiva crónica, síndrome de apnea-hipopnea obstructiva del sueño, ictus, enfermedad vascular periférica, frecuencia cardiaca, presión arterial sistólica, etiología isquémica, hemoglobina, filtrado glomerular (CKD-EPI)5, fracción aminoterminal del propéptido natriurético cerebral > 1.500 ng/l, índices de edad-comorbilidad de Charlson6, índice de fragilidad de Barthel7, test de cribado de deterioro cognitivo de Pfeiffer8 y tratamiento farmacológico (inhibidores de la enzima de conversión de la angiotensina o antagonistas del receptor de la angiotensina II y bloqueadores beta antialdosterónicos). Mediante dicho análisis se obtuvieron 2 grupos de 212 pacientes emparejados por la condición FEVI 40-49% frente a < 40% y 208 pacientes por la condición FEVI 40-49% frente a ≥ 50%.
Primero se realizó un análisis de curvas de supervivencia para toda la cohorte mediante el método de Kaplan-Meier, y se compararon mediante log-rank test. Después, se realizaron análisis de supervivencia en las cohortes emparejadas. Se construyó un modelo de regresión de Cox con la variable explicativa «grupo de FEVI (%)» para el evento muerte por cualquier causa. Para el análisis de incidencia de reingreso por IC, se trazaron las curvas de incidencia acumulada y las diferencias entre grupos se analizaron con la prueba de Gray9; el efecto del riesgo se determinó mediante un modelo de regresión de Fine y Gray10,11 para riesgos competitivos.
El supuesto de proporcionalidad del riesgo se evaluó mediante el análisis de los residuos de Schoenfeld.
Los datos faltantes se imputaron mediante el paquete MICE (Multivariate Imputation by Chained Equations) de R. Se realizó 1 imputación, dado que el porcentaje de datos faltantes era < 5%, excepto en la variable de la fracción aminoterminal del propéptido natriurético cerebral, que se categorizó en 3 grupos: si era < 1.500 ng/l, si era ≥ 1.500 ng/l y «datos no disponibles» si le faltaban datos, ya que no medir este parámetro también podría estar relacionado con el evento.
Los análisis estadísticos se realizaron con los programas estadísticos SPSS 22 y R 3.2. Se consideró un resultado estadísticamente significativo si p < 0,05.
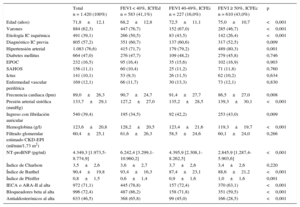
RESULTADOSCaracterísticas basales del grupo totalLas características basales al ingreso de los 1.420 pacientes incluidos en el análisis se recogen en la tabla 1.
Características basales al ingreso y tratamiento al alta según la fracción de eyección del ventrículo izquierdo
| Total n = 1.420 (100%) | FEVI < 40%, ICFEd n = 583 (41,1%) | FEVI 40-49%, ICFEi n = 227 (16,0%) | FEVI ≥ 50%, ICFEc n = 610 (43,0%) | p | |
|---|---|---|---|---|---|
| Edad (años) | 71,8±12,1 | 68,2±12,8 | 72,5±11,1 | 75,0±10,7 | <0,001 |
| Varones | 884 (62,3) | 447 (76,7) | 152 (67,0) | 285 (46,7) | <0,001 |
| Etiología IC isquémica | 491 (39,1) | 266 (50,5) | 83 (43,5) | 142 (26,4) | <0,001 |
| Diagnóstico IC previa | 805 (57,2) | 351 (60,7) | 137 (60,6) | 317 (52,5) | 0,009 |
| Hipertensión arterial | 1.083 (76,6) | 415 (71,7) | 179 (79,2) | 489 (80,3) | 0,001 |
| Diabetes mellitus | 664 (47,0) | 276 (47,7) | 109 (48,2) | 279 (45,8) | 0,746 |
| EPOC | 232 (16,5) | 95 (16,4) | 35 (15,6) | 102 (16,9) | 0,903 |
| SAHOS | 156 (11,1) | 60 (10,4) | 25 (11,2) | 71 (11,8) | 0,760 |
| Ictus | 141 (10,1) | 53 (9,3) | 26 (11,5) | 62 (10,2) | 0,634 |
| Enfermedad vascular periférica | 169 (12,1) | 66 (11,7) | 30 (13,3) | 73 (12,1) | 0,830 |
| Frecuencia cardiaca (lpm) | 89,0±26,3 | 90,7±24,7 | 91,4±27,7 | 86,5±27,0 | 0,008 |
| Presión arterial sistólica (mmHg) | 133,7±29,1 | 127,2±27,0 | 135,2±28,5 | 139,3±30,1 | <0,001 |
| Ingreso con fibrilación auricular | 540 (39,4) | 195 (34,5) | 92 (42,2) | 253 (43,0) | 0,009 |
| Hemoglobina (g/l) | 123,6±20,8 | 128,2±20,5 | 123,4±21,6 | 119,3±19,7 | <0,001 |
| Filtrado glomerular estimado CKD-EPI (ml/min/1,73 m2) | 60,4±25,1 | 61,6±26,3 | 58,5±24,6 | 60,1±24,0 | 0,266 |
| NT-proBNP (pg/ml) | 4.349,3 [1.973,5-8.774,9] | 6.242,4 [3.299,1-10.960,2] | 4.395,9 [2.308,1-8.262,5] | 2.845,9 [1.287,4-5.903,6] | <0,001 |
| Índice de Charlson | 3,5±2,6 | 3,6±2,7 | 3,7±2,6 | 3,4±2,6 | 0,220 |
| Índice de Barthel | 90,4±19,8 | 93,4±16,3 | 87,4±23,1 | 88,6±21,2 | <0,001 |
| Índice de Pfeiffer | 0,8±1,5 | 0,6±1,4 | 0,9±1,6 | 1,0±1,6 | 0,001 |
| IECA o ARA-II al alta | 972 (71,1) | 445 (78,8) | 157 (72,4) | 370 (63,1) | <0,001 |
| Bloqueadores beta al alta | 996 (72,4) | 487 (86,2) | 158 (71,8) | 351 (59,5) | <0,001 |
| Antialdosterónicos al alta | 633 (46,5) | 368 (65,8) | 99 (45,0) | 166 (28,5) | <0,001 |
ARA-II: antagonistas del receptor de la angiotensina II; CKD-EPI: Chronic Kidney Disease Epidemiology Collaboration; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; ICFEd: insuficiencia cardiaca con fracción de eyección deprimida; ICFEi: insuficiencia cardiaca con fracción de eyección intermedia; ICFEc: insuficiencia cardiaca con fracción de eyección conservada; IECA: inhibidor de la enzima de conversión de la angiotensina; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; SAHOS: síndrome de apnea-hipopnea obstructiva del sueño.
Las variables continuas se representan mediante media ± desviación estándar o mediana [intervalo intercuartílico] y las categóricas, como n (%).
La media de edad del grupo total de pacientes analizados era 71,8 ± 12,1 años, y 884 (62,3%) eran varones. El factor de riesgo más frecuente fue la hipertensión arterial en 1.083 pacientes (76,6%), y 664 (47%) eran diabéticos. Más de la mitad, 805 pacientes (57,2%), tenía diagnóstico previo de IC. En cuanto a la etiología de la IC, la más frecuente fue la isquémica, 491 pacientes (39,1%). También hubo una alta prevalencia de fibrilación auricular, pues 540 (39,4%) la presentaban en el momento del ingreso.
Características de los grupos definidos por fracción de eyección del ventrículo izquierdoDe todos los pacientes incluidos, 583 (41%) tenían FEVI < 40% (ICFEd); 227 (16%), FEVI 40-49% (ICFEi) y 610 (43%), FEVI ≥ 50% (ICFEc).
Se observaron diferencias significativas entre los 3 grupos en variables como la edad y el sexo, en el antecedente de hipertensión arterial o de etiología isquémica y en variables clínicas al ingreso como la presencia de fibrilación auricular, la hemoglobina o la fracción aminoterminal del propéptido natriurético cerebral. En términos generales, la ICFEi se asemeja más a la ICFEc en características como la edad, la prevalencia de hipertensión arterial o la presencia de fibrilación auricular, pero comparte con la ICFEd el predominio del sexo masculino y la alta prevalencia de etiología isquémica.
También hubo diferencias significativas entre los 3 grupos en cuanto a la capacidad funcional medida por el índice de Barthel y el estado cognitivo medido por el índice de Pfeiffer; se observó cierta similitud entre la ICFEi y la ICFEc. Sin embargo, no se observaron diferencias entre los 3 grupos en el nivel de edad-comorbilidad medido por el índice de Charlson.
Tratamiento farmacológico al altaSe observan diferencias significativas entre los 3 grupos en los principales tratamientos al alta (tabla 1). En el grupo ICFEi destaca una elevada prescripción de tratamientos considerados de clase I en ICFEd; más del 70% de los pacientes con ICFEi reciben inhibidores de la enzima de conversión de la angiotensina o antagonistas del receptor de la angiotensina II y bloqueadores beta al alta (el 72,4 y el 71,8% respectivamente) y casi la mitad (45%), antialdosterónicos.
Eventos en el seguimientoDe todos los pacientes ingresados por IC aguda incluidos en el análisis, murieron durante el ingreso 53 (3,9%): 21 con ICFEd (mortalidad, 3,8%), 9 con ICFEi (mortalidad, 4,1%) y 23 con ICFEc (mortalidad, 3,9%) (p = 0,972) (tabla 2). No se encontraron diferencias significativas entre los 3 grupos en la mortalidad hospitalaria (ICFEd frente a ICFEc, odds ratio [OR] = 0,96; intervalo de confianza del 95% [IC95%], 0,53-1,76; p = 0,896; ICFEi frente a ICFEc, OR = 1,06; IC95%, 0,48-2,31; p = 0,891). Tras el primer mes de seguimiento, se observó una tendencia a mayor mortalidad en el grupo de ICFEi (el 5,3% en ICFEd, el 8,4% en ICFEi y el 6,1% en ICFEc), aunque no resultó significativa (p = 0,265) (ICFEd frente a ICFEc, OR = 0,87; IC95%, 0,53-1,42; p = 0,578; ICFEi frente a ICFEc, OR = 1,42; IC95%, 0,80-2,52; p = 0,237).
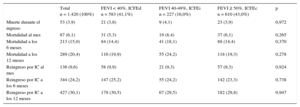
Mortalidad y reingresos por insuficiencia cardiaca durante el seguimiento de la cohorte total
| Total n = 1.420 (100%) | FEVI < 40%, ICFEd n = 583 (41,1%) | FEVI 40-49%, ICFEi n = 227 (16,0%) | FEVI ≥ 50%, ICFEc n = 610 (43,0%) | p | |
|---|---|---|---|---|---|
| Muerte durante el ingreso | 53 (3,9) | 21 (3,8) | 9 (4,1) | 23 (3,9) | 0,972 |
| Mortalidad al mes | 87 (6,1) | 31 (5,3) | 19 (8,4) | 37 (6,1) | 0,265 |
| Mortalidad a los 6 meses | 213 (15,0) | 84 (14,4) | 41 (18,1) | 88 (14,4) | 0,370 |
| Mortalidad a los 12 meses | 289 (20,4) | 116 (19,9) | 55 (24,2) | 118 (19,3) | 0,278 |
| Reingreso por IC al mes | 136 (9,6) | 58 (9,9) | 21 (9,3) | 57 (9,3) | 0,924 |
| Reingreso por IC a los 6 meses | 344 (24,2) | 147 (25,2) | 55 (24,2) | 142 (23,3) | 0,738 |
| Reingreso por IC a los 12 meses | 427 (30,1) | 178 (30,5) | 67 (29,5) | 182 (29,8) | 0,947 |
FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; ICFEc: insuficiencia cardiaca con fracción de eyección conservada; ICFEd: insuficiencia cardiaca con fracción de eyección deprimida; ICFEi: insuficiencia cardiaca con fracción de eyección intermedia.
Los valores expresan n (%).
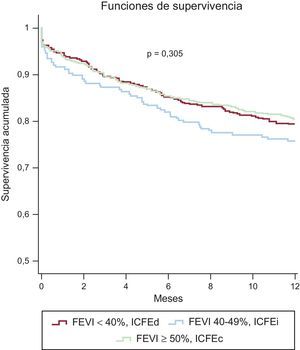
Tampoco se observaron diferencias significativas en la mortalidad a los 6 meses (p = 0,37) (ICFEd frente a ICFEc, OR = 1,00; IC95%, 0,73-1,38; p = 0,993; ICFEi frente a ICFEc, OR = 1,31; IC95%, 0,87-1,96; p = 0,196] ni al año (p = 0,278) (ICFEd frente a ICFEc, OR = 1,04; IC95%, 0,78-1,39; p = 0,810; ICFEi frente a ICFEc, OR = 1,33; IC95%, 0,93-1,92; p = 0,122), con mortalidades del 15 y el 20,4% del grupo total. En la figura 1 se muestra las curvas de Kaplan-Meier de supervivencia al año de los 3 grupos de FEVI en la cohorte total.
Curvas de Kaplan-Meier de supervivencia al año de los 3 grupos de fracción de eyección del ventrículo izquierdo en la cohorte total. FEVI: fracción de eyección del ventrículo izquierdo; ICFEc: insuficiencia cardiaca con fracción de eyección conservada; ICFEd: insuficiencia cardiaca con fracción de eyección deprimida; ICFEi: insuficiencia cardiaca con fracción de eyección intermedia.
Al analizar la distribución de las muertes en la cohorte total, no hubo diferencias significativas entre los grupos de IC deprimida, intermedia y preservada, y la muerte por IC refractaria fue la más frecuente en los 3 grupos, seguida de la muerte de causa no cardiovascular (tabla 3).
Tipo de mortalidad al año en los 3 grupos de FEVI de la cohorte total
| Tipo de mortalidad (12 meses) | Total n = 1.420 (100%) | FEVI < 40%, ICFEd n = 583 (41,1%) | FEVI 40-49%, ICFEi n = 227 (16,0%) | FEVI ≥ 50%, ICFEc n = 610 (43,0%) | p |
|---|---|---|---|---|---|
| Muerte súbita | 45 (3,2) | 17 (2,9) | 5 (2,2) | 23 (3,8) | 0,465 |
| IC refractaria | 137 (9,6) | 60 (10,3) | 25 (11,0) | 52 (8,5) | 0,439 |
| Otra cardiovascular | 37 (2,6) | 12 (2,1) | 6 (2,6) | 19 (3,1) | 0,519 |
| Extracardiaca | 70 (4,9) | 27 (4,6) | 19 (8,4) | 24 (3,9) | 0,028 |
FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; ICFEc: insuficiencia cardiaca con fracción de eyección conservada; ICFEd: insuficiencia cardiaca con fracción de eyección deprimida; ICFEi: insuficiencia cardiaca con fracción de eyección intermedia.
Los valores expresan n (%).
La tasa de reingresos por IC en el grupo total fue del 9,6% al mes, el 24,2% a los 6 meses y el 30,1% al año (tabla 2).
No se encontraron diferencias significativas entre los 3 grupos en ningún momento del seguimiento.
Ajuste por puntuación de propensiónTras el análisis por la puntuación de propensión, se obtuvieron 2 grupos de 212 pacientes emparejados por la condición FEVI 40-49% frente a < 40%, y 208 pacientes por la condición FEVI 40-49% frente a ≥ 50%. El equilibrio de la distribución de las variables entre los pacientes adecuadamente emparejados se presenta en las tabla 4A y la tabla 4B.
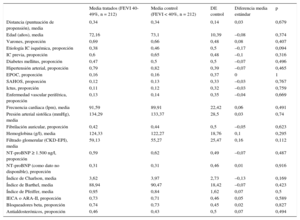
Características basales emparejadas después de la puntuación de propensión emparejada en los grupos ICFEi e ICFEd
| Media tratados (FEVI 40-49%, n = 212) | Media control (FEVI < 40%, n = 212) | DE control | Diferencia media estándar | p | |
|---|---|---|---|---|---|
| Distancia (puntuación de propensión), media | 0,34 | 0,34 | 0,14 | 0,03 | 0,679 |
| Edad (años), media | 72,16 | 73,1 | 10,39 | –0,08 | 0,374 |
| Varones, proporción | 0,69 | 0,66 | 0,48 | 0,08 | 0,407 |
| Etiología IC isquémica, proporción | 0,38 | 0,46 | 0,5 | –0,17 | 0,094 |
| IC previa, proporción | 0,6 | 0,65 | 0,48 | –0,1 | 0,316 |
| Diabetes mellitus, proporción | 0,47 | 0,5 | 0,5 | –0,07 | 0,496 |
| Hipertensión arterial, proporción | 0,79 | 0,82 | 0,39 | –0,07 | 0,465 |
| EPOC, proporción | 0,16 | 0,16 | 0,37 | 0 | 1 |
| SAHOS, proporción | 0,12 | 0,13 | 0,33 | –0,03 | 0,767 |
| Ictus, proporción | 0,11 | 0,12 | 0,32 | –0,03 | 0,759 |
| Enfermedad vascular periférica, proporción | 0,13 | 0,14 | 0,35 | –0,04 | 0,669 |
| Frecuencia cardiaca (lpm), media | 91,59 | 89,91 | 22,42 | 0,06 | 0,491 |
| Presión arterial sistólica (mmHg), media | 134,29 | 133,37 | 28,5 | 0,03 | 0,74 |
| Fibrilación auricular, proporción | 0,42 | 0,44 | 0,5 | –0,05 | 0,623 |
| Hemoglobina (g/l), media | 124,33 | 122,27 | 18,76 | 0,1 | 0,295 |
| Filtrado glomerular (CKD-EPI), media | 59,13 | 55,27 | 25,47 | 0,16 | 0,112 |
| NT-proBNP ≥ 1.500 ng/l, proporción | 0,59 | 0,62 | 0,49 | –0,07 | 0,487 |
| NT-proBNP (como dato no disponible), proporción | 0,31 | 0,31 | 0,46 | 0,01 | 0,916 |
| Índice de Charlson, media | 3,62 | 3,97 | 2,73 | –0,13 | 0,169 |
| Índice de Barthel, media | 88,94 | 90,47 | 18,42 | –0,07 | 0,423 |
| Índice de Pfeiffer, media | 0,95 | 0,84 | 1,62 | 0,07 | 0,5 |
| IECA o ARA-II, proporción | 0,73 | 0,71 | 0,46 | 0,05 | 0,589 |
| Bloqueadores beta, proporción | 0,74 | 0,73 | 0,45 | 0,02 | 0,827 |
| Antialdosterónicos, proporción | 0,46 | 0,43 | 0,5 | 0,07 | 0,494 |
ARA-II: antagonistas del receptor de la angiotensina II; CKD-EPI: Chronic Kidney Disease Epidemiology Collaboration; DE: desviación estándar; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; ICFEd: insuficiencia cardiaca con fracción de eyección deprimida; ICFEi: insuficiencia cardiaca con fracción de eyección intermedia; IECA: inhibidor de la enzima de conversión de la angiotensina; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; SAHOS: síndrome de apnea-hipopnea obstructiva del sueño.
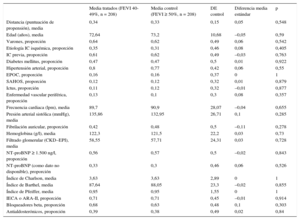
Características basales emparejadas después de la puntuación de propensión emparejada en los grupos ICFEi e ICFEc
| Media tratados (FEVI 40-49%, n = 208) | Media control (FEVI ≥ 50%, n = 208) | DE control | Diferencia media estándar | p | |
|---|---|---|---|---|---|
| Distancia (puntuación de propensión), media | 0,34 | 0,33 | 0,15 | 0,05 | 0,548 |
| Edad (años), media | 72,64 | 73,2 | 10,68 | –0,05 | 0,59 |
| Varones, proporción | 0,64 | 0,62 | 0,49 | 0,06 | 0,542 |
| Etiología IC isquémica, proporción | 0,35 | 0,31 | 0,46 | 0,08 | 0,405 |
| IC previa, proporción | 0,61 | 0,62 | 0,49 | –0,03 | 0,763 |
| Diabetes mellitus, proporción | 0,47 | 0,47 | 0,5 | 0,01 | 0,922 |
| Hipertensión arterial, proporción | 0,8 | 0,77 | 0,42 | 0,06 | 0,55 |
| EPOC, proporción | 0,16 | 0,16 | 0,37 | 0 | 1 |
| SAHOS, proporción | 0,12 | 0,12 | 0,32 | 0,01 | 0,879 |
| Ictus, proporción | 0,11 | 0,12 | 0,32 | –0,01 | 0,877 |
| Enfermedad vascular periférica, proporción | 0,13 | 0,1 | 0,3 | 0,08 | 0,357 |
| Frecuencia cardiaca (lpm), media | 89,7 | 90,9 | 28,07 | –0,04 | 0,655 |
| Presión arterial sistólica (mmHg), media | 135,86 | 132,95 | 26,71 | 0,1 | 0,285 |
| Fibrilación auricular, proporción | 0,42 | 0,48 | 0,5 | –0,11 | 0,278 |
| Hemoglobina (g/l), media | 122,3 | 121,5 | 22,2 | 0,03 | 0,73 |
| Filtrado glomerular (CKD–EPI), media | 58,55 | 57,71 | 24,31 | 0,03 | 0,728 |
| NT-proBNP ≥ 1.500 ng/l, proporción | 0,56 | 0,57 | 0,5 | –0,02 | 0,843 |
| NT-proBNP (como dato no disponible), proporción | 0,33 | 0,3 | 0,46 | 0,06 | 0,526 |
| Índice de Charlson, media | 3,63 | 3,63 | 2,89 | 0 | 1 |
| Índice de Barthel, media | 87,64 | 88,05 | 23,3 | –0,02 | 0,855 |
| Índice de Pfeiffer, media | 0,95 | 0,95 | 1,55 | 0 | 1 |
| IECA o ARA-II, proporción | 0,71 | 0,71 | 0,45 | –0,01 | 0,914 |
| Bloqueadores beta, proporción | 0,68 | 0,63 | 0,48 | 0,1 | 0,303 |
| Antialdosterónicos, proporción | 0,39 | 0,38 | 0,49 | 0,02 | 0,84 |
ARA-II: antagonistas del receptor de la angiotensina II; CKD-EPI: Chronic Kidney Disease Epidemiology Collaboration; DE: desviación estándar; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; ICFEc: insuficiencia cardiaca con fracción de eyección conservada; ICFEi: insuficiencia cardiaca con fracción de eyección intermedia; IECA: inhibidor de la enzima de conversión de la angiotensina; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; SAHOS: síndrome de apnea-hipopnea obstructiva del sueño.
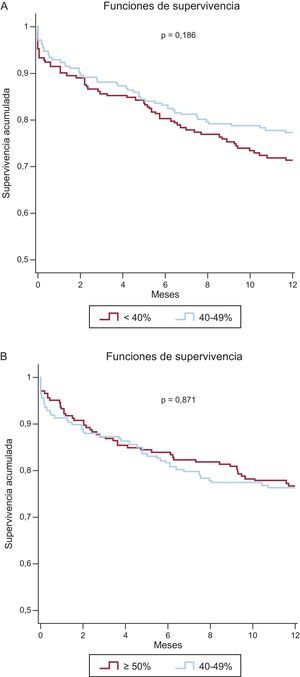
Siguiendo el modelo de regresión de Cox con la variable explicativa grupo de FEVI, se realizaron análisis de supervivencia a los 12 meses en las cohortes emparejadas, sin que se identificasen diferencias significativas en la mortalidad por cualquier causa entre los grupos de ICFEi e ICFEd (hazard ratio [HR] = 0,77; IC95%, 0,53-1,13; p = 0,19) ni entre los grupos de ICFEi e ICFEc (HR = 1,03; IC95%, 0,69-1,54; p = 0,87). En las figuras 2A y B se muestran las curvas de Kaplan-Meier de supervivencia al año de las cohortes emparejadas.
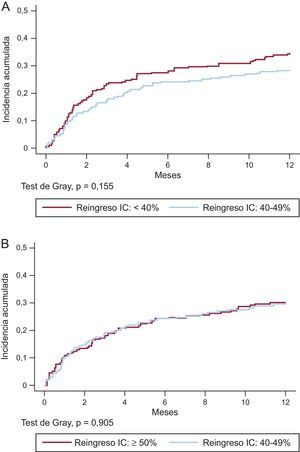
Tampoco se observaron diferencias significativas en los reingresos por IC (figuras 3A y B) y la distribución de las causas de muerte al año (tabla 2A y tabla 2B del material suplementario) en las cohortes emparejadas, aunque se observaba una tendencia a mayores tasas de reingresos por IC y de muerte por progresión de la IC en el grupo de ICFEd.
DISCUSIÓNLos hallazgos más relevantes de nuestro estudio indican que la nueva categorización de pacientes con ICFEi identifica una población con características clínicas de transición entre el grupo de ICFEd y el de ICFEc, pero no discrimina un grupo con peor pronóstico.
En nuestro conocimiento se describen por primera vez las características y el pronóstico de una cohorte de pacientes hospitalizados con ICFEi (FEVI 40-49%), nueva categoría incluida en la reciente guía de diagnóstico y tratamiento de la IC de la ESC1. La FEVI en pacientes con diagnóstico de IC constituye un continuo y es un parámetro que clásicamente ha permitido clasificar 2 patrones fenotípicos de la enfermedad (ICFEd e ICFEc) que presentan diferencias en sus características clínicas. La prevalencia de ambos patrones de IC varía en los diferentes registros en función de la procedencia de los pacientes12–15. En el registro europeo de IC (ESC-HF Long-Term Registry), la prevalencia de IC con FEVI > 45% entre los pacientes hospitalizados era del 32,8% y entre los pacientes ambulatorios con IC crónica, del 23,1%12. En el registro americano de IC aguda (OPTIMIZE-HF), la prevalencia de IC con FEVI ≥ 40% era del 51,2%13. En nuestro registro, la prevalencia de ICFEd, ICFEi e ICFEc son del 41, el 16 y el 43% respectivamente, lo que supone que el 59% tenía FEVI ≥ 40%, en la línea del registro OPTIMIZE-HF y otros registros contemporáneos. Debe tenerse en cuenta el punto de corte para definir las formas de IC en los diferentes registros, ya que podría condicionar las comparaciones entre ellos.
Tradicionalmente los pacientes con FEVI deprimida suelen ser más jóvenes, predominantemente varones y con elevada prevalencia de cardiopatía isquémica; por el contrario, las series de ICFEc muestran predominio del sexo femenino, edad más avanzada y elevada prevalencia de hipertensión arterial, diabetes mellitus y fibrilación auricular.
En este sentido, una publicación reciente del TOPCAT donde se analizan las características basales y el pronóstico de los pacientes según 4 grupos de FEVI (45-49%, 50-54%, 55-59%, ≥ 60%) encuentra que el grupo con FEVI 45-49% tiene una mayor proporción de varones y de cardiopatía isquémica que los grupos con mayor FEVI16.
Múltiples registros y ensayos clínicos han analizado, con hallazgos dispares, el pronóstico y sus determinantes en pacientes con IC, con FEVI tanto deprimida como conservada13,17–23. En general, los grupos de pacientes crónicos con ICFEd suelen mostrar una mortalidad significativamente mayor que aquellos con ICFEc; sin embargo, los registros que incluyen a los pacientes durante la hospitalización suelen mostrar un pronóstico similar. Publicaciones del registro MAGGIC describen un peor pronóstico de la ICFEd, aunque sin mencionar de manera específica el origen hospitalario o ambulatorio de los pacientes incluidos17. En el registro OPTIMIZE-HF se describe una mortalidad hospitalaria no ajustada ligeramente superior en ICFEd (FEVI < 40%) que en IC con FEVI ≥ 40% (el 3,9 frente al 2,9%; OR = 1,34; p < 0,0001), pero sin diferencias entre los grupos de IC con FEVI 40-50% y FEVI > 50% (el 3,0 frente al 2,9%; p = 0,65)13. En el seguimiento a 60-90 días no hubo diferencias significativas entre los grupos en la mortalidad y las rehospitalizaciones. Un estudio reciente, que incluye algo más de 19.000 pacientes beneficiarios de Medicare dados de alta con el diagnóstico principal de IC, compara la estancia hospitalaria, la mortalidad y los reingresos a 30 días entre los grupos de ICFEd e ICFEc y encuentra tasas ajustadas de mortalidad ligeramente mayores para la ICFEd (el 10% de más mortalidad al mes), aunque con tasas similares de reingreso a 30 días15. Cabe destacar que en este estudio se asignó a los pacientes a un tipo de IC u otro según el código de diagnóstico al alta, sin especificar el punto de corte de FEVI empleado. Otras publicaciones que incluyen a pacientes hospitalizados describen una mortalidad similar entre la deprimida y la conservada, y la muerte relacionada con la IC (muerte súbita o muerte por progresión de la IC) es la principal causa de mortalidad en ambas, aunque con mayor peso de la muerte cardiovascular no relacionada con la IC en el grupo con FEVI conservada18,19,22,23.
Los resultados de nuestro estudio son acordes con lo descrito en series de pacientes hospitalizados, ya que entre los grupos de FEVI deprimida, conservada o intermedia no se observan diferencias significativas en la mortalidad en el seguimiento (1, 6 y 12 meses) y en los reingresos por IC. El abordaje estadístico empleado en nuestro análisis, en el que se emparejan los grupos de pacientes para minimizar el sesgo que supone estudiar el efecto de los grupos de FEVI a partir de un estudio observacional, permite obtener conclusiones más robustas en este tipo de comparaciones.
LimitacionesEl registro REDINSCOR II incluye una cohorte de pacientes hospitalizados por descompensación de IC o IC de novo en servicios de cardiología españoles y seguidos prospectivamente durante 1 año. Por lo tanto, nuestros resultados se limitan a ese grupo de pacientes, de los que se tiene información más escasa, ya que la mayoría de los registros incluyen a pacientes ambulatorios crónicos y estables o mezclan ambos grupos de pacientes.
Hubo un porcentaje no despreciable de pacientes (411 [22,4%]) a los que no se incluyó en este análisis por falta de determinación de la FEVI al ingreso o en los 6 meses previos, aunque cuando se los comparó con el grupo analizado no se observaron diferencias significativas en mortalidad u hospitalizaciones por IC.
Por otro lado, la división de los grupos se llevó a cabo con la FEVI obtenida durante la hospitalización, en una fase de inestabilidad clínica. Por lo tanto, se desconoce la evolución de la FEVI durante el seguimiento, en el que podría haber pacientes que sufrieran cambios dinámicos en esta, en particular recuperando la FEVI y pasando de ICFEd a ICFEi o ICFEc. Los valores obtenidos de FEVI, la mayoría (76,3%) durante la hospitalización, fueron los descritos por los investigadores de cada centro (cardiólogos) sin una auditoría de sus resultados, por lo que podría haber cierta variabilidad de la medición que supusiese reclasificaciones de los pacientes dentro de los grupos de FEVI y condicionase de alguna forma nuestros resultados. El tratamiento es el pautado al alta hospitalaria, por lo que tampoco se puede confirmar que sea la estrategia terapéutica mantenida durante todo el seguimiento, hecho que podría tener algún tipo de influencia en el pronóstico.
Aunque pudieran existir limitaciones a la hora de clasificar las causas de muerte, en especial la mortalidad extrahospitalaria, es la primera vez que se describen específicamente las causas de muerte de pacientes con ICFEi, y no se observan diferencias significativas entre los tres grupos analizados, ni en el análisis general ni en el de grupos emparejados.
Si bien no se han encontrado diferencias estadísticamente significativas en la comparación de grupos con magnitudes clínicamente relevantes, es posible que la falta de potencia estadística en estas comparaciones pueda condicionar en cierto modo nuestros resultados. Por otra parte, a pesar de que el análisis por puntuación de propensión emparejada es más robusto que las regresiones clásicas, adolece de ciertas debilidades, como que no es posible corregir ciertos factores de confusión no medidos, con lo que siempre queda un margen de confusión residual.
CONCLUSIONESSe describen por primera vez de manera específica las características clínico-epidemiológicas y el pronóstico al año de pacientes hospitalizados con ICFEi. Se observa que este nuevo grupo comparte características con los otros dos patrones (ICFEc e ICFEd), aunque con mayor similitud con el grupo de FEVI conservada. Tras un seguimiento prospectivo de 1 año, no se observan diferencias entre los 3 grupos de pacientes en la mortalidad total, las causas de muerte y la necesidad de rehospitalización por IC.
CONFLICTO DE INTERESESNinguno.
Este estudio se ha realizado con el respaldo del Programa de Insuficiencia Cardiaca de la Red de Investigación Cardiovascular del Instituto de Salud Carlos III, Madrid, España (RD12/0042) y el Fondo Europeo de Desarrollo Regional (FEDER).
Se puede consultar la lista de los investigadores de la Red Española de Insuficiencia Cardiaca en el apéndice del material suplementario.