La cardiorresonancia magnética (CRM) es una herramienta diagnóstica bien establecida en medicina. Para mejorar la calidad de la imagen, a menudo se emplean sustancias químicas derivadas del gadolinio. Dado que los medios de contraste derivados del gadolinio (MCDG) se excretan principalmente por los riñones, los pacientes con una reducción de la función renal presentan un aumento del riesgo de retención de los MCDG, que implica un posible riesgo de fibrosis sistémica nefrogénica. Desde hace unos años se ha venido observando una hiperintensidad de señal de resonancia magnética debida a la retención de gadolinio en el sistema nervioso central de pacientes a los que se han administrado múltiples dosis de MCDG a lo largo del tiempo, incluso cuando la función renal es normal1. Esto llevó a que la Food and Drug Administration de Estados Unidos, la agencia de productos sanitarios de Japón y la Agencia Europea de Medicamentos hicieran advertencias públicas al respecto. En el ámbito de la cardiología, las exploraciones de imagen desempeñan también un papel importante en un campo en rápida expansion, el de la ablación percutánea de la fibrilación auricular (FA). El objetivo de este estudio es evaluar la viabilidad y aplicabilidad de un protocolo sin uso de MCDG para la evaluación anatómica del corazón para el aislamiento de las venas pulmonares.
En una serie de pacientes consecutivos remitidos para ablación percutánea de la fibrilación auricular, la adquisición de imágenes de CRM se realizó con un protocolo sin uso de MCDG. El estudio se realizó cumpliendo los criterios establecidos en la declaración de Helsinki y se obtuvo el consentimiento informado de cada uno de los participantes en el estudio.
La CRM se realizó con escáneres de 1,5 T (Magnetom Avanto/Espree, Siemens, Alemania). Se utilizó una secuencia de precesión sin equilibrio estable, con sincronización respiratoria de navegador y respiración libre, tridimensional. Con este método se reduce al mínimo el movimiento respiratorio al adquirir los datos dentro de una ventana de sincronización pequeña en una posición respiratoria predefinida. Los parámetros de CRM fueron: TR, 206,50ms; TE, 1,2ms; ángulo de flip, 90°. La ventana de adquisición y el retraso del disparo dependieron de cada paciente. El tamaño de vóxel fue de 0,9 × 0,9 × 2,0 mm3. El grosor de corte fue de 2mm, con un sobremuestreo de cortes de un 20%. El tiempo de adquisición de la CRM se determinó desde el inicio del primer examen hasta el final del último y la duración del examen fue la transcurrida desde el inicio hasta el final de la secuencia de precesión sin equilibrio estable.
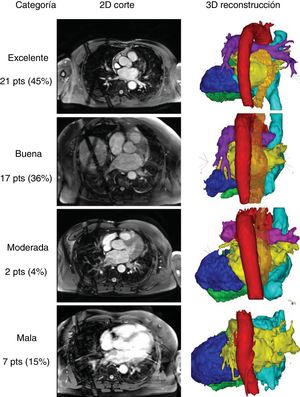
La segmentación y reconstrucción se realizaron con el programa informático CartoMerge (Biosense Webster, Estados Unidos). En primer lugar, se estableció un filtro de umbral basado en la intensidad de la imagen para excluir los vóxeles con una intensidad de imagen inferior a la de los vóxeles de la estructura cardiaca de interés. En segundo lugar, se señalaron las cámaras de interés con puntos en su superficie para una segmentación basada en un algoritmo de crecimiento de la región. Si las cámaras no se segmentaban correctamente, se permitió un procesado manual para eliminar las estructuras no relevantes o crear unos límites detectables. Por último, se realizaron reconstrucciones de superficie tridimensionales. La evaluación cualitativa se basó en la facilidad de segmentación y la calidad de las cámaras cardiacas reconstruidas para mostrar con exactitud la anatomía y la orientación de la vena pulmonar hasta la primera bifurcación. Las reconstrucciones se clasificaron como: excelente (sin interacción manual), buena (poca interacción manual), moderada (interacción manual amplia) y mala (no fue posible reconstruir la anatomía de la aurícula izquierda [AI] y la orientación de la vena pulmonar). En la figura 1 se muestran ejemplos representativos de estas categorías. La segmentación del esófago se realizó después de la segmentación cardiaca debido a su menor intensidad de señal.
Ejemplos de cortes bidimensionales (2D) y reconstrucciones tridimensionales (3D). Clasificación: excelente (sin interacción manual); buena (poca interacción manual); moderada (interacción manual amplia); mala (no fue posible reconstruir la anatomía de la aurícula izquierda y la orientación de la vena pulmonar). Rojo: aorta; amarillo: aurícula izquierda; naranja: esófago; azul claro: aurícula derecha; azul oscuro: ventrículo izquierdo; verde: ventrículo derecho; pts.: pacientes. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
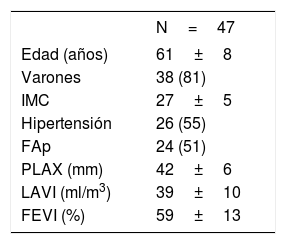
Se incluyó a 47 pacientes en el estudio. En la tabla 1 se presentan las características iniciales y los datos ecocardiográficos de los pacientes. Se pudo obtener una visualización completa del corazón, incluidas todas las cámaras cardiacas y el esófago, en 40 pacientes. El tiempo de adquisición y la duración del examen fueron de 25,8 (22,0-32,5) y 8,3 (6,3-11,5) min respectivamente. La calidad de imagen fue suficiente (excelente, buena o moderada) para todas las estructuras cardiacas y segmentos en el 85% de los pacientes. Se pudo visualizar y segmentar el esófago en el 91% de los pacientes. No pudieron identificarse diferencias entre las exploraciones con calidad suficiente y las malas en ninguno de los datos iniciales o de la exploración.
Características basales
| N=47 | |
|---|---|
| Edad (años) | 61±8 |
| Varones | 38 (81) |
| IMC | 27±5 |
| Hipertensión | 26 (55) |
| FAp | 24 (51) |
| PLAX (mm) | 42±6 |
| LAVI (ml/m3) | 39±10 |
| FEVI (%) | 59±13 |
FAp: fibrilación auricular paroxística; FEVI: fracción de eyección del ventrículo izquierdo; IMC: índice de masa corporal; LAVI: volumen auricular izquierdo indexado; PLAX: tamaño de la aurícula izquierda en el eje longitudinal paraesternal.
Los valores expresan n (%) o media ± desviación estándar.
Los principales resultados de este estudio son: a) el protocolo de adquisición sin uso de MCDG fue viable sin complicaciones en todos los pacientes remitidos para ablación percutánea de la fibrilación auricular; b) la evaluación anatómica del corazón y en concreto la de la AI para las intervenciones electrofisiológicas con un protocolo de CRM nativa sin uso de contraste es factible en el 85% de los pacientes, y c) el trayecto del esófago se pudo visualizar en el 91% de los pacientes.
Además de la posible toxicidad de los MCDG, se han documentado también otras complicaciones muy infrecuentes, como las reacciones alérgicas2. Con un protocolo de adquisición sin uso de MCDG, es posible prevenirlas. Por otra parte, no se requiere una vía venosa para la inyección de contraste. Además de la posible reducción de las complicaciones, se pueden visualizar las cámaras cardiacas derechas, lo que facilita la colocación de catéteres y la punción transeptal. Para visualizar el trayecto y la anchura del esófago, se ha descrito el empleo de un mapeo electroanatómico con el catéter de ablación3 o la visualización radiológica de la papilla baritada deglutida4. Se puede realizar una evaluación no invasiva previa a la intervención usando, por ejemplo, una secuencia de RM con realce tardío de gadolinio tridimensional, que permite visualizar el trayecto y la anchura del esófago además de la presencia de fibrosis en la AI5. A diferencia de lo que ocurre con estas estrategias complejas o invasivas, el método de CRM sin MCDG brinda la posibilidad de usarlo como evaluación simplificada del corazón y las estructuras circundantes previa a la intervención. Los candidatos ideales podrían ser los pacientes que pueden estar cómodos en decúbito supino y tienen un patrón respiratorio y un intervalo RR regulares. Sin embargo, no se ha determinado aún si la visualización del esófago y su posición respecto a la AI y las lesiones de ablación pueden prevenir complicaciones como la fístula auriculoesofágica.
En conclusión, la evaluación anatómica de todo el corazón y en particular de la AI para las intervenciones electrofisiológicas con un protocolo de RM nativa sin uso de contraste es suficiente en el 85% de los pacientes. A pesar de la duración relativamente larga de la adquisición, el protocolo resulta especialmente útil en los pacientes con insuficiencia renal o para visualizar el trayecto del esófago además de la anatomía del corazón.
CONFLICTO DE INTERESESM. Kühne es mentor de Medtronic, forma parte del panel de conferenciantes de Boston Scientific, St. Jude Medical y Biotronik. C. Sticherling forma parte del consejo asesor de Medtronic y Biotronik, ha recibido subvenciones de formación de Biotronik y una subvención de investigación de Biosense Webster, sin relación con el trabajo presentado.