Palabras clave
INTRODUCCIÓN
La clasificación de Thrombolysis in Myocardial Infarction (TIMI) y el parámetro denominado grado de perfusión miocárdica (GPM) son marcadores angiográficos de la eficacia de la reperfusión coronaria a nivel de la arteria epicárdica y de la microcirculación1,2. Estos marcadores predicen la evolución clínica adversa, incluida la mortalidad a corto3,4 y largo plazo2,5,6. Hay interrelación e interdependencia entre estos marcadores. El restablecimiento de un flujo epicárdico óptimo es un requisito para restablecer una reperfusión microcirculatoria normal3,4 y ello es condición necesaria para que haya un flujo sin impedimentos en el sistema coronario epicárdico. Stone et al3 y Constantini et al4, así como un trabajo anterior de nuestro propio grupo7, pusieron de manifiesto que ninguno de los pacientes con un restablecimiento subóptimo del flujo epicárdico (grado TIMI ≤ 2) alcanzó un flujo microcirculatorio óptimo (GPM 3). El restablecimiento de un flujo epicárdico subóptimo (grado TIMI ≤ 2) denota un aumento de la resistencia coronaria segmentaria como consecuencia de una obstrucción vascular importante, y se asocia a una necrosis miocárdica extensa, una reducción del rescate miocárdico con la intervención coronaria percutánea (ICP) primaria, un remodelado ventricular izquierdo negativo y un aumento de la mortalidad8,9. No obstante, el restablecimiento de un flujo sanguíneo epicárdico normal (grado TIMI 3) no implica una reperfusión micro-circulatoria óptima. En varios estudios se ha demostrado que una parte considerable de los pacientes con un grado TIMI 3 presenta una reperfusión miocárdica subóptima en la microcirculación3-5. Específicamente, sigue habiendo controversia respecto al valor pronóstico del GPM 23-6,10.
En este estudio, hemos analizado el valor pronóstico del GPM en pacientes con infarto de miocardio con elevación del segmento ST (IAMEST) en los que se restableció un flujo de grado TIMI 3 mediante una ICP primaria. El objetivo del estudio fue doble: en primer lugar, evaluar la relación entre GPM, área inicial en riesgo, rescate miocárdico y tamaño del infarto, y en segundo lugar, la repercusión pronóstica del GPM en la mortalidad a largo plazo (5 años). La exclusión de los pacientes con un grado TIMI ≤ 2 redujo la interferencia de las variaciones del flujo sanguíneo epicárdico y permitió evaluar la influencia pura del GPM en los resultados clínicos.
MÉTODOS
Pacientes
Formaron la muestra principal del estudio 1.861 pacientes con IAMEST que acudieron en las 24 h siguientes al inicio de los síntomas al Deutsches Herzzentrum y el Medizinische Klinik rechts der Isar de Múnich entre enero de 2002 y diciembre de 2007. Se ha presentado una información detallada sobre la muestra principal del estudio en otro trabajo de nuestro grupo7. Tras la exclusión de los pacientes en los que se utilizó un tratamiento conservador (n = 112) y de aquellos en los que se utilizó como estrategia primaria de reperfusión la trombolisis o la cirugía de bypass arterial coronario (n = 53), los casos de fallos mecánicos en el intento de desobstruir arterias coronarias ocluidas (n = 31), los casos en que no se dispuso de exploraciones gammagráficas (n = 173) o los datos eran de calidad insuficiente (n = 86) y los pacientes con un flujo TIMI ≤ 2 (n = 193), quedó un total de 1.213 pacientes con IAMEST y un flujo de grado TIMI 3 al final de la ICP primaria, que fueron los incluidos en este estudio. Se realizaron dos exploraciones gammagráficas a todos los pacientes del estudio, una antes y otra 7-14 días después de la ICP. El diagnóstico de IAMEST se estableció por dolor torácico de duración > 20 min asociado a alteraciones electrocardiográficas (elevación del segmento ST ≥ 1 mm en al menos dos derivaciones electrocardiográficas de extremidades o ≥ 2 mm en al menos dos derivaciones precordiales contiguas o bloqueo de rama izquierda del haz de nueva aparición). El diagnóstico se confirmó mediante angiografía coronaria en todos los pacientes. La gravedad de la insuficiencia cardiaca se evaluó con la clasificación de Killip11.
Análisis angiográfico
La angiografía coronaria se llevó a cabo aplicando criterios estándar. Se realizó un análisis de las angiografías digitales después de terminada la exploración en el laboratorio central, con el empleo de un sistema de detección automática de bordes (CMS; Medis Medical Imaging Systems, Neuen, Países Bajos), sin que quienes lo realizaban conocieran el diagnóstico clínico. La ICP primaria (mayoritariamente con implantación de stents) y la asistencia periintervención se llevaron a cabo con criterios estándar. Se utilizaron stents (en su mayor parte de tipo metálico sin recubrimiento) en el 88% de los pacientes (n = 1.066). El tratamiento antiagregante plaquetario consistió en clopidogrel (600 mg en dosis de carga, seguida de 75 mg/día durante un periodo de al menos 4 semanas y hasta 6 meses) y ácido acetilsalicílico (200 mg/día por tiempo indefinido).
Se determinó el grado del flujo sanguíneo epicárdico en la arteria relacionada con el infarto, así como el GPM, utilizando las definiciones del grupo TIMI1. El grado TIMI del flujo se definió de la siguiente forma: TIMI 0, ausencia de perfusión (ausencia de flujo anterógrado más allá del punto de la oclusión); TIMI 1, penetración sin perfusión (el medio de contraste supera el área de la obstrucción, pero no opacifica la totalidad del lecho coronario distal a la obstrucción durante el periodo de grabación de imágenes); TIMI 2, reperfusión parcial (el medio de contraste supera la obstrucción y opacifica el lecho coronario distal a la obstrucción, con una rapidez de entrada y de eliminación del lecho distal perceptiblemente inferior a la de su entrada y/o desaparición de otras áreas comparables perfundidas por una arteria contralateral no relacionada con el infarto o con el lecho coronario proximal a la obstrucción); TIMI 3, perfusión completa (el medio de contraste entra y sale del lecho distal a la obstrucción con la misma rapidez que en el lecho proximal a la obstrucción o en el lecho arterial coronario contralateral no afectado).
El GPM se definió de la siguiente forma: GPM 0, el contraste no entra en la microcirculación; GPM 1, el medio de contraste entra lentamente, pero no sale de la microcirculación; GPM 2, retraso en la entrada y la salida del medio de contraste en la microcirculación; GPM 3, entrada y salida del contraste en la microcirculación normales1. En una muestra de 50 pacientes, las coincidencias en cada observador y entre observadores fueron del 94% (47/50) y del 88% (44/50), respectivamente, en la determinación del GPM. No se observó ninguna discrepancia > 1 en la determinación del GPM.
Exploración gammagráfica
Se realizó una tomografía computarizada de emisión monofotónica (SPECT) con 99mTc-sestamibi en la situación basal (antes de la ICP) y a los 7-14 días de practicada la ICP. Se administró a los pacientes una inyección intravenosa de 27 mCi (1.000 MBq) de 99mTc-sestamibi y se realizó la SPECT 6-8 h después de la inyección del agente radiactivo. Para obtener las imágenes miocárdicas, se utilizó un sistema de cámara de multicabezal, equipada con colimadores de alta resolución y baja energía. La adquisición de imágenes se realizó en una matriz de 64 × 64 con un tiempo de adquisición de 40 s por imagen. La reconstrucción de cortes transaxiales se llevó a cabo con un programa informático específico para este fin (ICON versión 6.0.2). Se utilizó un instrumento de muestreo volumétrico para crear mapas polares de la distribución relativa en todo el ventrículo izquierdo. Cada mapa polar se normalizó respecto a su máximo individual. El tamaño del defecto se definió como el área con una captación < 50%. Los parámetros gammagráficos fueron los siguientes: defecto de perfusión inicial (defecto de perfusión en la gammagrafía basal, antes de la intervención), tamaño final del infarto (defecto de perfusión en la gammagrafía de seguimiento), rescate absoluto (defecto de perfusión inicial menos tamaño del infarto final) e índice de rescate (defecto de perfusión inicial menos tamaño del infarto final dividido por el defecto de perfusión inicial). Los primeros tres parámetros se expresaron en forma de porcentaje del ventrículo izquierdo. El cuarto parámetro indica la proporción del defecto de perfusión inicial rescatada mediante la reperfusión. Todas las mediciones las llevaron a cabo en el laboratorio central de gammagrafía investigadores que no conocían el diagnóstico clínico.
Variables de valoración y seguimiento
La variable de valoración principal de este análisis fue la mortalidad a 5 años. Se evaluó también la extensión inicial del área en riesgo (defecto de perfusión inicial), el tamaño final del infarto y el índice de rescate en los grupos de pacientes con los distintos valores de GPM. La información de seguimiento se obtuvo mediante una llamada telefónica realizada a los 30 días, una visita a los 6 meses, una llamada telefónica al año y nuevas llamadas anuales posteriores. A los pacientes que referían manifestaciones clínicas cardiacas se les realizó una evaluación clínica, electrocardiográfica y de laboratorio completa. Se obtuvo información respecto a la muerte de los pacientes a partir de las historias clínicas hospitalarias, los certificados de defunción o el contacto telefónico con familiares del paciente o con el médico que lo había remitido. De la obtención de la información de seguimiento se encargaron investigadores que no conocían las características clínicas ni angiográficas de los pacientes.
Análisis estadístico
Los datos se presentan en forma de mediana (con los percentiles 25-75) o porcentaje. La prueba de Kolmogorov-Smirnov para una muestra puso de manifiesto una distribución no normal de los datos para todas las variables continuas. Los datos de variables discretas se compararon con la prueba de la χ2. Los de variables continuas se compararon con la prueba de suma de rangos de Kruskal-Wallis. La estimación de la mortalidad a 5 años se efectuó aplicando el método de Kaplan-Meier y el log-rank test, que permite calcular las odds ratio (OR) (con sus intervalos de confianza [IC] del 95% y los valores de p correspondientes) asociadas a los diversos grados GPM. La asociación entre GPM y mortalidad a 5 años se evaluó con el modelo de riesgos proporcionales de Cox. Con objeto de reducir el sobreajuste del modelo, se introdujeron en él los datos de GPM y los parámetros de las tablas 1 y 2 que mostraban un valor de p < 0,05, con la exclusión de la creatincinasa y la troponina cardiaca (se introdujo en su lugar el tamaño gammagráfico del infarto en la gammagrafía obtenida a los 7-14 días). Todos los análisis se llevaron a cabo con el programa estadístico S-plus (S-PLUS, Insightful Corp., Seattle, Washington). Se consideró que un valor de p < 0,05 indica significación estadística.
RESULTADOS
Características basales
Se incluyó en este estudio a 1.213 pacientes con IAMEST y un flujo de grado TIMI 3 al final de una ICP primaria. En total, 217 pacientes tenían un GPM 0-1, 195 tenían un GPM 2 y 801, un GPM 3. En la tabla 1 se presentan las características clínicas basales de los tres grupos. No había diferencias significativas entre los grupos en cuanto a edad, proporción de pacientes con antecedentes de cirugía de bypass arterial coronario previo, localización del infarto, clase Killip, actividad de la fracción MB de la creatincinasa, concentraciones de troponina cardiaca, proteína C reactiva y creatinina sérica y tiempo hasta el ingreso. Es interesante señalar que los grupos con GPM 0-1 y 2 muestran pocas diferencias en cuanto a casi todas las características basales (con la excepción de la ubicación del infarto en la cara anterior, que fue más frecuente en los pacientes con un GPM 2), lo cual indica que ambos grupos tienen perfiles de riesgo cardiovascular similares. En cambio, el grupo de GPM 3 presentaba un perfil de riesgo cardiovascular más favorable, y este grupo era la principal fuente de las tendencias indicativas de diferencias estadísticamente significativas entre los grupos. Las características angiográficas se presentan en la tabla 2. Los pacientes con un GPM 3 presentaban una fracción de eyección ventricular izquierda superior a la de los otros dos grupos. Había diferencias en lo relativo a la arteria relacionada con el infarto. Los pacientes con GPM 3 presentaban un porcentaje inferior de casos con un TIMI 0 o 1 previo a la intervención y un porcentaje más elevado de pacientes con un TIMI 2 o 3 que los otros dos grupos. Es interesante señalar que entre los pacientes con un GPM 3 había un porcentaje más elevado de casos en los que no se documentó ninguna circulación colateral en la angiografía, en comparación con lo observado en los pacientes con GPM 0-1 o 2 (tabla 2).
Datos gammagráficos
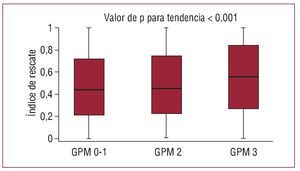
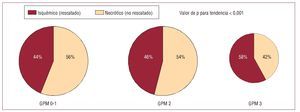
Los resultados de las exploraciones gammagráficas se presentan en la tabla 3. Según lo indicado en dicha tabla, los cuatro parámetros gammagráficos parecen diferir poco entre los pacientes con GPM 0-1 o 2. En comparación con los pacientes con un GPM 0-1 o 2, los que tenían un GPM 3 presentaban valores significativamente menores del defecto de perfusión inicial (equivalente al área de riesgo inicial) y del tamaño del infarto (defecto de perfusión en la gammagrafía realizada a los 7-14 días). Es de destacar que, en los pacientes con un GPM 3, el índice de rescate o la proporción del defecto de perfusión inicial rescatada mediante la ICP primaria fue significativamente superior a lo observado en los pacientes con GPM 0-1 o 2 (fig. 1). Con el empleo del índice de rescate (proporción del defecto de perfusión inicial rescatado), se estimaron las proporciones de isquemia/necrosis del área de riesgo inicial (fig. 2). En la figura se muestra que la proporción de tejido rescatado (isquémico) en el área de riesgo inicial fue significativamente mayor en los pacientes con GPM 3 que en los pacientes con GPM 0-1 o 2. En cambio, la parte necrótica (proporción del defecto de perfusión inicial no rescatado mediante la reperfusión) fue más prominente en los pacientes con GPM 0-1 o 2 que en los que tenían un GPM 3 (fig. 2).
Fig. 1. Índice de rescate (proporción del defecto de perfusión inicial que se rescata mediante la ICP primaria) en los distintos grupos de GPM. ICP: intervención coronaria percutánea; GPM: grado de perfusión miocárdica
Fig. 2. Proporción del defecto de perfusión inicial rescatada (isquémica) y no rescatada (necrótica) en los distintos grupos de GPM. GPM: grado de perfusión miocárdica.
Grado de perfusión miocárdica y mortalidad a 5 años
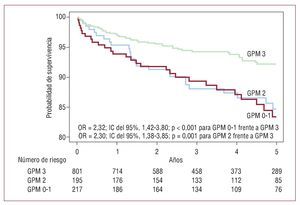
La mediana [percentiles 25-75] de seguimiento fue de 4,1 [2,1-4,9] años. Se produjeron 101 muertes durante el seguimiento: 28 pacientes con GPM 0-1, 25 pacientes con GPM 2 y 48 pacientes con GPM 3 (estimaciones de Kaplan-Meier de la mortalidad a 5 años, el 16,6, el 15,3 y el 7,8%, respectivamente; OR = 2,32; IC del 95%, 1,42-3,8; p < 0,001 para GPM 0-1 frente a GPM 3, y OR = 2,3; IC del 95%, 1,38-3,85; p = 0,001 para GPM 2 frente a GPM 3) (fig. 3).
Fig. 3. Curvas de Kaplan-Meier de la mortalidad a 5 años en pacientes con GPM 0-1, 2 y 3 tras una ICP primaria. IC: intervalo de confianza; ICP: intervención coronaria percutánea; GPM: grado de perfusión miocárdica; OR: odds ratio.
La asociación entre el GPM y la mortalidad por todas las causas a 5 años se analizó con el modelo de riesgos proporcionales de Cox (véanse las variables introducidas en el modelo en el apartado «Métodos»). Dado que la probabilidad a 5 años fue similar entre los pacientes con GPM 0-1 y con GPM 2, se combinaron estos dos grupos en uno solo, designado como GPM 0-2. El modelo de riesgos proporcionales de Cox identificó el GPM como parámetro independiente correlacionado con la mortalidad a 5 años (razón de riesgos [HR] ajustada = 0,65; IC del 95%, 0,41-0,97; p = 0,037 para GPM 3 frente a GPM 0-2). Otros parámetros correlacionados con la mortalidad a 5 años fueron los siguientes: edad (HR = 1,67; IC del 95%, 1,38-2,03; p < 0,001 para un aumento de edad de 10 años), clase de Killip (HR = 1,41; IC del 95%, 1,11-1,79; p = 0,005 para un aumento de 1 clase) y antecedentes de infarto de miocardio previo (HR = 2,14; IC del 95%, 1,29-3,55; p = 0,003).
DISCUSIÓN
En este estudio hemos evaluado las repercusiones del GPM en los índices de reperfusión gammagráficos y en la mortalidad a largo plazo en una serie relativamente amplia de pacientes con IAMEST tratados con una ICP primaria. Con objeto de evitar la variabilidad derivada de las determinaciones del GPM efectuadas en diferentes laboratorios12, todas las determinaciones de marcadores de la reperfusión se llevaron a cabo en un laboratorio central. Los principales resultados pueden resumirse de la siguiente forma: a) en los pacientes con un restablecimiento del grado TIMI 3, la reperfusión miocárdica subóptima (GPM ≤ 2) se asoció al área de riesgo inicial más amplia y a un menor rescate miocárdico mediante la ICP primaria; b) la reperfusión miocárdica subóptima se asoció a un aumento de la mortalidad por todas las causas hasta 5 años después del episodio agudo, y c) los pacientes con un IAMEST y GPM 0-1 o 2 parecen diferir poco en cuanto al área de riesgo inicial, la cantidad de miocardio rescatado con la ICP primaria, el tamaño del infarto y la mortalidad a 5 años.
Nuestro estudio puso de relieve que los pacientes con reperfusión tisular subóptima (GPM ≤ 2) presentaban unas áreas de riesgo iniciales más grandes en la cuantificación realizada mediante gammagrafía. En un estudio previo de Dibra et al10, el área de riesgo inicial no presentó diferencias significativas entre los pacientes con microcirculación obstruida (GPM 0-1) y los que tenían microcirculación permeable (GPM > 2). Sin embargo, en ese estudio10 se agrupó a los pacientes con GPM 2 y 3, mientras que en el estudio que se presenta aquí se analizó a los pacientes con GPM 2 como grupo aparte. En ambos estudios se observó un menor rescate miocárdico y un aumento del tamaño del infarto en los pacientes con una reperfusión tisular subóptima. En la misma línea de resultados, Angeja et al13 han descrito que el tamaño gammagráfico del infarto fue menor en los pacientes con restablecimiento de la reperfusión tisular.
La obtención de dos exploraciones gammagráficas nos permitió cuantificar las proporciones de tejido necrótico e isquémico del área de riesgo inicial. Nuestros datos aportan evidencia adicional sobre los componentes estructurales y funcionales de la obstrucción microvascular y falta de restablecimiento del flujo miocárdico (no-reflow) según lo propuesto por Galiuto et al14. Además, hemos observado que la parte necrótica del defecto de perfusión inicial fue mayor en los pacientes con GPM ≤ 2 que en los que tenían un GPM 3. Por consiguiente, los pacientes con un GPM 3 tenían una proporción superior de miocardio isquémico pero todavía viable en la zona del defecto de perfusión inicial. Esta observación podría tener importancia para explicar la evaluación angiográfica de la reperfusión tisular. Los estudios morfológicos de Kloner et al15 han puesto de relieve que la lesión celular miocárdica se produce antes que la lesión microvascular en el transcurso de la isquemia miocárdica, lo cual indica que el tejido microvascular es más resistente a la isquemia que el tejido miocárdico. En este estudio hemos utilizado la combinación de un trazador extracelular (medio de contraste), del que se supone que refleja la permeabilidad de la microcirculación2, con un trazador intracelular (99mTc-sestamibi), que presuntamente muestra la viabilidad del miocardio operativo circundante16. Por un lado, la presencia de áreas extensas de tejido miocárdico isquémico pero viable dentro de las áreas de riesgo iniciales en pacientes con una reperfusión tisular óptima explica el mayor rescate miocárdico, el menor tamaño del infarto y el mejor pronóstico de estos pacientes. Por otro lado, al desobstruir la arteria relacionada con el infarto mediante una ICP primaria, el lecho vascular de las áreas isquémicas puede permitir el flujo de una cantidad de sangre considerable como consecuencia de la vasodilatación inducida por la isquemia17. Esto podría tener dos consecuencias. En primer lugar, la entrada de un flujo de sangre superior al normal en el lecho vascular isquémico puede compensar la oclusión vascular segmentaria existente en el núcleo necrótico, con lo que se facilitaría un flujo sanguíneo epicárdico sin impedimento (grado TIMI 3). La redistribución de sangre hacia las regiones isquémicas y el menor tamaño de las áreas de riesgo iniciales podrían ser cruciales para explicar un flujo sanguíneo epicárdico normal a pesar de la obstrucción vascular segmentaria en pacientes con un flujo sanguíneo epicárdico preservado y diversos grados de reperfusión tisular subóptima. En segundo lugar, la opacificación de las regiones isquémicas por el contraste puede ocultar áreas con alteraciones de la reperfusión y, por lo tanto, dificultar la determinación de la perfusión tisular segmentaria, lo que limitaría la exactitud de los métodos angiográficos en la valoración de la reperfusión tisular12.
Varios estudios previos han investigado la asociación existente entre una perfusión tisular subóptima y el aumento de la mortalidad en pacientes con IAMEST a los que se trata con una técnica de reperfusión3-6. En los pacientes con infarto agudo de miocardio y restablecimiento de un flujo de grado TIMI 3 mediante angioplastia, Henriques et al5 no observaron diferencias de supervivencia entre los pacientes con GPM 2 o 3 en un periodo medio de seguimiento de 16 meses. Haager et al6 han publicado resultados similares. En los estudios de Stone et al3 y Constantini et al4, los pacientes con GPM 2 presentaron una curva de supervivencia diferenciada, que era intermedia entre las curvas de supervivencia de los pacientes con GPM 0-1 y de los pacientes con GPM 3. La observación novedosa que aporta el presente estudio es el hecho de que los pacientes con GPM 0-1 o 2 tuvieran una mortalidad a 5 años similar. Por el momento no se conocen las razones de la discrepancia entre esos estudios previos y el que aquí se presenta en cuanto a la mortalidad. Es interesante señalar que los pacientes con GPM 0-1 o 2 presentaban una notable semejanza en cuanto al riesgo basal, el área de riesgo inicial, la cantidad de miocardio rescatado y el tamaño del infarto. Estas semejanzas pueden estar en la base de la observación de una mortalidad a largo plazo similar e indican claramente que el GPM 2 no es un índice de la perfusión tisular óptima y no debe considerarse un signo angiográfico benigno. En un estudio de 27 pacientes con IAMEST, Porto et al18 han puesto de relieve que los pacientes con un GPM 2 presentan una perfusión relativamente preservada, similar a la de los pacientes con un GPM 3, pero con un tamaño del infarto mayor, similar al de los pacientes con GPM 0-1. Así pues, el estudio de Porto et al18 y el presente indican que, al evaluar los resultados de la reperfusión tisular tras la ICP primaria, no está justificada la agrupación de los pacientes con un GPM 2 y los que tienen un GPM 3 y que estos grupos deben analizarse por separado al evaluar la repercusión pronóstica del GPM.
CONCLUSIONES
En los pacientes con un IAMEST y restablecimiento de grado TIMI 3 mediante una ICP primaria, la reperfusión miocárdica subóptima (GPM ≤ 2) se asoció a áreas de riesgo iniciales más grandes, menor rescate miocárdico, mayor tamaño del infarto y aumento de la mortalidad a 5 años respecto a los pacientes con restablecimiento de la perfusión tisular (GPM 3). Los pacientes con un GPM 2 no presentaron diferencias respecto a los pacientes con GPM 0-1 en lo relativo al área de riesgo inicial, la cantidad de miocardio rescatado, el tamaño del infarto o la supervivencia a 5 años.
ABREVIATURAS
GPM: grado de perfusión miocárdica.
IAMEST: infarto de miocardio con elevación del segmento ST.
IC: intervalo de confianza.
ICP: intervención coronaria percutánea.
TIMI: Thrombolysis in Myocardial Infarction.
Full English text available from: www.revespcardiol.org
Correspondencia: Dr. G. Ndrepepa.
Deutsches Herzzentrum.
Lazarettstrasse 36. 80636 München. Alemania.
Correo electrónico: ndrepepa@dhm.mhn.de
Recibido el 8 de enero de 2010.
Aceptado para su publicación el 22 de febrero de 2010.