El implante percutáneo de prótesis aórtica en pacientes con estenosis aórtica grave y alto riesgo quirúrgico es un procedimiento ya establecido por ser más efectivo que el tratamiento médico1 y similar o superior2 a la cirugía convencional según la experiencia acumulada con las prótesis de Edwards-SAPIEN (Edwards Lifesciences; Irvine, California, Estados Unidos) y Medtronic CoreValve (Medtronic; Minneapolis, Minnesotta, Estados Unidos) tanto en ensayos clínicos1,2 como en registros de práctica clínica3.
Recientemente se ha comercializado la prótesis DirectFlow4,5 (DirectFlow Medical; Santa Rosa, California, Estados Unidos), cuyas ventajas potenciales sobre los dispositivos ya existentes son la posibilidad de reposicionamiento/recaptura, la estabilidad hemodinámica durante el procedimiento y la baja tasa de insuficiencia aórtica significativa.
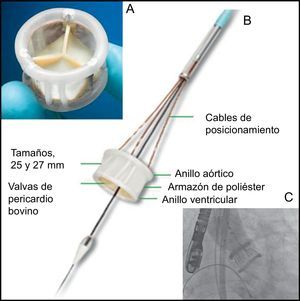
La prótesis DirectFlow (figura) no tiene elementos metálicos y su estructura es un sistema de vasos comunicantes que, al llenarse de líquido, configura dos anillos (entrada de fluidos por el anillo distal, salida por el proximal) unidos por un armazón de poliéster; el anillo inferior estabiliza la prótesis y el superior fija las 3 cúspides de pericardio bovino. El sistema de liberación está constituido por tres cables que se anclan al anillo inferior y permiten el llenado de los anillos y el posicionamiento y la liberación de la válvula.
A: prótesis DirectFlow vista desde la aorta. B: vista lateral de la prótesis y sistema de liberación (cables de posicionamiento y luz interna que alberga la guía de soporte). C: vista de la prótesis en posición con los 2 anillos llenos de contraste; en esta situación se valora la funcionalidad hemodinámica y la permeabilidad de las coronarias; en este momento todavía se puede reposicionar la prótesis e incluso recuperarla.
La válvula montada en su vaina (compatible con un introductor de 18 Fr) se avanza hasta el ventrículo izquierdo, donde se llenan ambos anillos con mezcla de contraste y agua. Se vacía entonces el anillo superior y se posiciona el inferior inmediatamente debajo de la válvula con la ayuda de los tres cables de tracción. Se llena entonces el anillo superior y se evalúan la posición, la funcionalidad y la permeabilidad coronaria. Si la posición no es óptima, se desinfla el anillo superior, se reposiciona el inferior, se vuelve a inflar el superior y se reevalúa el resultado. Cuando este es satisfactorio, se sustituye el contraste por un polímero que pasa a estado sólido en 10min y se liberan los cables de fijación.
Los criterios de selección son: anillo de 20–26mm (para válvulas de 25 y 27 mm; el tamaño 23 permitirá tratar anillos desde 18 mm), distancia anillo-ostium coronarios > 12mm y ausencia de calcificación masiva. La valvuloplastia previa es imprescindible en todos los casos.
Presentamos nuestra experiencia inicial con esta válvula. Se evaluó a 12 pacientes, de los que se consideró no apropiados a 7 (5 por anillo pequeño, 1 por distancia anillo-coronarias < 12mm y otro por ambas razones); finalmente, se trató a 5 pacientes (tabla), y se logró implantar la válvula en posición correcta y con regurgitación aórtica leve o trivial en todos ellos. El resultado hemodinámico fue bueno en 4 pacientes, aunque los gradientes resultaron algo mayores que los registrados con otras válvulas percutáneas, pero similares a los descritos con las prótesis biológicas quirúrgicas6; en 1 paciente con una válvula funcionalmente bicúspide por fusión y calcificación de la comisura entre los senos derecho y no coronario, el gradiente postoperatorio inicial subió de 12 a 35mmHg a los 3 días, y se documentó por tomografía computarizada y fluoroscopia una deformidad geométrica del armazón de poliéster. A pesar del gradiente residual (estable desde entonces), y probablemente por reducción de la insuficiencia aórtica (de grado 3 a 1), el paciente mejoró clínicamente y permanece en buena situación funcional. En el resto de los pacientes tanto la funcionalidad protésica como la evolución clínica fueron favorables.
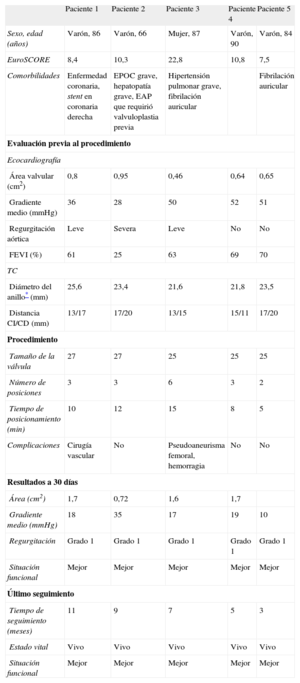
Datos basales, del procedimiento y del seguimiento de los 5 pacientes tratados
| Paciente 1 | Paciente 2 | Paciente 3 | Paciente 4 | Paciente 5 | |
| Sexo, edad (años) | Varón, 86 | Varón, 66 | Mujer, 87 | Varón, 90 | Varón, 84 |
| EuroSCORE | 8,4 | 10,3 | 22,8 | 10,8 | 7,5 |
| Comorbilidades | Enfermedad coronaria, stent en coronaria derecha | EPOC grave, hepatopatía grave, EAP que requirió valvuloplastia previa | Hipertensión pulmonar grave, fibrilación auricular | Fibrilación auricular | |
| Evaluación previa al procedimiento | |||||
| Ecocardiografía | |||||
| Área valvular (cm2) | 0,8 | 0,95 | 0,46 | 0,64 | 0,65 |
| Gradiente medio (mmHg) | 36 | 28 | 50 | 52 | 51 |
| Regurgitación aórtica | Leve | Severa | Leve | No | No |
| FEVI (%) | 61 | 25 | 63 | 69 | 70 |
| TC | |||||
| Diámetro del anillo* (mm) | 25,6 | 23,4 | 21,6 | 21,8 | 23,5 |
| Distancia CI/CD (mm) | 13/17 | 17/20 | 13/15 | 15/11 | 17/20 |
| Procedimiento | |||||
| Tamaño de la válvula | 27 | 27 | 25 | 25 | 25 |
| Número de posiciones | 3 | 3 | 6 | 3 | 2 |
| Tiempo de posicionamiento (min) | 10 | 12 | 15 | 8 | 5 |
| Complicaciones | Cirugía vascular | No | Pseudoaneurisma femoral, hemorragia | No | No |
| Resultados a 30 días | |||||
| Área (cm2) | 1,7 | 0,72 | 1,6 | 1,7 | |
| Gradiente medio (mmHg) | 18 | 35 | 17 | 19 | 10 |
| Regurgitación | Grado 1 | Grado 1 | Grado 1 | Grado 1 | Grado 1 |
| Situación funcional | Mejor | Mejor | Mejor | Mejor | Mejor |
| Último seguimiento | |||||
| Tiempo de seguimiento (meses) | 11 | 9 | 7 | 5 | 3 |
| Estado vital | Vivo | Vivo | Vivo | Vivo | Vivo |
| Situación funcional | Mejor | Mejor | Mejor | Mejor | Mejor |
CD: coronaria derecha; CI: coronaria izquierda; EAP: edema agudo de pulmón; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; TC: tomografía computarizada.
Las principales ventajas de la prótesis DirectFlow respecto a las prótesis Edwards-SAPIEN y Medtronic CoreValve son:
- •
Mayor flexibilidad.
- •
Mayor estabilidad hemodinámica durante la liberación (válvula operativa durante el implante, no precisa estimulación a alta frecuencia).
- •
Permite valorar la funcionalidad de la prótesis antes de liberarla.
- •
Posibilidad de reposicionamiento/recaptura.
- •
Tasa baja de insuficiencia aórtica.
Entre las desventajas cabe destacar:
- •
Menor fuerza radial.
- •
Gradiente transvalvular algo mayor.
La información disponible sobre esta válvula todavía es escasa. Los resultados presentados en el PCR de 2014 parecen confirmar la estabilidad de los resultados hemodinámicos a 1 año de los primeros 100 pacientes tratados. No obstante, hay aspectos, como el impacto del gradiente residual o los criterios de selección, que precisan estudio en series más amplias y con seguimiento más largo. Actualmente no hay datos para comparar los resultados clínicos con los de las prótesis Edwards-SAPIEN y Medtronic CoreValve.