Palabras clave
INTRODUCCIÓN
La estenosis subaórtica (ESA) tardía tras una cirugía de comunicación interauricular (CIA) es infrecuente. Suele diagnosticarse 6-8 años tras la corrección de CIA en la infancia. Presentamos el caso de una paciente intervenida en la edad adulta y diagnosticada 22 años después de ESA severa.
CASO CLÍNICO
Mujer de 69 años, intervenida a los 48 años por CIA tipo ostium primum con disnea de medianos esfuerzos. Se cerró quirúrgicamente el defecto con parche de teflón y se corrigió, mediante sutura, la hendidura de la valva anterior mitral. Precisó implante de marcapasos VVI por bloqueo auriculoventricular completo. Permaneció asintomática hasta 22 años después, cuando presentó dolor torácico inespecífico y una prueba de esfuerzo interrumpida por la disnea. Ecocardiográficamente presentaba un ventrículo izquierdo hipertrófico con función conservada e hipertensión pulmonar severa. La válvula mitral estaba fibrosada, con insuficiencia moderada e insuficiencia aórtica ligera. Presentaba un gradiente sistólico fijo en el tracto de salida del ventrículo izquierdo (TSVI) de 84 mmHg, ocasionado por una membrana, que parecía partir de la valva anterior mitral. En el cateterismo cardíaco se diagnosticó una estenosis severa del tronco de la coronaria izquierda.
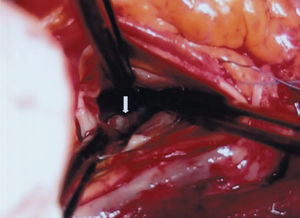
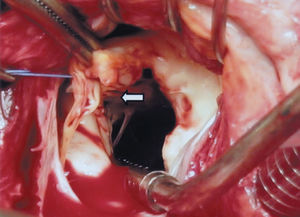
Durante la intervención se encontró un rodete fibroso a 2 mm de la válvula aórtica (fig. 1) y un tracto fibromuscular en la porción septal, extendido hacia continuidad mitroaórtica, donde se insertaba de manera anormal un músculo papilar mitral (fig. 2). Se resecó el rodete fibroso y parte del tejido muscular subyacente, seccionando la inserción anómala del papilar, se sustituyó la válvula mitral desestructurada por una prótesis mecánica y se realizó revascularización coronaria. La paciente no presentó incidencias postoperatorias y el gradiente ecocardiográfico residual en el TSVI fue de 16 mmHg.
Fig. 1. Rodete fibromuscular en el tracto de salida del ventrículo izquierdo, 2 mm por debajo del anillo valvular aórtico.
Fig. 2. Inserción anómala de las cuerdas tendinosas del músculo papilar mitral, que se implantan en la parte alta del septo y contribuyen a la estenosis del tracto de salida del ventrículo izquierdo.
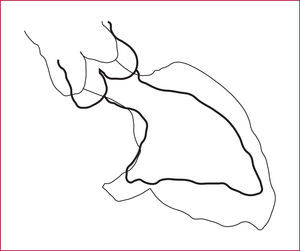
En la revisión de la angiografía previa a la primera cirugía no se apreciaba gradiente en el TSVI y sí morfología sistodiastólica en «cuello de cisne» (fig. 3). El ecocardiograma mostraba una hipoplasia relativa de las cavidades izquierdas y una aparente inserción de cuerdas tendinosas en la parte alta del septo.
Fig. 3. Representación gráfica de la ventriculografía en sístole y diástole realizada antes de la primera intervención. La imagen en cuello de ganso y la deformidad del tracto de salida del ventrículo izquierdo permanecen en sístole. La relación entre la longitud de los tractos de salida y de entrada del ventrículo izquierdo es < 1.
DISCUSIÓN
La ESA tras cirugía correctora de CIA de tipo ostium primum es infrecuente. Afecta al 2-15% de los casos y suele diagnosticarse 6-8 años tras corrección del defecto en la infancia1-4. Hay escasos seguimientos postoperatorios en adultos1,4,5, en los que la evolución es más lenta. Su incidencia puede subestimarse ya que (como en este caso) un 60-70% permanece silente durante años3.
La ESA puede ser adquirida y progresiva, y puede recurrir tras cirugía6,7. Su etiología es multifactorial. Rasgos morfológicos y posiblemente genéticos8 predisponen a su desarrollo. La ESA adquirida cursa con hiperplasia fibrosa secundaria a la aparición de un flujo turbulento en el TSVI. A este flujo contribuye el cierre de la hendidura mitral estrechando el tracto y limitando el desplazamiento sistólico de las valvas lejos del septo interventricular3. Su progresión provoca hipertrofia ventricular izquierda y septal sobreañadida a la estenosis inicial del TSVI6. Igual que en el caso que nos ocupa, un cociente entre la distancia válvula mitral-ápex (tracto de entrada del ventrículo izquierdo) y la válvula aórtica-ápex (TSVI) < 0,7 (en condiciones normales es de 1) favorece la aparición de ESA en el seguimiento9,10. Esta característica provoca una morfología angiográfica en «cuello de ganso» en diástole ventricular. Su persistencia en sístole (nuestro caso) se considera un factor predisponente para el posterior desarrollo de ESA2. Su traducción ecocardiográfica sería la reducción del ángulo formado entre el TSVI y el septo interventricular10 que, asociado a un desplazamiento inferior del plano de inserción de las valvas auriculoventriculares hacia el ventrículo izquierdo, predice el riesgo de desarrollo de ESA en el seguimiento. Aunque también es el mecanismo causal de las ESA congénitas, es más infrecuente que el diagnóstico tardío se deba a la inserción anómala del músculo papilar en la parte alta del septo2,6.
CONCLUSIONES
Siempre que haya imágenes indicativas de esta morfología especial dentro del espectro de los defectos septales auriculares incompletos, aunque se haya descartado ESA intraoperatoriamente, se evaluará de manera periódica mediante ecocardiografía para descartar su aparición, pues un alto porcentaje de pacientes permanece asintomático.
Correspondencia: Dra. Y. Carrascal.
Servicio de Cirugía Cardíaca. Hospital Universitario de Valladolid.
Avda. Ramón y Cajal, s/n. 47003 Valladolid. España.
Correo electrónico: aguerrerop@medynet.com
Recibido el 11 de marzo de 2005.
Aceptado para su publicación el 26 de mayo de 2005.