Los electrodos de desfibrilación Sprint Fidelis presentan riesgo de disfunción precoz. La mayor parte de las series en la literatura provienen de un solo centro. Describimos la experiencia clínica en nueve centros españoles.
MétodosSe analizaron los datos clínicos, del implante y el seguimiento de todos los pacientes con un electrodo Sprint Fidelis, describiendo los casos problema, calculando la supervivencia del electrodo a medio plazo e identificando posibles predictores de disfunción.
ResultadosSe incluyó un total de 378 electrodos en 376 pacientes (el 85,7% varones), con una media de edad de 64,9±13,6 años. El 59,8% se implantó en pacientes con cardiopatía isquémica. La fracción de eyección ventricular izquierda era 33,4%±14,5%. En el 74,8% de los casos se implantó por punción subclavia izquierda. Tras un seguimiento medio de 30,9±14 meses, 16 pacientes presentaron disfunción del electrodo; la supervivencia a 36 meses fue del 96,1%. En 11 electrodos ocurrió una disfunción aislada del sistema de sensado/estimulación; en 3, del sistema de alta energía, y en 2, de ambos. Una mejor función ventricular se asoció con una mayor probabilidad de fractura del electrodo (el 42,4%±16% frente al 33%±14,3%; p=0,011); tres centros presentaron una tasa de fracturas superior al 10% y los seis restantes, inferior al 5%.
ConclusionesEn esta serie multicéntrica de 378 electrodos, la supervivencia estimada a 3 años resultó mayor que en series previas, con un perfil de presentación clínica similar de las disfunciones. La fracción de eyección ventricular izquierda y el centro implantador fueron variables asociadas a la presencia de disfunción.
Palabras clave
La publicación de numerosos ensayos clínicos aleatorizados multicéntricos internacionales ha demostrado el efecto beneficioso, en cuanto a reducción de mortalidad, del desfibrilador automático implantable (DAI) en determinados grupos de pacientes en riesgo, en prevención tanto secundaria como primaria1. Esta expansión de las indicaciones ha llevado al aumento exponencial en el número de implantes2. Por el contrario, el implante de un DAI en un paciente lleva implícita la posibilidad de una serie de complicaciones tanto en el momento del implante como en el seguimiento, entre las que se incluyen infección, decúbito del generador, hematoma, desplazamiento de electrodos, perforación cardiaca, disminución de los parámetros de calidad de vida por recibir choques, proarritmia, fallo de estimulación o de desfibrilación y terapias inapropiadas por arritmias supraventriculares o sobresensado3. Algunas de ellas se deben a disfunción de los electrodos de desfibrilación, y su no despreciable incidencia se ha puesto de manifiesto con datos de series con seguimientos prolongados y modelos diversos de electrodos4,5,6. Los avances tecnológicos no sólo se han dirigido a ir corrigiendo problemas de los modelos de electrodos previos, sino que han permitido desarrollar generadores de menor tamaño y electrodos de pequeño diámetro que potencialmente aminorarían las complicaciones inherentes al tamaño de los sistemas. Sin embargo, la experiencia en general ha sido diferente y los electrodos de pequeño diámetro se han asociado a tasas superiores de complicaciones6,7. Uno de estos nuevos electrodos de pequeño diámetro es el electrodo Sprint Fidelis (Medtronic, Minneapolis, Minnesota, Estados Unidos). Los electrodos Sprint Fidelis, de 6,6 Fr (2,2 mm), fueron aprobados por la Food and Drug Administration estadounidense en septiembre de 2004 y fueron retirados del mercado en octubre de 2007 debido a una tasa de fracturas mayor de la esperable8; se estima que se han implantado unos 268.000 electrodos en todo el mundo. Diversas series internacionales, la mayoría procedentes de centros aislados, han descrito la presentación clínica, estimando su incidencia y evaluando posibles predictores de fallo de los electrodos, si bien con resultados no homogéneos8,9,10,11,12,13,14, especialmente en cuanto a la incidencia del problema. El presente trabajo expone la experiencia general con electrodos Sprint Fidelis en nueve centros españoles.
MétodosPacientesSe incluyó a todos los pacientes a los que se implantó un electrodo Sprint Fidelis (6930, 6931, 6948 o 6949). Se recogieron datos demográficos generales, como edad y sexo, así como datos sobre la indicación del implante, función ventricular, vía de acceso del electrodo, subtipo de electrodo Sprint Fidelis implantado, presencia de terapias apropiadas e inapropiadas durante el seguimiento y tiempo desde el implante hasta la aparición de la disfunción de electrodo (en los casos en que sucedió) o hasta la última revisión contabilizada. Para el análisis de los datos, se contabilizó el número de electrodos Sprint Fidelis, de tal manera que si a algún paciente se implantó más de uno de estos electrodos por algún motivo, se contabilizaron de forma repetida sus características generales. Se evaluaron de forma global los datos del implante, así como a lo largo del seguimiento de los pacientes a través de las grabaciones de la interrogaciones y sus informes técnicos, incluyendo la interrogación previa y la del momento en que se produjo la disfunción del electrodo. Se identificaron todos los casos de disfunción del electrodo y en estos se recopilaron los datos sobre la forma de presentación clínica, así como la actitud posterior una vez identificado el problema. La disfunción del electrodo se clasificó en función de que se tratara de un fallo del sistema de sensado/estimulación (S/E) o un fallo del sistema de alta energía. Se calculó la supervivencia global de los electrodos Sprint Fidelis en esta serie, y se analizaron los datos de forma total y separadamente por centros.
DefinicionesDisfunción por fractura del electrodo. Cualquiera de las siguientes circunstancias:
– Descargas inapropiadas como consecuencia de sobresensado de «ruido» debido a señales no fisiológicas.
– Cambio brusco y súbito en la impedancia crónica de estimulación o de desfibrilación (> 20% en un periodo de 24 h)10.
Los datos se han analizado con el programa SPSS (versión 16.0, SPSS Inc., Chicago, Illinois, Estados Unidos). Las variables categóricas se expresan en valor absoluto y porcentajes; las cuantitativas, en medias ± desviación estándar e intervalos intercuartílicos. Las variables categóricas se compararon mediante el test de Fisher o el test de la χ2, mientras que las variables continuas se compararon mediante el test de la t de Student. La tasa media de disfunciones de electrodos por año se calculó mediante el número de electrodos fracturados observados durante el seguimiento entre el número de electrodos, multiplicado por la duración media del seguimiento. El análisis de supervivencia se realizó mediante el método de Kaplan-Meier. Se consideraron estadísticamente significativos los valores de p<0,05.
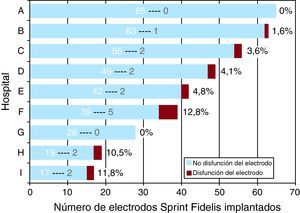
ResultadosEntre enero de 2005 y octubre de 2007, se implantó en nueve centros españoles un total de 378 electrodos Sprint Fidelis en 376 pacientes. Se utilizaron exclusivamente dos modelos de Sprint Fidelis, el modelo de fijación activa 6949 (231 electrodos, 61,1%) y el modelo de fijación pasiva 6948 (147 electrodos, 38,9%). La vía de acceso venosa para el implante del electrodo Sprint Fidelis más frecuente fue la punción directa de la vena subclavia izquierda (74,8%), seguida de la disección de la vena cefálica izquierda (19,1%) y la punción directa de la vena subclavia derecha (5,2%). El número total de electrodos implantados en cada centro queda reflejado en la Figura 1. Las características demográficas de los pacientes estudiados pueden observarse en la Tabla 1. Destaca que la gran mayoría eran varones (85,7%) con una media de edad próxima a los 65 años, y con una fracción de eyección ventricular izquierda (FEVI) deprimida (33,4±14,45%). La cardiopatía isquémica fue la indicación principal de implante de DAI en prevención tanto primaria como secundaria (226 pacientes; 59,8%), seguida de la miocardiopatía dilatada no isquémica (100 pacientes; 26,5%). El seguimiento medio de los pacientes fue de 30,9±14 (mediana, 33 [24-41]) meses. Durante el seguimiento, sólo un 23% de los pacientes (87 sujetos) recibieron terapias apropiadas del dispositivo, y un 10,3% (39 pacientes) recibió terapias inapropiadas, fundamentalmente por arritmias supraventriculares (71,1%).
Figura 1. Número de electrodos Sprint Fidelis implantados en cada centro (número en blanco), indicando el número de electrodos disfuncionantes (gris) y el porcentaje que suponen sobre el total de electrodos implantados en cada centro.
Tabla 1. Características generales de los pacientes y comparación entre el grupo de pacientes con disfunción del electrodo y el grupo sin disfunción del mismo
| Total pacientes (n=378) | Con disfunción (n=16) | Sin disfunción (n=362) | p | |
| Varones | 324 (85,7) | 13 (81,3) | 311 (85,9) | 0,602 |
| Edad (años) | 64,9±13,6 | 61,4±16,4 | 65±13,5 | 0,297 |
| FEVI (%) | 33,4±14,45 | 42,4±16 | 33±14,3 | 0,011 |
| Seguimiento (meses) | 30,9±14 | 1.140±446,5 | 964,3±415,4 | 0,109 |
| Indicación implante | ||||
| Cardiopatía isquémica secundaria | 115 (30,4) | 4 (25) | 111 (30,7) | 0,014 |
| Cardiopatía isquémica primaria | 111 (29,4) | 4 (25) | 107 (29,6) | |
| Miocardiopatía dilatada no isquémica secundaria | 46 (12,2) | 1 (6,3) | 45 (12,4) | |
| Miocardiopatía dilatada no isquémica primaria | 54 (14,3) | 2 (12,5) | 52 (14,4) | |
| Miocardiopatía hipertrófica | 15 (4) | 2 (12,5) | 13 (3,6) | |
| Síndrome de Brugada | 13 (3,4) | 1 (6,3) | 12 (3,3) | |
| Síndrome de QT Largo | 6 (1,6) | 2 (12,5) | 4 (1,1) | |
| Otras | 18 (4,8) | 0 | 18 (5) | |
| Vía de acceso (subclavia izquierda) | 283 (74,8) | 14 (87,5) | 269 (74,1) | 0,775 |
| Modelo Sprint Fidelis (6949) | 231 (61,1) | 12 (75) | 219 (60,5) | 0,127 |
| Terapias apropiadas | 87 (23) | 3 (18,8) | 84 (23,2) | 0,679 |
| Terapias inapropiadas | 39 (10,3) | 8 (50) | 31 (8,6) | < 0,001 |
FEVI: fracción de eyección ventricular izquierda.
Los datos expresan media±desviación estándar o n (%).
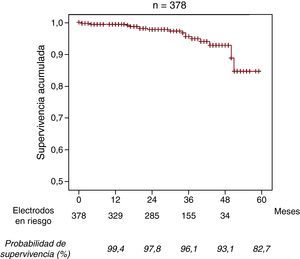
Se documentó un total de 16 disfunciones de electrodos (4,2%). El tiempo medio en el que se produjo la disfunción fue de 29,1±14,9 (intervalo, 1,5-52; mediana, 32 [20-38,5]) meses. La tasa media fue de 0,016 disfunciones/electrodoaño. En la Tabla 2 se caracterizan los casos individualmente. La distribución de los casos de disfunción de los electrodos por centro se observa en la Figura 1. Es resaltable el hecho de que los tres centros con mayor número de electrodos implantados están entre los cuatro con menor frecuencia de aparición de disfunción de los electrodos. Además, la mayor parte de los casos de disfunción de electrodo (9 electrodos; 56,2%) se concentra en tres centros, que superan una incidencia individual de disfunción del 10%. De los 16 casos de electrodos disfuncionantes, en la mayor parte de ellos (13 electrodos) se produjo disfunción del sistema de S/E, siendo su disfunción aislada la forma de presentación más frecuente (11 casos; 68,75%), mientras que la disfunción aislada del sistema de alta energía ocurrió en 3 electrodos (18,75%). Todos los casos de disfunción del sistema de alta energía corresponden a electrodos del modelo 6949. En 2 pacientes con disfunción del electrodo Sprint Fidelis, se implantó un nuevo electrodo Sprint Fidelis, por haber sucedido en un momento previo al aviso de seguridad comunicado. La proporción de electrodos Sprint Fidelis que sobrevivieron al primer año de seguimiento fue del 99,4% (intervalo de confianza [IC] del 95%, 98,7-100%). De los que sobrevivieron el primer año, la proporción de supervivencia entre los 12 y los 24 meses fue del 98,4% (IC del 95%, 96,9-99,8%). De los que sobrevivieron 2 años, la probabilidad de supervivencia 1 año más fue del 98,2% (IC del 95%, 96-100%). De los que no fallaron durante los primeros 3 años, la probabilidad de supervivencia 1 año más fue del 96,9% (IC del 95%, 93,4-100%), mientras que de los que sobrevivieron 4 años fue del 88,9% (IC del 95%, 75,3-100%). Así, la supervivencia acumulada estimada a 3 y 4 años fue del 96,1 y el 93,1%, respectivamente (Figura 2).
Tabla 2. Descripción de los casos de disfunción del electrodo Sprint Fidelis
| Caso | Hospital | Edad (años) | Sexo | Indicación | FEVI (%) | Vía de acceso | Modelo | Seguimiento (meses) | Presentación | Tipo de disfunción | Actitud tomada | Complicaciones revisión |
| 1 | H | 74 | Varón | Isquémica, 1a | 25 | Subclavia izquierda | 6949 | 35,5 | Alertas | Alta Energía | Extracción+implante diferente ED | No |
| 2 | H | 57 | Varón | Isquémica, 1a | 30 | Subclavia izquierda | 6949 | 50,5 | Terapias inapropiadas | S/E | Abandono+implante diferente ED | No |
| 3 | C | 49 | Varón | Isquémica, 2a | 30 | Cefálica izquierda | 6949 | 17,9 | Terapias inapropiadas | S/E | Abandono+implante Sprint Fidelis | No |
| 4 | C | 65 | Varón | Miocardiopatía hipertrófica, 2a | 55 | Cefálica izquierda | 6949 | 43,5 | Terapias inapropiadas | S/E | Abandono+implante diferente ED | No |
| 5 | E | 63 | Mujer | Dilatada no isquémica, 1a | 28 | Subclavia izquierda | 6949 | 1,5 | Revisión periódica | S/E | Se mantuvo electrodo para desfibrilación y estimulación con electrodo VI | — |
| 6 | E | 59 | Varón | Isquémica, 2a | 55 | Subclavia izquierda | 6949 | 30,7 | Terapias inapropiadas | S/E | Abandono+implante diferente ED | No |
| 7 | I | 61 | Varón | Síndrome de Brugada | 65 | Subclavia izquierda | 6948 | 34 | Alertas | S/E | Extracción+implante diferente ED | No |
| 8 | I | 74 | Varón | Dilatada no isquémica, 1a | 25 | Subclavia izquierda | 6948 | 37,8 | Terapias inapropiadas | S/E | Abandono+implante diferente ED | No |
| 9 | F | 79 | Varón | Isquémica, 2a | 35 | Subclavia izquierda | 6949 | 52 | Terapias inapropiadas | S/E | Implante electrodo S/E | Pérdida captura VI |
| 10 | F | 50 | Mujer | Sídrome de QT Largo | 60 | Subclavia izquierda | 6949 | 35,8 | Terapias inapropiadas | S/E | Abandono+implante diferente ED | No |
| 11 | F | 73 | Varón | Isquémica, 1a | 60 | Subclavia izquierda | 6949 | 4,5 | Terapias inapropiadas | Alta energía y S/E | Extracción+implante Sprint Fidelis | No |
| 12 | F | 82 | Varón | Miocardiopatía hipertrófica, 2a | 45 | Subclavia izquierda | 6949 | 16,6 | Terapias inapropiadas | Alta energía y S/E | Abandono+implante diferente ED | Infección tardía |
| 13 | F | 13 | Varón | Síndrome de QT Largo | 70 | Subclavia izquierda | 6949 | 20,7 | Alertas | Alta energía | Abandono+implante diferente ED | No |
| 14 | B | 63 | Mujer | Isquémica, 2a | 40 | Subclavia izquierda | 6948 | 40,3 | Revisión periódica | S/E | Abandono+implante diferente ED | No |
| 15 | D | 51 | Varón | Dilatada no isquémica, 2a | 31 | Subclavia izquierda | 6949 | 23,6 | Alertas | S/E | Abandono+implante diferente ED | No |
| 16 | D | 69 | Varón | Isquémica, 1a | 25 | Subclavia izquierda | 6949 | 20,8 | Alertas | Alta energía | Extracción+implante diferente ED | No |
1a: prevención primaria; 2a: prevención secundaria; ED: electrodo de desfibrilación; FEVI: fracción de eyección ventricular izquierda; S/E: sensado/estimulación; VI: ventrículo izquierdo.
Figura 2. Curva de supervivencia del electrodo Sprint Fidelis.
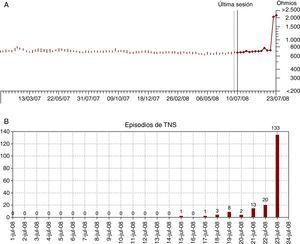
La forma de presentación clínica mayoritaria de las disfunciones del sistema de S/E (9 de 13 pacientes, 69,2%) fueron las terapias inapropiadas por sobresensado de señales no fisiológicas acompañadas de incrementos bruscos previos de la impedancia de estimulación (Figura 3). Tres casos de disfunción del sistema de S/E ocurrieron en pacientes con el algoritmo especial de alertas (LIA, lead integrity alert) activado (casos 2, 7 y 15) (Tabla 2): en 2 de ellos previno las terapias inapropiadas, pero no en 1 caso, debido a la falta de reconocimiento de la señal acústica activada varios días antes de las terapias recibidas (caso 2). En el resto de los casos, el problema de la disfunción ocurrió sin tener activado dicho algoritmo y las alertas convencionales no fueron eficaces en la prevención de las terapias inapropiadas. Por el contrario, las alertas sonoras del dispositivo fueron la forma de presentación cuando la disfunción ocurrió aisladamente en el sistema de alta energía.
Figura 3. Gráfico de tendencias de la impedancia de estimulación (A) y episodios de taquicardia ventricular no sostenida (B), en un paciente (paciente 8) con disfunción del sistema de sensado/estimulación que se presentó en forma de tormenta eléctrica con más de 30 choques. Es muy evidente el aumento brusco de la impedancia de estimulación por encima de 2.000 Ω que ocurre el día previo a la presentación clínica, y el aumento del número de TNS por sobresensado 1 día después del aumento de la impedancia de estimulación. TNS: taquicardia ventricular no sostenida.
En 15 de los 16 casos de disfunción del electrodo, la actitud tras el diagnóstico fue la revisión quirúrgica, con abandono del electrodo disfuncionante e implante de un nuevo electrodo de desfibrilación en la mayoría (Tabla 2), sin producirse complicaciones agudas graves intraprocedimiento en ningún caso. Un paciente (caso 12) presentó, 9 meses después de la revisión quirúrgica, una infección del nuevo sistema que se complicó, pese a haberlo extraído, con un cuadro de endocarditis bacteriana que ocasionó el fallecimiento del paciente.
La comparación de características generales entre los pacientes con disfunción del electrodo y los que no la presentaron se muestra en la Tabla 1. La edad, el sexo y el tiempo de seguimiento fueron variables no asociadas estadísticamente a la presencia de disfunción del electrodo. Igualmente, la vía de acceso para el implante o el modelo de Sprint Fidelis tampoco resultaron variables con diferencia significativa entre ambos grupos. En el grupo de pacientes con disfunción del electrodo fue más habitual la miocardiopatía hipertrófica, el síndrome de Brugada, el síndrome de QT largo y otras indicaciones menos frecuentes, si bien en las indicaciones más habituales del implante los grupos resultaron porcentualmente más homogéneos. Los pacientes con disfunción del electrodo Sprint Fidelis presentaban una FEVI significativamente menos deprimida (42,4 frente a 33%; p=0,011). Por el contrario, la comparación de los pacientes entre los centros con una incidencia de disfunción superior al 10% y los centros con una incidencia inferior no demuestra diferencias significativas en cuanto a la función ventricular. Sin embargo, dicha comparación demuestra una mayor frecuencia de acceso por vía cefálica izquierda (23 frente a 6,8%; p=0,01) y un menor tiempo de seguimiento (29,8 frente a 35,2 meses; p=0,002) en el grupo total de pacientes de los centros con una incidencia de disfunción menor del 10%; además, es más frecuente el modelo 6948 (41,6 frente a 27,4%; p=0,026) en este último grupo.
DiscusiónEn este estudio multicéntrico que analizó todos los electrodos Sprint Fidelis implantados en nueve hospitales, se estimó una supervivencia a los 3 años desde el implante del 96,1% y a los 4 años del 93,1%. La forma de presentación clínica más habitual fue la presencia de descargas inapropiadas en relación con sobresensado no fisiológico por fracturas del sistema de S/E del electrodo.
Supervivencia del electrodo Sprint FidelisLa supervivencia estimada a los 3 años del implante del electrodo Sprint Fidelis en esta serie fue significativamente superior a la informada en las principales series previas, procedentes de estudios de uno o dos centros (el 90,811; el 87,913; el 89,3% a 30 meses15). Sin embargo, los datos se aproximan más a los aportados por Medtronic en sus informes de supervivencia del System Longevity Study y el CareLink, con supervivencias a 3 años del 95 y el 97%16,17 respectivamente. Las causas de tales discrepancias deben de ser multifactoriales y no resultan fácilmente identificables, como diferencias en el tamaño de las muestras y los centros participantes y la forma de recogida de datos. Aunque algún autor ha señalado que los estudios no procedentes directamente de Medtronic tendrían un seguimiento más estrecho y más rigor en la identificación de los casos problema y, por lo tanto, sus datos serían más fiables que los de la compañía fabricante18, esta hipótesis no resulta operativa en nuestro trabajo y no explicaría las diferencias observadas.
Los factores que influyen en la disfunción de un electrodo son variados, entre ellos las características inherentes al electrodo, la vía de acceso, el operador y características individuales del paciente. En el caso de los electrodos Sprint Fidelis, su comparación repetida con otros electrodos de características similares e implantados en los mismos años, corroborando una tasa de disfunciones superior, confirma la influencia de factores propios de la configuración y estructura del electrodo en su mayor vulnerabilidad a la fractura11,13.
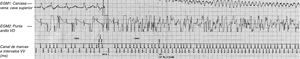
Presentación clínicaLa forma de presentación clínica mayoritaria de los casos de disfunción del electrodo Sprint Fidelis fueron las terapias inapropiadas por sobresensado secundario al «ruido» ocasionado por la fractura del sistema de S/E (9 pacientes) (Figura 4). Sólo en 2 casos de fractura del sistema de S/E, la detección del problema fue consecuencia del previo aviso de las alertas sonoras programadas en el dispositivo. Una de estas alertas habituales, la activada por aumentos de impedancia, se demostró ineficaz para reducir los choques inapropiados en los casos de disfunción de electrodos Sprint Fidelis19. En nuestra serie, los aumentos de impedancia de estimulación no fueron preventivos en ningún caso. Sin embargo, en España, a partir de septiembre de 2009, estuvo disponible la instalación en la mayoría de los dispositivos ya implantados (e incorporada en modelos nuevos), de un algoritmo, el LIA, que engloba parámetros de sobresensado y aumento de impedancias, del que se ha demostrado, pese a no ser perfecto, que reduce las terapias inapropiadas en estos pacientes al permitir una detección precoz preclínica de la disfunción de los electrodos20,21,22. Este fue el caso en 2 de los 3 pacientes en los que ocurrió una disfunción del sistema de S/E en pacientes con el LIA activado.
Figura 4. Ejemplo de descarga inapropiada y proarritmia en un paciente de la serie. A la izquierda, electrogramas intracavitarios (electrograma de descarga arriba y electrograma bipolar abajo) en ritmo de fibrilación auricular durante el que se produce sobresensado continuo de «ruido» que ocasiona sensado en zona de fibrilación ventricular, lo que produce un choque de máxima energía que desencadena un episodio verdadero de fibrilación ventricular.
Variables asociadas a disfunciónEn los 16 casos de disfunción del electrodo Sprint Fidelis, una mejor función ventricular se asoció a una mayor tasa de disfunción de electrodos. Esta asociación es acorde con la informada en varias series previas10,12. En la serie de Farwell et al10, los autores observaron que una FEVI mejor y un acceso venoso diferente de la disección cefálica resultaron variables predictoras independientes de disfunción. En su trabajo, cada 10% de incremento de la FEVI aumentaba 2,42 veces el riesgo de fractura. Una mejor función ventricular podría asociarse a un mayor estrés de la punta del electrodo en cada ciclo cardiaco por una contracción más enérgica, lo que justificaría dicha asociación. En este sentido, una menor edad también se ha propuesto como variable de influencia al asociarse a una potencial mayor actividad física15. En la serie que presentamos no se encontró asociación entre la disfunción del electrodo y la menor o mayor edad de los pacientes. Igualmente, en otras series tampoco se ha asociado la edad al riesgo de fractura10,12, y es que se puede presumir en general que el vigor de la contracción cardiaca y, por ende, del estrés del electrodo esté más relacionado con la FEVI (más reducida, menor estrés sobre el electrodo) que con el grado de actividad en esta población de pacientes con FEVI mayoritariamente reducida.
En nuestro estudio se observaron diferencias significativas en la tasa de disfunción entre centros, de tal forma que tres centros con volumen variable de implantes superaron la incidencia del 10% de disfunciones de electrodo. En concreto, uno de los centros acumuló 5 de las 16 disfunciones producidas. Estos datos no son equiparables a los publicados en un estudio multicéntrico previo, en el que no se observaron diferencias estadísticamente significativas por centros u operadores, si bien la incidencia del problema varió entre 0 y 3,2%14. Aunque en los centros con mayor incidencia la vía de acceso no cefálica fue más frecuente que en los demás, en 14 de los 16 casos de disfunción la vía de acceso fue la punción subclavia izquierda, lo que dificulta el análisis del efecto de dicha variable. Es posible que otros factores como la propia manipulación del electrodo por el operador o la duración del implante pudieran tener algún papel en estas diferencias observadas23.
Longevidad del electrodo y riesgo de disfunciónOtro aspecto interesante de este estudio es que el riesgo de disfunción va aumentando con la vida del electrodo y no es elevado en la fase periprocedimiento, lo que indica que la fractura no se produce, al menos completamente, durante el implante y que factores del paciente y la vía de acceso puedan influir en cada paciente individual. En el estudio inicial que alertó de la disfunción precoz de estos electrodos8, no se disponía de datos a largo plazo, pero series posteriores han confirmado que el riesgo de fractura y su incidencia van aumentando con el tiempo. En un estudio de dos centros con un gran volumen de implante de estos electrodos, Hauser et al13 observaron que la tasa de disfunción de los electrodos Sprint Fidelis era del 3,75% al año y la total de otros cuatro modelos diferentes de electrodos fue del 0,58% al año, con una supervivencia estimada a los 3 años desde el implante del 87,9%, lo que contrasta con el 95% calculado del otro grupo de electrodos. Dichos datos van en la línea de otros trabajos posteriores10,11. Este hecho hace que los pacientes con un electrodo Sprint Fidelis implantado presenten un riesgo creciente de disfunción del electrodo que exige su vigilancia extrema. En nuestra serie, pese a que la supervivencia estimada a los 3 años es superior al de estudios previos, se observa una caída llamativa con seguimientos más largos (Figura 2).
Actitud ante los electrodos disfuncionantes y no disfuncionantesSi bien el recambio sistemático de los electrodos en todos los pacientes con un Sprint Fidelis normofuncionante no parece aconsejable, pues se considera que el riesgo de la revisión quirúrgica es mayor24 que el de que se produzca un fallo del electrodo, algunos autores insinúan esta posibilidad en determinadas poblaciones de pacientes con un mayor potencial riesgo, como los afectos de canalopatías o miocardiopatía hipertrófica13. En nuestra serie de pacientes con disfunción del electrodo, la actitud de los investigadores fue variable, con predominio del abandono del electrodo o su extracción, con implante de un nuevo electrodo de desfibrilación, y no se ha producido más que una complicación grave relacionada con la revisión quirúrgica (6,25%), aunque resultó fatal. Los datos de la literatura indican mayor seguridad en el abandono de los electrodos más que en su extracción24, y el abandono parece una opción segura25.
LimitacionesLas principales limitaciones del presente trabajo incluyen su carácter retrospectivo y el número de pacientes estudiado, ya que la relativamente baja incidencia del problema determina un número reducido de casos con disfunción del electrodo. Sin embargo, que se pueda conocer datos de una variedad de centros permite valorar el papel de la variable del centro implantador y sus operadores. El trabajo no compara los resultados de los electrodos Sprint Fidelis con los de otros modelos de electrodos implantados por los mismos centros y en época similar, si bien, como refleja el trabajo de Hauser et al13, no sería esperable encontrar en los centros con más disfunciones de electrodos Sprint Fidelis tasas también más elevadas de disfunción de otros modelos de electrodos. El reducido número de electrodos disfuncionantes extraídos no permite conocer datos sobre lugar y modo de la fractura del electrodo. El periodo de seguimiento es corto, lo que no permite en este análisis conocer la evolución del riesgo de disfunción más allá del periodo observado.
ConclusionesEn esta serie multicéntrica de 378 electrodos de desfibrilación Sprint Fidelis, la supervivencia estimada a los 3 años desde el implante fue mayor que la informada en otras series previas de la literatura. Nuestros resultados, sin embargo, confirman que la supervivencia es claramente dependiente del tiempo, lo que obliga a seguir estrechamente a estos pacientes e implementar en ellos los avances de alertas y programación de los dispositivos que permitan una detección precoz que minimice la posibilidad de terapias inapropiadas y otros problemas relacionados con la disfunción del electrodo. La presentación clínica de los casos de disfunción fue similar a la informada previamente, y la función ventricular izquierda y el centro de implante resultaron variables relacionadas con la disfunción del electrodo.
Conflicto de interesesNinguno.
Recibido 20 Septiembre 2010
Aceptado 20 Noviembre 2010
Autor para correspondencia: Unidad de Arritmias y Electrofisiología Cardiaca, Hospital Virgen de la Salud, Avda, Barber 30, 45004 Toledo, España. maapalomares@secardiologia.es