Actualmente existen pocos datos sobre la incidencia y el pronóstico de la insuficiencia cardiaca (IC) y la fracción de eyección del ventrículo izquierdo (FEVI) en el escenario del síndrome coronario agudo (SCA). El objetivo del estudio fue determinar la relación de la FEVI y la IC con el pronóstico a largo plazo en una cohorte de pacientes con SCA.
MétodosSe trata de un estudio retrospectivo observacional de 6.208 pacientes consecutivos ingresados por SCA en 2 hospitales españoles. Se determinaron las características clínicas y se consideró como objetivo primario la mortalidad y/o el reingreso por IC durante el seguimiento.
ResultadosEntre los 5.064 participantes, presentaron SCA sin IC durante el ingreso: 290 (5,8%) con FEVI <40%, 540 (10,6%) con FEVI 40-49% y 4.234 (83,6%) con FEVI ≥ 50%. De los 1.144 pacientes restantes 395 (34,6%) con FEVI <40%, 251 (21,9%) FEVI 40-49% y 498 (43,5%) FEVI ≥ 50%. Los pacientes con FEVI del 40-49% tenían un perfil clínico y demográfico con características intermedias entre los pacientes presentaban FEVI <40% y FEVI ≥ 50%. Las curvas de Kaplan-Meier mostraron que la mortalidad y el reingreso por IC eran significativamente distintos en función de la FEVI únicamente en los pacientes sin IC. En este grupo, la FEVI ≥ 50% fue un factor pronóstico independiente.
ConclusionesEn el SCA, el pronóstico a largo plazo es considerablemente peor en los pacientes que desarrollan IC durante el ingreso, independientemente del valor de la FEVI. Este parámetro solo es en un factor pronóstico en los pacientes sin IC.
Palabras clave
La insuficiencia cardiaca (IC) y los síndromes coronarios agudos (SCA) son las principales causas de muerte y hospitalización en los países industrializados1. Es bien sabido que la presencia de IC durante un SCA es una de las manifestaciones clínicas más importantes que conducen a una mala evolución clínica2. Aunque las mejoras en el tratamiento del SCA a lo largo de la última década han reducido la mortalidad a corto plazo, la IC en el contexto de un SCA continúa siendo un verdadero reto, ya que se asocia con alto riesgo de mortalidad a 1 año3,4.
Las guías de práctica clínica actuales recomiendan determinar la fracción de eyección del ventrículo izquierdo (FEVI) tras un SCA5, ya que entre un tercio y la mitad de los pacientes que sufren un SCA reciben el alta con una disfunción sistólica ventricular izquierda6. La reducción de la FEVI es un potente predictor de mortalidad y rehospitalizaciones7–11 y estudios recientes indican que los pacientes con IC y FEVI conservada tras un SCA tienen un pronóstico solo ligeramente mejor que los pacientes con FEVI reducida12.
La nueva guía de 2016 de la Sociedad Europea de Cardiología (ESC) propone una nueva clasificación en función de la FEVI: la FEVI reducida es la < 40%, la FEVI intermedia está entre el 40 y el 49%, y la FEVI conservada es ≥ 50%13. La información actual sobre las consecuencias clínicas, pronósticas y terapéuticas de esta clasificación es escasa14.
El objetivo de este estudio es analizar la relación de la FEVI y la IC con el pronóstico a largo plazo en una cohorte de pacientes con SCA, y determinar el impacto pronóstico de la nueva clasificación de la FEVI propuesta por la guía ESC 2016 sobre IC.
MÉTODOSDiseño del estudioSe diseñó un estudio retrospectivo de pacientes consecutivos ingresados en las unidades coronarias o salas de hospitalización de 2 hospitales españoles por un SCA entre noviembre de 2003 y mayo de 2014 (n = 7.033). La cohorte contemporánea fue totalmente inclusiva y el único criterio de exclusión fue la ausencia de datos de FEVI durante la hospitalización índice (825 pacientes); formaron la cohorte final 6.208 pacientes. El protocolo del estudio y el examen de las historias clínicas recibieron la autorización del comité de ética del hospital.
Definición de las variablesSe clasificó a los pacientes según presentaran un infarto de miocardio con elevación del segmento ST (IAMCEST) o un SCA sin elevación del segmento ST, incluida la angina inestable y el IAMSEST. El diagnóstico de infarto de miocardio se estableció según la definición de la ESC de 201215. El diagnóstico de angina inestable exigía la presencia de síntomas indicativos, junto con signos objetivos de isquemia miocárdica en la prueba de esfuerzo, o la detección de una lesión culpable de un 50% en la angiografía coronaria, además de unos biomarcadores cardiacos por debajo del límite superior normal del laboratorio15. Los 2 centros participan en los sistemas regionales de asistencia del IAMCEST, y se practicó angioplastia coronaria, que fue la estrategia de elección durante el periodo de inclusión, a más del 90% de los pacientes con IAMCEST en ambos centros.
Personal médico adecuadamente capacitado obtuvo la información sobre factores de riesgo, antecedentes clínicos, tratamientos, exploraciones complementarias y diagnóstico principal al alta de todos los pacientes. Los protocolos diagnóstico y terapéutico del SCA en ambos centros incluían análisis de sangre en el servicio de urgencias y en ayunas tras el ingreso en el hospital. Se identificó a los pacientes con una enfermedad coronaria previa mediante la búsqueda de los que tenían ya un diagnóstico clínico de infarto de miocardio o antecedentes de angina o de revascularización coronaria motivada por angina. Se identificó la presencia de IC previa si los pacientes habían tenido como mínimo 1 hospitalización en la que la IC hubiera sido el diagnóstico principal o si habían tenido signos y síntomas típicos indicativos de un síndrome de IC junto con exploraciones de diagnóstico por la imagen compatibles (radiografía o ecocardiografía).
Se definió la IC índice por la presencia de estertores pulmonares o por el uso de diuréticos intravenosos o fármacos inotrópicos intravenosos durante el ingreso por SCA y se describió la gravedad de la IC mediante la clase de Killip16. En este análisis se utilizó la clase más alta observada durante los primeros 7 días de hospitalización. Un ecografista con certificación de nivel III realizó una ecocardiografía transtorácica bidimensional a todos los participantes, como parte de la práctica clínica ordinaria durante la hospitalización, y determinó la FEVI con el método de Simpson al alta17.
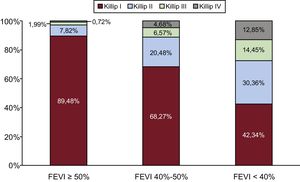
Clasificación de los pacientesFormaron la población final 6.208 pacientes. Se los dividió en 2 grupos según la evolución de la IC (Killip 1 o ≥ 2). En cada grupo se clasificó a los pacientes según la FEVI, aplicando el valor de corte actual de la guía sobre la IC de la ESC13 (figura 1).
Seguimiento y parámetros de valoraciónSe utilizó un protocolo bien establecido para el seguimiento posterior al alta: después del alta, los pacientes fueron objeto de seguimiento en una consulta dedicada específicamente a la cardiopatía isquémica y la atención primaria. El seguimiento estructurado se llevó a cabo mediante el examen de las historias clínicas electrónicas, evaluando toda la asistencia médica, así como los registros hospitalarios, y recurriendo en ciertos casos al contacto telefónico.
Los objetivos principales fueron la mortalidad por cualquier causa y la IC después del alta hospitalaria. Se identificó la aparición de una IC en el seguimiento si el paciente tenía como mínimo 1 hospitalización por IC como diagnóstico principal.
Análisis estadísticoLas variables cuantitativas se presentan en forma de media±desviación estándar y las diferencias se evaluaron con la prueba de la t de Student o un ANOVA. Las variables cualitativas se presentan como porcentajes y diferencias y se analizaron con la prueba de la χ2. Se rechazó la multicolinealidad entre la FEVI y la IC durante la hospitalización, la revascularización y la edad, puesto que los factores de inflación de la varianza eran bajos.
La mortalidad por cualquier causa después del alta hospitalaria se evaluó mediante un análisis de supervivencia. El riesgo de eventos observado se calculó mediante la estimación de Kaplan-Meier con log-rank test.
Los factores predictivos de la mortalidad por cualquier causa se evaluaron mediante modelos de regresión de Cox, tras la verificación del supuesto de riesgos proporcionales con la prueba de residuos de Schoenfeld, utilizando todas las variables con p < 0,1 en el análisis univariable o que podían tener consecuencias clínicas plausibles; los resultados se presentan en forma de hazard ratio (HR) e intervalos de confianza del 95% (IC95%). En el primer modelo se incluyeron todas las variables y, tras la identificación de una interacción positiva entre la IC y las categorías de FEVI, se elaboró un segundo modelo estratificado según la IC durante el ingreso índice. Las capacidades discriminativa y de calibración de los modelos de supervivencia se evaluaron mediante el estadístico C de Harrell y la prueba de Gronnesby y Borgan respectivamente. La incidencia de IC podía verse afectada por la muerte del paciente y, por consiguiente, las técnicas habituales de análisis de tiempo hasta el evento habrían aportado unos resultados sesgados o ininterpretables debido a la presencia de riesgos en competencia. Para evitar esos efectos, se aplicó el modelo introducido por Fine y Gray18 para evaluar eventos en competencia. La incidencia de la IC se presenta mediante gráficos de función de incidencia acumulada y los resultados del análisis multivariable, mediante una subhazard ratio (sHR). Se utilizó la prueba del estadístico C de Harrell para evaluar la discriminación del modelo, mientras que la calibración se evaluó con la prueba de Gronnesby y Borgan. Se clasificó como no disponibles a los pacientes perdidos para el seguimiento, al igual que aquellos de los que faltaba alguna de las variables principales para los análisis, aunque estos fueron muy pocos.
Se aceptó la significación estadística con un valor de p < 0,05. Todos los análisis se realizaron con el programa Stata 14.2 (Stata Statistical Software, versión 14, StataCorp LP; College Station, Texas, Estados Unidos).
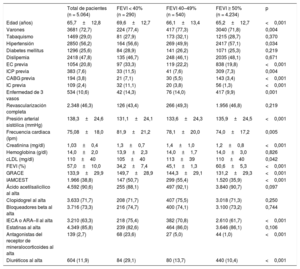
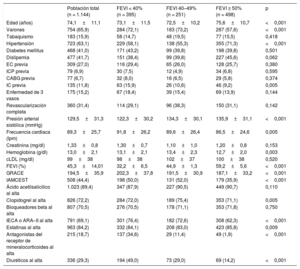
RESULTADOSCaracterísticas de los pacientes sin insuficiencia cardiaca según la fracción de eyección del ventrículo izquierdoEn total, 5.064 pacientes presentaron un SCA sin IC y se los asignó a uno de los 3 grupos siguientes definidos según la FEVI: 290 (5,7%) con FEVI < 40%, 540 (10,7%) con FEVI 40–49% y 4.234 (83,6%) con FEVI ≥ 50%. Las características de los pacientes se indican en la tabla 1. Se observaron diferencias estadísticamente significativas entre los grupos en cuanto a los parámetros de edad, antecedentes de hipertensión, enfermedad coronaria, revascularización previa (quirúrgica o percutánea), IC previa, función renal, presión arterial, frecuencia cardiaca, IAMCEST, tratamiento con inhibidores de la enzima de conversión de la angiotensina (IECA) o antagonistas del receptor de la angiotensina II, antagonistas del receptor de mineralocorticoides y diuréticos.
Características de los pacientes con síndrome coronario agudo sin insuficiencia cardiaca como función de la fracción de eyección del ventrículo izquierdo
| Total de pacientes (n = 5.064) | FEVI < 40% (n = 290) | FEVI 40–49% (n = 540) | FEVI ≥ 50% (n = 4.234) | p | |
|---|---|---|---|---|---|
| Edad (años) | 65,7±12,8 | 69,6±12,7 | 66,1±13,4 | 65,2±12,7 | <0,001 |
| Varones | 3681 (72,7) | 224 (77,4) | 417 (77,3) | 3040 (71,8) | 0,004 |
| Tabaquismo | 1469 (29,0) | 81 (27,9) | 173 (32,1) | 1215 (28,7) | 0,370 |
| Hipertensión | 2850 (56,2) | 164 (56,6) | 269 (49,9) | 2417 (57,1) | 0,034 |
| Diabetes mellitus | 1296 (25,6) | 84 (28,9) | 141 (26,2) | 1071 (25,3) | 0,219 |
| Dislipemia | 2418 (47,8) | 135 (46,7) | 248 (46,1) | 2035 (48,1) | 0,671 |
| EC previa | 1054 (20,8) | 97 (33,3) | 119 (22,2) | 838 (19,8) | <0,001 |
| ICP previa | 383 (7,6) | 33 (11,5) | 41 (7,6) | 309 (7,3) | 0,004 |
| CABG previa | 194 (3,8) | 21 (7,1) | 30 (5,5) | 143 (3,4) | <0,001 |
| IC previa | 109 (2,4) | 32 (11,1) | 20 (3,8) | 56 (1,3) | <0,001 |
| Enfermedad de 3 vasos | 534 (10,6) | 42 (14,3) | 76 (14,0) | 417 (9,9) | 0,001 |
| Revascularización completa | 2.348 (46,3) | 126 (43,4) | 266 (49,3) | 1.956 (46,8) | 0,219 |
| Presión arterial sistólica (mmHg) | 138,3±24,6 | 131,1±24,1 | 133,6±24,3 | 135,9±24,5 | <0,001 |
| Frecuencia cardiaca (lpm) | 75,08±18,0 | 81,9±21,2 | 78,1±20,0 | 74,0±17,2 | 0,005 |
| Creatinina (mg/dl) | 1,03±0,4 | 1,3±0,7 | 1,4±1,0 | 1,2±0,8 | <0,001 |
| Hemoglobina (g/dl) | 14,0±2,0 | 13,9±2,3 | 14,0±1,7 | 14,0±3,0 | 0,826 |
| cLDL (mg/dl) | 110±40 | 105±40 | 113±39 | 110±40 | 0,042 |
| FEVI (%) | 57,0±10,0 | 34,2±7,4 | 45,1±1,3 | 60,6±5,3 | <0,001 |
| GRACE | 133,9±29,9 | 149,7±28,9 | 144,3±29,1 | 131,2±29,3 | <0,001 |
| IAMCEST | 1.966 (38,8) | 147 (50,7) | 299 (55,4) | 1.520 (35,9) | <0,001 |
| Ácido acetilsalicílico al alta | 4.592 (90,6) | 255 (88,1) | 497 (92,1) | 3.840 (90,7) | 0,097 |
| Clopidogrel al alta | 3.633 (71,7) | 208 (71,7) | 407 (75,5) | 3.018 (71,3) | 0,250 |
| Bloqueadores beta al alta | 3.716 (73,3) | 216 (74,7) | 400 (74,1) | 3.100 (73,2) | 0,744 |
| IECA o ARA–II al alta | 3.210 (63,3) | 218 (75,4) | 382 (70,8) | 2.610 (61,7) | <0,001 |
| Estatinas al alta | 4.349 (85,8) | 239 (82,6) | 464 (86,0) | 3.646 (86,1) | 0,106 |
| Antagonistas del receptor de mineralocorticoides al alta | 139 (2,7) | 68 (23,6) | 27 (5,0) | 44 (1,0) | <0,001 |
| Diuréticos al alta | 604 (11,9) | 84 (29,1) | 80 (13,7) | 440 (10,4) | <0,001 |
ARA–II: antagonistas del receptores de la angiotensina II; CABG: cirugía de revascularización aortocoronaria; cLDL: colesterol unido a lipoproteínas de baja densidad; EC: enfermedad coronaria; FEVI: fracción de eyección del ventrículo izquierdo; GRACE: Global Registry of Acute Coronary Events; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IC: insuficiencia cardiaca; ICP: intervención coronaria percutánea; IECA: inhibidores de la enzima de conversión de la angiotensina.
Los datos expresan n (%) o media±desviación estándar.
Los 1.144 pacientes restantes presentaron IC (Killip ≥ 2) durante la hospitalización: 395 (34,6%) con FEVI < 40%, 251 (21,9%) con FEVI del 40–49% y 498 (43,5%) con FEVI ≥ 50%. Sus características se describen en la tabla 2. Las principales diferencias entre los grupos de FEVI fueron las observadas en los parámetros de edad, sexo y antecedentes de hipertensión, IC previa, presión arterial sistólica, frecuencia cardiaca, hemoglobina, forma de presentación del IAMCEST y tratamiento con IECA, antagonistas del receptor de mineralocorticoides y diuréticos.
Características de los pacientes con síndrome coronario agudo e insuficiencia cardiaca como función de la fracción de eyección del ventrículo izquierdo
| Población total (n = 1.144) | FEVI < 40% (n = 395) | FEVI 40–49% (n = 251) | FEVI ≥ 50% (n = 498) | p | |
|---|---|---|---|---|---|
| Edad (años) | 74,1±11,1 | 73,1±11,5 | 72,5±10,2 | 75,6±10,7 | <0,001 |
| Varones | 754 (65,9) | 284 (72,1) | 183 (73,2) | 287 (57,6) | <0,001 |
| Tabaquismo | 183 (15,9) | 58 (14,7) | 48 (19,5) | 77 (15,5) | 0,418 |
| Hipertensión | 723 (63,1) | 229 (58,1) | 138 (55,3) | 355 (71,3) | <0,001 |
| Diabetes mellitus | 468 (41,0) | 171 (43,2) | 99 (39,8) | 198 (39,8) | 0,501 |
| Dislipemia | 477 (41,7) | 151 (38,4) | 99 (39,8) | 227 (45,6) | 0,062 |
| EC previa | 309 (27,0) | 116 (29,4) | 65 (26,0) | 128 (25,7) | 0,380 |
| ICP previa | 79 (6,9) | 30 (7,5) | 12 (4,9) | 34 (6,8) | 0,595 |
| CABG previa | 77 (6,7) | 32 (8,0) | 16 (6,5) | 29 (5,8) | 0,374 |
| IC previa | 135 (11,8) | 63 (15,9) | 26 (10,6) | 46 (9,2) | 0,005 |
| Enfermedad de 3 vasos | 175 (15,2) | 67 (18,4) | 39 (15,4) | 69 (13,9) | 0,144 |
| Revascularización completa | 360 (31,4) | 114 (29,1) | 96 (38,3) | 150 (31,1) | 0,142 |
| Presión arterial sistólica (mmHg) | 129,5±31,3 | 122,3±30,2 | 134,3±30,1 | 135,9±31,1 | <0,001 |
| Frecuencia cardiaca (lpm) | 89,3±25,7 | 91,8±26,2 | 89,6±26,4 | 86,5±24,6 | 0,005 |
| Creatinina (mg/dl) | 1,33±0,8 | 1,30±0,7 | 1,10±1,0 | 1,20±0,8 | 0,153 |
| Hemoglobina (g/dl) | 13,0±2,1 | 13,1±2,1 | 13,4±2,3 | 12,7±2,0 | 0,003 |
| cLDL (mg/dl) | 99±38 | 98±38 | 102±37 | 100±38 | 0,520 |
| FEVI (%) | 45,3±14,01 | 32,2±6,5 | 44,9±1,3 | 59,2±5,6 | <0,001 |
| GRACE | 194,5±35,9 | 202,3±37,8 | 191,5±30,9 | 187,1±33,2 | <0,001 |
| IAMCEST | 508 (44,4) | 198 (50,0) | 131 (52,0) | 179 (35,9) | <0,001 |
| Ácido acetilsalicílico al alta | 1.023 (89,4) | 347 (87,9) | 227 (90,5) | 449 (90,7) | 0,110 |
| Clopidogrel al alta | 826 (72,2) | 284 (72,0) | 189 (75,4) | 353 (71,1) | 0,005 |
| Bloqueadores beta al alta | 807 (70,5) | 276 (70,5) | 178 (71,1) | 353 (71,8) | 0,750 |
| IECA o ARA–II al alta | 791 (69,1) | 301 (76,4) | 182 (72,6) | 308 (62,3) | <0,001 |
| Estatinas al alta | 963 (84,2) | 332 (84,1) | 208 (83,0) | 423 (85,8) | 0,009 |
| Antagonistas del receptor de mineralocorticoides al alta | 215 (18,7) | 137 (34,6) | 29 (11,4) | 49 (1,9) | <0,001 |
| Diuréticos al alta | 336 (29,3) | 194 (49,0) | 73 (29,0) | 69 (14,2) | <0,001 |
ARA–II: antagonistas del receptores de la angiotensina II; CABG: cirugía de revascularización aortocoronaria; cLDL: colesterol unido a lipoproteínas de baja densidad; EC: enfermedad coronaria; FEVI: fracción de eyección del ventrículo izquierdo; GRACE: Global Registry of Acute Coronary Events; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IC: insuficiencia cardiaca; ICP: intervención coronaria percutánea; IECA: inhibidores de la enzima de conversión de la angiotensina.
Los datos expresan n (%) o media±desviación estándar.
La incidencia de IC fue progresivamente superior en cada categoría de FEVI (figura 2). La mortalidad hospitalaria fue del 4,0% (IC95%, 3,4-4,5) y aumentó de manera gradual en cada categoría de FEVI: el 1,75% (FEVI ≥ 50%), el 5,44% (FEVI 40–49%) y el 17,60% (FEVI < 40%) (p < 0,01), así como en los pacientes que presentaron IC en comparación con los que no: el 22,5 frente al 1,4% (p < 0,01).
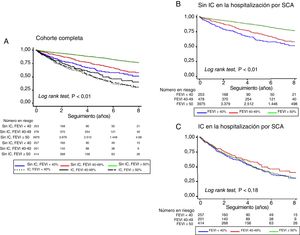
Pronóstico tras el altaSe dispuso de seguimiento tras el alta del 91,8% de los pacientes, con una mediana de 4,4 [intervalo intercuartílico, 2,2-6,5] años. La mortalidad por cualquier causa fue del 22,5% (IC95%, 21,5-23,5) y muy superior en los pacientes con IC durante la hospitalización por SCA (el 50,4 frente al 17,6%; p < 0,001). Tal como se muestra en la figura 3A, en los pacientes sin IC durante la hospitalización por SCA, la tasa más baja se observó en aquellos con FEVI ≥ 50% (15,4%), seguidos de los pacientes con FEVI del 40–49% (25,4%) y < 40% (29,4%); en cambio, no se observaron diferencias en los pacientes que sufieron IC durante la hospitalización por SCA (figura 3B).
Curvas de Kaplan-Meier para el tiempo sin eventos de muerte por cualquier causa, según las categorías de FEVI en el conjunto de la cohorte (A), en los pacientes sin IC (B) y en los pacientes con IC (C) durante la hospitalización. FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; SCA: síndrome coronario agudo.
Se realizó un análisis de la supervivencia con punto temporal de referencia (landmark analysis) con una evaluación de la mortalidad a 1 año, y los resultados en cuanto a la mortalidad por cualquier causa fueron los mismos (figura del material suplementario).
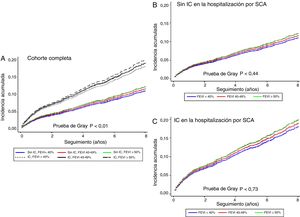
La incidencia de IC después del alta del hospital fue del 13,3% (IC95%, 12,5-14,1) y fue más alta en los pacientes con IC durante la hospitalización por SCA (el 31,5 frente al 10,0%; p < 0,001). Tal como se muestra en la figura 4A, entre los pacientes sin IC durante la hospitalización por SCA, la tasa más alta fue la observada en aquellos con FEVI < 40% (18,2%) o del 40–49% (17,2%), mientras que fue muy inferior en los pacientes con FEVI ≥ 50% (8,3%). No obstante, no se observaron diferencias según la FEVI entre los pacientes con IC durante la hospitalización por SCA (figura 4B).
Gráficos de incidencia acumulada de la función de IC después del alta según las categorías de FEVI en el conjunto de la cohorte (A), los pacientes sin IC (B) y los pacientes con IC (C) durante la hospitalización. FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; SCA: síndrome coronario agudo.
El análisis multivariable de la mortalidad por cualquier causa y la IC se ajustó según los factores edad, sexo, diabetes mellitus, enfermedad coronaria previa, IC previa, revascularización completa, tratamiento con diuréticos, IECA y bloqueadores beta y FEVI.
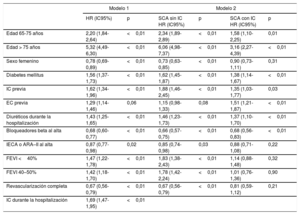
La IC durante la hospitalización, la FEVI < 40% y la FEVI del 40–49% se asociaron con la mortalidad por cualquier causa y la IC tras el alta en un primer análisis (tabla 3), y se observó una interacción positiva entre la IC al ingreso y la FEVI; en consecuencia, el modelo final se diseñó con estas interacciones. La capacidad discriminatoria (estadístico C de Harrell = 0,79; IC95%, 0,78-0,80) y la capacidad de calibración (prueba de Gronnesby y Borgan, p = 0,73) de los modelos de supervivencia fueron altas. Una FEVI más alta, una revascularización completa y el sexo femenino se asociaron con menor mortalidad tan solo en los pacientes sin IC durante la hospitalización por SCA. El efecto de la edad en la mortalidad a largo plazo fue menor entre los pacientes que sufrieron IC durante la hospitalización (p = 0,01).
Resultados del análisis multivariable de evaluación de los factores independientes predictivos de la mortalidad por cualquier causa
| Modelo 1 | Modelo 2 | |||||
|---|---|---|---|---|---|---|
| HR (IC95%) | p | SCA sin IC HR (IC95%) | p | SCA con IC HR (IC95%) | p | |
| Edad 65-75 años | 2,20 (1,84-2,64) | <0,01 | 2,34 (1,89-2,89) | <0,01 | 1,58 (1,10-2,25) | 0,01 |
| Edad > 75 años | 5,32 (4,49-6,30) | <0,01 | 6,06 (4,98-7,37) | <0,01 | 3,16 (2,27-4,39) | <0,01 |
| Sexo femenino | 0,78 (0,69-0,89) | <0,01 | 0,73 (0,63-0,85) | <0,01 | 0,90 (0,73-1,11) | 0,31 |
| Diabetes mellitus | 1,56 (1,37-1,73) | <0,01 | 1,62 (1,45-1,87) | <0,01 | 1,38 (1,14-1,67) | <0,01 |
| IC previa | 1,62 (1,34-1,96) | <0,01 | 1,88 (1,46-2,45) | <0,01 | 1,35 (1,03-1,77) | 0,03 |
| EC previa | 1,29 (1,14-1,46) | 0,06 | 1,15 (0,98-1,33) | 0,08 | 1,51 (1,21-1,87) | <0,01 |
| Diuréticos durante la hospitalización | 1,43 (1,25-1,65) | <0,01 | 1,46 (1,23-1,73) | <0,01 | 1,37 (1,10-1,70) | <0,01 |
| Bloqueadores beta al alta | 0,68 (0,60-0,77) | <0,01 | 0,66 (0,57-0,75) | <0,01 | 0,68 (0,56-0,83) | <0,01 |
| IECA o ARA–II al alta | 0,87 (0,77-0,98) | 0,02 | 0,85 (0,74-0,98) | 0,03 | 0,88 (0,71-1,08) | 0,22 |
| FEVI <40% | 1,47 (1,22-1,78) | <0,01 | 1,83 (1,38-2,43) | <0,01 | 1,14 (0,88-1,48) | 0,32 |
| FEVI 40–50% | 1,42 (1,18-1,70) | <0,01 | 1,78 (1,42-2,24) | <0,01 | 1,01 (0,76-1,36) | 0,90 |
| Revascularización completa | 0,67 (0,56-0,79) | <0,01 | 0,67 (0,56-0,79) | <0,01 | 0,81 (0,59-1,12) | 0,21 |
| IC durante la hospitalización | 1,69 (1,47-1,95) | <0,01 | ||||
ARA–II: antagonistas del receptor de la angiotensina II; EC: enfermedad coronaria; FEVI: fracción de eyección del ventrículo izquierdo; HR: hazard ratio; IC: insuficiencia cardiaca; IC95%: intervalo de confianza del 95%; IECA: inhibidores de la enzima de conversión de la angiotensina; SCA: síndrome coronario agudo.
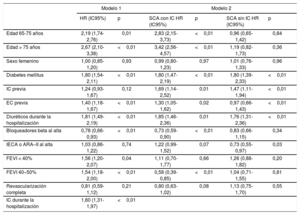
Los predictores independientes de IC tras el alta se indican en la tabla 4. La FEVI del 40-49% se asoció de manera independiente con la tasa más baja de IC tras el alta solo en los pacientes que no sufrieron IC durante la hospitalización. La capacidad discriminatoria (estadístico C de Harrell = 0,76; IC95%, 0,72-0,81) y la capacidad de calibración (prueba de Gronnesby y Borgan, p = 0,73) de los modelos de regresión de riesgos en competencia fueron suficientes para los fines pretendidos. Como análisis de sensibilidad interno, se investigaron posibles cambios de las características clínicas de los pacientes en todo el prolongado periodo de inclusión dividiendo la cohorte en 3 periodos (2004-2006, 2007-2010 y 2011-2014). No se observaron diferencias en cuanto a edad o sexo, y solo hubo un ligero aumento en la prevalencia de la hipertensión. El porcentaje de pacientes con IAMCEST aumentó significativamente durante el periodo de inclusión, pero no así la media de la puntuación GRACE. Las prevalencias de FEVI < 40% (el 15,7, el 15,8 y el 18,6%; p = 0,09) y de IC durante la hospitalización (el 18,3, el 19,3 y el 17,6%; p = 0,337) no mostraron diferencias entre los 3 periodos.
Resultados del análisis multivariable de evaluación de los factores independientes predictivos de insuficiencia cardiaca tras el alta
| Modelo 1 | Modelo 2 | |||||
|---|---|---|---|---|---|---|
| HR (IC95%) | p | SCA con IC HR (IC95%) | p | SCA sin IC HR (IC95%) | p | |
| Edad 65-75 años | 2,19 (1,74-2,76) | 0,01 | 2,83 (2,15-3,73) | <0,01 | 0,96 (0,65-1,42) | 0,84 |
| Edad > 75 años | 2,67 (2,10-3,38) | <0,01 | 3,42 (2,56-4,57) | <0,01 | 1,19 (0,82-1,73) | 0,36 |
| Sexo femenino | 1,00 (0,85-1,20) | 0,93 | 0,99 (0,80-1,23) | 0,97 | 1,01 (0,76-1,33) | 0,96 |
| Diabetes mellitus | 1,80 (1,54-2,11) | <0,01 | 1,80 (1,47-2,19) | <0,01 | 1,80 (1,39-2,33) | <0,01 |
| IC previa | 1,24 (0,93-1,67) | 0,12 | 1,69 (1,14-2,52) | 0,01 | 1,47 (1,11-1,94) | <0,01 |
| EC previa | 1,40 (1,18-1,67) | <0,01 | 1,30 (1,05-1,62) | 0,02 | 0,97 (0,66-1,43) | <0,01 |
| Diuréticos durante la hospitalización | 1,81 (1,49-2,19) | <0,01 | 1,85 (1,46-2,36) | 0,01 | 1,76 (1,31-2,36) | <0,01 |
| Bloqueadores beta al alta | 0,78 (0,66-0,93) | <0,01 | 0,73 (0,59-0,90) | <0,01 | 0,83 (0,66-1,15) | 0,34 |
| IECA o ARA–II al alta | 1,03 (0,86-1,22) | 0,74 | 1,22 (0,99-1,52) | 0,07 | 0,73 (0,55-0,97) | 0,03 |
| FEVI < 40% | 1,56 (1,20-2,07) | 0,04 | 1,11 (0,70-1,77) | 0,66 | 1,26 (0,88-1,82) | 0,20 |
| FEVI 40–50% | 1,54 (1,18-2,00) | <0,01 | 0,58 (0,39-0,85) | <0,01 | 1,04 (0,71-1,55) | 0,81 |
| Revascularización completa | 0,81 (0,59-1,12) | 0,21 | 0,80 (0,63-1,02) | 0,08 | 1,13 (0,75-1,70) | 0,55 |
| IC durante la hospitalización | 1,60 (1,31-1,97) | <0,01 | ||||
ARA–II: antagonistas del receptor de la angiotensina II; EC: enfermedad coronaria; FEVI: fracción de eyección del ventrículo izquierdo; HR: hazard ratio; IC: insuficiencia cardiaca; IC95%: intervalo de confianza del 95%; IECA: inhibidores de la enzima de conversión de la angiotensina; SCA: síndrome coronario agudo.
En el presente estudio de pacientes con SCA de 2 hospitales españoles, se observó que la FEVI de los pacientes con IC no estaba relacionada con el pronóstico a largo plazo. En cambio, en los pacientes sin IC durante la hospitalización, la FEVI fue un predictor pronóstico potente. Ello indica que el tratamiento del SCA complicado con IC continúa siendo un verdadero reto, con independencia de la categoría de la FEVI. Nuestras observaciones confirman y resaltan que un diagnóstico clínico de IC en los pacientes con SCA es un signo de muy mal pronóstico, también para los pacientes con FEVI normal, incluso ahora que se aplican a los pacientes con SCA estrategias de tratamiento invasivo y no invasivo de alta eficacia.
Independientemente de la presencia de IC, los pacientes con FEVI < 40% eran predominantemente varones con antecedentes de enfermedad coronaria y revascularización y con más comorbilidades, como se ha descrito con anterioridad19 (tabla 1 y tabla 2). Estos pacientes eran mayoritarios en el grupo de IC (34,6%) en comparación con lo observado en el grupo sin IC, en el que la FEVI ≥ 50% fue la forma predominante (83,4%).
El grupo con valores medios de FEVI constituyó una pequeña parte de los pacientes con SCA, y estos pacientes tenían un perfil demográfico y clínico intermedio, con muchas características intermedias entre las de los grupos de FEVI reducida y conservada (tabla 1 y tabla 2). Estos resultados son similares a los observados en los pacientes con IC aguda descompensada o IC crónica14,20. El grupo de pacientes con SCA e IC con FEVI ≥ 50% mostró un perfil similar al de los pacientes con IC y fracción de eyección conservada, eran de más edad e incluían un mayor porcentaje de mujeres y de individuos hipertensos en comparación con los demás grupos21.
De manera similar a lo observado en investigaciones previas12,19, se observó que, durante el seguimiento, los pacientes con IC tenían una mortalidad superior y más reingresos por IC que los pacientes sin IC.
Han transcurrido más de 40 años desde que Killip describiera por primera vez la importancia de los signos clínicos de disfunción e IC tras el infarto agudo de miocardio en la evaluación del riesgo de mortalidad22. Desde entonces, numerosos estudios han identificado la IC en el contexto del infarto de miocardio como un importante factor predictivo del pronóstico22,23. Actualmente, en una era de estrategias terapéuticas de gran eficacia, se asiste a un notable descenso de la incidencia de la IC como complicación de los SCA. Sin embargo, la IC continúa empeorando el riesgo pronóstico temprano, intermedio y a largo plazo tras el SCA23, y hay poca información acerca del tratamiento de este síndrome en la actual era intervencionista.
No se ha descrito claramente el valor pronóstico de la FEVI en pacientes con SCA e IC. En el registro VALIANT, la IC con disfunción sistólica se asoció con más complicaciones, hospitalizaciones más largas y mayor mortalidad a largo plazo7. En 1988, en la era del tratamiento no invasivo del SCA, Nicod et al.24 señalaron que el valor pronóstico de la IC como complicación del SCA no dependía de la FEVI.
El reciente estudio Acute Coronary Syndrome Israeli Survey observó que la FEVI era un potente predictor de la mortalidad 1 año tras el SCA, con independencia de la presencia de IC25, pero en el registro SWEDEHEART se ha observado que los pacientes con SCA e IC con FEVI conservada presentaban un pronóstico a largo plazo tan solo ligeramente mejor que los pacientes con IC y FEVI reducida12, cuya tasa de mortalidad fue muy superior a la de los pacientes dados de alta sin signos de IC, con independencia de cuál fuera la FEVI12.
En nuestro estudio se obtuvieron resultados similares; los pacientes que sufrieron IC durante la hospitalización tuvieron tasas más altas de mortalidad y de reingresos por IC durante el seguimiento. Sin embargo, este mal pronóstico no dependía de la FEVI (figura 3 y figura 4), lo cual indica que, en los pacientes con SCA, una vez establecido el síndrome de IC durante la hospitalización, el pronóstico a largo plazo no estaba relacionado con la FEVI, por lo que todos estos pacientes deben ser tratados como pacientes en muy alto riesgo. Con independencia de estas observaciones, varios registros han observado que existe la posibilidad de mejorar el tratamiento de esta población en alto riesgo4,23.
El papel de la revascularización completa de los pacientes con SCA con y sin IC en cuanto a la reducción del riesgo de mortalidad y morbilidad (agravamiento o aparición de la IC) es una cuestión controvertida26. Las guías actuales recomiendan una estrategia de revascularización de la lesión culpable y el tratamiento de las lesiones crónicas en función de la presencia de isquemia/angina13. Sin embargo, los resultados del subanálisis del estudio STICH recientemente publicado ponen en duda la utilidad de la revascularización sistemática de los pacientes con angina y FEVI reducida27. En nuestros centros se aplica esta estrategia, y ello podría influir en el porcentaje de pacientes con revascularización completa.
En cohortes históricas y contemporáneas de pacientes con SCA, se ha descrito que la FEVI es un importante predictor de los resultados clínicos tras el infarto agudo de miocardio19,28,29. El deterioro de la FEVI después de un SCA puede deberse a una lesión miocárdica irreversible y al proceso de remodelado, que causa dilatación progresiva y un deterioro de la función contráctil que conduce a IC, muerte y arritmias mortales30.
Nuestras observaciones pusieron de manifiesto que la FEVI durante la hospitalización era un poderoso determinante de la mortalidad de los pacientes sin IC. El grupo con FEVI < 40% tuvo un pronóstico mucho peor que los otros 2 grupos (FEVI 40–49% y ≥ 50%). Además, en los pacientes sin IC, la FEVI < 40% se asoció con IC después del alta; el grupo con valores de FEVI medios mostró tendencia a mejores resultados por lo que respecta al reingreso por IC, probablemente porque eran más parecidos a los pacientes con FEVI conservada14.
De manera similar a lo resaltado por otros autores en pacientes sin IC19,31,32, se observó que los factores edad, sexo femenino, diabetes mellitus, enfermedad coronaria previa, IC previa, revascularización completa y tratamiento con diuréticos, IECA y bloqueadores beta eran factores que predecían los resultados (tabla 3 y tabla 4).
En nuestro estudio, las mujeres de ambos grupos (con y sin IC) tenían con mayor probabilidad una función sistólica conservada y tendían a tener más comorbilidades. El mecanismo que subyace a estas observaciones no se conoce, aunque algunas publicaciones indican la posible existencia de diferencias intrínsecas en función del sexo en el proceso de remodelado cardiaco tras el SCA12,23.
Puntos fuertes y limitacionesEste estudio tiene varios puntos fuertes: presenta una cohorte contemporánea con una muestra amplia y una potencia estadística elevada, por lo que los resultados se pueden generalizar a la práctica clínica real. Se incluyó un gran número de pacientes con seguimiento muy largo. Se examinó el diferente pronóstico de los pacientes con SCA y FEVI < 40%, del 40–49% y ≥ 50%, y se analizaron también los factores pronósticos a largo plazo en función de la aparición de IC.
El estudio tiene también algunas limitaciones. En primer lugar, se trata de un análisis observacional y retrospectivo y no se pudo determinar la FEVI de un 12,2% de la población en estudio; en estudios previos se ha descrito que la falta de datos ecocardiográficos no es infrecuente en la práctica clínica33. Además, se perdió el seguimiento del 8,2% de los pacientes. Se utilizó la clasificación propuesta por la guía ESC de IC en el contexto del SCA, lo que podría ser una limitación del estudio. Como ocurre en cualquier estudio observacional, no se puede descartar un efecto de confusión residual debido a variables no medidas. Además, puede haber contraindicaciones apropiadas a la farmacoterapia adyuvante o a la angiografía invasiva que no se identificaran o que se desconocieran. Se utilizó el método de Simpson para estimar la FEVI según lo indicado por las recomendaciones internacionales, con las limitaciones inherentes a ello. No se dispuso de datos sobre biomarcadores útiles en la IC, como el péptido natriurético cerebral, la región media del propéptido natriurético auricular, el ST2 soluble o la galectina-3. El presente estudio se inició en 2004, lo que explica que el uso de bloqueadores beta e IECA fuera inferior al estimado. A lo largo de los años, el uso de estos fármacos ha aumentado progresivamente en ambos centros. No se identificaron la adherencia al tratamiento ni los cambios de la FEVI durante el seguimiento. Además, se desconoce el porcentaje de uso de IECA, bloqueadores beta y antagonistas del receptor de mineralocorticoides que se mantuvo durante el ingreso. Por último, las tasas de revascularización y revascularización completa no fueron demasiado altas, lo cual refleja simplemente la práctica clínica diaria de los 2 centros, que disponen de laboratorios de hemodinámica, tal como se ha descrito anteriormente.
CONCLUSIONESEn una cohorte amplia de pacientes con SCA, se ha puesto de manifiesto que la FEVI en el subgrupo con IC no estaba relacionada con el pronóstico a largo plazo. En el subgrupo de pacientes sin síndrome de IC clínico durante la hospitalización, la FEVI fue un predictor pronóstico potente. El pronóstico desfavorable de los pacientes con SCA e IC indica que los esfuerzos terapéuticos deben centrarse en este grupo de pacientes, con independencia de la FEVI.
FINANCIACIÓNEste estudio fue patrocinado por el Complejo Hospitalario Universitario de Santiago de Compostela (Santiago de Compostela, A Coruña, España) y contó con la financiación conjunta del Instituto de Salud Carlos III-Subdirección General de Evaluación y Fomento de la Investigación y del Fondo Europeo de Desarrollo Regional.
CONFLICTO DE INTERESESNo se declara ninguno.
- -
Escasean datos contemporáneos sobre la incidencia y el pronóstico de la IC y la influencia de la FEVI y la nueva clasificación de la IC de la ESC basada en este parámetro en el contexto del SCA.
- -
En los pacientes con SCA, se observa que la aparición de la IC durante la hospitalización se asocia con peor pronóstico a largo plazo que el de los pacientes sin IC, con independencia de la FEVI. Este parámetro es un potente predictor pronóstico solo en los pacientes sin IC.
- -
El mal pronóstico de los pacientes con SCA e IC indica que los esfuerzos terapéuticos deben centrarse en este grupo, con independencia de la FEVI.