OBJETIVO: Analizar y cuantificar las modificaciones de los electrogramas auriculares tras la realización de lesiones lineales en la pared auricular utilizando procedimientos de ablación con radiofrecuencia.
MÉTODOS: En 12 preparaciones de corazón aislado de conejo según la técnica de Langendorff se ha utilizado un electrodo múltiple epicárdico (221 electrodos unipolares) para analizar la activación auricular antes y después de la realización de una lesión lineal en la pared auricular izquierda mediante aplicaciones sucesivas de radiofrecuencia. Tras comprobar la existencia de bloqueo de la conducción en la zona lesionada mediante cartografía epicárdica y análisis de los vectores de propagación, en cada experimento se han seleccionado seis electrodos en la zona lesionada y otros seis en la no lesionada. En ambas zonas se ha comparado la amplitud, la máxima pendiente negativa y la morfología de los electrogramas antes (control) y después de las aplicaciones de radiofrecuencia.
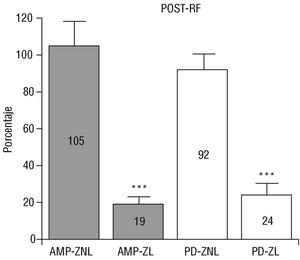
RESULTADOS: El análisis de la reproducibilidad de las mediciones en dos ciclos consecutivos ha puesto de manifiesto una variación en la amplitud de un 1 ± 5% (NS) y en la pendiente de un 1 ± 9% (NS). En la zona no lesionada, la amplitud (105 ± 22%) y la pendiente (92 ± 16%) (valores normalizados con respecto a los obtenidos en el control) no han variado significativamente tras las aplicaciones de radiofrecuencia, y los registros de electrogramas simples han sido los más frecuentes (el 82 frente al 83% en el control; NS). En la zona lesionada, la amplitud (19 ± 7%, p < 0,001) y la pendiente (24 ± 11%; p < 0,001) han disminuido significativamente, así como los porcentajes de electrogramas simples (el 6 frente al 86% en el control; p < 0,001). En esta zona no se ha podido determinar la morfología en un 12% de los registros, se han obtenido electrogramas múltiples en un 15% (frente a un 2% en el control; p < 0,01) y el tipo más frecuente ha correspondido al de electrogramas dobles (el 67 frente al 12% en el control; p < 0,001) cuyos dos componentes han coincidido en el tiempo con la activación auricular en la zonas situadas proximal y distalmente a la lesión.
CONCLUSIÓN: Los electrogramas obtenidos directamente sobre líneas de bloqueo originadas con radiofrecuencia se caracterizan por presentar una reducción significativa de la amplitud y de la máxima pendiente negativa. En estos registros predominan los electrogramas dobles cuyos dos componentes representan la activación a ambos lados de la lesión. En la línea de bloqueo pueden registrarse también en un porcentaje reducido de casos electrogramas simples y múltiples.
Palabras clave
Ablación con radiofrecuencia
Lesiones lineales
Activación auricular
Cartografía
Electrofisiología cardíaca
Modelos experimentales
INTRODUCCIÓN
La utilización de la ablación con radiofrecuencia (RF) para el tratamiento de diversas arritmias supraventriculares como la fibrilación auricular 1-12, taquicardias auriculares 13-15 o el flúter auricular 16-20 requiere el análisis de los efectos que producen las aplicaciones de RF sobre los patrones de activación auricular y sobre los mecanismos que inducen o sustentan este tipo de arritmias. La utilización de la RF requiere también conocer las repercusiones estructurales y funcionales de las lesiones producidas 1-3,5,7,10,21-25 para aumentar la seguridad del procedimiento y evitar posibles complicaciones. La realización de lesiones lineales ha subrayado la importancia de disponer de indicadores que aporten información sobre su localización y extensión, además de sus repercusiones funcionales. Los procedimientos cartográficos permiten conocer con exactitud las modificaciones de los patrones de activación y, por tanto, ayudan a demostrar la consecución de líneas de bloqueo completo 11,12,26-29; sin embargo, tanto durante como tras la realización de las lesiones es útil disponer de indicadores basados en el análisis de los electrogramas auriculares, registrados tanto en las zonas afectadas como en las sanas, que puedan orientar durante la realización del procedimiento. Por otra parte, la obtención de mapas de activación auricular mediante técnicas cartográficas requiere la identificación y valoración adecuadas de los electrogramas obtenidos. La aplicación de RF en el tejido miocárdico se caracteriza por la lesión térmica del mismo 21-23,30-35 y por la supresión de las propiedades eléctricas activas de las fibras destruidas, que implica modificaciones en las características de los electrogramas, tanto extra como intracelulares 36,37. En el presente trabajo se utiliza un modelo experimental con corazones aislados y perfundidos de conejo en los que, mediante cartografía epicárdica de alta resolución y análisis de los vectores de propagación, se comprueba la obtención de líneas de bloqueo completo aplicando técnicas de ablación con RF. Se pretende analizar y cuantificar las modificaciones inducidas en los electrogramas auriculares registrados en la zona lesionada y establecer las diferencias existentes con respecto a los obtenidos en las zonas no afectadas directamente por las lesiones. MÉTODOS
Preparación experimental
Se han estudiado 12 conejos de raza California (peso medio 3,9 ± 0,4 kg). Tras anestesia (ketamina, 25 mg/kg i.m.) y heparinización, se ha extraído el corazón sumergiéndolo en Tyrode frío (4 oC). Tras aislar la aorta se ha conectado a un sistema de Langendorff para perfundir retrógradamente Tyrode a una presión de 60 mmHg y una temperatura de 37 ± 0,5 oC. La composición milimolar del líquido de perfusión es: ClNa 125, CO 3HNa 24,2, ClK 4,7, Cl 2Ca 2,2, PO 4H 2Na 1,2, Cl 2Mg 0,6 y glucosa 12. La oxigenación se ha efectuado con una mezcla de 95% de O 2 y 5% de CO 2.
Tras abrir la aurícula derecha mediante una incisión desde la zona de entrada de la vena cava superior hasta la inferior, paralela a la crista terminalis, se ha seccionado la parte central del tabique interauricular, en la zona de la fosa oval, para introducir en la aurícula izquierda un soporte ovoideo de 2,5 x 2 cm con el objeto de facilitar el contacto del electrodo epicárdico múltiple utilizado para efectuar los registros del proceso de activación auricular izquierdo. Los registros se han efectuado con una placa-electrodo (2,5 x 2,5 cm) compuesta por 221 electrodos unipolares de acero inoxidable (diámetro de 0,125 mm), que se ha situado sobre la pared libre auricular izquierda. La zona central del electrodo está compuesta por 121 electrodos dispuestos según una disposición cuadrangular, con 11 electrodos en cada lado (distancia interelectrodo de 1 mm) y rodeando a esta zona central existen 108 electrodos situados según una disposición también cuadrangular (filas de 12 electrodos con una separación interelectrodo de 2 mm). Los dos electrodos situados en la zona media de cada una de las filas más periféricas se han utilizado para efectuar estimulación auricular y no se han empleado para obtener registros. Se ha utilizado como electrodo indiferente una placa de Ag/AgCl (0,5 x 1 cm) situada sobre la aorta previamente canulada. Además, se ha usado un electrodo bipolar de acero inoxidable (diámetro de 0,125 mm, distancia interelectrodo de 1 mm) para efectuar registros epicárdicos en la pared lateral del ventrículo derecho. Se ha empleado un estimulador GRASS S88 provisto de una unidad de aislamiento de estímulos (SIU5) y se han emitido estímulos rectangulares con una duración de 2 ms e intensidad doble del umbral diastólico. Los registros se han efectuado utilizando un sistema de cartografía de la actividad eléctrica cardíaca (MAPTECH). Los electrogramas se han amplificado con una ganancia de 300-500, que se ha mantenido constante a lo largo de todo el experimento, se han filtrado (banda de 1 a 400 Hz) y se han multiplexado. La frecuencia de muestreo en cada canal ha sido de 1 kHz. Los datos obtenidos en cada experimento se han almacenado en cinta magnética para efectuar un análisis posterior.
Protocolo experimental
Antes y después de efectuar las lesiones con RF se ha registrado la activación auricular durante la estimulación con ciclos constantes (250 ms) que se ha realizado con los electrodos de estimulación localizados en la zona posterior de la pared auricular izquierda. Las lesiones con RF se han llevado a cabo desde el epicardio de la pared auricular izquierda mediante un electrodo unipolar de Ag/AgCl aislado con teflón hasta su extremo distal (diámetro de 1 mm, longitud de la zona libre distal de 1 mm). Se ha utilizado un generador de corriente HAT 100 con una potencia de 5 W y un tiempo de emisión en cada aplicación de 8 s, empleando como electrodo indiferente una placa de 8 x 12 mm situada alrededor de la cánula de perfusión. Para mantener una impedancia baja durante las aplicaciones de RF se ha bañado con Tyrode la zona en la que se situaba el electrodo. Las lesiones lineales en la pared auricular izquierda se han obtenido según un procedimiento secuencial efectuando aplicaciones sucesivas de RF. En primer lugar se han realizado tres lesiones separadas entre sí y dispuestas verticalmente en la zona central (media, superior e inferior) de la pared libre auricular izquierda. A continuación se han añadido dos lesiones más, situándolas entre la lesión central y las lesiones superior e inferior efectuadas con anterioridad, y por último se han añadido cuatro lesiones entre las efectuadas anteriormente para hacerlas confluentes por completo. Así se ha obtenido una lesión única que atraviesa verticalmente la zona media de la pared libre auricular izquierda, dejando tejido no lesionado entre los extremos superior e inferior de la lesión y los bordes de la aurícula.
Parámetros analizados
Activación auricular
Se han construido los mapas de activación auricular tras determinar el tiempo de activación local en cada electrodo unipolar del electrodo múltiple 7,23,38,39. Para ello se ha identificado el momento de máxima pendiente negativa (-dV/dt) de los electrogramas auriculares y se han construido las isócronas semiautomáticamente. La codificación en color de los intervalos entre un tiempo de referencia (el estímulo) y los tiempos de activación local (fig. 1), así como la determinación de los vectores de propagación, ha permitido caracterizar los patrones de activación durante el control y tras efectuar las lesiones con RF. Para determinar los vectores de propagación se ha utilizado el procedimiento descrito previamente 23; así, tras seleccionar agrupaciones de cuatro electrodos en disposición cuadrangular con lados de 2 mm, cada cuadripolo se ha dividido en dos triángulos, calculando el vector de propagación en cada triángulo. Se ha tomado el promedio de ambos para determinar la dirección de la propagación en cada cuadripolo. Se ha considerado que existía bloqueo completo de la conducción a través de las lesiones cuando éstas daban lugar a una modificación de la dirección del proceso de activación en la zona distal a la lesión, adoptando en dicha zona una dirección paralela a la lesión lineal al tener que rodearla para alcanzar esta zona. Para ello se han comparado el mapa de activación y los vectores de propagación obtenidos una vez transcurridos 20 min desde la finalización de las aplicaciones de RF con los obtenidos en la fase de control (figs. 2 y 3). La situación de la zona lesionada en la matriz del electrodo múltiple se ha identificado utilizando las referencias anatómicas de las lesiones y precisando la posición del electrodo en relación con las mismas referencias.
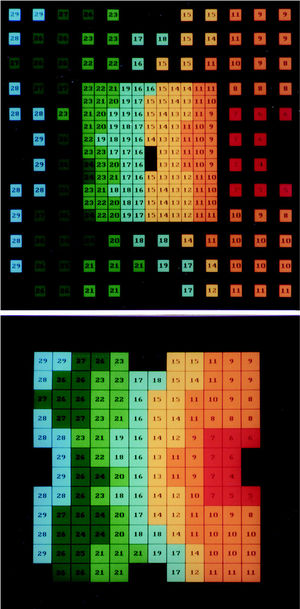
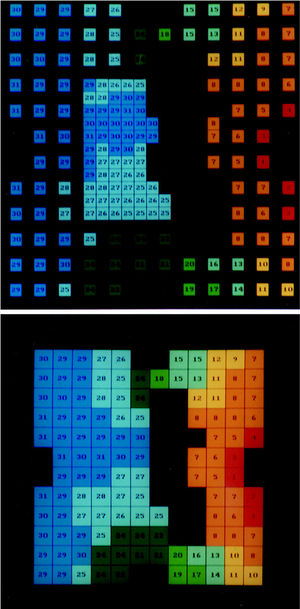
Fig. 1. Arriba: mapa de activación auricular izquierda obtenido en la fase de control durante la estimulación desde la zona posterior de la aurícula (situada a la derecha de la figura). En la zona central la distancia interelectrodo es de 1 mm y en la periferia de 2 mm. Los tiempos de activación local se han codificado en color y los cambios en la escala de colores se han efectuado cada 4 ms, de modo que la activación más precoz corresponde al color rojo y la más tardía al azul. Abajo: mapa de activación del mismo experimento, también durante la fase de control, en cuya representación se han suprimido uno de cada dos electrodos de la parte central del mismo con el objeto de visualizar mejor el proceso de activación auricular (distancia interelectrodo de 2 mm).
Fig. 2. Mapas de activación auricular izquierda similares a los representados en la figura 1 y obtenidos en el mismo experimento tras efectuar las lesiones con radiofrecuencia. Se observa la modificación del proceso de activación originada por la zona lesionada (zona vertical no coloreada) que condiciona que la activación alcance la zona distal rodeando a la zona lesionada.
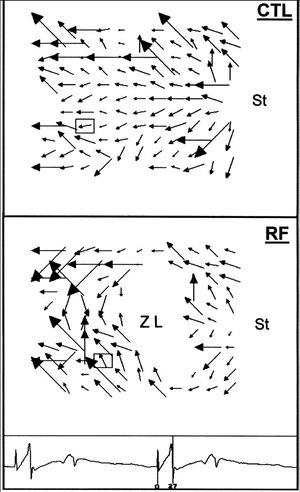
Fig. 3. Arriba: vectores de propagación obtenidos en el mismo experimento que en las figuras 1 y 2 a partir de los tiempos de activación local y durante la fase de control. Los vectores indican la dirección del proceso de activación desde la zona de estimulación, situada en la pared posterior auricular izquierda, hacia el lado opuesto de la pared auricular. Abajo: vectores de propagación obtenidos en el mismo experimento una vez efectuadas las aplicaciones de radiofrecuencia. Se observa que el proceso de activación modifica su dirección en la zona distal a la lesión al tener que rodearla para alcanzar dicha zona. CTL: control; RF: radiofrecuencia; St: zona de estimulación; ZL: zona lesionada.
Análisis de los electrogramas auriculares
En cada experimento se han seleccionado seis electrodos situados a ambos lados de la zona lesionada, a una distancia superior a 4 mm del borde de las lesiones, y otros seis electrodos a lo largo de la zona de las lesiones. En los registros obtenidos con estos electrodos se ha determinado la amplitud de los electrogramas, la máxima pendiente negativa de los mismos y su morfología, indicando, en relación con esta última variable, si los electrogramas presentaban una única deflexión (electrogramas simples), dos deflexiones (electrogramas dobles) o múltiples deflexiones (electrogramas múltiples). En los electrogramas dobles o múltiples, al determinar la amplitud y la pendiente, se han utilizado los valores correspondientes al componente de mayor amplitud y de mayor pendiente negativa.
Análisis de las lesiones
El análisis macroscópico de las lesiones se ha efectuado magnificando las imágenes con una lupa y utilizando un compás para determinar sus dimensiones (longitud y anchura). Se ha comprobado la transmuralidad mediante el análisis de las lesiones desde el endocardio al finalizar los experimentos y efectuando un estudio histológico de las preparaciones tras fijar el tejido con formaldehído, e incluirlo en parafina. Sobre las secciones se han efectuado tinciones con hematoxilina-eosina o técnicas tricrómicas.
Cálculos estadísticos
Los datos de las variables continuas se presentan como promedios ± desviación estándar. La significación estadística de las variaciones de estos parámetros tras efectuar las lesiones con RF se ha determinado mediante el análisis de la t de Student para datos apareados. Las diferencias entre variables no continuas se han analizado utilizando el test de la χ 2. Las diferencias se han considerado significativas para valores de p menores de 0,05. RESULTADOS
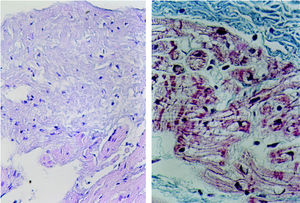
Las lesiones efectuadas en los 12 experimentos han presentado características transmurales y su dimensión media ha sido de 14,0 ± 1,5 mm x 2,8 ± 0 2 mm. En el análisis histológico de las lesiones se ha observado una distorsión severa de la organización de las miofibrillas, con bandas transversales densas que dan lugar a imágenes de hipercontracción, necrosis de las fibras y pérdida de la organización miofibrilar (fig. 4).
Fig. 4. Análisis microscópico de la zona lesionada en dos preparaciones distintas en el que se observa una distorsión severa de la organización de las miofibrillas, bandas transversales densas que dan lugar a imágenes de hipercontracción y pérdida de la estructura sarcomérica. Derecha: tinción tricrómica. Izquierda: hematoxilina-eosina.
Mediante la construcción de los mapas de activación auricular y la obtención de los vectores de propagación se ha observado que, tras la realización de las lesiones, el proceso de activación auricular rodeaba a la zona lesionada en 11 de los 12 experimentos, de modo que para alcanzar la zona distal a la lesión se modificaba la dirección del frente de activación originado desde la zona de estimulación. Este hecho no se ha observado en los mapas de activación obtenidos en la fase de control, en los que se ha objetivado una activación uniforme de la pared auricular desde la zona de estimulación, sin evidencia de líneas de bloqueo. En uno de los experimentos no se ha podido demostrar que el proceso de activación rodeaba la zona lesionada y por este motivo ha sido excluido del análisis de las características de los electrogramas, tanto de la línea de bloqueo como de la zona no lesionada.
Con el objeto de estudiar la reproducibilidad de las determinaciones de la amplitud y de la máxima pendiente negativa de los electrogramas auriculares obtenidos se ha analizado una muestra de 32 señales en las que las mediciones se han repetido en dos ciclos sucesivos. Las señales han correspondido a las dos zonas estudiadas en cada experimento. Las diferencias entre la primera y la segunda determinación no han sido significativas y, expresadas como porcentajes de variación con respecto a la primera determinación, han sido del 1 ± 5% en el caso de la amplitud y del 1 ± 9% en el caso de la máxima pendiente negativa.
Al estudiar las características de los electrogramas registrados en las dos áreas de estudio seleccionadas en cada experimento (11 experimentos, 66 electrogramas en la zona no afectada directamente por las lesiones y 66 electrogramas en la zona lesionada), en la zona no afectada directamente por las lesiones se ha observado que tanto la amplitud como la máxima pendiente negativa de los electrogramas auriculares no han presentado variaciones significativas tras las aplicaciones de RF, mientras que se ha observado una reducción significativa en ambos parámetros (p < 0,001) en los registros obtenidos en la zona lesionada (figs. 5 y 6).
Fig. 5. Valores normalizados de la amplitud y de la máxima pendiente negativa de los electrogramas obtenidos en las dos zonas estudiadas, la no afectada directamente por las lesiones (ZNL) y la correspondiente a las lesiones (ZL). Se observa la reducción significativa de ambos parámetros en la zona lesionada. AMP: amplitud; PD: máxima pendiente negativa; RF: radiofrecuencia ***p < 0,001.
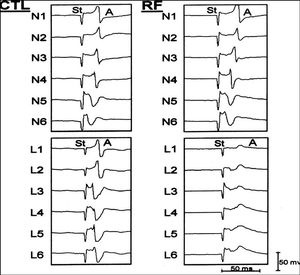
Fig. 6. Electrogramas correspondientes a la dos zonas estudiadas antes (CTL) y después (RF) de aplicar la radiofrecuencia en uno de los casos estudiados. Los electrogramas de la zona no lesionada (N1 a N6) no demuestran variaciones significativas, mientras que en la zona lesionada (electrogramas L1 a L6) se observa una reducción importante de la amplitud y de la pendiente de los electrogramas. A: auriculograma; St: estímulo.
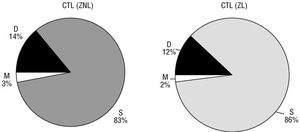
Se ha analizado la morfología de los electrogramas obtenidos en ambas zonas antes y después de las aplicaciones de RF. Antes de efectuar las lesiones, el tipo de electrograma observado con mayor frecuencia en ambas zonas es el simple, siendo muy reducido el porcentaje de electrogramas dobles o múltiples (fig. 7a). Una vez aplicada la RF, en la zona lesionada se ha observado un incremento significativo de la proporción de electrogramas dobles y, en menor medida, de electrogramas múltiples, a expensas de una reducción importante de la proporción de electrogramas simples (fig. 7b). En un 12% de los registros no se ha identificado el patrón morfológico de los electrogramas debido a la ausencia de señales o a su baja amplitud.
Fig. 7 . Porcentajes de los tipos de electrogramas obtenidos en las dos zonas estudiadas (a) antes de efectuar las lesiones y (b) después de aplicar la radiofrecuencia. CTL: control; P-RF: posradiofrecuencia; ZL: zona lesionada; ZNL: zona no lesionada. Tipos de electrogramas: S: simples; D: dobles; M: múltiples; I: indeterminados.
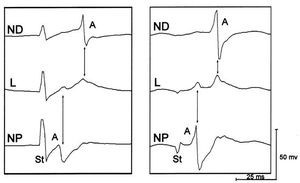
El análisis de la relación temporal de los dos componentes de los electrogramas dobles obtenidos en la zona lesionada ha puesto de manifiesto la coincidencia cronólogica de ambos con la activación auricular registrada a ambos lados de la lesión, de modo que el componente más precoz ha coincidido con la activación registrada en la zona proximal a la lesión y el más tardío con la activación registrada con retraso en la zona distal a la lesión (fig. 8). El análisis de los vectores de propagación ha demostrado que este retraso era originado por la prolongación del camino recorrido por el frente de activación hasta alcanzar, rodeándola, la zona distal a la lesión.
Fig. 8. Registros obtenidos en dos experimentos distintos tras efectuar las lesiones con radiofrecuencia. Se han seleccionado dos electrodos situados a ambos lados de la lesión en las zonas distal (ND) y proximal (NP), así como un electrodo, situado entre ambos, en la zona lesionada (L). En el registro correspondiente a la zona lesionada se observan electrogramas dobles cuyos dos componentes coinciden en el tiempo con los electrogramas obtenidos en la zona no lesionada; el primero de ellos coincide con la activación en la zona proximal y el segundo con la activación más tardía en la zona distal. A: auriculograma; St: estímulo.
DISCUSIÓN
El tratamiento de diversas arritmias auriculares mediante procedimientos basados en la ablación con RF implica la realización de lesiones cuyas características en cuanto a extensión y localización varían según el tipo de arritmia considerado. En los procedimientos propuestos para el control de la fibrilación auricular, basados inicialmente en la experiencia previa de los tratamientos quirúrgicos descritos por Cox et al 40-44, de manera habitual se acepta que es necesario producir lesiones lineales extensas y transmurales 11,28. Mediante la creación de este tipo de lesiones se pretende obtener zonas con bloqueo de la conducción que limiten el número de frentes de onda simultáneos que caracterizan y sustentan a los procesos fibrilatorios 1,3,7,10-12,24. Si se demuestra que el origen de la arritmia es focal, la realización de las lesiones con RF persigue anular la fuente de actividad ectópica y/o evitar la conducción hacia el resto del tejido auricular 13-15. En el caso de arritmias como el flúter auricular, las lesiones lineales se efectúan en una zona seleccionada del circuito implicado en el mantenimiento de la actividad reentrante, habitualmente relacionado con los obstáculos anatómicos que definen la arquitectura auricular, evitando así la aparición de nuevos episodios al bloquear la conducción en dicha zona 13,16-20,45. Así pues, en términos generales, con la producción de lesiones lineales fundamentalmente se persigue interrumpir la conducción en la zona lesionada, y la efectividad del procedimiento se basa en gran medida en este hecho, aunque también pueden estar implicados otros mecanismos, como las modificaciones en la inervación vegetativa y en la irrigación miocárdica producidas tras las aplicaciones de RF, el bloqueo dependiente de la frecuencia o la reducción de la masa miocárdica disponible para sustentar la arritmia, entre otros 7,46. Por otra parte, se ha señalado también que el procedimiento de ablación con RF para el tratamiento de la fibrilación auricular puede ser efectivo a pesar de obtener lesiones discontinuas 5.
Para evaluar el proceso de realización de las lesiones y la eficacia del procedimiento se emplean diversos criterios, de los cuales los principales son la interrupción de la arritmia y, sobre todo, la no inducibilidad de la misma. Aunque este último es el mejor indicador de la eficacia del tratamiento, durante la aplicación del mismo es necesario obtener de manera rápida y fiable información sobre diversos aspectos que determinan su desarrollo. Entre ellos se encuentran la delimitación de la situación y extensión de las lesiones, y la valoración de los efectos de la RF sobre el tejido afectado y sobre la conducción en la zona lesionada.
Existen diversos métodos para evaluar la extensión y localización de las lesiones y sus efectos sobre los patrones de activación auricular. Uno de los criterios utilizados para demostrar la producción de bloqueo completo es evidenciar la ausencia de transmisión a través de la línea de lesiones, objetivando las modificaciones en la propagación del frente de onda hasta alcanzar la región distal a la lesión. El análisis del proceso de activación efectuado mediante catéteres multielectrodos o procedimientos cartográficos, tanto secuenciales como instantáneos, permite obtener mapas de activación que demuestran que los frentes de activación que despolarizan cada uno de los lados de una lesión están disociados y que existen diferencias en la dirección de propagación en las dos zonas adyacentes a la línea de lesiones, a pesar de la contigüidad espacial de las mismas 11,12,26-29. Otros procedimientos, como los mapas de isopotenciales, en el contexto de la utilización de los sistemas cartográficos, también son útiles para localizar tanto las líneas de bloqueo como, en el caso de lesiones incompletas, las zonas en las que no se ha interrumpido la transmisión 11.
Junto a estos procedimientos, y como complemento de los mismos, se dispone de la información que aporta el análisis de los electrogramas registrados antes, durante y después de completar las aplicaciones de RF y que sirven de guía durante la realización del tratamiento 11,47. Así, las diferencias existentes en los tiempos de activación local a ambos lados de las líneas de bloqueo, la modificación del aspecto morfológico de los electrogramas en las zonas lesionadas y las variaciones en la amplitud o en la rapidez de las deflexiones registradas pueden ser indicadores útiles a la hora de localizar las zonas lesionadas, determinar su extensión o sus efectos sobre la conducción auricular 11,28,29,47.
En nuestro estudio hemos utilizado dos criterios para evaluar las lesiones producidas y sus efectos sobre la conducción auricular: el análisis macroscópico e histológico de las lesiones y la obtención de los mapas y de los vectores de propagación cuya interpretación y comparación con los obtenidos antes de efectuar las lesiones permite objetivar los cambios en la dirección del frente de activación impuestos por las mismas. La reducción de la amplitud de los electrogramas en la línea de lesiones es un hecho señalado en diversos estudios 11,28,29,47 y en los procedimientos de ablación para el tratamiento de la FA es utilizado como guía durante la aplicación de la RF en aproximaciones conservadoras en las que se ha propuesto como criterio para controlar la duración de las aplicaciones de la RF 11. Los resultados del presente trabajo confirman la reducción de la amplitud de los electrogramas obtenidos en las zonas correspondientes a las líneas de bloqueo y, junto a ello, hemos observado la reducción de la máxima pendiente negativa de los electrogramas registrados, indicador que se uniría al de la reducción de la amplitud de los electrogramas. En estudios experimentales, en los que se han monitorizado los cambios en los potenciales de acción o en los potenciales monofásicos 36,37, se ha observado que en las zonas afectadas directamente por la RF se obtiene una abolición irreversible de los potenciales de acción 36, mientras que en regiones cercanas a la lesión pueden ocurrir cambios reversibles 36,37. La desestructuración del tejido miocárdico afectado por la aplicación de la RF 30-35 suprime su capacidad de generar potenciales de acción y convierte a ésta en una zona de conducción pasiva o de tipo electrotónico de los potenciales generados en áreas vecinas. Por este motivo, en las zonas lesionadas se registran, a distancia, los potenciales generados en las áreas limítrofes. Este hecho queda reflejado también en la frecuencia elevada de potenciales dobles en los registros obtenidos en la línea de lesiones, relacionados con la activación en tiempos diferentes a ambos lados de las lesiones, ya que el proceso de activación alcanza la zona distal a las mismas tras rodearlas 28.
El registro de dobles potenciales, especialmente en zonas de bloqueo, es un hecho señalado en diversos estudios 11,26-28,48-51 y su identificación en la zona de lesión informa sobre las características de la conducción en la misma. Sin embargo, este indicador presenta limitaciones 27,49, entre ellas las derivadas de la reducción de la amplitud de los registros obtenidos que en ocasiones dificulta la descripción de sus características. De hecho, en el presente trabajo, en un 12% de los electrogramas de la zona lesionada no se han podido identificar las características de los mismos. Por otra parte, el intervalo entre los dos componentes de los electrogramas dobles depende de la diferencia entre el tiempo de activación a ambos lados de la línea de bloqueo que, a su vez, está influenciado por varios factores 11,26-28,49, entre ellos la dirección de propagación del frente de onda en relación con la lesión, las dimensiones de la lesión o su relación con los límites anatómicos de la pared auricular. La utilidad del criterio basado en la obtención de electrogramas dobles para indicar la existencia de una línea de bloqueo completo será óptima cuando la disparidad temporal entre los frentes de onda que activan las zonas del miocardio a ambos lados de la línea de bloqueo sea acentuada 11,26. Por otra parte, hemos podido observar también que en el tejido no lesionado pueden registrarse ocasionalmente potenciales dobles o múltiples, hecho que se ha relacionado con las características estructurales de la pared auricular y la activación asincrónica en dos zonas contiguas del miocardio auricular 29,50,52. Asimismo, en la línea de lesiones, aunque el tipo de señales predominante han sido los dobles potenciales, también se han registrado electrogramas simples y múltiples, hecho a tener en cuenta si se pretende valorar la existencia de líneas de bloqueo mediante el análisis de los registros obtenidos en la zona lesionada. CONCLUSIÓN
Los electrogramas obtenidos directamente sobre líneas de bloqueo originadas con radiofrecuencia se caracterizan por presentar una reducción significativa de la amplitud y de la máxima pendiente negativa. En estos registros predominan los electrogramas dobles cuyos dos componentes representan la activación a ambos lados de la lesión. En la línea de bloqueo pueden registrarse también, en un porcentaje reducido de casos, electrogramas simples y múltiples. AGRADECIMIENTOS
Los autores desean expresar su agradecimiento a D. César Avellaneda Esteban por su ayuda en la realización de los electrodos.
La utilización de la ablación con radiofrecuencia (RF) para el tratamiento de diversas arritmias supraventriculares como la fibrilación auricular 1-12, taquicardias auriculares 13-15 o el flúter auricular 16-20 requiere el análisis de los efectos que producen las aplicaciones de RF sobre los patrones de activación auricular y sobre los mecanismos que inducen o sustentan este tipo de arritmias. La utilización de la RF requiere también conocer las repercusiones estructurales y funcionales de las lesiones producidas 1-3,5,7,10,21-25 para aumentar la seguridad del procedimiento y evitar posibles complicaciones. La realización de lesiones lineales ha subrayado la importancia de disponer de indicadores que aporten información sobre su localización y extensión, además de sus repercusiones funcionales. Los procedimientos cartográficos permiten conocer con exactitud las modificaciones de los patrones de activación y, por tanto, ayudan a demostrar la consecución de líneas de bloqueo completo 11,12,26-29; sin embargo, tanto durante como tras la realización de las lesiones es útil disponer de indicadores basados en el análisis de los electrogramas auriculares, registrados tanto en las zonas afectadas como en las sanas, que puedan orientar durante la realización del procedimiento. Por otra parte, la obtención de mapas de activación auricular mediante técnicas cartográficas requiere la identificación y valoración adecuadas de los electrogramas obtenidos. La aplicación de RF en el tejido miocárdico se caracteriza por la lesión térmica del mismo 21-23,30-35 y por la supresión de las propiedades eléctricas activas de las fibras destruidas, que implica modificaciones en las características de los electrogramas, tanto extra como intracelulares 36,37. En el presente trabajo se utiliza un modelo experimental con corazones aislados y perfundidos de conejo en los que, mediante cartografía epicárdica de alta resolución y análisis de los vectores de propagación, se comprueba la obtención de líneas de bloqueo completo aplicando técnicas de ablación con RF. Se pretende analizar y cuantificar las modificaciones inducidas en los electrogramas auriculares registrados en la zona lesionada y establecer las diferencias existentes con respecto a los obtenidos en las zonas no afectadas directamente por las lesiones. MÉTODOS
Preparación experimental
Se han estudiado 12 conejos de raza California (peso medio 3,9 ± 0,4 kg). Tras anestesia (ketamina, 25 mg/kg i.m.) y heparinización, se ha extraído el corazón sumergiéndolo en Tyrode frío (4 oC). Tras aislar la aorta se ha conectado a un sistema de Langendorff para perfundir retrógradamente Tyrode a una presión de 60 mmHg y una temperatura de 37 ± 0,5 oC. La composición milimolar del líquido de perfusión es: ClNa 125, CO 3HNa 24,2, ClK 4,7, Cl 2Ca 2,2, PO 4H 2Na 1,2, Cl 2Mg 0,6 y glucosa 12. La oxigenación se ha efectuado con una mezcla de 95% de O 2 y 5% de CO 2.
Tras abrir la aurícula derecha mediante una incisión desde la zona de entrada de la vena cava superior hasta la inferior, paralela a la crista terminalis, se ha seccionado la parte central del tabique interauricular, en la zona de la fosa oval, para introducir en la aurícula izquierda un soporte ovoideo de 2,5 x 2 cm con el objeto de facilitar el contacto del electrodo epicárdico múltiple utilizado para efectuar los registros del proceso de activación auricular izquierdo. Los registros se han efectuado con una placa-electrodo (2,5 x 2,5 cm) compuesta por 221 electrodos unipolares de acero inoxidable (diámetro de 0,125 mm), que se ha situado sobre la pared libre auricular izquierda. La zona central del electrodo está compuesta por 121 electrodos dispuestos según una disposición cuadrangular, con 11 electrodos en cada lado (distancia interelectrodo de 1 mm) y rodeando a esta zona central existen 108 electrodos situados según una disposición también cuadrangular (filas de 12 electrodos con una separación interelectrodo de 2 mm). Los dos electrodos situados en la zona media de cada una de las filas más periféricas se han utilizado para efectuar estimulación auricular y no se han empleado para obtener registros. Se ha utilizado como electrodo indiferente una placa de Ag/AgCl (0,5 x 1 cm) situada sobre la aorta previamente canulada. Además, se ha usado un electrodo bipolar de acero inoxidable (diámetro de 0,125 mm, distancia interelectrodo de 1 mm) para efectuar registros epicárdicos en la pared lateral del ventrículo derecho. Se ha empleado un estimulador GRASS S88 provisto de una unidad de aislamiento de estímulos (SIU5) y se han emitido estímulos rectangulares con una duración de 2 ms e intensidad doble del umbral diastólico. Los registros se han efectuado utilizando un sistema de cartografía de la actividad eléctrica cardíaca (MAPTECH). Los electrogramas se han amplificado con una ganancia de 300-500, que se ha mantenido constante a lo largo de todo el experimento, se han filtrado (banda de 1 a 400 Hz) y se han multiplexado. La frecuencia de muestreo en cada canal ha sido de 1 kHz. Los datos obtenidos en cada experimento se han almacenado en cinta magnética para efectuar un análisis posterior.
Protocolo experimental
Antes y después de efectuar las lesiones con RF se ha registrado la activación auricular durante la estimulación con ciclos constantes (250 ms) que se ha realizado con los electrodos de estimulación localizados en la zona posterior de la pared auricular izquierda. Las lesiones con RF se han llevado a cabo desde el epicardio de la pared auricular izquierda mediante un electrodo unipolar de Ag/AgCl aislado con teflón hasta su extremo distal (diámetro de 1 mm, longitud de la zona libre distal de 1 mm). Se ha utilizado un generador de corriente HAT 100 con una potencia de 5 W y un tiempo de emisión en cada aplicación de 8 s, empleando como electrodo indiferente una placa de 8 x 12 mm situada alrededor de la cánula de perfusión. Para mantener una impedancia baja durante las aplicaciones de RF se ha bañado con Tyrode la zona en la que se situaba el electrodo. Las lesiones lineales en la pared auricular izquierda se han obtenido según un procedimiento secuencial efectuando aplicaciones sucesivas de RF. En primer lugar se han realizado tres lesiones separadas entre sí y dispuestas verticalmente en la zona central (media, superior e inferior) de la pared libre auricular izquierda. A continuación se han añadido dos lesiones más, situándolas entre la lesión central y las lesiones superior e inferior efectuadas con anterioridad, y por último se han añadido cuatro lesiones entre las efectuadas anteriormente para hacerlas confluentes por completo. Así se ha obtenido una lesión única que atraviesa verticalmente la zona media de la pared libre auricular izquierda, dejando tejido no lesionado entre los extremos superior e inferior de la lesión y los bordes de la aurícula.
Parámetros analizados
Activación auricular
Se han construido los mapas de activación auricular tras determinar el tiempo de activación local en cada electrodo unipolar del electrodo múltiple 7,23,38,39. Para ello se ha identificado el momento de máxima pendiente negativa (-dV/dt) de los electrogramas auriculares y se han construido las isócronas semiautomáticamente. La codificación en color de los intervalos entre un tiempo de referencia (el estímulo) y los tiempos de activación local (fig. 1), así como la determinación de los vectores de propagación, ha permitido caracterizar los patrones de activación durante el control y tras efectuar las lesiones con RF. Para determinar los vectores de propagación se ha utilizado el procedimiento descrito previamente 23; así, tras seleccionar agrupaciones de cuatro electrodos en disposición cuadrangular con lados de 2 mm, cada cuadripolo se ha dividido en dos triángulos, calculando el vector de propagación en cada triángulo. Se ha tomado el promedio de ambos para determinar la dirección de la propagación en cada cuadripolo. Se ha considerado que existía bloqueo completo de la conducción a través de las lesiones cuando éstas daban lugar a una modificación de la dirección del proceso de activación en la zona distal a la lesión, adoptando en dicha zona una dirección paralela a la lesión lineal al tener que rodearla para alcanzar esta zona. Para ello se han comparado el mapa de activación y los vectores de propagación obtenidos una vez transcurridos 20 min desde la finalización de las aplicaciones de RF con los obtenidos en la fase de control (figs. 2 y 3). La situación de la zona lesionada en la matriz del electrodo múltiple se ha identificado utilizando las referencias anatómicas de las lesiones y precisando la posición del electrodo en relación con las mismas referencias.
Fig. 1. Arriba: mapa de activación auricular izquierda obtenido en la fase de control durante la estimulación desde la zona posterior de la aurícula (situada a la derecha de la figura). En la zona central la distancia interelectrodo es de 1 mm y en la periferia de 2 mm. Los tiempos de activación local se han codificado en color y los cambios en la escala de colores se han efectuado cada 4 ms, de modo que la activación más precoz corresponde al color rojo y la más tardía al azul. Abajo: mapa de activación del mismo experimento, también durante la fase de control, en cuya representación se han suprimido uno de cada dos electrodos de la parte central del mismo con el objeto de visualizar mejor el proceso de activación auricular (distancia interelectrodo de 2 mm).
Fig. 2. Mapas de activación auricular izquierda similares a los representados en la figura 1 y obtenidos en el mismo experimento tras efectuar las lesiones con radiofrecuencia. Se observa la modificación del proceso de activación originada por la zona lesionada (zona vertical no coloreada) que condiciona que la activación alcance la zona distal rodeando a la zona lesionada.
Fig. 3. Arriba: vectores de propagación obtenidos en el mismo experimento que en las figuras 1 y 2 a partir de los tiempos de activación local y durante la fase de control. Los vectores indican la dirección del proceso de activación desde la zona de estimulación, situada en la pared posterior auricular izquierda, hacia el lado opuesto de la pared auricular. Abajo: vectores de propagación obtenidos en el mismo experimento una vez efectuadas las aplicaciones de radiofrecuencia. Se observa que el proceso de activación modifica su dirección en la zona distal a la lesión al tener que rodearla para alcanzar dicha zona. CTL: control; RF: radiofrecuencia; St: zona de estimulación; ZL: zona lesionada.
Análisis de los electrogramas auriculares
En cada experimento se han seleccionado seis electrodos situados a ambos lados de la zona lesionada, a una distancia superior a 4 mm del borde de las lesiones, y otros seis electrodos a lo largo de la zona de las lesiones. En los registros obtenidos con estos electrodos se ha determinado la amplitud de los electrogramas, la máxima pendiente negativa de los mismos y su morfología, indicando, en relación con esta última variable, si los electrogramas presentaban una única deflexión (electrogramas simples), dos deflexiones (electrogramas dobles) o múltiples deflexiones (electrogramas múltiples). En los electrogramas dobles o múltiples, al determinar la amplitud y la pendiente, se han utilizado los valores correspondientes al componente de mayor amplitud y de mayor pendiente negativa.
Análisis de las lesiones
El análisis macroscópico de las lesiones se ha efectuado magnificando las imágenes con una lupa y utilizando un compás para determinar sus dimensiones (longitud y anchura). Se ha comprobado la transmuralidad mediante el análisis de las lesiones desde el endocardio al finalizar los experimentos y efectuando un estudio histológico de las preparaciones tras fijar el tejido con formaldehído, e incluirlo en parafina. Sobre las secciones se han efectuado tinciones con hematoxilina-eosina o técnicas tricrómicas.
Cálculos estadísticos
Los datos de las variables continuas se presentan como promedios ± desviación estándar. La significación estadística de las variaciones de estos parámetros tras efectuar las lesiones con RF se ha determinado mediante el análisis de la t de Student para datos apareados. Las diferencias entre variables no continuas se han analizado utilizando el test de la χ 2. Las diferencias se han considerado significativas para valores de p menores de 0,05. RESULTADOS
Las lesiones efectuadas en los 12 experimentos han presentado características transmurales y su dimensión media ha sido de 14,0 ± 1,5 mm x 2,8 ± 0 2 mm. En el análisis histológico de las lesiones se ha observado una distorsión severa de la organización de las miofibrillas, con bandas transversales densas que dan lugar a imágenes de hipercontracción, necrosis de las fibras y pérdida de la organización miofibrilar (fig. 4).
Fig. 4. Análisis microscópico de la zona lesionada en dos preparaciones distintas en el que se observa una distorsión severa de la organización de las miofibrillas, bandas transversales densas que dan lugar a imágenes de hipercontracción y pérdida de la estructura sarcomérica. Derecha: tinción tricrómica. Izquierda: hematoxilina-eosina.
Mediante la construcción de los mapas de activación auricular y la obtención de los vectores de propagación se ha observado que, tras la realización de las lesiones, el proceso de activación auricular rodeaba a la zona lesionada en 11 de los 12 experimentos, de modo que para alcanzar la zona distal a la lesión se modificaba la dirección del frente de activación originado desde la zona de estimulación. Este hecho no se ha observado en los mapas de activación obtenidos en la fase de control, en los que se ha objetivado una activación uniforme de la pared auricular desde la zona de estimulación, sin evidencia de líneas de bloqueo. En uno de los experimentos no se ha podido demostrar que el proceso de activación rodeaba la zona lesionada y por este motivo ha sido excluido del análisis de las características de los electrogramas, tanto de la línea de bloqueo como de la zona no lesionada.
Con el objeto de estudiar la reproducibilidad de las determinaciones de la amplitud y de la máxima pendiente negativa de los electrogramas auriculares obtenidos se ha analizado una muestra de 32 señales en las que las mediciones se han repetido en dos ciclos sucesivos. Las señales han correspondido a las dos zonas estudiadas en cada experimento. Las diferencias entre la primera y la segunda determinación no han sido significativas y, expresadas como porcentajes de variación con respecto a la primera determinación, han sido del 1 ± 5% en el caso de la amplitud y del 1 ± 9% en el caso de la máxima pendiente negativa.
Al estudiar las características de los electrogramas registrados en las dos áreas de estudio seleccionadas en cada experimento (11 experimentos, 66 electrogramas en la zona no afectada directamente por las lesiones y 66 electrogramas en la zona lesionada), en la zona no afectada directamente por las lesiones se ha observado que tanto la amplitud como la máxima pendiente negativa de los electrogramas auriculares no han presentado variaciones significativas tras las aplicaciones de RF, mientras que se ha observado una reducción significativa en ambos parámetros (p < 0,001) en los registros obtenidos en la zona lesionada (figs. 5 y 6).
Fig. 5. Valores normalizados de la amplitud y de la máxima pendiente negativa de los electrogramas obtenidos en las dos zonas estudiadas, la no afectada directamente por las lesiones (ZNL) y la correspondiente a las lesiones (ZL). Se observa la reducción significativa de ambos parámetros en la zona lesionada. AMP: amplitud; PD: máxima pendiente negativa; RF: radiofrecuencia ***p < 0,001.
Fig. 6. Electrogramas correspondientes a la dos zonas estudiadas antes (CTL) y después (RF) de aplicar la radiofrecuencia en uno de los casos estudiados. Los electrogramas de la zona no lesionada (N1 a N6) no demuestran variaciones significativas, mientras que en la zona lesionada (electrogramas L1 a L6) se observa una reducción importante de la amplitud y de la pendiente de los electrogramas. A: auriculograma; St: estímulo.
Se ha analizado la morfología de los electrogramas obtenidos en ambas zonas antes y después de las aplicaciones de RF. Antes de efectuar las lesiones, el tipo de electrograma observado con mayor frecuencia en ambas zonas es el simple, siendo muy reducido el porcentaje de electrogramas dobles o múltiples (fig. 7a). Una vez aplicada la RF, en la zona lesionada se ha observado un incremento significativo de la proporción de electrogramas dobles y, en menor medida, de electrogramas múltiples, a expensas de una reducción importante de la proporción de electrogramas simples (fig. 7b). En un 12% de los registros no se ha identificado el patrón morfológico de los electrogramas debido a la ausencia de señales o a su baja amplitud.
Fig. 7 . Porcentajes de los tipos de electrogramas obtenidos en las dos zonas estudiadas (a) antes de efectuar las lesiones y (b) después de aplicar la radiofrecuencia. CTL: control; P-RF: posradiofrecuencia; ZL: zona lesionada; ZNL: zona no lesionada. Tipos de electrogramas: S: simples; D: dobles; M: múltiples; I: indeterminados.
El análisis de la relación temporal de los dos componentes de los electrogramas dobles obtenidos en la zona lesionada ha puesto de manifiesto la coincidencia cronólogica de ambos con la activación auricular registrada a ambos lados de la lesión, de modo que el componente más precoz ha coincidido con la activación registrada en la zona proximal a la lesión y el más tardío con la activación registrada con retraso en la zona distal a la lesión (fig. 8). El análisis de los vectores de propagación ha demostrado que este retraso era originado por la prolongación del camino recorrido por el frente de activación hasta alcanzar, rodeándola, la zona distal a la lesión.
Fig. 8. Registros obtenidos en dos experimentos distintos tras efectuar las lesiones con radiofrecuencia. Se han seleccionado dos electrodos situados a ambos lados de la lesión en las zonas distal (ND) y proximal (NP), así como un electrodo, situado entre ambos, en la zona lesionada (L). En el registro correspondiente a la zona lesionada se observan electrogramas dobles cuyos dos componentes coinciden en el tiempo con los electrogramas obtenidos en la zona no lesionada; el primero de ellos coincide con la activación en la zona proximal y el segundo con la activación más tardía en la zona distal. A: auriculograma; St: estímulo.
DISCUSIÓN
El tratamiento de diversas arritmias auriculares mediante procedimientos basados en la ablación con RF implica la realización de lesiones cuyas características en cuanto a extensión y localización varían según el tipo de arritmia considerado. En los procedimientos propuestos para el control de la fibrilación auricular, basados inicialmente en la experiencia previa de los tratamientos quirúrgicos descritos por Cox et al 40-44, de manera habitual se acepta que es necesario producir lesiones lineales extensas y transmurales 11,28. Mediante la creación de este tipo de lesiones se pretende obtener zonas con bloqueo de la conducción que limiten el número de frentes de onda simultáneos que caracterizan y sustentan a los procesos fibrilatorios 1,3,7,10-12,24. Si se demuestra que el origen de la arritmia es focal, la realización de las lesiones con RF persigue anular la fuente de actividad ectópica y/o evitar la conducción hacia el resto del tejido auricular 13-15. En el caso de arritmias como el flúter auricular, las lesiones lineales se efectúan en una zona seleccionada del circuito implicado en el mantenimiento de la actividad reentrante, habitualmente relacionado con los obstáculos anatómicos que definen la arquitectura auricular, evitando así la aparición de nuevos episodios al bloquear la conducción en dicha zona 13,16-20,45. Así pues, en términos generales, con la producción de lesiones lineales fundamentalmente se persigue interrumpir la conducción en la zona lesionada, y la efectividad del procedimiento se basa en gran medida en este hecho, aunque también pueden estar implicados otros mecanismos, como las modificaciones en la inervación vegetativa y en la irrigación miocárdica producidas tras las aplicaciones de RF, el bloqueo dependiente de la frecuencia o la reducción de la masa miocárdica disponible para sustentar la arritmia, entre otros 7,46. Por otra parte, se ha señalado también que el procedimiento de ablación con RF para el tratamiento de la fibrilación auricular puede ser efectivo a pesar de obtener lesiones discontinuas 5.
Para evaluar el proceso de realización de las lesiones y la eficacia del procedimiento se emplean diversos criterios, de los cuales los principales son la interrupción de la arritmia y, sobre todo, la no inducibilidad de la misma. Aunque este último es el mejor indicador de la eficacia del tratamiento, durante la aplicación del mismo es necesario obtener de manera rápida y fiable información sobre diversos aspectos que determinan su desarrollo. Entre ellos se encuentran la delimitación de la situación y extensión de las lesiones, y la valoración de los efectos de la RF sobre el tejido afectado y sobre la conducción en la zona lesionada.
Existen diversos métodos para evaluar la extensión y localización de las lesiones y sus efectos sobre los patrones de activación auricular. Uno de los criterios utilizados para demostrar la producción de bloqueo completo es evidenciar la ausencia de transmisión a través de la línea de lesiones, objetivando las modificaciones en la propagación del frente de onda hasta alcanzar la región distal a la lesión. El análisis del proceso de activación efectuado mediante catéteres multielectrodos o procedimientos cartográficos, tanto secuenciales como instantáneos, permite obtener mapas de activación que demuestran que los frentes de activación que despolarizan cada uno de los lados de una lesión están disociados y que existen diferencias en la dirección de propagación en las dos zonas adyacentes a la línea de lesiones, a pesar de la contigüidad espacial de las mismas 11,12,26-29. Otros procedimientos, como los mapas de isopotenciales, en el contexto de la utilización de los sistemas cartográficos, también son útiles para localizar tanto las líneas de bloqueo como, en el caso de lesiones incompletas, las zonas en las que no se ha interrumpido la transmisión 11.
Junto a estos procedimientos, y como complemento de los mismos, se dispone de la información que aporta el análisis de los electrogramas registrados antes, durante y después de completar las aplicaciones de RF y que sirven de guía durante la realización del tratamiento 11,47. Así, las diferencias existentes en los tiempos de activación local a ambos lados de las líneas de bloqueo, la modificación del aspecto morfológico de los electrogramas en las zonas lesionadas y las variaciones en la amplitud o en la rapidez de las deflexiones registradas pueden ser indicadores útiles a la hora de localizar las zonas lesionadas, determinar su extensión o sus efectos sobre la conducción auricular 11,28,29,47.
En nuestro estudio hemos utilizado dos criterios para evaluar las lesiones producidas y sus efectos sobre la conducción auricular: el análisis macroscópico e histológico de las lesiones y la obtención de los mapas y de los vectores de propagación cuya interpretación y comparación con los obtenidos antes de efectuar las lesiones permite objetivar los cambios en la dirección del frente de activación impuestos por las mismas. La reducción de la amplitud de los electrogramas en la línea de lesiones es un hecho señalado en diversos estudios 11,28,29,47 y en los procedimientos de ablación para el tratamiento de la FA es utilizado como guía durante la aplicación de la RF en aproximaciones conservadoras en las que se ha propuesto como criterio para controlar la duración de las aplicaciones de la RF 11. Los resultados del presente trabajo confirman la reducción de la amplitud de los electrogramas obtenidos en las zonas correspondientes a las líneas de bloqueo y, junto a ello, hemos observado la reducción de la máxima pendiente negativa de los electrogramas registrados, indicador que se uniría al de la reducción de la amplitud de los electrogramas. En estudios experimentales, en los que se han monitorizado los cambios en los potenciales de acción o en los potenciales monofásicos 36,37, se ha observado que en las zonas afectadas directamente por la RF se obtiene una abolición irreversible de los potenciales de acción 36, mientras que en regiones cercanas a la lesión pueden ocurrir cambios reversibles 36,37. La desestructuración del tejido miocárdico afectado por la aplicación de la RF 30-35 suprime su capacidad de generar potenciales de acción y convierte a ésta en una zona de conducción pasiva o de tipo electrotónico de los potenciales generados en áreas vecinas. Por este motivo, en las zonas lesionadas se registran, a distancia, los potenciales generados en las áreas limítrofes. Este hecho queda reflejado también en la frecuencia elevada de potenciales dobles en los registros obtenidos en la línea de lesiones, relacionados con la activación en tiempos diferentes a ambos lados de las lesiones, ya que el proceso de activación alcanza la zona distal a las mismas tras rodearlas 28.
El registro de dobles potenciales, especialmente en zonas de bloqueo, es un hecho señalado en diversos estudios 11,26-28,48-51 y su identificación en la zona de lesión informa sobre las características de la conducción en la misma. Sin embargo, este indicador presenta limitaciones 27,49, entre ellas las derivadas de la reducción de la amplitud de los registros obtenidos que en ocasiones dificulta la descripción de sus características. De hecho, en el presente trabajo, en un 12% de los electrogramas de la zona lesionada no se han podido identificar las características de los mismos. Por otra parte, el intervalo entre los dos componentes de los electrogramas dobles depende de la diferencia entre el tiempo de activación a ambos lados de la línea de bloqueo que, a su vez, está influenciado por varios factores 11,26-28,49, entre ellos la dirección de propagación del frente de onda en relación con la lesión, las dimensiones de la lesión o su relación con los límites anatómicos de la pared auricular. La utilidad del criterio basado en la obtención de electrogramas dobles para indicar la existencia de una línea de bloqueo completo será óptima cuando la disparidad temporal entre los frentes de onda que activan las zonas del miocardio a ambos lados de la línea de bloqueo sea acentuada 11,26. Por otra parte, hemos podido observar también que en el tejido no lesionado pueden registrarse ocasionalmente potenciales dobles o múltiples, hecho que se ha relacionado con las características estructurales de la pared auricular y la activación asincrónica en dos zonas contiguas del miocardio auricular 29,50,52. Asimismo, en la línea de lesiones, aunque el tipo de señales predominante han sido los dobles potenciales, también se han registrado electrogramas simples y múltiples, hecho a tener en cuenta si se pretende valorar la existencia de líneas de bloqueo mediante el análisis de los registros obtenidos en la zona lesionada. CONCLUSIÓN
Los electrogramas obtenidos directamente sobre líneas de bloqueo originadas con radiofrecuencia se caracterizan por presentar una reducción significativa de la amplitud y de la máxima pendiente negativa. En estos registros predominan los electrogramas dobles cuyos dos componentes representan la activación a ambos lados de la lesión. En la línea de bloqueo pueden registrarse también, en un porcentaje reducido de casos, electrogramas simples y múltiples. AGRADECIMIENTOS
Los autores desean expresar su agradecimiento a D. César Avellaneda Esteban por su ayuda en la realización de los electrodos.
Bibliografía
[1]
Radiofrequency catheter ablation of the atria reduces inducibility and duration of atrial fibrillation in dogs. Circulation 1995; 91: 2235-2244.
[2]
Epicardial maps of atrial fibrillation after linear ablation lesions. J Cardiovasc Electrophysiol 1997; 8: 1046-1054.
[3]
Radiofrequency catheter ablation of the atria eliminates pacing-induced sustained atrial fibrillation and reduces connexin 43 in dogs. Circulation 1997; 96: 1675-1685.
[4]
Successful catheter ablation of atrial fibrillation. J Cardiovasc Electrophysiol 1994; 5: 1045-1052.
[5]
Linear atrial ablations in a canine model of chronic atrial fibrillation. Morphological and electrophysiological observations. Circulation 1998; 97: 1176-1185.
[6]
Right and left atrial radiofrequency catheter therapy of paroxysmal atrial fibrillation. J Cardiovasc Electrophysiol 1996; 7: 1132-1144.
[7]
Reduction of atrial fibrillation inducibility by radiofrequency ablation: an experimental study. Pacing Clin Electrophysiol 1999; 22: 421-436.
[8]
Atrial mapping and radiofrequency catheter ablation in patients with idiopatic atrial fibrillation. Electrophysiological findings and ablation results. Circulation 1998; 97: 2136-2145.
[9]
Long-term follow-up after right atrial radiofrequency catheter treatment of paroxysmal atrial fibrillation. Pacing Clin Electrophysiol 1998; 21: 2533-2538.
[10]
Thoracoscopic epicardial radiofrequency ablation for vagal atrial fibrillation in dogs. Pacing Clin Electrophysiol 1999; 22: 880-886.
[11]
Anatomy-guided linear atrial lesions for radiofrequency catheter ablation of atrial fibrillaton. Pacing Clin Electrophysiol 1998; 21: 1959-1978.
[12]
Catheter ablation of paroxysmal atrial fibrillation using a 3D Mapping system. Circulation 1999; 100: 1203-1208.
[13]
Radiofrequency catheter ablation of atrial arrhythmias: Results and mechanisms. Circulation 1994; 89: 1074-1089.
[14]
Radiofrequency catheter ablation of atrial tachycardias. Am Heart J 1996; 131: 481-489.
[15]
Initiation of atrial fibrillation by ectopic beats originating from the pulmonary veins. Electrophysiological characteristics, pharmacological responses, and effects of radiofrequency ablation. Circulation 1999; 100: 1879-1886.
[16]
Radiofrequency catheter ablation for the treatment of human type I atrial flutter. Identification of a critical zone in the reentrant circuit by endocardial mapping techniques. Circulation 1992; 86: 1233-1240.
[17]
Radiofrequency ablation of the inferior vena cava-tricuspid valve isthmus in common atrial flutter. Am J Cardiol 1993; 71: 705-709.
[18]
Electrophysiologic characteristics and radiofrequency catheter ablation in patients with clockwise atrial flutter. J Cardiovasc Electrophysiol 1997; 8: 24-34.
[19]
Radiofrequency catheter ablation of common atrial flutter in 200 patients. J Cardiovasc Electrophysiol 1996; 7: 1225-1233.
[20]
Radiofrequency catheter ablation of type I atrial flutter: Prediction of late success by electrophysiological criteria. Circulation 1995; 92: 1389-1392.
[21]
Transcatheter ablation of the sinus node in dogs using high-frequency current. Eur Heart J 1990; 11: 82-89.
[22]
Closed chest radiofrequency ablation of the sinoatrial node in dogs. Pacing Clin Electrophysiol 1990; 13: 745-756.
[23]
Acute effects of radiofrequency ablation upon atrial conduction in proximity to the lesion site. Pacing Clin Electrophysiol 1998; 21: 659-668.
[24]
The creation of linear contiguous lesions in the atria with an expandable loop catheter. J Am Coll Cardiol 1999; 33: 972-984.
[25]
Morphological and physiological characteristics of discontinuous linear atrial ablations during atrial pacing and atrial fibrillation. J Cardiovasc Electrophysiol 1999; 10: 378-386.
[26]
Electrophysiological effects of long, linear atrial lesions placed under intracardiac ultrasound guidance. Circulation 1997; 96: 2715-2721.
[27]
High-density mapping of activation through an incomplete isthmus ablation line. Circulation 1999; 99: 211-215.
[28]
Verification of linear lesions using a noncontact multielectrode array catheter versus conventional contact mapping techniques. J Cardiovasc Electrophysiol 1999; 10: 791-798.
[29]
High-resolution mapping and histologic examination of long radiofrequency lesions in canine atria. J Cardiovasc Electrophysiol 1999; 10: 1467-1477.
[30]
Electrophysiologic and histologic observations of chronic atrioventricular block induced by closed-chest catheter desiccation with radiofrequency energy. Pacing Clinical Electrophysiol 1987; 10: 805-816.
[31]
Tissue heating during radiofrequency catheter ablation: A thermodynamic model and observations in isolated perfused and superfused canine right ventricular free wall. Pacing Clin Electrophysiol 1989; 12: 962-976.
[32]
Induction of complete AV block in dogs by transcatheter ablation using high-frequency current: An alternative to direct current high energy shock. Eur Heart J 1989; 10: 113-119.
[33]
Induction of partial alterations in atrioventricular conduction in dogs by percutaneous emission of high-frequency currents. Am Heart J 1988; 115: 1214-1221.
[34]
Biophysics and pathology of catheter energy delivery systems. Prog Cardiovasc Dis 1995; 37: 185-204.
[35]
Ablación transcatéter por corrientes de radiofrecuencia. Bases biofísicas. Rev Esp Cardiol 1992; 45: 627-636.
[36]
Sequential changes in action potential of rabbit epicardium during and following radiofrequency ablation. J Cardiovasc Electrophysiol 1999; 10: 1252-1261.
[37]
Real-time monitoring of radiofrequency-induced myocardial lesions by simultaneous recording of monophasic action potentials. En: Franz MR, editor. Monophasic action potentials: bridging cell and bedside. Armonk, NuevaYork: Futura Publishing, 2000; 807-821.
[38]
Modificaciones agudas de la longitud de onda del proceso de activación auricular inducidas por la dilatación. Estudio experimental. Rev Esp Cardiol 1998; 51: 874-883.
[39]
Patrones de activación durante la fibrilación auricular en un modelo experimental. Rev Esp Cardiol 1999; 52: 327-338.
[40]
The surgical treatment of atrial fibrillation. I. Summary of the current concepts of the mechanisms of atrial flutter and atrial fibrillation. J Thorac Cardiovasc Surg 1991; 101: 402-405.
[41]
The surgical treatment of atrial fibrillation. II. Intraoperative electrophysiologic mapping and description of the electrophysiologic basis of atrial flutter and atrial fibrillation. J Thorac Cardiovasc Surg 1991; 101: 406-426.
[42]
The surgical treatment of atrial fibrillation. III. Development of a definitive surgical procedure. J Thorac Cardiovasc Surg 1991; 101: 569-583.
[43]
Modification of the maze procedure for atrial flutter and atrial fibrillation. I. Rationale and surgical results. J Thorac Cardiovasc Surg 1995; 110: 473-484.
[44]
Risks and benefits of combined maze procedure for atrial fibrillation associated with organic heart disease. J Am Coll Cardiol 1996; 28: 985-990.
[45]
Is 8-mm more effective than 4-mm tip electrode catheter for ablation of typical atrial flutter? Circulation 1999; 100: 768-771.
[46]
Efferent vagal innervation of the canine atria and sinus and atrioventricular nodes. The third fat pad. Circulation 1997; 95: 2573-2584.
[47]
Segment by segment linear ablation with an articulated bilimb catheter: Initial experimental results. Pacing Clin Electrophysiol 1998; 21: 2539-2546.
[48]
Conduction block in the inferior vena caval-tricuspid valve isthmus: Association with outcome of radiofrequency ablation of type I atrial flutter. J Am Coll Cardiol 1996; 28: 1519-1531.
[49]
Identification of conduction block in cardiac muscle: in vitro observations in canine epicardium. Cardiovasc Res 1994; 28: 259-269.
[50]
Atrial electrograms during electrically induced atrial fibrillation in humans. Circulation 1997; 95: 1231-1241.
[51]
Validation of double-spike electrograms as markers of conduction delay or block in atrial flutter. Am J Cardiol 1988; 61: 775-780.
[52]
Are double potentials markers of a specific zone of the atrioventricular junction in the isolated rabbit heart? Pacing Clinical Electrophysiol 1997; 20: 2385-2393.