En los últimos años, la creciente importancia clínica de la insuficiencia tricuspídea (IT) funcional ha contribuido al mayor interés actual en el diagnóstico y el tratamiento tempranos de esta enfermedad, a la que históricamente se ha prestado poca atención. La IT tiene una gran prevalencia y conlleva un pronóstico adverso, puesto que una IT moderada o grave se asocia per se con un aumento de la morbimortalidad. Por otro lado, el tratamiento quirúrgico solo de la IT presenta una alta morbimortalidad y hospitalización prolongada. En un reciente estudio se demostró que la cirugía tricuspídea no se asociaba con una mejor supervivencia a largo plazo en comparación con el tratamiento médico solo1. En este contexto, las experiencias iniciales de las técnicas percutáneas para el tratamiento de la IT han demostrado viabilidad y seguridad, con unos resultados hemodinámicos y clínicos prometedores.
La válvula percutánea TRICENTO (VPT) (NVT AG, Suiza) tiene como objetivo eliminar el flujo retrógrado sistólico en las venas cavas superior e inferior, aunque no actúa directamente en la IT. La VPT está formada por un stent recubierto de nitinol, con un componente valvular bicuspídeo lateral de pericardio porcino. Desde el primer implante realizado en humanos en 20182, solo se han publicado datos de experiencias unicéntricas iniciales, limitadas y con resultados de seguimiento a corto plazo3,4.
Entre noviembre de 2018 y agosto de 2019, se implantó unA VPT a 6 pacientes consecutivos en 4 centros de España. Las características basales de los pacientes y de la intervención se presentan en la tabla 1. Todos los pacientes presentaban insuficiencia cardiaca (IC) congestiva y se encontraban en clase funcional III-IV de la New York Heart Association (NYHA) en relación con una IT funcional grave, a pesar de un tratamiento médico óptimo. En todos se observó dilatación de la vena cava inferior y flujo sistólico inverso en las venas suprahepáticas. El equipo multidisciplinario evaluó todos los casos y consideró que los pacientes no eran candidatos a tratamiento quirúrgico. Se realizó a todos los pacientes una ecocardiografía transtorácica, un cateterismo cardiaco derecho y una tomografía computarizada multicorte (TCMC) basales. Atendiendo a las recomendaciones del fabricante, se excluyó a los pacientes con desplazamiento sistólico del plano anular tricuspídeo (TAPSE) ≤ 13mmHg, fracción de eyección del ventrículo izquierdo ≤ 30%, presión arterial pulmonar sistólica > 70mmHg o anatomía desfavorable en la TCMC. El estudio se llevó a cabo cumpliendo los principios de la Declaración de Helsinki.
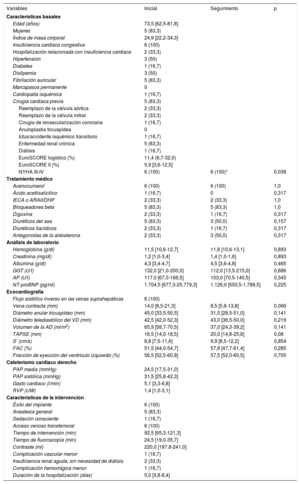
Características clínicas, ecocardiográficas y de la intervención de los pacientes sometidos a implante de la válvula percutánea TRICENTO
| Variables | Inicial | Seguimiento | p |
|---|---|---|---|
| Características basales | |||
| Edad (años) | 73,5 [62,5-81,8] | ||
| Mujeres | 5 (83,3) | ||
| Índice de masa corporal | 24,9 [22,2-34,3] | ||
| Insuficiencia cardiaca congestiva | 6 (100) | ||
| Hospitalización relacionada con insuficiencia cardiaca | 2 (33,3) | ||
| Hipertensión | 3 (50) | ||
| Diabetes | 1 (16,7) | ||
| Dislipemia | 3 (50) | ||
| Fibrilación auricular | 5 (83,3) | ||
| Marcapasos permanente | 0 | ||
| Cardiopatía isquémica | 1 (16,7) | ||
| Cirugía cardiaca previa | 5 (83,3) | ||
| Reemplazo de la válvula aórtica | 2 (33,3) | ||
| Reemplazo de la válvula mitral | 2 (33,3) | ||
| Cirugía de revascularización coronaria | 1 (16,7) | ||
| Anuloplastia tricuspídea | 0 | ||
| Ictus/accidente isquémico transitorio | 1 (16,7) | ||
| Enfermedad renal crónica | 5 (83,3) | ||
| Diálisis | 1 (16,7) | ||
| EuroSCORE logístico (%) | 11,4 (6,7-32,0) | ||
| EuroSCORE II (%) | 5,9 [3,6-12,5] | ||
| NYHA III-IV | 6 (100) | 6 (100)* | 0,038 |
| Tratamiento médico | |||
| Acenocumarol | 6 (100) | 6 (100) | 1,0 |
| Ácido acetilsalicílico | 1 (16,7) | 0 | 0,317 |
| IECA o ARAII/DHP | 2 (33,3) | 2 (33,3) | 1,0 |
| Bloqueadores beta | 5 (83,3) | 5 (83,3) | 1,0 |
| Digoxina | 2 (33,3) | 1 (16,7) | 0,317 |
| Diuréticos del asa | 5 (83,3) | 3 (50,0) | 0,157 |
| Diuréticos tiacídicos | 2 (33,3) | 1 (16,7) | 0,317 |
| Antagonistas de la aldosterona | 2 (33,3) | 3 (50,0) | 0,317 |
| Análisis de laboratorio | |||
| Hemoglobina (g/dl) | 11,5 [10,6-12,7] | 11,8 [10,6-13,1] | 0,893 |
| Creatinina (mg/dl) | 1,2 [1,0-3,4] | 1,4 [1,0-1,6] | 0,893 |
| Albúmina (g/dl) | 4,3 [3,4-4,7] | 4,5 [3,6-4,8] | 0,465 |
| GGT (U/l) | 132,0 [21,0-200,0] | 112,0 [13,5-215,0] | 0,686 |
| AP (U/l) | 117,0 [67,0-166,5] | 103,0 [70,5-140,5] | 0,345 |
| NT-proBNP (pg/ml) | 1.704,5 [677,3-25.779,3] | 1.126,0 [550,5-1.788,5] | 0,225 |
| Ecocardiografía | |||
| Flujo sistólico inverso en las venas suprahepáticas | 6 (100) | ||
| Vena contracta (mm) | 14,0 [8,5-21,3] | 8,5 [5,8-13,8] | 0,066 |
| Diámetro anular tricuspídeo (mm) | 45,0 [33,5-50,5] | 31,0 [28,5-51,0] | 0,141 |
| Diámetro telediastólico del VD (mm) | 42,5 [42,0-52,3] | 43,0 [36,5-50,0] | 0,219 |
| Volumen de la AD (ml/m2) | 65,9 [58,7-70,5] | 37,0 [24,3-39,2] | 0,141 |
| TAPSE (mm) | 16,5 [14,0-18,5] | 20,0 [14,8-25,8] | 0,08 |
| S’ (cm/s) | 8,8 [7,5-11,6] | 9,9 [8,5-12,2] | 0,854 |
| FAC (%) | 51,5 [44,0-54,7] | 57,8 [47,7-61,4] | 0,285 |
| Fracción de eyección del ventrículo izquierdo (%) | 56,5 [52,5-60,8] | 57,5 [52,0-60,5] | 0,705 |
| Cateterismo cardiaco derecho | |||
| PAP media (mmHg) | 24,5 [17,5-31,0] | ||
| PAP sistólica (mmHg) | 31,5 [25,8-42,3] | ||
| Gasto cardiaco (l/min) | 5,1 [3,3-6,8] | ||
| RVP (UW) | 1,4 [1,0-3,1] | ||
| Características de la intervención | |||
| Éxito del implante | 6 (100) | ||
| Anestesia general | 5 (83,3) | ||
| Sedación consciente | 1 (16,7) | ||
| Acceso venoso transfemoral | 6 (100) | ||
| Tiempo de intervención (min) | 92,5 [65,3-121,3] | ||
| Tiempo de fluoroscopia (min) | 24,5 [19,0-35,7] | ||
| Contraste (ml) | 220,0 [187,8-241,0] | ||
| Complicación vascular menor | 1 (16,7) | ||
| Insuficiencia renal aguda, sin necesidad de diálisis | 2 (33,3) | ||
| Complicación hemorrágica menor | 1 (16,7) | ||
| Duración de la hospitalización (días) | 5,0 [3,8-8,4] | ||
AD: aurícula derecha; AP: fosfatasa alcalina; ARAII: antagonistas del receptor de la angiotensina II; DHP: antagonistas del calcio dihidropiridínicos; EuroSCORE: European System for Cardiac Operative Risk Evaluation; FAC: cambio del área fraccional; GGT: gammaglutamil transferasa; IECA: inhibidores de la enzima de conversión de la angiotensina; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; NYHA: clase funcional de la New York Heart Association; PAP: presión arterial pulmonar; RVP: resistencia vascular pulmonar; S’: velocidad sistólica lateral por el anillo tricuspídeo obtenida mediante Doppler tisular; TAPSE: desplazamiento sistólico del plano del anillo tricuspídeo; VD: ventrículo derecho.
Las variables continuas se presentan en forma de mediana [intervalo intercuartílico] y las cualitativas, como n (%).
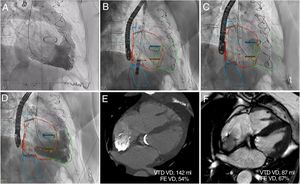
Para los implantes se empleó anestesia general (n=5) o sedación consciente (n=1) con guía por imagen mediante ecocardiografía transesofágica y fluoroscopia. En 2 casos se guio con éxito mediante un sistema de fusión de fluoroscopia-TCMT 3D (figura 1). En primer lugar, se realizó una ventriculografía derecha, y un catéter orientable marcó la entrada de la vena cava inferior en la aurícula derecha (AD). El sistema de liberación de la VPT (24 Fr) se avanzó desde la vena femoral derecha. El implante del dispositivo se realizó mediante un despliegue gradual y controlado desde la vena cava superior a la inferior, tras alinear los marcadores radiopacos que presenta el stent para conseguir una orientación correcta del componente valvular del dispositivo con respecto al plano anular nativo. La ventriculografía derecha final mostró la competencia del sistema valvular bicava, sin flujo inverso a las venas suprahepáticas, y la ausencia de fugas u obstrucción de las venas hepáticas. El implante tuvo éxito en el 100% de los pacientes (figura 1). Se dio el alta a los pacientes en un plazo de 48 días tras el procedimiento, sin que se produjeran complicaciones importantes relacionadas con la intervención.
Implante del dispositivo valvular percutáneo TRICENTO guiado por imagen tridimensional de fusión de TCMC-fluoroscopia, y CRM de seguimiento. A: la ventriculografía derecha basal mostró una insuficiencia tricuspídea grave. B y C: el modelo 3D segmentado con marcas de referencia se fusionó con la fluoroscopia; implante del dispositivo facilitado por las imágenes de fusión de TCMC-fluoroscopia; la ventriculografía final no demostró flujo retrógrado sistólico en la cava y evidenció una opacificación densa de la aurícula derecha (AD). E y F: las CRM obtenidas a los 3 y a los 6 meses mostraro una reducción significativa de los volúmenes del VD y una mejoría de su función. CRM: cardiorresonancia magnética; FE: fracción de eyección; TCMC: tomografía computarizada multicorte; VTD: volumen telediastólico; VD: ventrículo derecho.
Durante el seguimiento (11±4,4 meses), todos los pacientes mostraron mejora de la clase funcional (todos en NYHA I-II). Ningún paciente falleció durante el tiempo de seguimiento. Un paciente ingresó por descompensación aguda de la IC (41 días después de la intervención) y otro necesitó tras el alta seguimiento en el hospital de día para optimizar el tratamiento diurético por datos de IC derecha. El ecocardiograma transtorácico de seguimiento realizado a los 6 meses mostró una reducción del grado de IT (4 de 6 pacientes presentaron una reducción de la IT ≥ 1 grado; p=0,059), la anchura de la vena contracta, el diámetro del anillo tricuspídeo y el volumen de la AD. La función del ventrículo derecho (VD), evaluada mediante TAPSE, S’ y FAC, mejoró tras la intervención, sin alcanzar la significación estadística. La posición de las prótesis fue correcta, sin flujo retrogrado hacia las venas cavas, obstrucción de las venas hepáticas o dehiscencia periprotésica. Todos los pacientes se mantuvieron anticoagulados y se pudo reducir las dosis de diuréticos durante el seguimiento; aún así, las concentraciones de NT-proBNP fueron inferiores, si bien esa disminución no fue estadísticamente significativa (vídeos 1-4 del material adicional).
La principal limitación de este estudio es su carácter observacional y el escaso número de pacientes incluidos. No se pudo obtener datos de seguimiento relevantes (valoración de capacidad funcional y calidad de vida, imagen multimodal y cateterismo cardiaco derecho), que habrá que valorar necesariamente en estudios posteriores.
Se presentan los datos del primer estudio prospectivo, multicéntrico y observacional sobre la seguridad y la viabilidad de la VPT para el tratamiento de la IT funcional grave. La VPT puede ser una alternativa segura y sencilla para pacientes seleccionados con IT grave y alto riesgo quirúrgico con objetivo de mejorar la clase funcional y los síntomas de la IC. Además de resultados prometedores desde el punto de vista clínico en el seguimiento a medio plazo, se demuestra un favorable remodelado inverso del VD, así como una mejora de los parámetros de función del VD. Durante el tiempo de seguimiento, que la VPT impida el flujo retrógado hacia las venas cavas podría proporcionar un flujo más dirigido hacia la AD y mejorar el gasto cardiaco, lo cual, en presencia de una función del VD conservada y ausencia de hipertensión pulmonar, mantendría las capacidades de autorregulación del VD. Esta es una cuestión importante, ya que este dispositivo, al menos teóricamente, podría conducir a una sobrecarga crónica y una ventriculización progresiva de la AD, así como a un remodelado progresivo del VD. Estos problemas hemodinámicos no se han observado en nuestro estudio. Sin embargo, recientemente Willbring et al. han descrito una compresión sistólica del stent a la altura de la AD y una ventriculización funcional de esta5. Se necesitan nuevos estudios para validar estos resultados iniciales.