La enfermedad cardiovascular arteriosclerótica sigue siendo la principal causa de muerte prematura en países tanto desarrollados como en vías de desarrollo. Pese a ello, los estudios muestran que la mayor parte de los pacientes no alcanzan los niveles recomendados en estilo de vida, control de los factores de riesgo o dianas terapéuticas en prevención primaria y secundaria. El objetivo de esta puesta al día es reflejar las más recientes novedades en lo que respecta a clasificación y estimación del riesgo cardiovascular y documentar los últimos cambios en campos como tabaquismo, dieta y nutrición, actividad física, lípidos, hipertensión, diabetes mellitus y rehabilitación, todo ello basado en estudios tanto experimentales como observacionales poblacionales.
Palabras clave
Hay un largo camino entre el inicio de la enfermedad arteriosclerótica y la aparición de sus manifestaciones clínicas, a menudo abruptas y de consecuencias irreversibles. Afortunadamente, se trata de una enfermedad generalmente predecible, cuyos factores de riesgo están bien identificados, y su prevención permite un amplio marco de actuación médica. El trabajo de prevención primaria es largo (décadas), se aplica a segmentos muy amplios de la población y consume otros recursos además de los propiamente asistenciales de la enfermedad clínica. A todo ello se suma la indispensable prevención secundaria y la rehabilitación integral tras el accidente cardiovascular (CV).
Aunque parece que los nuevos fármacos aparecen más lentamente, fiel reflejo de un mundo en crisis, las novedades en todos los campos no cesan de surgir, y viejos conceptos y paradigmas dan paso a otros nuevos que no dejan de sorprender. Por otro lado, en 2012 se ha publicado una puesta al día de las guías europeas en prevención CV1, un extenso documento que actualiza todo el conocimiento desde las guías previas de 2007 y sirve de eje vertebrador de la presente revisión.
Presentamos un análisis de la literatura médica reciente, junto con las comunicaciones a reuniones médicas más relevantes en 2012, todo ello contrastado con las novedades aportadas en los documentos de consenso.
ESTIMACIÓN Y ESTRATIFICACIÓN DEL RIESGO CARDIOVASCULARLa Sociedad Europea de Cardiología1,2 sigue aconsejando (indicación IC) la escala SCORE (Systematic COronary Risk Evaluation) que calcula el riesgo de muerte de causa CV de sujetos asintomáticos en los siguientes 10 años, con algunas novedades: a) se incluye como pacientes de riesgo alto o muy alto, en los que no es necesario calcular el riesgo SCORE, a los que tienen enfermedad renal crónica (filtrado glomerular <60ml/min/1,73m2); b) hay otras circunstancias que no se consideraban previamente, pues sólo se consideraban los factores de riesgo CV (FRCV), que pueden modular el riesgo (tabla 1); c) se incorpora una tabla suplementaria con ajuste del riesgo teniendo en cuenta el valor de colesterol unido a lipoproteínas de alta densidad (cHDL), lo que parece muy relevante en nuestro país3, y d) la aproximación a riesgo de morbimortalidad multiplicando por 3 el valor obtenido del riesgo de muerte.
Circunstancias que pueden aumentar o disminuir el riesgo cardiovascular
| Pueden aumentar el riesgo |
| Precariedad social |
| Sedentarismo y obesidad central |
| Concentraciones bajas de cHDL o apoA1 |
| Aumento de las concentraciones de TG, fibrinógeno, homocisteína, apoB y Lp(a) |
| Hipercolesterolemia familiar |
| Aumento de la PCR-us |
| Función renal alterada |
| Historia familiar de ECV prematura (riesgo×1,7 en mujeres y×2 en varones) |
| Pueden disminuir el riesgo |
| Concentraciones elevadas de cHDL |
| Historia familiar de longevidad |
apoA1: apolipoproteína A1; apoB: apolipoproteína B; cHDL: colesterol unido a lipoproteínas de alta densidad; ECV: enfermedad cardiovascular; Lp(a): lipoproteína(a); PCR-us: proteína C reactiva ultrasensible; TG: triglicéridos.
Modificado de Perk et al1.
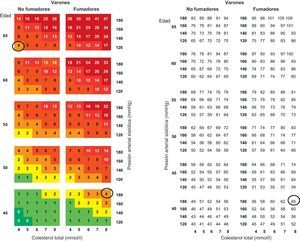
Un aspecto que merece comentario es el de la edad, incorporando el concepto cardiovascular risk age, que hace referencia a la edad estimada según el riesgo CV del paciente. En ediciones anteriores se aconsejaba calcular el «riesgo relativo» del individuo joven con FRCV en comparación con las personas de la misma edad sin dichos factores, pero ahora se trata de equiparar a los más jóvenes con múltiples FRCV con los de más edad sin FRCV pero que presentan el mismo nivel de riesgo, derivado únicamente de su edad más avanzada4. Se han desarrollado tablas específicas para calcularlo (fig. 1).
Riesgo cardiovascular de varón fumador de 40 años, con presión arterial sistólica de 180 mmHg y colesterol total de 8 mmol/l: 4%, que equivale al de un varón de 65 años sin factores de riesgo (no fumador, presión arterial sistólica de 120 mmHg y colesterol total de 4 mmol/l). En el recuadro de la derecha se calcula la edad según el riesgo cardiovascular (cardiovascular risk age) que equivale a 65 años. Modificado de Cooney et al4.
Se ha publicado un metaanálisis que ha demostrado que el análisis de variantes genéticas no mejora la predicción de aterosclerosis subclínica, evaluada por ecografía carotídea, más allá del cálculo basado en FRCV clásicos5. Hay controversia sobre la incorporación de la ecografía carotídea o la tomografía computarizada para detectar calcio coronario6; sin necesidad de recurrir a técnicas sofisticadas, evaluar la lesión en el órgano diana o el síndrome metabólico permite mejorar la estimación del riesgo7.
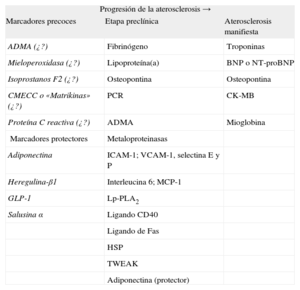
BIOMARCADORESSe considera biomarcadores a los indicadores biológicos relacionados con la aparición de una enfermedad8. Este concepto difiere de factor de riesgo, que implica una relación causal. El modelo que utiliza los FRCV clásicos, contenido en las tablas SCORE, tiene algunas limitaciones, lo que ha propiciado interés por nuevos marcadores que puedan mejorar la capacidad predictora, aunque pocos de ellos estén recomendados en clínica (tabla 2)9–11.
Biomarcadores en el continuo cardiovascular9–11
| Progresión de la aterosclerosis → | ||
| Marcadores precoces | Etapa preclínica | Aterosclerosis manifiesta |
| ADMA (¿?) | Fibrinógeno | Troponinas |
| Mieloperoxidasa (¿?) | Lipoproteína(a) | BNP o NT-proBNP |
| Isoprostanos F2 (¿?) | Osteopontina | Osteopontina |
| CMECC o «Matrikinas» (¿?) | PCR | CK-MB |
| Proteína C reactiva (¿?) | ADMA | Mioglobina |
| Marcadores protectores | Metaloproteinasas | |
| Adiponectina | ICAM-1; VCAM-1, selectina E y P | |
| Heregulina-β1 | Interleucina 6; MCP-1 | |
| GLP-1 | Lp-PLA2 | |
| Salusina α | Ligando CD40 | |
| Ligando de Fas | ||
| HSP | ||
| TWEAK | ||
| Adiponectina (protector) | ||
ADMA: dimetilarginina asimétrica; BNP: péptido natriurético cerebral; CMECC: componentes de la matriz extracelular cardiaca (procolágenos tipos I y III); CK-MB: fracción MB de la creatincinasa; GLP-1: glucagon-like peptide-1; HSP: heat shock proteins; ICAM-1: intercellular adhesion molecule-1; Lp-PLA2: fosfolipasa A2 asociada a lipoproteínas; MCP-1: monocyte chemoattractant protein-1; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; PCR: proteína C reactiva; TWEAK: tumor necrosis factor-like weak inducer of apoptosis; VCAM-1: vascular cell adhesion molecule-1.
Los signos de interrogación indican que todavía no está suficientemente claro que estos biomarcadores sean realmente útiles para el propósito señalado en la columna respectiva.
De los biomarcadores de inflamación más próximos a su utilización clínica, la proteína C reactiva ultrasensible (PCR-us) es el mejor estudiado. En el estudio ASCOT (Anglo-Scandinavian Cardiac Outcomes Trial)12, la PCR-us y el colesterol unido a lipoproteínas de baja densidad (cLDL) basal se correlacionaban con la aparición de eventos CV, pero la inclusión de la PCR-us en el modelo de predicción de riesgo de Framingham no añadía ventajas, un aspecto controvertido13.
Asimismo, cabe destacar la escasa información adicional a los factores de riesgo tradicionales ofrecida por la lipoproteina(a) o por la fosfolipasa A2 asociada a lipoproteínas en un reciente metaanálisis14. El papel de la inflamación en la aterogénesis ha recibido un nuevo impulso con la publicación de un estudio reciente15, en el que se demuestra la relación entre una variante genética conocida por afectar a la función del receptor de la interleucina 6 (Asp358Ala; rs2228145) y menor riesgo CV.
TÉCNICAS DE IMAGEN EN PREDICCIÓN DEL RIESGO CARDIOVASCULARLas técnicas de imagen pueden determinar la carga aterosclerótica y afinar la estratificación del riesgo16. En el último año no se han presentado novedades de gran impacto en este campo. Las recomendaciones del ACCF/AHA (American College of Cardiology Foundation/American Heart Association) del 2010 señalan la determinación del score de calcio coronario como razonable para la valoración del riesgo en adultos con riesgo intermedio (clase IIa)17 y las guías europeas la colocan como clase IIa, pero con un grado de evidencia débil.
Un estudio poblacional prospectivo de la población de Rotterdam analizó el impacto de nuevos marcadores de riesgo e incluyó la fracción aminoterminal del propéptido natriurético cerebral, el fibrinógeno, la PCR-us, la homocisteína, la puntuación de calcio coronario, el grosor intimomedial carotídeo (GIMc), la velocidad de la onda de pulso y la presencia de enfermedad vascular periférica. La puntuación de calcio es la única que mejoraba sustancialmente la predicción del riesgo CV respecto a los FRCV convencionales18.
El GIMc parece tener un papel débil cuando se estudia en población con FRCV convencionales. En el Strong Heart Study, la presencia de placa carotídea era un predictor de eventos, pero no el GIMc. Sin embargo, el estadístico C cambiaba relativamente poco (de 0,700 a 0,714; p=0,011), valores que ponen en duda la utilidad práctica de examinar a este tipo de población con ecografía carotídea19.
NUTRICIÓNEn las últimas guías europeas de prevención CV1 se insiste en una dieta equilibrada que permita mantener un índice de masa corporal <25; se reconoce el efecto del consumo de alcohol en una curva tipo J (máximo, 20g/día los varones y 10g/día las mujeres); se avala el beneficio de la dieta DASH (Dietary Approaches to Stop Hypertension) para hipertensos y se destaca que no hay evidencia para tratar el exceso de homocisteína.
No hay un posicionamiento sobre los ácidos grasos omega 3, que sí se recomiendan en las guías europeas de dislipemia (indicación IIa B)2. En cualquier caso, la evidencia en prevención secundaria no es consistente. Un reciente metaanálisis no observó reducción de eventos o mortalidad CV20.
Actualmente no hay evidencia de que los fitosteroles prevengan la enfermedad CV, si bien el consumo a dosis de 2g/día puede disminuir el cLDL un 7-10%21.
La Sociedad Española para el Estudio de la Obesidad no recomienda las dietas hiperproteicas tipo Dukan; si bien pueden inducir a corto plazo mayor pérdida de peso que una dieta cardiosaludable, la reducción del peso no se mantiene tras 12meses y la eficacia a largo plazo no está demostrada22.
EJERCICIO FÍSICOEl ejercicio físico se reconoce como una intervención clave en la prevención CV. Hay suficiente evidencia científica de que consigue beneficios en la reducción de la morbimortalidad y mejora la capacidad funcional23, aunque hay controversia sobre el tipo y la intensidad24. El entrenamiento de alta intensidad obtiene mejores resultados en la capacidad aeróbica, incluso cuando se compensa la menor intensidad con mayor duración o frecuencia25, aunque se debate sobre su seguridad. Estudios recientes han objetivado que el entrenamiento de alta intensidad, realizado a intervalos, es más eficaz que la metodología tradicional del ejercicio moderado de tipo continuo, con mejores resultados en la capacidad funcional y otras variables pronósticas26.
TABACOSegún se deduce de los registros EUROASPIRE (European Action on Secondary and Primary Prevention through Intervention to Reduce Events), el tabaquismo sigue siendo una asignatura pendiente27. Confluyen dos circunstancias contradictorias: el riesgo para la salud que supone el tabaquismo (no sólo CV) y la preocupante desatención de esta enfermedad por parte del colectivo médico, especialmente los cardiólogos. En la actualización de las guías europeas1 se resalta el papel de las leyes que restringen el consumo de tabaco en lugares públicos como herramienta de prevención y control del tabaquismo. En enero de 2011 entró en vigor en España la ley que extendió la prohibición de fumar a cualquier tipo de espacio cerrado de uso colectivo, además de prohibir el consumo en algunos lugares abiertos. Aunque esta ley ha cosechado ya algunos éxitos en la reducción de la prevalencia del tabaquismo, queda por confirmar su efecto en la reducción de ingresos por infarto o angina y su consecuente impacto económico, como se ha demostrado en un estudio reciente en Alemania28. Se resalta que el impacto del tabaquismo en el riesgo de infarto es más importante entre los jóvenes29 y que la prevalencia de tabaquismo ha seguido aumentando preocupantemente entre las mujeres.
La guía europea actualizada menciona los tres fármacos de primera línea en deshabituación (sustitutos de la nicotina, bupropión y vareniclina), de los cuales la vareniclina es el más efectivo, con efectos secundarios raros, pero con ciertas incertidumbres sobre su seguridad neuropsiquiátrica y CV. Un metaanálisis inicial señaló un aumento de eventos CV30. La metodología de este estudio fue discutida, pero su publicación ensombreció el uso de la vareniclina. La Food and Drug Administration se pronunció de manera prudente afirmando que el discreto aumento de riesgo CV no anula el amplio beneficio que supone dejar de fumar. Posteriormente se ha publicado un metaanálisis más ortodoxo, que analiza la tasa de eventos CV en 22 ensayos aleatorizados y a doble ciego de vareniclina en comparación con placebo. La tasa de eventos CV fue baja y no hubo diferencias entre la vareniclina y el placebo. Se concluye que el uso de vareniclina no se asocia con un aumento significativo de eventos CV, lo que despeja el horizonte sobre su papel31.
HIPERTENSIÓN ARTERIALEn cuanto al diagnóstico de la hipertensión arterial (HTA), se ha publicado una comparación, en población general, de la utilidad de la monitorización ambulatoria de la presión arterial (MAPA), la efectuada en domicilio (AMPA) y la casual para predecir las enfermedades cerebrovasculares subclínicas (ECS)32. La MAPA y la AMPA se relacionaron con el riesgo de ECS y aterosclerosis carotídea. La MAPA nocturna fue el más potente predictor de ECS. La AMPA se relacionó más estrechamente con el riesgo de aterosclerosis carotídea que cualquiera de los valores de MAPA. La determinación casual de la presión arterial no se asoció con el riesgo de ECS.
En cuanto al tratamiento farmacológico de la HTA, se han publicado dos metaanálisis importantes en el último año. El primero33 analizó la eficacia de la hidroclorotiazida frente a la clortalidona, y concluyó que esta produce mayor reducción de enfermedad CV que la hidroclorotiazida, con un número de pacientes que es necesario tratar = 27 para prevenir un episodio CV en 5 años. En el segundo estudio34, se evidenció que la combinación de aliskiren con inhibidores de la enzima de conversión de la angiotensina o antagonistas de los receptores de la angiotensina II aumentaba el riesgo de hiperpotasemia en comparación con las monoterapias de cada uno de ellos. La reciente interrupción del ensayo ALTITUDE (Aliskiren Trial in Type 2 Diabetes Using Cardio-Renal Endpoints) —no incluido en el estudio34—, por una inesperada incidencia de efectos adversos en los pacientes diabéticos que recibían la combinación de aliskiren con otros inhibidores del sistema renina-angiotensina, es otra llamada de alerta.
En cuanto a la novedosa técnica de denervación renal mediante ablación de las arterias renales con radiofrecuencia, que consigue notables descensos de presión arterial en sujetos con HTA refractaria, un grupo de expertos ha escrito un artículo en el que se describen los requisitos, las evidencias y el desarrollo futuro de la técnica35. Por otro lado, se han publicado seguimientos más a largo plazo de los ensayos clínicos SIMPLICITY que avalan su eficacia y su seguridad.
En cuanto al control de la HTA en nuestro medio, se ha publicado un metaanálisis36 para conocer la prevalencia de HTA no controlada en 341.632 pacientes de distintas características de riesgo, y el panorama es desolador. Entre los pacientes hipertensos, la prevalencia de HTA no controlada era del 67%, y en pacientes con alto riesgo CV llegaba al 87,6% (objetivo <130/80mmHg). También un grupo español ha demostrado en un estudio de 6.675 participantes que el conocimiento de la HTA aumenta con la frecuentación del sistema sanitario y los factores asociados a ello son el sexo femenino, la edad y tener problemas de salud37.
En cuanto al pronóstico, un nuevo estudio con 5.788 pacientes observa una curva en J, con un incremento de eventos CV y mortalidad por encima y por debajo del nadir de presión arterial de 143/82 mmHg38.
LÍPIDOSLas principales novedades en lípidos se enmarcan en nuevos hallazgos del valor de control del cLDL y el colesterol no-HDL. Un metaanálisis de 60.000 pacientes tratados con estatinas demostró que el control del cLDL por debajo de 100mg/dl no se acompaña de reducción de la incidencia de enfermedad CV si no se acompaña de reducciones del colesterol no-HDL por debajo de 130 mg/dl39. Otro hallazgo importante de este metaanálisis es que únicamente cerca del 60% de los pacientes que recibieron estatinas alcanzaron el control del cLDL y el no-HDL, lo que refleja las carencias de los tratamientos actuales para el completo control del perfil lipídico. Este concepto se ha denominado riesgo residual lipídico. En un registro de pacientes con cardiopatía isquémica realizado en España, se observó que el 30% de los pacientes tenían este riesgo residual lipídico40.
En el campo terapéutico, una de las estrategias más esperanzadoras para la reducción del cLDL es el bloqueo de la PCSK9 (proproteína convertasa subtilisina/kexin tipo 9) implicada en la degradación del receptor hepático de LDL, mediante anticuerpos monoclonales. Un estudio de fase I demostró que la utilización de estos anticuerpos, administrados por vía subcutánea cada 15 o 30 días, reduce la concentración de cLDL un 40-60%, con excelente tolerabilidad41. La eficacia clínica en reducción de eventos clínicos no se conocerá hasta que finalicen dos grandes ensayos clínicos que van a iniciarse en 2013.
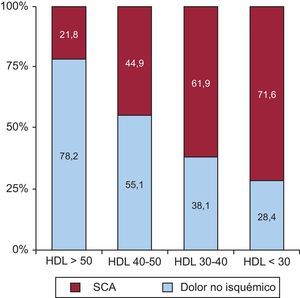
Los inhibidores selectivos de la proteína de transferencia de ésteres de colesterol evitan la degradación de las HDL y elevan sus concentraciones séricas entre un 60 y un 90%. Sin embargo, en mayo de 2012 se suspendió precozmente el ensayo clínico DAL-OUTCOMES, con dalcetrapib en pacientes coronarios, por falta de eficacia. Por otra parte, se han identificado determinadas mutaciones genéticas que conducen a valores de cHDL más elevados pero que no se asocian con menor riesgo de enfermedad CV42. Sin embargo, en la comparación de los pacientes ingresados en un único centro por dolor torácico, se observó que los pacientes dados de alta con diagnóstico de dolor torácico no coronario tenían valores de cHDL un 22% más elevados que los pacientes diagnosticados de síndrome coronario agudo, sin hallarse diferencias en los valores de cLDL43. El análisis multivariable demostró una asociación entre cHDL bajo y diagnóstico de síndrome coronario. Además, se observó que cuanto menor es la concentración media de cHDL mayor es la prevalencia de síndrome coronario agudo (fig. 2).
Relación entre concentración de lipoproteínas de alta densidad y síndrome coronario agudo43. HDL: lipoproteínas de alta densidad; SCA: síndrome coronario agudo.
La elección del punto de corte de glucohemoglobina (HbA1c) del 6,5% para el diagnóstico de diabetes mellitus (DM) sigue en controversia. Para muchos, esta cifra debería ser más baja, ya que en la franja del 6 al 6,4% puede haber pacientes sin diagnosticar44.
En cuanto al papel de la glucemia posprandial para el pronóstico, destaca un estudio con 14 años de seguimiento de diabéticos45, en quienes la glucemia posprandial y no la glucemia en ayunas predijo tanto los eventos CV como la mortalidad.
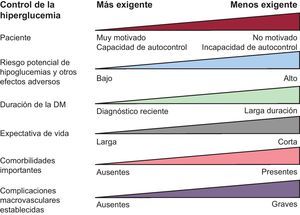
Ha habido cambios en los objetivos del control glucémico a favor del control multifactorial. Las guías europeas de prevención1 recomiendan un objetivo de HbA1c <7% para pacientes diabéticos con cardiopatía. Un objetivo por debajo del 6,5% podría ser útil en pacientes con diagnóstico reciente y podría reducir las complicaciones microvasculares en pacientes con DM de larga evolución, según los resultados del estudio ADVANCE (Action in Diabetes and Vascular disease: PreterAx and DiamicroN MR Controlled Evaluation)46. Las guías de prevención secundaria de la AHA/ACCF de 201147 plantean un objetivo general de HbA1c<7% y especifican que se podría considerar un objetivo menos ambicioso para pacientes con antecedentes de hipoglucemia, enfermedad macrovascular o microvascular o presencia de otras comorbilidades, ya que la enfermedad macrovascular, que causa más muertes en diabéticos que la microvascular, no se ve afectada tan claramente por la intensidad del control glucémico, sino más bien por el adecuado control de los otros factores de riesgo. La American Association for Diabetes y la European Association for the Study of Diabetes ponen énfasis en individualizar las cifras objetivo de HbA1c en cada paciente (fig. 3)48. Además, hay serias dudas sobre la seguridad de buscar objetivos demasiado ambiciosos en pacientes con una aterosclerosis avanzada, a raíz de los resultados del estudio ACCORD (Action to Control Cardiovascular Risk in Diabetes)49, interrumpido precozmente por aumento de la mortalidad en la rama de tratamiento intensivo. En diabéticos con insuficiencia cardiaca, cifras más altas de HbA1c se asocian con una mejora de la supervivencia50. Como conclusiones, se establece: a) el mayor control de las glucemias no siempre obtiene mayor beneficio, y b) el mejor tratamiento para la DM es el control estricto de los FRCV, sobre todo el control de la presión arterial y los lípidos.
Los objetivos de control de la glucemia en la diabetes mellitus deben pasar, hoy en día, por un abordaje individualizado a cada paciente sopesando varios factores. DM: diabetes mellitus. Modificado de Zannad et al6.
Actualmente hay un debate respecto a los factores que causan la enfermedad macrovascular en el contexto del síndrome metabólico y la prediabetes. La resistencia a la insulina antes del inicio de la DM se define por hiperinsulinemia, y se especula con la posibilidad de que tenga una relación causal con la enfermedad vascular51.
En el tratamiento farmacológico del paciente diabético con cardiopatía, el impacto en los eventos CV y la mortalidad de los fármacos secretagogos está en debate. Estudios recientes han demostrado un aumento de mortalidad y eventos CV mayores en pacientes que tomaban glimepirida, glibenclamida, glipizida o tolbutamida frente a los que tomaron metformina52. Un metaanálisis sobre la insulina53 ha descartado que haya riesgo de cáncer con el empleo de la insulina glargina.
REHABILITACIÓN CARDIACASe ha demostrado que los programas de rehabilitación cardiaca (PRC) disminuyen la mortalidad CV y total, el infarto no fatal y la necesidad de revascularización y mejoran la calidad de vida en comparación con la intervención convencional después de un evento coronario54.
En las guías europeas de prevención1, es una indicación clase IIa B que todos los pacientes que han sido sometidos a revascularización coronaria (quirúrgica o percutánea) después de un síndrome coronario agudo sean remitidos a un PRC para mejorar el estilo de vida y la adherencia al tratamiento farmacológico.
A pesar de los claros beneficios de los PRC, su uso sigue siendo decepcionantemente bajo. El bajo número de unidades de rehabilitación cardiaca y la falta de acceso a estos programas contribuyen a la infrautilización; pero otro factor importante es que los cardiólogos derivan a un bajo porcentaje de los pacientes, sobre todo de mujeres y ancianos. Para corregir estos obstáculos, se ha publicado en un documento de consenso de la AHA54 que da alternativas a los modelos tradicionales de los PRC hospitalarios, como la realización de programas ambulatorios en los centros de salud o domiciliarios. Los programas domiciliarios para pacientes de bajo riesgo se recomiendan con base en que no hay diferencias en cuanto al pronóstico y la evolución de los pacientes frente a los PRC tradicionales hospitalarios55.
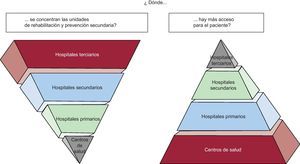
También se incluyen, por su mayor accesibilidad, programas ambulatorios dirigidos por médicos de atención primaria para pacientes de bajo riesgo (fig. 4), así como programas dirigidos por asistencia a distancia. La Sociedad Española de Cardiología ha publicado estudios que avalan esta postura56,57 y demuestran, además, beneficios en la disminución de las complicaciones CV y mejora de la calidad de vida de los pacientes.
La infrautilización de los programas de rehabilitación cardiaca se debe a muchos factores; uno de los más importantes es la falta de acceso de los pacientes a los hospitales de nivel terciario. Se plantean nuevos modelos de centros de prevención y rehabilitación cardiaca, como son la creación de programas coordinados en los centros de salud para facilitar el acceso a los pacientes.
Pese a la intensa crisis socioeconómica que nuestra sociedad ha vivido en el tiempo que nuestra generación pueda recordar, el avance en el conocimiento no se ha detenido, como refleja fielmente esta revisión. Por otro lado, asistimos simultáneamente a una fase de reflexión y asentamiento de muchos de los avances, en que el análisis y el consenso de las estrategias en el campo de la prevención CV han sido importantes. Todo ello no esconde las numerosas lagunas que restan para completar la evidencia, y el amplio espacio que nos queda para mejorarla.
CONFLICTO DE INTERESESNinguno.