En este artículo se revisan los trabajos más relevantes en el campo de las arritmias publicados en 2012, incluyendo aritmología clínica, técnicas de ablación, estimulación cardiaca y genética de la muerte súbita.
Palabras clave
El área de conocimiento de las arritmias incluye tanto aspectos clínicos de pacientes con alteraciones del ritmo como aspectos más específicos referidos al tratamiento farmacológico o no farmacológico de las arritmias, ya sea la ablación o la estimulación cardiaca, que actualmente implica el tratamiento tanto de las bradiarritmias como de las taquiarritmias o el manejo de pacientes con insuficiencia cardiaca (IC).
En este artículo se revisan las novedades aparecidas en la literatura relacionadas con la ablación de la fibrilación auricular (FA) o las taquicardias ventriculares (TV), síncope o estimulación cardiaca, así como en el campo de la genética de la muerta súbita.
ABLACIÓN DE LA FIBRILACIÓN AURICULARResultados y complicacionesLos resultados y las complicaciones de la ablación de la FA siguen siendo un tema discutido1. En un estudio reciente, Calvo et al2 analizaron la mejora evolutiva en los resultados y las complicaciones en relación con la optimización del procedimiento y la curva de aprendizaje. El estudio recoge la experiencia de un solo centro e incluye 726 procedimientos consecutivos de ablación. La eficacia general, incluida la realización de varios procedimientos en algunos pacientes, fue del 61% con un seguimiento medio de 8 meses. Al dividir la serie en dos grupos, un primer grupo (A), que incluyó a 419 pacientes a los que se realizó la ablación antes de enero de 2008, y un segundo grupo (B), compuesto por 307 pacientes a los que se realizó la ablación después y se les aplicó un protocolo riguroso de anticoagulación y sedación, se observó una mejora en los resultados y una disminución en las complicaciones mayores, que pasaron del 6,2% en el grupo A al 1,2% en el grupo B. Los predictores de éxito independientes fueron el tipo de FA (paroxística frente a persistente), diámetro auricular anteroposterior < 45 mm y ausencia de hipertensión y apnea obstructiva del sueño. Cabe destacar que el porcentaje de complicaciones y los resultados pueden mejorar de manera importante con una buena curva de aprendizaje, la aplicación de protocolos estrictos y una buena selección de pacientes. Por otro lado, hay que tener en cuenta que la valoración del éxito, medida como tiempo hasta la primera recurrencia documentada, es un objetivo estadístico que no tiene en cuenta la auténtica mejoría clínica del paciente, que probablemente sea superior.
Nuevas tecnologíasEntre las mejoras técnicas que pueden facilitar la práctica de la ablación de FA, destaca la incorporación de la angiografía rotacional (AR). Hadid et al3 analizaron la utilidad de la AR en la visualización de la aurícula izquierda. La técnica se realizó mediante inyección de adenosina para inducir una pausa suficiente para contrastar la aurícula izquierda. Se obtuvieron imágenes analizables en 12 de 15 pacientes, si bien se había excluido previamente a 5 pacientes por diversas causas. Los autores hallaron buena concordancia con las imágenes de resonancia. Por ello, la práctica de AR podría ahorrar el uso de otras técnicas de imagen previas al procedimiento y disminuir costes y tiempo. Sin embargo, la AR se realizó con anestesia general, que no es un procedimiento habitual en todos los medios para la ablación de FA.
Recientemente se ha introducido en el procedimiento de ablación la tecnología que permite medir la fuerza de contacto aplicada al electrodo distal del catéter de ablación. Se conoce experimentalmente la estrecha relación entre la fuerza ejercida contra la pared del corazón y la extensión de la lesión. Sin embargo, los datos clínicos de que disponemos para valorar la utilidad clínica son muy escasos. Recientemente se han publicado los resultados del estudio TOCCATA4. El estudio se realizó en 32 pacientes y muestra que recurrieron todos los pacientes en que la fuerza media aplicada fue < 10 g, mientras que cuando la fuerza media fue > 20 g, el 80% de los pacientes estaban libres de recurrencia. Los autores concluyen que hay buena correlación entre el contacto y el resultado de la ablación y, por lo tanto, esta mejora técnica podría mejorar los resultados significativamente.
EstrategiasLa ablación quirúrgica utilizando una técnica por toracoscopia mínimamente invasiva puede resultar una opción alternativa a la ablación de FA en pacientes con FA no permanente. El estudio FAST5 ha sido el primero en realizar una comparación aleatorizada entre la ablación por catéter y el aislamiento quirúrgico de las venas pulmonares en un grupo de pacientes con recurrencias tras un primer procedimiento o con aurículas dilatadas. Se aleatorizó a 124 pacientes en dos centros. Tras un seguimiento de 12 meses con Holter de 7 días, solamente el 36,5% de los pacientes tratados con catéter estaban totalmente libres de recurrencia, en comparación con el 65,6% de los pacientes quirúrgicos. Estos presentaron una tasa de complicaciones perioperatorias mayor. El estudio indica que la lesión realizada mediante cirugía es más transmural y permanente y, por lo tanto, más eficaz. Sin embargo, la mayor morbimortalidad y la curva de aprendizaje hacen que por el momento esta técnica se pueda aplicar en muy pocos centros.
La ablación de FA sigue estando limitada por la comprensión del mecanismo subyacente. Mientras la concepción predominante propone la presencia de múltiples ondas circulantes, otros autores defienden formas más focales, en las que se podría realizar la ablación focalmente. En el estudio CONFIRM6 se ha analizado la presencia de mecanismos focales mediante un complejo sistema cartográfico, y se ha comparado la eficacia de la ablación guiada por cartografía frente a la ablación convencional. Se incluyeron 107 procedimientos de ablación. Se identificaron rotores o focos en el 97% de los casos. En la mitad de los pacientes, la ablación se guió por el sistema cartográfico. El 82% de los pacientes tratados mediante ablación guiada estaba libres de recurrencia tras un seguimiento medio de 273 días, en comparación con un 45% de los pacientes tratados con ablación convencional. Los autores concluyen que en la FA en humanos frecuentemente hay rotores y mecanismos focales y que la ablación de estos focos puede mejorar la eficacia del procedimiento de ablación.
TAQUICARDIA VENTRICULARDurante los últimos meses se ha producido una eclosión de conocimientos en el campo de la ablación de las TV, que presentaremos en tres apartados.
Nuevos procedimientos de ablación de sustratoDos estudios recientes se refieren a este aspecto. El primero compara una técnica convencional/sustrato de ablación endocárdica guiada por las TV inducidas frente a un abordaje endoepicárdico mucho más extenso, denominado homogeneización de la cicatriz7. En ese estudio se incluyó a 92 pacientes con tormenta eléctrica: 49 se sometieron a la ablación de sustrato limitada y circunscrita a las zonas de la cicatriz relacionadas con las TV inducidas y 43 a la ablación de todas las zonas de endocardio y epicardio con electrogramas anormales. En este segundo grupo se identificaron zonas con electrogramas anormales en el epicardio en el 33% de los pacientes. En ambos grupos, el objetivo final era la supresión de todas las TV inducibles, objetivo que se alcanzó en todos los casos. Con un seguimiento de 25 ± 10 meses, la tasa de recurrencias fue significativamente mayor en el primer grupo (el 47 frente al 19%; p = 0,006). Un paciente en cada grupo murió durante el seguimiento. Este estudio pone de manifiesto: a) la supresión de la inducibilidad no es el objetivo final de la ablación, y b) la eliminación de todo el sustrato endocárdico y epicárdico, aunque no se pruebe su relación con una taquicardia específica, debe ser el objetivo final.
El siguiente estudio se basó en la hipótesis de que la eliminación de los electrogramas anormales relacionados con la cicatriz y caracterizados por la presencia de potenciales tardíos podía ser un objetivo eficaz y útil durante la ablación de sustrato8. En este estudio se incluyó a 70 pacientes, el 80% presentaba cardiopatía isquémica y en el 95,7% se encontraron zonas de electrogramas anormales. Durante la ablación, se eliminó o se disoció el 70% de los electrogramas. Cuando se analizaron los predictores de recurrencia de taquicardia o muerte durante un seguimiento de 22 meses en un análisis multivariable, la eliminación de los electrogramas anormales fue el único predictor (p = 0,02), mientras que la no inducibilidad (p = 0,11) y el tipo de cardiopatía (p = 0,29) no se identificaron como predictores.
Valoración de los objetivos del procedimiento de ablaciónTal como se ha visto en el apartado anterior, la supresión de la inducibilidad durante la estimulación eléctrica programada es un objetivo final de la ablación sobre el que existen muchas dudas7,8. El artículo que comentamos a continuación aporta datos que explican las limitaciones de los objetivos agudos de la ablación9. El estudio evaluó el valor de la estimulación programada no invasiva días después de un procedimiento de ablación. En un grupo de 132 pacientes, se procedió a la estimulación programada con un desfibrilador automático implantable (DAI) al menos 3 días después de un procedimiento de ablación. En el 44% de los pacientes no se indujo ninguna TV, en el 37% sólo se indujeron TV no clínicas y en el 18%, la taquicardia clínica. Los pacientes libres de TV al año eran el 80, el 65 y el 30% respectivamente. En el estudio inmediatamente tras la ablación, se indujo una TV clínica en el 6% de los pacientes, mientras que en el estudio diferido se indujo en un 18%. Estos datos indican que los resultados de la estimulación eléctrica programada diferida tienen implicaciones pronósticas. Además, dicho estudio diferido probablemente sea más sensible en cuanto a la inducibilidad de TV clínicas.
Procedimientos alternativos a la ablación con radiofrecuenciaCrioablación epicárdicaAunque la ablación percutánea con radiofrecuencia (RF) es segura y eficaz, sigue habiendo taquicardias no abordables con esta técnica, principalmente las taquicardias relacionadas con la miocardiopatía no isquémica. La ablación quirúrgica es una alternativa y el estudio que analizamos a continuación evalúa la utilidad de esta técnica como complemento a la caracterización electrofisiológica y electroanatómica previa10. En 8 pacientes con estudio electroanatómico previo y ablación con RF ineficaz, se realizó crioablación quirúrgica en los puntos identificados y tratados previamente. Durante un seguimiento medio de 23 ± 6 meses, 6 pacientes tuvieron una reducción significativa de choques por paciente de 6,6 a 0,6 (p = 0,026). Los 2 pacientes restantes murieron de IC y de causa no cardiaca. El estudio demuestra que la crioablación epicárdica sobre dianas identificadas previamente es eficaz en la mayoría de los pacientes no respondedores a la ablación con RF.
Ablación intracoronaria con etanolOtras de las terapias alternativas que se puede ofrecer cuando la ablación convencional endoepicárdica fracasa es la ablación intracoronaria con etanol, particularmente eficaz en los casos en que los circuitos están profundos en la pared ventricular. En el siguiente estudio se describe esta estrategia11. De 274 pacientes consecutivos sometidos a ablación de TV, en 27 se recurrió a la ablación intracoronaria. En 5 pacientes el procedimiento no se completó por anatomía coronaria no favorable. Después de la ablación se suprimió la inducibilidad en el 82% de los pacientes. Aunque se observó recurrencia de TV en el 64% de los pacientes, de los 11 pacientes con tormenta eléctrica como indicación de la ablación, sólo 2 tuvieron recurrencia de la tormenta eléctrica.
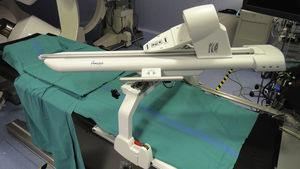
NAVEGACIÓN A DISTANCIADurante 2012 se ha aprobado para uso clínico una nueva generación de navegadores a distancia. El Amigo™ Remote Catheter System de Catheter Robotics consiste en un brazo robótico que permite manipular a distancia catéteres convencionales de ablación (fig. 1)12. No aporta a priori ninguna ventaja sustancial en la navegabilidad o la estabilidad del catéter frente a la navegación convencional manual, dado que utiliza el mismo catéter y se basa asimismo en empuje mecánico. Sin embargo, la posibilidad de estar alejado del campo estéril del paciente y de que el operador pueda manejar al mismo tiempo otros sistemas, como el navegador electroanatómico, facilita y hace más fluido el procedimiento. El sistema no requiere espacio o infraestructura especial y es sustancialmente más barato que los sistemas de navegación de la primera generación. El otro sistema de segunda generación es el CGCI® de Magnetecs. Este sistema se basa en ocho electroimanes que, una vez emplazado el paciente entre ellos, permiten dirigir un catéter de punta magnética mediante cambios muy rápidos del campo magnético al variarse la cantidad de corriente eléctrica que circula por cada electroimán (fig. 2). El sistema se controla a distancia desde una consola con dos joysticks, lo que permite obtener una navegación muy intuitiva y prácticamente sin retrasos, a diferencia de lo que ocurre con otros navegadores a distancia magnéticos, como el sistema Niobe®, que son más lentos. Esta agilidad de respuesta permite un modo de navegación y ablación automática con sólo marcar los puntos objetivo mediante un ratón sobre el modelo tridimensional de la cavidad cardiaca representada en un sistema electroanatómico convencional. Hasta la fecha, se han presentado como comunicaciones a congresos resultados excelentes con este navegador sobre un modelo animal13 y preliminares de ablación de sustratos arrítmicos complejos en humanos14,15.
Brazo robótico sobre el que se sustenta el catéter de ablación en el Amigo™ Remote Catheter System. El mango del catéter se aplica sobre dicho brazo, introduciéndose la parte distal del catéter a través del introductor femoral. Los movimientos se transmiten al catéter a través del brazo robótico, desde una consola a distancia mediante un joystick.
Al mismo tiempo, se ha continuado presentando resultados clínicos y mejoras de los sistemas de navegación a distancia de primera generación. Entre estas mejoras destacan las del navegador Niobe® de Stereotaxis, que ahora incorpora la posibilidad de utilizar un brazo robótico que permite navegar a distancia otro catéter, en concreto uno circular de cartografía de venas pulmonares, además de mantener la navegación magnética del de ablación16. Esto es especialmente importante para procedimientos como el de desconexión eléctrica de venas pulmonares para ablación de la FA que requieren ir desplazando el catéter circular de vena en vena según se va desconectando cada una de ellas.
En cuanto a resultados clínicos, se han publicado resultados sobre el uso de navegadores a distancia para la ablación de sustratos arrítmicos complejos. Así, se ha descrito la utilización de navegadores magnéticos para la ablación en pacientes con cardiopatías congénitas complejas, con buenos resultados y ventajas sobre la navegación manual convencional en estas situaciones anatómicas complejas17. También se ha presentado un registro mundial de la experiencia con el navegador robótico Sensei® de Hansen Medical para la ablación de FA, que ha mostrado que se requiere un curva de aprendizaje de 50 casos para reducir el porcentaje de complicaciones en la ablación de FA comparado con la ablación convencional18.
Finalmente, se ha publicado una eficacia significativamente superior para la ablación de TV con la navegación magnética a distancia, especialmente en pacientes sin cardiopatía estructural19.
SÍNCOPELo más relevante en cuanto al síncope en 2012 se refiere a aspectos terapéuticos, tanto en la confirmación de la ausencia de efectividad del tratamiento farmacológico como en el papel de la estimulación cardiaca permanente en algunas formas de síncope neuromediado.
Tratamiento farmacológicoHa habido dos artículos que abundan en la ineficacia de los tratamientos farmacológicos en pacientes con síncope neuromediado. Durante los últimos años, con base en estudios controlados realizados en pocos pacientes, se había propuesto que la midodrina podría ser el único fármaco útil en el tratamiento de pacientes con síncope neuromediado recurrente. Teniendo en cuenta que en la mayoría de las publicaciones que han estudiado la efectividad de la midodrina el fármaco se ha evaluado como primera opción terapéutica frente a medidas convencionales, y dado que actualmente parece claro que el tratamiento no farmacológico (como maniobras de contrapresión) es el de primera elección y además efectivo en más del 50% de los pacientes, Romme et al20 han realizado un estudio controlado y cruzado de midodrina frente a placebo en pacientes con síncope vasovagal recurrente en los que ya hubieran fallado las medidas de tratamiento no farmacológico. En este grupo de pacientes, no han hallado ningún efecto beneficioso de la midodrina frente a placebo. Este mismo grupo ha realizado un metaanálisis de 46 estudios aleatorizados en el que se estudia la efectividad de distintos fármacos en síncope vasovagal (40 estudios) o síncope por síndrome del seno carotídeo (6 estudios), y concluyen que actualmente no hay datos que permitan recomendar ningún tratamiento farmacológico para el síncope vasovagal o el secundario al síndrome del seno carotídeo21.
Estimulación cardiaca en el síncope neuromediadoA inicios de 2012 se publicaron dos estudios que contribuyen a aclarar el papel de la estimulación cardiaca en pacientes con síncopes neuromediados y asistolias. En el primero de ellos22 se estudió a 80 pacientes con síncopes inexplicados; en los que, tras la administración endovenosa de 20 mg de ATP (adenosintrifosfato), se observó asistolia > 10 s. A estos pacientes se les implantó un marcapasos de doble cámara (marca y modelo a elegir por el investigador) y se los aleatorizó a una programación DDD a 70 lpm (modo activo) frente AAI a 30 lpm (modo pasivo o placebo). En un seguimiento de 5 años, la tasa de recurrencias fue del 21% en los pacientes que tenían el marcapasos en modo activo frente al 66% en los que lo tenían en modo AAI. Por otra parte, el estudio ISSUE-323 incluyó a pacientes > 40 años de edad con síncope neuromediado recurrente, en los que se había documentado mediante registrador de eventos implantable una pausa > 3 s durante un episodio sincopal espontáneo o > 6 s independientemente de la presencia de síntomas. A estos pacientes, se les implantó un marcapasos con algoritmo rate drop response y, tras el implante, se los aleatorizó a modo DDD o ausencia de estimulación. En un seguimiento de 2 años, la tasa de recurrencia fue del 57% en el grupo de pacientes sin estimulación frente al 25% en los pacientes con estimulación en modo activo.
Estos datos apuntan a que pacientes seleccionados, con síncope de causa desconocida o neuromediada en los que se documente una asistolia, ya sea durante un episodio sincopal espontáneo o mediante el test de ATP, pueden beneficiarse de la implantación de un marcapasos. De todas maneras, esta terapéutica debe reservarse como última alternativa para pacientes muy sintomáticos y se debe evitarla en pacientes jóvenes.
Síncope en pacientes con bloqueo de ramaLa actitud ante pacientes con episodios sincopales, bloqueo de rama y ausencia de cardiopatía estructural sigue sin estar totalmente aclarada. Mientras que algunos autores proponen la implantación de marcapasos en la mayoría de estos pacientes, otros proponen una estrategia escalonada, consistente en realizar primero un estudio electrofisiológico y, si este es normal, implantar después un registrador de eventos. Azocar et al24 han publicado un artículo en que usan esta estrategia en un grupo de 85 pacientes con síncope y bloqueo de rama, y hallan que el estudio electrofisiológico fue diagnóstico en 36 (42%). De los 38 pacientes a los que se implantó un registrador de eventos, hubo un hallazgo diagnóstico en 13 (34%). En general, el diagnóstico más frecuente fue bloqueo paroxístico, hallado en 37 pacientes (43%), seguido de la TV, en 6 (7%). Durante el seguimiento hubo 2 muertes (2,3%), ninguna de ellas de causa cardiaca. Estos hallazgos son similares a los publicados por Moya et al25 y confirman que esta es una estrategia segura que permite establecer el diagnóstico en un porcentaje relativamente elevado de pacientes.
ESTIMULACIÓN CARDIACAMarcapasosDurante 2012 se han publicado 895 artículos con el término cardiac pacing como palabra clave. Resumimos a continuación los más relevantes, distribuidos por temas.
Marcapasos en el implante percutáneo de válvula aórticaEn 2012 se han publicado dos artículos de especial relevancia en relación con la menor necesidad de implante de marcapasos tras implante transcatéter de válvula aórtica. El primero26 aplica una estrategia conservadora en pacientes que presentan bloqueo completo de rama izquierda durante el procedimiento para evitar la estimulación cardiaca, sin encontrar diferencias de mortalidad al año entre los pacientes con bloqueo de rama izquierda a los que no se implantó marcapasos y aquellos sin bloqueo de rama izquierda.
El segundo artículo27 analiza los factores que predicen y afectan a la necesidad de implante de marcapasos después de implante transcatéter de válvula aórtica con la prótesis CoreValve, utilizando un nuevo sistema de liberación que teóricamente origina menor trauma en el tracto de salida del ventrículo izquierdo (VI), con lo que habría menos probabilidad de alteraciones de la conducción auriculoventricular.
Estimulación selectiva de ventrículo derechoSe ha publicado un metaanálisis que realiza una revisión sistemática de los estudios aleatorizados que comparan los beneficios de la estimulación no apexiana con respecto a la apexiana28; concluye que, si bien los pacientes con estimulación no apexiana tenían una fracción de eyección del ventrículo izquierdo mayor que los pacientes con estimulación apexiana, no había diferencias en la capacidad de ejercicio, la clase funcional, la calidad de vida ni la supervivencia.
También es destacable un artículo de revisión de Hillock y Mond29 en el que se analizan todos los aspectos de la estimulación del septo del ventrículo derecho (VD).
Estimulación cardiaca y fibrilación auricularEl estudio EPASS30 tuvo como objetivo principal analizar la prevención de FA en pacientes con enfermedad del nodo sinusal estimulados desde la orejuela derecha o desde el septo interauricular bajo. Concluye que, en el subgrupo de pacientes con enfermedad del nodo sinusal y retraso de la conducción intraauricular, la estimulación desde el septo interauricular bajo es superior para prevenir la progresión a FA.
El estudio multicéntrico ASSERT31 ha analizado la presencia de FA subclínica y el riesgo embólico en 2.580 pacientes portadores de marcapasos o DAI sin antecedentes conocidos de FA. Se detectó FA asintomática en un 10% de los pacientes a los 3 meses de seguimiento, tasa que se elevó hasta un 24% a los 2,5 años de seguimiento. Los pacientes en los que se detectaron arritmias auriculares subclínicas tuvieron mayor incidencia de FA clínica y de ictus o embolia periférica en un seguimiento medio de 2,5 años.
Brignole et al32 han realizado un estudio aleatorizado en el que se analizó la respuesta clínica a la ablación de la conducción auriculoventricular e implantación de marcapasos en pacientes con FA rápida, sintomática y refractaria a medicamentos, comparando la estimulación en VD frente a la terapia de resincronización cardiaca (TRC). Se definió como variable de resultado principal la combinación de muerte, hospitalización por IC y empeoramiento de esta. La tasa de respondedores, definida como ausencia de estos tres eventos, fue del 63% en el grupo de estimulación de VD frente a un 83% en el grupo con TRC32, a costa de una disminución en la hospitalización por IC y el empeoramiento de esta, sin que se observaran diferencias en la mortalidad. El modo de estimulación TRC y la optimización de TRC con ecocardiograma fueron los únicos indicadores de beneficio clínico33.
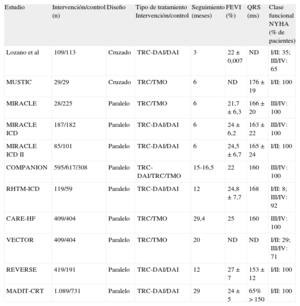
Terapia de resincronización cardiacaSelección de candidatosCada vez es mayor la utilización de los sistemas de TRC para el tratamiento de la IC34. Tres metaanálisis han evaluado la respuesta de distintos grupos de pacientes a la TRC. Wells et al35 analizaron 12 estudios aleatorizados (tabla 1) en los que se estudió la utilidad de agregar TRC al tratamiento farmacológico óptimo o al DAI. Concluyeron que, en pacientes con IC, el implante de un dispositivo de TRC combinado con tratamiento óptimo o DAI reduce la mortalidad y que este beneficio es particularmente evidente en pacientes con síntomas moderados (clase funcional II de la New York Heart Association).
Estudios referidos en el metaanálisis de Wells et al35
| Estudio | Intervención/control (n) | Diseño | Tipo de tratamiento Intervención/control | Seguimiento (meses) | FEVI (%) | QRS (ms) | Clase funcional NYHA (% de pacientes) |
| Lozano et al | 109/113 | Cruzado | TRC-DAI/DAI | 3 | 22 ± 0,007 | ND | I/II: 35; III/IV: 65 |
| MUSTIC | 29/29 | Cruzado | TRC/TMO | 6 | ND | 176 ± 19 | I/II: 100 |
| MIRACLE | 28/225 | Paralelo | TRC/TMO | 6 | 21,7 ± 6,3 | 166 ± 20 | III/IV: 100 |
| MIRACLE ICD | 187/182 | Paralelo | TRC-DAI/DAI | 6 | 24 ± 6,2 | 163 ± 22 | III/IV: 100 |
| MIRACLE ICD II | 85/101 | Paralelo | TRC-DAI/DAI | 6 | 24,5 ± 6,7 | 165 ± 24 | I/II: 100 |
| COMPANION | 595/617/308 | Paralelo | TRC-DAI/TRC/TMO | 15-16,5 | 22 | 160 | III/IV: 100 |
| RHTM-ICD | 119/59 | Paralelo | TRC-DAI/DAI | 12 | 24,8 ± 7,7 | 168 | I/II: 8; III/IV: 92 |
| CARE-HF | 409/404 | Paralelo | TRC/TMO | 29,4 | 25 | 160 | III/IV: 100 |
| VECTOR | 409/404 | Paralelo | TRC/TMO | 20 | ND | ND | I/II: 29; III/IV: 71 |
| REVERSE | 419/191 | Paralelo | TRC-DAI/DAI | 12 | 27 ± 7 | 153 ± 12 | I/II: 100 |
| MADIT-CRT | 1.089/731 | Paralelo | TRC-DAI/DAI | 29 | 24 ± 5 | 65% > 150 | I/II: 100 |
DAI: desfibrilador automático implantable; FEVI: fracción de eyección del ventrículo izquierdo; ND: no documentado; NYHA: New York Heart Association; TMO: tratamiento médico óptimo; TRC: terapia de resincronización cardiaca.
Salvo otra indicación, los datos expresan media ± desviación estándar.
Los resultados del metaanálisis realizado por Al-Majed et al36 abundan en el hallazgo de que la TRC es beneficiosa en pacientes con disfunción ventricular y QRS ancho, independientemente de la intensidad de los síntomas.
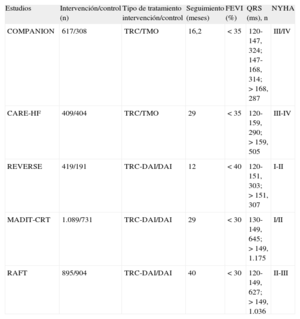
En el tercer metaanálisis, Sipahi et al37 analizaron cinco estudios (tabla 2) con la finalidad de determinar la importancia de la anchura del QRS como predictor de la utilidad de la TRC y concluyeron que la resincronización reducía la incidencia de eventos clínicos adversos en pacientes con IC y QRS ≥ 150 ms.
Estudios referidos en el metaanálisis de Sipahi et al37
| Estudios | Intervención/control (n) | Tipo de tratamiento intervención/control | Seguimiento (meses) | FEVI (%) | QRS (ms), n | NYHA |
| COMPANION | 617/308 | TRC/TMO | 16,2 | < 35 | 120-147, 324; 147-168, 314; > 168, 287 | III/IV |
| CARE-HF | 409/404 | TRC/TMO | 29 | < 35 | 120-159, 290; > 159, 505 | III-IV |
| REVERSE | 419/191 | TRC-DAI/DAI | 12 | < 40 | 120-151, 303; > 151, 307 | I-II |
| MADIT-CRT | 1.089/731 | TRC-DAI/DAI | 29 | < 30 | 130-149, 645; > 149, 1.175 | I/II |
| RAFT | 895/904 | TRC-DAI/DAI | 40 | < 30 | 120-149, 627; > 149, 1.036 | II-III |
DAI: desfibrilador automático implantable; FEVI: fracción de eyección del ventrículo izquierdo; NYHA: New York Heart Association; TMO: tratamiento médico óptimo; TRC: terapia de resincronización cardiaca.
Basándose en estos estudios, la Heart Failure Society of America ha elaborado una actualización de las guías38, cuya conclusión final se resume en que la evidencia científica actual sustenta la utilidad de la TRC en pacientes con disfunción ventricular izquierda con síntomas desde leves a graves. Esta evidencia se hace «convincente» en pacientes con QRS ≥ 150 ms si no tienen bloqueo de rama derecha.
Estimulación sólo del ventrículo izquierdoThibault et al39 publican un estudio multicéntrico, a doble ciego y cruzado en el que comparan los efectos de la estimulación sólo de VI frente a la biventricular en cuanto a tolerancia al ejercicio y remodelado del VI. El estudio incluyó a 211 pacientes con fracción de eyección del ventrículo izquierdo ≤ 35%, QRS ≥ 120 ms y síntomas de IC. Los resultados concluyen que la estimulación sólo de VI no es mejor que la estimulación biventricular; sin embargo, los pacientes no respondedores a la estimulación biventricular podrían responder a la estimulación del VI, de forma que para los pacientes no respondedores a la estimulación biventricular se podría valorar la respuesta a la estimulación sólo de VI.
Seguimiento a distancia en estimulación cardiacaLos sistemas de monitorización domiciliaria (MD) dirigidos a pacientes portadores de dispositivos de estimulación cardiaca están experimentando una serie de cambios estructurales que los convierten en punto de atención para los profesionales de la arritmología. No obstante, la implantación de esta estrategia asistencial sigue teniendo una aceptación muy variable en España, por lo que nos parece de interés incluir las novedades en este campo con el ánimo de impulsar su uso en todas las unidades especializadas.
Contamos actualmente con un número creciente de estudios que han mostrado que la MD es fiable y segura y que está bien aceptada por los pacientes y los profesionales40,41. Asimismo, el estudio ALTITUDE42, un estudio no aleatorizado en el que se incluyó a 194.006 pacientes con un seguimiento de 5 años, observó una mejora en la supervivencia de los pacientes sometidos a MD frente al seguimiento presencial convencional.
En 2012 se han publicado varios estudios aleatorizados que muestran que el uso de los sistemas de MD reduce visitas a los servicios de urgencias43, las visitas presenciales en las unidades de seguimiento de dispositivos43–45 y el tiempo transcurrido entre la aparición de eventos clínicos y su solución44. Asimismo se ha publicado al respecto un documento de consenso46 en el que se resume el estado actual de esta tecnología, hacia dónde se dirige y qué aspectos quedan por responder.
Por último, destacamos que la implementación de la MD llega acompañada del desarrollo de un grupo de herramientas electrónicas que facilitan la compilación y homogeneización de la información de las revisiones presenciales y a distancia de manera automática, independientemente del fabricante, lo que facilita su uso para controles de calidad e investigación clínica y su inclusión automática en la historia clínica electrónica. Actualmente hay algunas iniciativas de ámbito nacional para constituir bancos de datos multicéntricos que han superado todas las expectativas en inclusión de pacientes y propuestas de estudios clínicos.
Interferencias electromagnéticas y resonancia magnéticaEn 2012 se ha publicado, en dos artículos consecutivos47,48, una revisión pormenorizada y actualizada acerca de las interferencias electromagnéticas en los dispositivos de estimulación y desfibrilación dentro y fuera del ambiente médico.
Nazarian et al49, con un estudio prospectivo de excelente diseño, concluyen que, con las precauciones adecuadas, los pacientes con marcapasos y DAI pueden realizarse una resonancia magnética con muy bajo riesgo.
Actualmente ya hay disponibles y aprobados para su uso clínico marcapasos compatibles para resonancia magnética. Destacarse, sin embargo, que el uso de estos dispositivos sigue estando sometido a la necesidad de ajuste y controles antes, durante y después de la realización de la resonancia, por lo que es importante conocer en qué condiciones se debe usarlos50.
GENÉTICA DE LA MUERTE SÚBITAEl dato más relevante en 2012 es la confirmación de la titina como gen asociado a miocardiopatías, tanto dilatada51 como hipertrófica51 o arritmogénica de VD52. TTN, el gen que codifica la titina, está poco estudiado debido al tamaño de su parte codificante (es la mayor proteína humana). Su asociación con la miocardiopatía dilatada se describió en 200253. Sin embargo, no se han realizado estudios de prevalencia de mutaciones de este gen en las miocardiopatías.
En 2011 se analizó a 27 familias con displasia arritmogénica de VD y se encontraron mutaciones en TTN en 7 familias, con segregación clara de la mutación entre los afectados de alguna familia52. Ese estudio confirmó la asociación entre las proteínas sarcoméricas y la displasia, lo que crea un nuevo solapamiento en el genotipo y el fenotipo de las miocardiopatías. Gracias al desarrollo de tecnología de ultrasecuenciación, en un estudio reciente51 se analizó a 312 pacientes con miocardiopatía dilatada y 231 con hipertrófica. Se identificó una prevalencia de mutaciones causantes de TTN truncado en el 25% de los pacientes con miocardiopatía dilatada y en el 18% de los pacientes con una forma esporádica de la enfermedad. La prevalencia de mutaciones en la miocardiopatía hipertrófica fue de un 1%.
Esos dos estudios confirman la asociación de la mayor proteína humana con las miocardiopatías. Los estudios genéticos empiezan a incorporar la tecnología de ultrasecuenciación, tecnología muy potente que permite el análisis de centenares de genes a la vez. Esta tecnología permitirá avanzar rápidamente en la investigación y el diagnóstico genético. Pero la cantidad de datos obtenidos sin duda añade complejidad a los estudios genéticos y ahonda en la necesidad de incorporar estudios genéticos de calidad con una valoración clínica altamente especializada.
CONFLICTO DE INTERESESNinguno.