Se describe el infrecuente caso de un paciente con síndrome coronario agudo (SCA) secundaria a embolia séptica en el contexto de endocarditis infecciosa (EI) en una prótesis mitral. Hasta el momento, la bibliografía indica mayor frecuencia de esta afección en la válvula aórtica. Se realiza una revisión de la enfermedad y el tratamiento considerado más adecuado actualmente.
Varón de 69 años de edad, desde 2005portador de prótesis mecánica en posición mitral St. Jude N.o 29 por EI en contexto de fiebre Q, que acudió a urgencias por un evento sincopal. A su llegada, en el electrocardiograma se observó bloqueo auriculoventricular completo con ritmo de escape nodular a 44 lpm y con la razón internacional normalizada (INR) en rango terapéutico. En las siguientes horas, en la sala de observación sufrió angina típica y el electrocardiograma mostró supradesnivel de 2 mm en ST en la cara anterior (V2-V4). Se activó el código infarto. A su llegada a la sala de hemodinámica presentaba fibrilación ventricular; se realizó cardioversión eléctrica inmediata, con recuperación del ritmo previo, tipo bloqueo auriculoventricular completo, y se implantó un marcapasos transitorio.
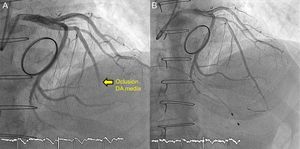
La coronariografía urgente mostró oclusión aguda de la descendente anterior media sin relleno del lecho distal (figura 1A y vídeo 1 del material suplementario). Por sospecha de origen embólico, se realizaron múltiples trombectomías con dispositivos de tromboaspiración Xport y Capturer, con las que se extrajo abundante material trombótico de aspecto blanquecino, sin placa ateroesclerótica subyacente (figura 1B y vídeo 2 del material suplementario). Se restableció flujo Thrombolysis In Myocardial Infarction (TIMI) 3 en la descendente anterior media y distal, aunque con embolización muy apical que persistió a pesar de la angioplastia coronaria transluminal percutánea con balón a bajas atmósferas y la administración de abciximab a dicho nivel.
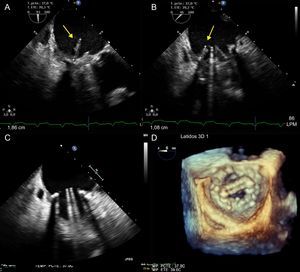
A las 48 h, presentó picos febriles con hemocultivos positivos a Enterococcus faecalis, y se inició tratamiento antibiótico dirigido con ceftriaxona y ampicilina. Se realizó ecocardiografía transesofágica, que mostró múltiples imágenes compatibles con vegetaciones en la prótesis mitral, por lo que se generó disfunción protésica de tipo estenótico (figuras 2A-B y vídeos 3 y 4 del material suplementario); la válvula aórtica nativa no mostraba EI. Tras estos hallazgos, se intervino quirúrgicamente de urgencia, y se confirmó el diagnóstico de EI con absceso anular. Se implantó una prótesis mitral mecánica St. Jude N.o 27. En el posoperatorio inmediato se recuperó el ritmo sinusal. La evolución posterior fue buena y se complentaron 6 semanas de tratamiento antibiótico. Los hemocultivos posteriores fueron negativos y el control ecocardiográfico no mostró imágenes compatibles con EI (figuras 2C-D).
El SCA es una complicación precoz e infrecuente de la EI1,2. Su incidencia es difícil de calcular; en la serie de Manzano et al.1, de 586 pacientes con EI, 14 (2,9%) presentaron SCA como complicación, con afección más frecuente de la válvula aórtica, generalmente en prótesis valvulares1. El SCA se presenta agudo, en la primera semana en la mayoría de los pacientes, y se asocia más a infección valvular aórtica, insuficiencia valvular grave, complicaciones perianulares de gran tamaño y gran mortalidad1. No se ha relacionado un microorganismo específico, aunque se asocia en gran porcentaje a patógenos virulentos como Staphylococcus aureus1.
En su mayoría, el territorio dañado es el anterior o el anterolateral1, mientras que es escasa la presentación de casos con elevación del segmento ST. La compresión extrínseca de las arterias coronarias secundaria a complicaciones perianulares de gran tamaño (seudoaneurismas y abscesos) es la causa más frecuente, seguida de la embolia coronaria séptica1,2. Otros mecanismos indicados son la isquemia precipitada por estado inflamatorio sistémico, con incremento de la demanda miocárdica de oxígeno en el síndrome febril, anemia y/o sepsis, así como la insuficiencia aórtica grave que genera isquemia miocárdica debido a reducción de la presión de perfusión y la reserva coronaria1,2.
Respecto al tratamiento, no se recomienda la terapia fibrinolítica si se sospecha esta complicación, pues tiene relación con mayores incidencia de hemorragia cerebral y mortalidad3,4. Se piensa que se debe a la alta prevalencia de infartos cerebrales silentes y aneurismas micóticos por embolias sépticas, junto con el riesgo de hemorragia que conlleva la bacteriemia4. Se ha demostrado que la cirugía temprana reduce significativamente los eventos embólicos5. Manzano et al.1 proponen como estrategia terapéutica remitir a cirugía sin coronariografía previa a los pacientes con SCA sin elevación del ST por EI aórtica y complicaciones perianulares, previa realización de ecocardiografía transesofágica1. En caso de SCA con elevación del ST y/o ausencia de complicación perianular, proponen realizar coronariografía y, si hay oclusión coronaria, optar por angioplastia con balón e implante de stent si se considera necesario1, con coronariografía de control a los 10-15 días por el riesgo de aneurisma micótico coronario tras el stent1.
Sin embargo, otros autores4 y nuestro grupo consideran que el riesgo que conlleva la estrategia del implante de stent1,6 en un contexto de bacteriemia y ausencia de placa ateroesclerótica posiciona el beneficio de la tromboaspiración como estrategia inicial para estos pacientes, y única, si es eficaz. Con la ventaja añadida de la monoterapia antiplaquetaria, que evita el riesgo de hemorragia cuando se compara con la doble antiagregación necesaria tras el stent. Finalmente, para los pacientes con complicaciones perianulares y sin elevación del segmento ST, la tomografía computarizada coronaria podría ser la alternativa de elección en el estudio de la anatomía coronaria previo a la intervención quirúrgica.