La crioablación con balón (CB) supuso en 2012 el 19% del total de ablaciones de fibrilación auricular (FA) en nuestro medio1. Se dispone de escasa información sobre la evolución a largo plazo tras CB, y ninguna de cuando esta se realiza en centros con bajo volumen2. Este es un dato importante, ya que cerca del 80% de nuestras unidades de electrofisiología realizan menos de 50 ablaciones de FA anuales1.
Analizamos prospectivamente los resultados de la CB como técnica de elección en un centro de bajo volumen. Desde noviembre de 2010 hasta junio de 2013, se incluyó a 63 pacientes (12 mujeres; media de edad, 55±10 años); 48 de ellos (76%) presentaban FA paroxística recurrente y 15, persistente de corta duración (< 6 meses). El diámetro de la aurícula izquierda era de 41±4mm, y 9 pacientes (14%) presentaban cardiopatía estructural; 11 pacientes (18%) puntuaban ≥ 2 en la escala CHA2DS2–VASc.
Antes de la CB, se administraron anticoagulantes orales durante al menos 1 mes. Tras la ablación, se mantuvo la anticoagulación 1 mes y el tratamiento antiarrítmico, 3 meses (6 meses en casos de FA persistente). Tras el primer mes se mantuvo la anticoagulación según escala CHA2DS2–VASc.
La CB se realizó inicialmente mediante doble punción transeptal, que pasó a punción simple tras la aparición del catéter circular intraluminal. Los últimos 19 casos se realizaron con el criobalón Advance® (Medtronic Inc.), con el que se consigue una aplicación más homogénea en toda la circunferencia de la desembocadura de la vena pulmonar. Se realizaba un mínimo de dos aplicaciones por vena, con estimulación frénica continua durante la ablación de venas pulmonares derechas para monitorizar la aparición de parálisis frénica.
Los tiempos de procedimiento y escopia fueron 168±22 y 30±12min, y disminuyeron significativamente a partir de los primeros 30 casos (antes frente a después, 189±18 frente a 147±34min y 35±7 frente a 23±5min; p<0,001). Se consiguió aislamiento eléctrico de 224 de las 231 venas pulmonares identificadas (97%). La inferior derecha es la que más frecuentemente quedó sin aislar (4 casos), siempre por documentación previa de parálisis frénica durante la aplicación en la vena pulmonar superior derecha. Seis pacientes presentaban vestíbulo común (4 izquierdo, 2 derecho).
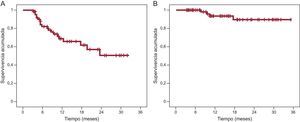
Durante un seguimiento de 12±8 meses, se registraron recurrencias de FA en 20 pacientes (32%), con una tasa de mantenimiento de ritmo sinusal tras 1 y 2 años del 69 y el 51% respectivamente. Usando fármacos antiarrítmicos, esas tasas aumentaron al 94 y el 86% (figura). En 5 pacientes persistieron episodios arrítmicos sintomáticos, y se documentó FA en 3 y aleteo auricular izquierdo en 2. A todos se les realizó nueva ablación, en esta ocasión con radiofrecuencia.
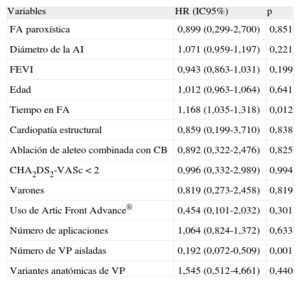
En el análisis multivariable, la única variable independiente predictora de recurrencia de FA tras CB fue el tiempo en FA previo al procedimiento (hazard ratio [HR]=1,17; intervalo de confianza del 95% [IC95%], 1,035-1,32; p=0,012). El número de venas pulmonares aisladas fue factor protector (HR=0,19; IC95%, 0,072-0,509; p=0,001) (tabla). De los 4 pacientes a los que no se aplicó en vena pulmonar inferior derecha, 2 recidivaron.
Predictores de recurrencia arrítmica tras crioablación con balón de fibrilación auricular
| Variables | HR (IC95%) | p |
| FA paroxística | 0,899 (0,299-2,700) | 0,851 |
| Diámetro de la AI | 1,071 (0,959-1,197) | 0,221 |
| FEVI | 0,943 (0,863-1,031) | 0,199 |
| Edad | 1,012 (0,963-1,064) | 0,641 |
| Tiempo en FA | 1,168 (1,035-1,318) | 0,012 |
| Cardiopatía estructural | 0,859 (0,199-3,710) | 0,838 |
| Ablación de aleteo combinada con CB | 0,892 (0,322-2,476) | 0,825 |
| CHA2DS2-VASc < 2 | 0,996 (0,332-2,989) | 0,994 |
| Varones | 0,819 (0,273-2,458) | 0,819 |
| Uso de Artic Front Advance® | 0,454 (0,101-2,032) | 0,301 |
| Número de aplicaciones | 1,064 (0,824-1,372) | 0,633 |
| Número de VP aisladas | 0,192 (0,072-0,509) | 0,001 |
| Variantes anatómicas de VP | 1,545 (0,512-4,661) | 0,440 |
AI: aurícula izquierda; CB: crioablación con balón; FA: fibrilación auricular; IC95%: intervalo de confianza del 95%; HR: hazard ratio;VI: ventrículo izquierdo; VP: venas pulmonares.
Se considera estadísticamente significativo un valor de p < 0,05.
Se recogió un total de 12 complicaciones (19%), fundamentalmente parálisis frénica derecha durante aplicación en venas pulmonares derechas (7 casos, 11%), que fue siempre transitoria, aunque de resolución tardía en dos ocasiones (9 y 12 meses). Tras revisión de los tiempos de aplicación (240–180 s) y temperatura (limitada a −55°C), no se registraron parálisis frénicas en las últimas 28 ablaciones, sin sacrificar por ello la eficacia del procedimiento (p=0,01). Además, se registraron un accidente isquémico transitorio por embolia gaseosa, un ictus talámico asintomático y dos episodios de hemoptisis menor. Finalmente hubo un caso de fístula auriculoesofágica atribuida a la aplicación en vena pulmonar inferior izquierda, que resultó en fallecimiento al mes del procedimiento, realizado con el nuevo criobalón.
La CB como tratamiento de elección para la FA paroxística recurrente o persistente de corta duración en centros de bajo volumen se acompaña de una probable corta curva de aprendizaje de la técnica, como se infiere de la alta eficacia aguda inicial y la rápida reducción en los tiempos de escopia y procedimiento (p<0,001) en nuestra serie. Las tasas de mantenimiento de ritmo sinusal con y sin fármacos antiarrítmicos y la incidencia de parálisis frénica y complicaciones graves (3 de 63 casos, 4,8%) parecen comparables con las de otras series con mayor número de pacientes3–5. Si bien el índice de complicaciones parece exagerado, se produjo fundamentalmente a expensas de la parálisis frénica transitoria, complicación que además se obvió al limitar los tiempos de aplicación y temperatura mínima alcanzada (p=0,01). Debemos destacar, sin embargo, que la modificación de los parámetros de ablación y el escaso número de pacientes incluidos impiden establecer con precisión la duración de la mencionada curva de aprendizaje, sobre todo en lo referente a la incidencia de complicaciones graves.