La insuficiencia mitral (IM) es una de las principales enfermedades valvulares. La reparación quirúrgica de la válvula mitral (VM) es la norma en el cuidado de los pacientes con una IM degenerativa debida a prolapso o inestabilidad de un velo de la válvula. La reparación quirúrgica de la VM se realiza combinando la anuloplastia con anillo con la reparación cordal y de los velos según sea necesario.
Con el creciente desarrollo de los tratamientos percutáneos en el campo de las valvulopatías, han aparecido técnicas como la reparación de la VM con dispositivo NeoChord y guiada mediante ecocardiografía (NeoChord Inc.; St. Louis Park, Minnesota, Estados Unidos), que ha mostrado unos primeros resultados de seguridad y eficacia buenos en un grupo seleccionado de pacientes con prolapso/inestabilidad posterior de la VM, sin requerir anuloplastia complementaria1.
Análisis recientes han proporcionado más conocimiento relacionado con la selección de pacientes para llevar a cabo la intervención con dispositivo NeoChord, que han puesto de relieve la existencia de criterios morfológicos y ecocardiográficos precisos1,2. En particular, la relación entre los velos y el área de superficie anular (leaflet-to annulus index [LAI]), que describe con exactitud a los pacientes sin desajuste entre los velos y el anillo que, por lo tanto, podrían beneficiarse de un tratamiento solo de los velos, sin anuloplastia concomitante.
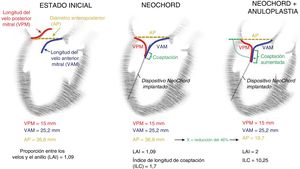
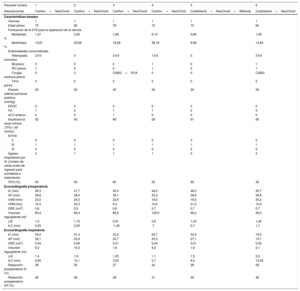
El LAI se define como la relación entre la suma de la longitud del velo anterior mitral (VAM) y la longitud del velo posterior mitral (VPM) con respecto al diámetro anteroposterior (AP) del anillo de la VM (LAI = VAM+VPM / AP). El LAI actuó como predictor posoperatorio positivo de la IM al menos leve al cabo de 1 año de seguimiento una vez que fue > 1,22.
Además, más recientemente se ha introducido el índice estimado de longitud de coaptación (LC) como una herramienta adicional para calcular la posible LC postoperatoria de los velos3. El índice LC se determina de acuerdo con la siguiente fórmula: [(VAM+VPM) – AP] / 2]. La LC postoperatoria es un factor que predice la durabilidad de la reparación de la VM cuando es > 6 mm4.
A partir de estas suposiciones, se propuso utilizar la combinación de las fórmulas de los índices LAI y LC validados para discriminar entre pacientes que se benefician únicamente de un procedimiento con dispositivo NeoCord sin anillo, porque la LC predicha final será suficiente para obtener un resultado efectivo y duradero, y aquellos que requieren un tratamiento anular complementario para reducir el diámetro AP, lo que resulta en una mejora de la LC (figura 1).
Representación esquemática de un paciente tratado, en la que puede verse el corazón en una proyección ecocardiográfica de eje largo, después del tratamiento solo de los velos con implante NeoChord y tras la combinación de NeoChord y procedimientos de anuloplastia directa. AP: diámetro anteroposterior; ILC: índice de longitud de coaptación; LAI: proporción entre los velos y el anillo o leaflet-to-annulus index; VAM: longitud de la valva anterior mitral; VPM: válvula posterior mitral.
Los procedimientos de anuloplastia percutánea también se han demostrado seguros y efectivos a la hora de reducir el diámetro AP del anillo. La anuloplastia percutánea puede realizarse con dispositivos que actúan directamente o indirecta en el anillo de la VM.
Se recomienda la anuloplastia indirecta a través del seno coronario (Carillon Mitral contour system, Cardiac Dimensions; Kirkland, Estados Unidos) cuando la tomografía computarizada preoperatoria muestra una alineación correcta y continuidad cerrada entre el seno coronario y el anillo de la VM.
La anuloplastia directa puede realizarse con el sistema Cardioband (Edwards Lifesciences; Irvine, California, Estados Unidos). Es recomendable que no haya calcificaciones anulares y proximidad de la arteria circunfleja. Ambos dispositivos permiten conseguir una reducción del diámetro AP del 20 al 45%5.
Seis pacientes considerados no aptos para la reparación convencional de la VM, dadas sus características específicas según el equipo cardiológico local (tabla 1), se sometieron a tratamientos percutáneos anular y de los velos en un procedimiento único. Todos padecían una afección degenerativa de la VM en una fase avanzada, con inestabilidad de la valva y dilatación anular concomitantes. Todos se sometieron al tratamiento de los velos con implante NeoChord, con un número medio de 3 cuerdas, y una intervención de anuloplastia concomitante en la que se implantó el dispositivo Cardioband en 2 pacientes (vídeo 1 del material adicional; ecocardiograma transesofágico que muestra el estado inicial, el implante del Cardioband seguido del implante del dispositivo NeoChord con estrangulación máxima del dispositivo de anuloplastia) y el dispositivo Carillon a 4 pacientes (vídeo 2 del material adicional; ecocardiograma transesofágico que muestra el estado inicial, el implante del dispositivo Carillon seguido del implante del dispositivo NeoChord). Al único paciente al que se implantó un dispositivo NeoChord además de un dispositivo Cardioband, también se le implantó un MitraClip comisural (Abbott; Menlo Park, Colorado, Estados Unidos) al final de la intervención para tratar la IM residual leve causada por un prolapso comisural, como resultado final quedó una IM ligera. La decisión para seleccionar el dispositivo de anuloplastia se adaptó en función de la integración de los datos anatómicos y ecocardiográficos del paciente (medidas del anillo y los velos de la VM, presencia/ausencia de calcificaciones anulares, localización de los senos coronarios y arteria circunfleja).
Características preoperatorias y posoperatorias de los pacientes tratados con procedimientos combinados de reparación de la válvula mitral
| Paciente número | 1 | 2 | 3 | 4 | 5 | 6 |
|---|---|---|---|---|---|---|
| Intervenciones | Carillon+NeoChord | Carillon+NeoChord | Carillon+NeoChord | Carillon+NeoChord | Cardioband+NeoChord+Mitraclip | Cardioband+NeoChord |
| Características basales | ||||||
| Varones | 1 | 1 | 1 | 1 | 1 | 1 |
| Edad (años) | 75 | 82 | 78 | 73 | 70 | 60 |
| Puntuación de la STS para la reparación de la válvula | ||||||
| Mortalidad, % | 1,27 | 2,65 | 1,86 | 6,10 | 0,80 | 1,59 |
| Morbilidad, % | 13,81 | 20,68 | 18,28 | 38,19 | 9,99 | 14,83 |
| Enfermedades concomitantes | ||||||
| Arteriopatía coronaria | 2 EV | 0 | 3 EV | 1 EV | 0 | 3 EV |
| IM previo | 0 | 0 | 0 | 1 | 0 | 1 |
| IPC previa | 1 | 0 | 0 | 1 | 0 | 1 |
| Cirugía cardiaca previa | 0 | 0 | CABG+RVA | 0 | 0 | CABG |
| TAVI previo | 0 | 0 | 0 | 0 | 0 | 0 |
| Presión arterial pulmonar sistólica (mmHg) | 45 | 50 | 40 | 30 | 30 | 50 |
| EPOC | 0 | 0 | 0 | 0 | 0 | 0 |
| FA | 1 | 0 | 1 | 1 | 0 | 0 |
| ACV anterior | 0 | 0 | 1 | 0 | 0 | 0 |
| Insuficiencia renal crónica (TFG < 60 ml/min) | 52 | 50 | 66 | 28 | 61 | 95 |
| NYHA | ||||||
| II | 0 | 0 | 0 | 0 | 0 | 0 |
| III | 1 | 1 | 1 | 1 | 1 | 1 |
| IV | 0 | 0 | 0 | 0 | 0 | 0 |
| Ingreso hospitalario por IC (número de veces antes de ingresar para someterse a tratamiento) | 0 | 1 | 1 | 1 | 0 | 2 |
| FEVI (%) | 50 | 50 | 60 | 20 | 65 | 30 |
| Ecocardiografía preoperatoria | ||||||
| IC (mm) | 48,3 | 41,7 | 45,4 | 44,0 | 48,0 | 45,7 |
| AP (mm) | 38,8 | 38,4 | 35,1 | 35,3 | 38,6 | 36,8 |
| VAM (mm) | 23,0 | 24,0 | 22,9 | 18,0 | 19,0 | 25,2 |
| VPM (mm) | 16,3 | 20,3 | 9,3 | 10,0 | 21,0 | 15,0 |
| ORE (cm2) | 0,6 | 0,5 | 0,6 | 0,7 | 0,7 | 0,7 |
| Volumen regurgitante (ml) | 85,4 | 69,4 | 88,5 | 125,0 | 88,2 | 58,0 |
| LAI | 1,0 | 1,15 | 0,91 | 0,8 | 1,03 | 1,09 |
| ILC (mm) | 0,25 | 2,95 | -1,45 | -7 | 0,7 | 1,7 |
| Ecocardiografía respiratoria | ||||||
| IC (mm) | 30,9 | 31,3 | 33,2 | 25,7 | 34,3 | 19,3 |
| AP (mm) | 28,1 | 23,9 | 25,7 | 25,3 | 27,1 | 19,7 |
| ORE (cm2) | 0,04 | 0,08 | 0,01 | 0,04 | 0,01 | 0,02 |
| Volumen regurgitante (ml) | 6,3 | 10,3 | 1,6 | 8,3 | 1,6 | 2,1 |
| LAI | 1,4 | 1,8 | 1,25 | 1,1 | 1,5 | 2,0 |
| ILC (mm) | 5,65 | 10,1 | 3,25 | 2,7 | 6,5 | 10,25 |
| Reducción posoperatoria IC (%) | 36 | 25 | 27 | 42 | 28 | 58 |
| Reducción posoperatoria AP (%) | 28 | 38 | 28 | 31 | 30 | 46 |
ACV: accidente cerebrovascular; AP: diámetro anteroposterior anillo mitral; CABG: cirugía de revascularización aortocoronaria; DIC: diámetro intercomisural; EPOC: enfermedad pulmonar obstructiva crónica; EV: enfermedad de los vasos; FA: fibrilación auricular; FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; ILC: índice de longitud de coaptación; IM: infarto de miocardio; IPC: intervención percutánea coronaria; LAI: leaflet-to-annulus index; NYHA: New York Heart Association; ORE: orificio regurgitante efectivo; RVA: reemplazo de válvula aórtica; TAVI: implante percutáneo de válvula aórtica; TFG: tasa de filtrado glomerular; VAM: longitud de la valva anterior mitral; VPM: longitud de la valva posterior mitral.
A todos los pacientes se les implantó primero el dispositivo de anuloplastia, tras lo cual se observó una reducción inmediata de la IM, aunque con inestabilidad persistente del velo que requirió tratamiento adicional para reducir su altura y generar una coaptación estable. Todas las intervenciones fueron satisfactorias, con una IM residual mínima (tabla 1). Todos los pacientes mostraron una reducción AP ecocardiográficamente efectiva, con el consiguiente aumento posoperatorio de los índices LAI y CL. Tras un seguimiento de 30 días, todos presentaban una IM residual menor que leve y una clase funcional I de la New York Heart Association.
Este artículo describe la experiencia clínica inicial de la aplicación de un nuevo abordaje percutáneo combinado en un procedimiento único para tratar a los pacientes con una enfermedad degenerativa de la VM en estado avanzado con la combinación de tratamientos percutáneos anulares y de los velos. Esta reparación percutánea de tipo quirúrgico de la VM fue segura, viable y efectiva a la hora de tratar a un subgrupo específico de pacientes seleccionados. Es importante resaltar que el algoritmo de la toma de decisiones se deriva del conocimiento adquirido en el campo de la reparación quirúrgica de la VM a lo largo de los últimos 50 años de práctica tras demostrarse que aquellos conceptos han proporcionado resultados excelentes. El concepto actual de caja de herramientas con dispositivos percutáneos de VM para tratar los velos y el anillo de la VM representa la evolución contemporánea de una amplia variedad de técnicas quirúrgicas descritas y utilizadas por los cirujanos para realizar la reparación de la VM. Se requieren futuros estudios clínicos para seguir validando este abordaje combinado de tipo quirúrgico de reparación mitral percutánea en un procedimiento único.
CONFLICTO DE INTERESESA. Colli ha recibido subvenciones para desplazamientos de NeoChord, Inc. A. Beiras-Fernandez ha recibido subvenciones para desplazamientos y es proctor de NeoChord, Inc. S. von Bardeleben ha recibido subvenciones para desplazamientos de NeoChord Inc., Edwards Lifesciences, Carillon Contour System y Cardiac Dimensions. Los demás autores no tienen nada que declarar.