Los pacientes con insuficiencia cardiaca en tratamiento con antagonistas de la vitamina K (AVK) por fibrilación auricular no valvular (FANV) a menudo presentan valores alterados de la razón internacional normalizada (INR). El objetivo es evaluar la asociación entre la INR al ingreso por insuficiencia cardiaca y el riesgo de mortalidad en el seguimiento.
MétodosEstudio observacional retrospectivo en el que se evaluó la INR al ingreso de 1.137 pacientes consecutivos con insuficiencia cardiaca aguda en tratamiento con AVK por FANV. Esta se categorizó en: INR en rango óptimo (INR = 2-3, n = 210), infraterapéutica (INR < 2, n = 660) o supraterapéutica (INR > 3, n = 267). La asociación independiente entre INR y mortalidad se evaluó mediante cálculo restringido de las diferencias en tiempos de supervivencia media, dado que la INR no cumple la condición de proporcionalidad de riesgos de mortalidad.
ResultadosTras una mediana de 2,15 [0,71-4,29] años, fallecieron 495 pacientes (43,5%). En el análisis multivariable, tanto la INR infraterapéutica como la supraterapéutica se asociaron con un mayor riesgo de mortalidad, con unas diferencias en tiempos de supervivencia media a 5 años de –0,50 años (IC95%,–0,77 a –0,23; p < 0,001) y –0,40 años (IC95%, –0,70 a –0,11; p = 0,007) con respecto a los pacientes con INR 2-3.
ConclusionesLa INR fuera de rango óptimo al ingreso de los pacientes con insuficiencia cardiaca aguda en tratamiento con AVK por FANV se asocia de manera independiente con un mayor riesgo de mortalidad en el seguimiento a largo plazo.
Palabras clave
La fibrilación auricular y la insuficiencia cardiaca (IC) son 2 entidades estrechamente ligadas desde un punto de vista clínico y fisiopatológico1. La fibrilación auricular es la arritmia más frecuente en pacientes con IC y condiciona un riesgo aumentado de eventos tromboembólicos, una peor clase funcional y un peor pronóstico2. Dado el alto riesgo de ictus o embolia sistémica, la gran mayoría de los pacientes con IC y fibrilación auricular no valvular (FANV) deben recibir anticoagulación oral crónica3. Sin embargo, y pese a la reciente evidencia disponible con los anticoagulantes de acción directa4,5, el tratamiento anticoagulante que recibe gran parte de los pacientes con IC y FANV en nuestro medio son los antagonistas de la vitamina K (AVK). El gran número de interacciones farmacológicas, la disfunción hepática o renal y la mayor labilidad de la razón internacional normalizada (INR) hacen que el control de la anticoagulación oral de los pacientes con IC sea especialmente complejo6,7. Esto se hace todavía más patente durante los episodios de descompensación aguda, ya que a menudo los pacientes con IC presentan una INR fuera del rango terapéutico óptimo8.
Recientemente, se ha descrito una asociación entre la INR y el riesgo de mortalidad en pacientes con IC aguda que no reciben tratamiento anticoagulante9. Algunos mecanismos fisiopatológicos que podrían explicar la importancia de la INR en la IC son la hipoxia tisular, la disfunción hepática o el grado de activación neurohormonal. Sin embargo, el valor pronóstico de la INR en pacientes bajo tratamiento con AVK es desconocido. El objetivo de este estudio fue valorar la asociación entre la INR y el riesgo de mortalidad a largo plazo en pacientes con IC aguda y FANV tratados con AVK.
MÉTODOSGrupo de estudio y protocoloSe incluyó una cohorte consecutiva de 2.604 pacientes hospitalizados con diagnóstico principal de IC aguda en el servicio de cardiología de un hospital universitario de tercer nivel, entre enero de 2004 y diciembre de 2016. La IC aguda se definió de acuerdo con las guías de práctica clínica10. Se incluyó tanto a pacientes con descompensación aguda de una IC crónica como a pacientes con IC de nueva aparición. De los 2.604 pacientes incluidos en el registro, se excluyó del estudio a 1.467 por: a) no tener diagnóstico de fibrilación auricular (n = 1.262); b) diagnóstico de fibrilación auricular valvular según las recomendaciones de la Sociedad Europea de Cardiología3 (n = 157), y c) recibir tratamiento con otros anticoagulantes distintos de los AVK (n = 48), con lo que la muestra final en estudio es de 1.137 pacientes.
Durante la hospitalización índice se recogió un amplio conjunto de variables clínicas, de exploración física, electrocardiográficas, bioquímicas o ecocardiográficas, así como los tratamientos concomitantes recibidos por los pacientes. Este se individualizó a criterio del cardiólogo responsable, de acuerdo con las guías de práctica clínica vigentes a lo largo del estudio.
El estudio cumple los principios establecidos en la Declaración de Helsinki y lo aprobó el comité ético de investigación clínica del centro.
Valor de razón internacional normalizadaEl valor de la INR se obtuvo en el primer contacto médico del paciente con IC aguda en el servicio de urgencias. Se consideró como INR en rango terapéutico óptimo un valor entre 2 y 3. Se categorizó a los pacientes en función del valor de la INR en: a) INR en rango óptimo (2–3); b) INR infraterapéutico (< 2), y c) INR supraterapéutico (> 3).
Seguimiento y adjudicación de eventosSe realizó seguimiento de la supervivencia del paciente tras el alta hospitalaria del episodio índice de IC aguda mediante revisión de la historia clínica electrónica. Los investigadores encargados de la adjudicación de eventos no tuvieron acceso al valor de la INR. El criterio de valoración principal fue la mortalidad por todas las causas durante el seguimiento. Como criterio de valoración secundario, se evaluó la asociación entre la INR y las causas específicas de muerte: a) muerte por causa cardiovascular (CV) o no CV, y b) muerte por IC o no. La muerte CV se definió según el criterio recomendado por la American Heart Association, que incluye las muertes súbita y por IC, infarto agudo de miocardio, ictus, hemorragia vascular o arteriopatía periférica, así como la de etiología desconocida. En los demás casos, se consideró como causa no CV11.
Análisis estadísticoLas variables continuas se expresan como media ± desviación estándar o mediana [intervalo intercuartílico] cuando no seguían una distribución normal. Las variables discretas se representan como porcentajes. Las características basales de los pacientes se compararon entre las categorías de INR mediante test de ANOVA, y se utilizó el test de Kruskall-Wallis para las variables no paramétricas.
Se evaluó la condición de proporcionalidad de riesgos (cPR) en las categorías de INR para todos los criterios de valoración a través de residuos escalados de Schoenfeld y curvas «log-log». En consecuencia, se utilizaron 2 diferentes métodos de análisis según se cumpliera la cPR o no: a) Royston-Parmar survival regression en presencia de la cPR, y b) diferencias en el tiempo de supervivencia media restringido (restricted mean survival time [RMST]) para el caso opuesto12. Las diferencias en el RMST se propusieron como método alternativo a la estimación de la hazard ratio (HR) cuando no se cumplía la cPR y representan la pérdida de expectativa de vida asociada con la variable en estudio12,13. Los criterios de valoración en que la variable INR no cumplía la cPR fueron: mortalidad por todas las causas, de origen CV y por IC; en cambio, sí se cumplía para el análisis de mortalidad no CV y no atribuible a IC. Para el análisis del RMST, el tiempo máximo de seguimiento se limitó a 5 años, y sus resultados se expresan como diferencia en cantidad de años para la anticipación del evento.
Todas las variables incluidas en la tabla 1 se evaluaron con fines pronósticos. Se utilizó una selección escalonada retrógada para la simplificación del modelo multivariable final. Simultáneamente con el proceso de selección, se determinó el polinomial óptimo para las variables continuas con el fin de sustentar el requisito de linealidad con el evento. Para el análisis de causas específicas de mortalidad, se utilizaron curvas de incidencia acumulada y sus diferencias se evaluaron mediante el test de Gray14. En el análisis multivariable de causas específicas de muerte, se utilizó el RMST adaptado para eventos competitivos.
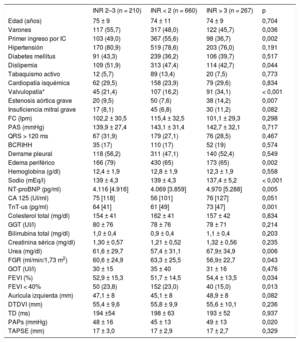
Características basales de los pacientes en función de las categorías de INR
| INR 2–3 (n = 210) | INR < 2 (n = 660) | INR > 3 (n = 267) | p | |
|---|---|---|---|---|
| Edad (años) | 75 ± 9 | 74 ± 11 | 74 ± 9 | 0,704 |
| Varones | 117 (55,7) | 317 (48,0) | 122 (45,7) | 0,036 |
| Primer ingreso por IC | 103 (49,0) | 367 (55,6) | 98 (36,7) | 0,002 |
| Hipertensión | 170 (80,9) | 519 (78,6) | 203 (76,0) | 0,191 |
| Diabetes mellitus | 91 (43,3) | 239 (36,2) | 106 (39,7) | 0,517 |
| Dislipemia | 109 (51,9) | 313 (47,4) | 114 (42,7) | 0,044 |
| Tabaquismo activo | 12 (5,7) | 89 (13,4) | 20 (7,5) | 0,773 |
| Cardiopatía isquémica | 62 (29,5) | 158 (23,9) | 79 (29,6) | 0,834 |
| Valvulopatía* | 45 (21,4) | 107 (16,2) | 91 (34,1) | < 0,001 |
| Estenosis aórtica grave | 20 (9,5) | 50 (7,6) | 38 (14,2) | 0,007 |
| Insuficiencia mitral grave | 17 (8,1) | 45 (6,8) | 30 (11,2) | 0,082 |
| FC (lpm) | 102,2 ± 30,5 | 115,4 ± 32,5 | 101,1 ± 29,3 | 0,298 |
| PAS (mmHg) | 139,9 ± 27,4 | 143,1 ± 31,4 | 142,7 ± 32,1 | 0,717 |
| QRS > 120 ms | 67 (31,9) | 179 (27,1) | 76 (28,5) | 0,467 |
| BCRIHH | 35 (17) | 110 (17) | 52 (19) | 0,574 |
| Derrame pleural | 118 (56,2) | 311 (47,1) | 140 (52,4) | 0,549 |
| Edema periférico | 166 (79) | 430 (65) | 173 (65) | 0,002 |
| Hemoglobina (g/dl) | 12,4 ± 1,9 | 12,8 ± 1,9 | 12,3 ± 1,9 | 0,558 |
| Sodio (mEq/l) | 139 ± 4,3 | 139 ± 4,3 | 137,4 ± 5,2 | < 0,001 |
| NT-proBNP (pg/ml) | 4.116 [4.916] | 4.069 [3.859] | 4.970 [5.288] | 0,005 |
| CA 125 (UI/ml) | 75 [118] | 56 [101] | 76 [127] | 0,051 |
| TnT-us (pg/ml) | 64 [41] | 61 [49] | 73 [47] | 0,001 |
| Colesterol total (mg/dl) | 154 ± 41 | 162 ± 41 | 157 ± 42 | 0,834 |
| GGT (UI/l) | 80 ± 76 | 78 ± 76 | 78 ± 71 | 0,214 |
| Bilirrubina total (mg/dl) | 1,0 ± 0,4 | 0,9 ± 0,4 | 1,1 ± 0,4 | 0,203 |
| Creatinina sérica (mg/dl) | 1,30 ± 0,57 | 1,21 ± 0,52 | 1,32 ± 0,56 | 0,235 |
| Urea (mg/dl) | 61,6 ± 29,7 | 57,4 ± 31,1 | 67,9± 34,9 | 0,006 |
| FGR (ml/min/1,73 m2) | 60,6 ± 24,9 | 63,3 ± 25,5 | 56,9± 22,7 | 0,043 |
| GOT (UI/l) | 30 ± 15 | 35 ± 40 | 31 ± 16 | 0,476 |
| FEVI (%) | 52,9 ± 15,3 | 51,7 ± 14,5 | 54,4 ± 13,5 | 0,034 |
| FEVI < 40% | 50 (23,8) | 152 (23,0) | 40 (15,0) | 0,013 |
| Aurícula izquierda (mm) | 47,1 ± 8 | 45,1 ± 8 | 48,9 ± 8 | 0,082 |
| DTDVI (mm) | 55,4 ± 9,6 | 55,8 ± 9,9 | 55,6 ± 10,1 | 0,236 |
| TD (ms) | 194 ±54 | 198 ± 63 | 193 ± 52 | 0,937 |
| PAPs (mmHg) | 48 ± 16 | 45 ± 13 | 49 ± 13 | 0,020 |
| TAPSE (mm) | 17 ± 3,0 | 17 ± 2,9 | 17 ± 2,7 | 0,329 |
BCRIHH: bloqueo completo de rama izquierda del haz de His; CA 125: antígeno carbohidrato 125; DTDVI: diámetro telediastólico del ventrículo izquierdo; FC: frecuencia cardiaca; FEVI: fracción de eyección del ventrículo izquierdo; FGR: filtrado glomerular renal; GGT: gammaglutamil tranferasa; GOT: glutamano oxalacetato transaminasa; IC: insuficiencia cardiaca; INR: razón internacional normalizada; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; PAPs: presión arterial pulmonar sistólica; PAS: presión arterial sistólica; TAPSE: tricuspid anular plane systolic excursion; TD: tiempo de deceleración; TnT-us: troponina T ultrasensible.
Los valores expresan n (%), media ± desviación estándar o mediana [intervalo intercuartílico].
Un valor de p bilateral < 0,05 se consideró como estadísticamente significativo para todos los análisis. MedStats Consulting (Reading, Pennsylvania, Estados Unidos) realizó el análisis estadístico mediante STATA 15,1 (StataCorp. LP; College Station, Texas, Estados Unidos).
RESULTADOSCaracterísticas basales de los pacientesLa media de edad de la muestra era 74 ± 10 años; 581 pacientes (51,1%) eran mujeres y 568 (50,2%) ya habían tenido un ingreso por IC. La mayoría de los pacientes tenían una INR fuera del rango terapéutico óptimo (n = 927 [81%]). La distribución de los pacientes en las categorías de INR fue: a) INR 2–3, 210 pacientes (18,5%); b) INR < 2, 660 (58,0%), y c) INR > 3, 267 (23,5%).
La distribución de las características basales de los pacientes en función de las categorías de INR se muestra en la tabla 1. En líneas generales, se encontró una asociación entre la INR fuera del rango terapéutico óptimo y diversas variables clínicas, bioquímicas o ecocardiográficas, típicamente asociadas con un pronóstico adverso en la IC, especialmente en el grupo de pacientes con INR supraterapéutico. Es de destacar que entre los 3 grupos no hubo diferencias en los parámetros bioquímicos hepáticos. Los pacientes con IC y fracción de eyección del ventrículo izquierdo conservada presentaron con más frecuencia valores de INR > 3 al ingreso que los pacientes con fracción de eyección del ventrículo izquierdo reducida (tabla 1).
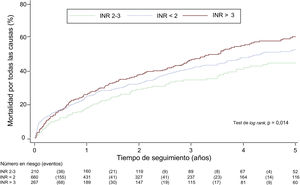
Razón internacional normalizada y mortalidad por todas las causasEn una mediana de seguimiento de 2,15 [0,71-4,29] años, fallecieron 495 pacientes (43,5%). Las tasas brutas de incidencia de mortalidad fueron superiores en los pacientes con la INR fuera de rango terapéutico óptimo (tabla 2). Así pues, en el análisis de supervivencia de Kaplan-Meier, el riesgo de mortalidad por todas las causas fue mayor en los pacientes con INR < 2 y > 3, especialmente en el rango supraterapéutico (test de log rank, p = 0,014) (figura 1).
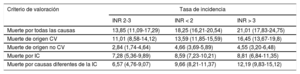
Tasa bruta de incidencia (cada 100 personas-año), y sus intervalos de confianza del 95%, de la muerte por todas las causas y por determinadas causas específicas, según las categorías de INR
| Criterio de valoración | Tasa de incidencia | ||
|---|---|---|---|
| INR 2-3 | INR < 2 | INR > 3 | |
| Muerte por todas las causas | 13,85 (11,09-17,29) | 18,25 (16,21-20,54) | 21,01 (17,83-24,75) |
| Muerte de origen CV | 11,01 (8,58-14,12) | 13,59 (11,85-15,59) | 16,45 (13,67-19,8) |
| Muerte de origen no CV | 2,84 (1,74-4,64) | 4,66 (3,69-5,89) | 4,55 (3,20-6,48) |
| Muerte por IC | 7,28 (5,36-9,89) | 8,59 (7,23-10,21) | 8,81 (6,84-11,35) |
| Muerte por causas diferentes de la IC | 6,57 (4,76-9,07) | 9,66 (8,21-11,37) | 12,19 (9,83-15,12) |
CV: cardiovascular; IC: insuficiencia cardiaca; INR: razón internacional normalizada.
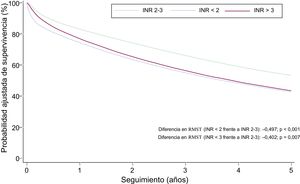
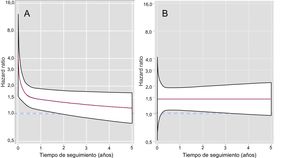
En el análisis multivariable de diferencias del RMST, se confirmó la asociación independiente entre la INR al ingreso y un mayor riesgo de mortalidad por todas las causas: RMSTINR<2 = –0,50 (IC95%, –0,77 a –0,23) años (p < 0,001) y RMSTINR>3 = –0,40 (IC95%, –0,70 a –0,11) años (p = 0,007) (tabla 3). El valor del estadístico C de Harrell fue 0,771. En la figura 2 se muestran las curvas de supervivencia ajustadas para mortalidad por todas las causas en función de las categorías de INR. Estas curvas se derivan del modelo multivariable del RMST e incluyen la interacción de la variable de la INR con el tiempo. Para la comparación de la INR < 2 con la INR 2-3, la intensidad de la asociación con el riesgo de mortalidad disminuyó a lo largo del seguimiento para hacerse no significativa a partir del segundo año. En cambio, la INR > 3 mostró un efecto relativamente constante, pero solo significativo a partir del tercer mes y hasta el tercer año (figura 3). La modelación de las HR dependientes del tiempo se presenta en la tabla 1 del material suplementario. En el modelo multivariable, y analizando la variable de la INR como variable continua, se observó que una INR fuera del rango óptimo se asocia con mayor riesgo de mortalidad tanto con valores infraterapéuticos como con los supraterapéuticos (p < 0,001) (figura del material suplementario).
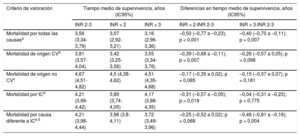
Estimaciones de riesgo (diferencias en tiempos medios de supervivencia) en los diferentes análisis para la evaluación de los criterios de valoración principal y secundarios, para las categorías de INR infraterapéutica o supraterapéutica, con respecto a la categoría de INR 2–3
| Criterio de valoración | Tiempo medio de supervivencia, años (IC95%) | Diferencias en tiempo medio de supervivencia, años (IC95%) | |||
|---|---|---|---|---|---|
| INR 2-3 | INR < 2 | INR > 3 | INR < 2-INR 2-3 | INR > 3-INR 2-3 | |
| Mortalidad por todas las causasa | 3,56 (3,34-3,79) | 3,07 (2,92-3,21) | 3,16 (2,96-3,36) | –0,50 (–0,77 a –0,23); p < 0,001 | –0,40 (–0,70 a –0,11); p = 0,007 |
| Mortalidad de origen CVb | 3,81 (3,57-4,04) | 3,42 (3,25-3,58) | 3,55 (3,34-3,76) | –0,39 (–0,68 a –0,11); p = 0,007 | –0,26 (–0,57 a 0,05); p = 0,098 |
| Mortalidad de origen no CVc | 4,67 (4,51-4,82) | 4,5 (4,38-4,62) | 4,51 (4,35-4,68) | –0,17 (–0,35 a 0,02); p = 0,085 | –0,15 (–0,37 a 0,07); p = 0,181 |
| Mortalidad por ICd | 4,21 (3,99-4,42) | 3,89 (3,74-4,05) | 4,17 (3,98-4,35) | –0,31 (–0,57 a –0,05); p = 0,018 | –0,04 (–0,31 a –0,23); p = 0,775 |
| Mortalidad por causa diferente a ICe,5 | 4,21 (3,98-4,44) | 3,96 (3,8-4,11) | 3,72 (3,49-3,96) | –0,25 (–0,52 a 0,02); p = 0,068 | –0,48 (–0,81 a –0,16); p = 0,004 |
CV: cardiovascular; FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; IC95%: intervalo de confianza del 95%; INR: razón internacional normalizada; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral.
Modelo ajustado por edad, primer ingreso por IC, bloqueo de rama, índice de Charlson, frecuencia cardiaca, urea, presión arterial sistólica, hemoglobina y NT–proBNP.
Modelo ajustado por edad, primer ingreso por IC, bloqueo de rama, FEVI < 40%, índice de Charlson, frecuencia cardiaca, urea, presión arterial sistólica, hemoglobina y NT–proBNP.
cModelo ajustado por edad, FEVI < 40%, índice de Charlson, frecuencia cardiaca, presión arterial sistólica y hemoglobina.
De los 495 fallecimientos, 378 (76,4%) fueron de origen CV. En la tabla 2 se muestran las tasas brutas de incidencia de las diferentes causas específicas de muerte en función de las categorías de INR.
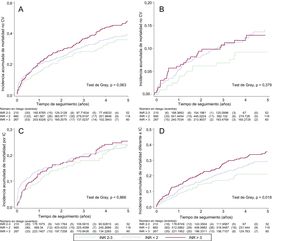
La incidencia de función de riesgo acumulada de mortalidad CV fue superior en los pacientes con INR fuera de rango terapéutico óptimo que en aquellos con INR 2–3 (test de Gray, p = 0,063), con un efecto más marcado con la INR > 3 (figura 4). Sin embargo, tras el ajuste estadístico multivariable, aunque las 2 categorías de INR se asociaron con mayor riesgo de mortalidad CV, esta asociación fue algo más intensa con la INR < 2 (diferencias en tiempo medio de supervivencia a 5 años: RMSTINR<2 = –0,39 (IC95%, –0,68 a –0,11) años; p = 0,007, y RMSTINR>3 = –0,26 (IC95%, –0,57 a 0,05) años; p = 0,098) (tabla 3).
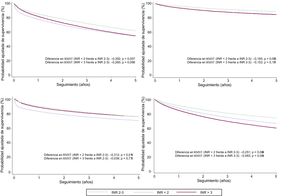
En la figura 5 se muestran las curvas de supervivencia ajustadas para los criterios de valoración secundarios. Con respecto a la muerte CV, la intensidad de la asociación con una INR < 2 es más marcada en las fases iniciales de seguimiento, lo cual se observa también en los HR dependientes del tiempo (tabla 1 del material suplementario). En cambio, la comparación entre INR > 3 e INR 2–3 revela un aumento de riesgo constante, aunque no alcanza la significación estadística.
Curvas de supervivencia ajustadas. A: mortalidad de causa CV. B: mortalidad de causa no CV. C: mortalidad por IC. D: mortalidad no atribuible a IC. CV: cardiovascular; IC: insuficiencia cardiaca; INR: razón internacional normalizada; RMST: tiempo de supervivencia media restringido.
Con respecto a las causas específicas de muerte CV, la tasa bruta de incidencia de muerte atribuible a cada evento específico fue baja (tabla 2 del material suplementario). No se observan diferencias significativas en la muerte atribuible a ictus isquémico, infarto agudo de miocardio, ictus hemorrágico o muerte súbita, aunque en estos 2 eventos se observa una mayor incidencia numérica en INR > 3. La causa de 84 muertes (el 16% del total) fue desconocida.
Razón internacional normalizada y mortalidad no cardiovascularFueron de origen no CV 117 fallecimientos (23,6%). Se observó una mayor incidencia en las categorías de INR < 2 o > 3 (tabla 2), aunque estas diferencias no son estadísticamente significativas (test de Gray, p = 0,379) (figura 4).
Debido a que la cPR se cumplía para este criterio de valoración, el valor pronóstico de las categorías de la INR se presenta en la tabla 4 en forma de HR única; dichos resultados corroboran la falta de asociación entre INR y mortalidad no CV hallada mediante el análisis de diferencias en el RMST (tabla 3).
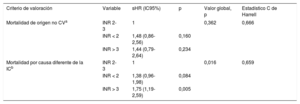
Estimaciones de riesgo en los diferentes análisis que cumplían el criterio de proporcionalidad de riesgo para las categorías de INR infraterapéutica o supraterapéutica respecto a la categoría de INR 2–3
| Criterio de valoración | Variable | sHR (IC95%) | p | Valor global, p | Estadístico C de Harrell |
|---|---|---|---|---|---|
| Mortalidad de origen no CVa | INR 2-3 | 1 | 0,362 | 0,666 | |
| INR < 2 | 1,48 (0,86-2,56) | 0,160 | |||
| INR > 3 | 1,44 (0,79-2,64) | 0,234 | |||
| Mortalidad por causa diferente de la ICb | INR 2-3 | 1 | 0,016 | 0,659 | |
| INR < 2 | 1,38 (0,96-1,98) | 0,084 | |||
| INR > 3 | 1,75 (1,19-2,59) | 0,005 |
CV: cardiovascular; FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; IC95%: intervalo de confianza del 95%; INR: razón internacional normalizada; sHR: subhazard ratio.
Con respecto a la muerte por hemorragia, la tasa de eventos fue muy baja (n = 26) (tabla 2 de material suplementario), y no se observaron diferencias en su riesgo acumulado entre las 3 categorías de INR (test de Gray, p = 0,949).
Razón internacional normalizada y mortalidad por insuficiencia cardiacaSe atribuyeron a IC 230 muertes (46,5%). Aunque la tasa bruta de incidencia fue superior en los pacientes con la INR fuera de rango óptimo (tabla 2), no se observaron diferencias significativas en su riesgo acumulado entre las 3 categorías (test de Gray, p = 0,866) (figura 4).
La categoría que se asoció con el mayor riesgo de mortalidad por IC fue la de INR < 2, fundamentalmente para eventos precoces. Así pues, en el análisis del RMST multivariable, solo en los pacientes con INR < 2 se observó un mayor riesgo de mortalidad por IC: RMSTINR<2 = –0,31 (IC95%, –0,57 a –0,05) años (p = 0,018) (tabla 3 y figura 5). Las HR dependientes del tiempo (tabla 1 del material suplementario) revelan un marcado y significativo aumento del riesgo en el grupo de INR < 2, pero que disminuye precozmente para hacerse no significativo a partir del tercer mes de seguimiento.
Razón internacional normalizada y mortalidad no atribuible a insuficiencia cardiacaLa incidencia acumulada de muerte no atribuible a IC muestra diferencias marcadas entre las 3 categorías de INR, con una mayor incidencia de este evento si la INR > 3 (test de Gray, p = 0,018) (figura 4).
En el análisis multivariable (tabla 3), destaca que los pacientes con INR > 3 presentaran un riesgo marcado de este tipo de muerte con respecto a los pacientes con la INR en rango óptimo: RMSTINR>3 = –0,48 (IC95%, –0,81 a –0,16) (p = 0,004) (figura 5). Debido a que la cPR se cumplía para este criterio de valoración, el valor pronóstico de las categorías de la INR se presenta en la tabla 4 en forma de HR única; dichos resultados respaldan los obtenidos por análisis de diferencias en el RMST.
DISCUSIÓNEl principal hallazgo de este estudio es que un valor de INR fuera del rango óptimo al ingreso, tanto infraterapéutico como supraterapéutico, en pacientes con IC aguda en tratamiento con AVK por FANV se asocia de manera independiente con un mayor riesgo de mortalidad en el seguimiento a largo plazo.
La IC y la fibrilación auricular son afecciones que frecuentemente coexisten, dado que comparten factores de riesgo y tienen mecanismos fisiopatológicos comunes15. La presencia de IC incrementa significativamente el riesgo de eventos tromboembólicos en pacientes con fibrilación auricular y constituye per se indicación de anticoagulación oral crónica3. Sin embargo, el control de la anticoagulación oral de los pacientes con IC y fibrilación auricular es complejo7,16. Entre las causas que pueden explicar esta complejidad se encuentran la polifarmacia, las frecuentes rehospitalizaciones, la disfunción hepática y renal o las alteraciones hemostáticas intrínsecamente asociadas con la IC7–9,17. Estas alteraciones son mucho más patentes en la IC aguda que en la crónica7.
En la presente serie cabe destacar que más del 80% de los pacientes tuvieran un valor de INR alterado al ingreso. Entre las posibles causas, se ha descrito que la hipoxia tisular producida por disminución del flujo hepático en estados de congestión y/o isquemia hepática puede tener consecuencias negativas en el metabolismo de los AVK18. A su vez, también se han correlacionado los valores de la INR en la IC con el grado de inflamación sistémica8 o la hemodilución asociada con la congestión venosa sistémica19. Los datos obtenidos respaldan en parte estas hipótesis. Valores alterados de la INR se asocian significativamente con valores elevados de biomarcadores como el antígeno carbohidrato 125 o la fracción aminoterminal del propéptido natriurético cerebral. Sin embargo, no se ha encontrado una asociación significativa entre la INR alterada y los marcadores de función hepática.
Los mecanismos fisiopatológicos que subyacen a la asociación entre el riesgo de mortalidad y la INR al ingreso son en gran parte desconocidos. Es de destacar que los factores mencionados previamente como potencial causa de la alteración de la INR son todos fenómenos negativos desde el punto de vista fisiopatológico y pronóstico en la IC. Sin embargo, la persistencia en la asociación de una INR alterada con la mortalidad tras ajuste multivariable y la intensidad de esta asociación en las fases más precoces del seguimiento indican que, además, pudiera existir una asociación causal con la mortalidad. Recientemente, en una cohorte de 294 pacientes con IC aguda que no recibían tratamiento anticoagulante, Okada et al.9 observaron también que los valores de la INR alterados al ingreso se asociaban de manera independiente con menor supervivencia en el seguimiento a 1 año. De modo similar que en este estudio, la alteración de la INR se asoció con un perfil más adverso de marcadores de activación neurohormonal. Sin embargo, hay que destacar que el presente estudio se realizó en pacientes anticoagulados con AVK, y en este contexto la INR no es únicamente un biomarcador, sino que supone un objetivo terapéutico, potencialmente modulable, del tratamiento anticoagulante que recibe el paciente.
El análisis exploratorio de causas de mortalidad no permite establecer una clara asociación entre un riesgo específico de muerte para cada categoría de INR, aunque sí destacan algunas asociaciones. Por ejemplo, los pacientes con INR < 2 tienen mayor riesgo de mortalidad por IC. Se ha descrito que las interacciones farmacológicas aumentan y la adherencia al tratamiento en la IC disminuye en contextos de empeoramiento clínico y/o estados avanzados de IC. Ambas situaciones se han relacionado con mal pronóstico en el paciente con IC20, lo cual podría contribuir a explicar estos hallazgos. Para la INR > 3, en cambio, destaca un mayor riesgo de mortalidad no atribuible a IC. Aunque las causas de esta asociación son especulativas, la presencia de una INR > 3 es más frecuente entre los pacientes con IC y fracción de eyección del ventrículo izquierdo conservada. Como es sabido, este es un síndrome multifactorial caracterizado por una compleja interacción de alteraciones CV con diferentes comorbilidades21, con especial vulnerabilidad a sufrir morbimortalidad por causas distintas de las directamente atribuibles a la IC22. A su vez, los pacientes con una INR > 3 mostraban una mayor prevalencia de valvulopatías, lo que también podría contribuir a explicar la mayor mortalidad de este grupo de pacientes.
Recientemente se ha demostrado que una intervención instructiva específica sobre la anticoagulación oral de los pacientes con IC es capaz de optimizar marcadamente el grado de control23. Sin embargo, no se conoce qué influencia puede tener un estrecho control de la ACO en el riesgo de mortalidad de los pacientes con IC.
El uso de anticoagulantes directos, con lo que se obvia la necesidad de monitorizar la INR, es otra alternativa terapéutica. En los ensayos clínicos pivotales que compararon estos fármacos frente a los AVK en la FANV, se incluyó en total a más de 25.000 pacientes con IC, de los que se trató con anticoagulantes directos a 13.2515. En el subgrupo de pacientes con IC se observó que estos fármacos reducen la incidencia de ictus o embolia sistémica, hemorragia mayor o hemorragia intracraneal, pero tienen un efecto neutro en la mortalidad por todas las causas o CV4. Una INR alterada al ingreso podría identificar a un subgrupo de pacientes para quienes estos fármacos pudieran tener un especial beneficio respecto a los AVK. Sin embargo, la definición de IC en los ensayos pivotales con anticoagulantes directos ha sido heterogénea y en ninguno de ellos se ha incluido a los pacientes en el contexto de una descompensación aguda de la IC, con lo que se necesita más evidencia al respecto.
La variable INR no cumple la cPR en su asociación con el riesgo de mortalidad. En este contexto, el análisis de diferencias por el RMST se ha recomendado como un método adecuado para evaluar las diferencias en la supervivencia atribuibles a una variable en estudio durante un periodo de tiempo determinado, y su uso va en aumento12,13. En el presente estudio implica que, tras ajuste multivariable, una INR < 2 y > 3 se asocia con un tiempo medio de supervivencia a 5 años 6 y 5 meses menor, respectivamente, que los pacientes con INR 2–3. El riesgo atribuible a la INR al ingreso, sin embargo, es mayor en la fase inicial del seguimiento del estudio, sobre todo para la INR < 2, mientras que para un valor de INR supraterapéutico, su asociación con la mortalidad es más constante en el seguimiento a largo plazo. Serán necesarios futuros estudios para explicar los mecanismos fisiopatológicos causales que subyacen a estos hallazgos y sus posibles implicaciones terapéuticas.
LimitacionesEn primer lugar, es un estudio observacional y unicéntrico cuyos resultados pueden estar afectados por diversos sesgos y aspectos inherentes a la práctica clínica. En segundo lugar, no se dispone de información acerca del tiempo en rango terapéutico de los pacientes en el momento del ingreso ni en la evolución posterior, con lo que no se puede conocer cómo era la calidad de la anticoagulación fuera del episodio agudo. En tercer lugar, la correcta adjudicación de causas específicas de muerte en el ámbito de un estudio observacional es compleja y presenta evidentes limitaciones11. En este sentido, la baja incidencia de muerte atribuible a algunos eventos CV concretos y las muertes de origen desconocido contribuyen a que no se pueda establecer conclusiones firmes sobre las causas específicas de muerte atribuible a la INR. Por último, la INR no se ha determinado de manera simultánea a otras variables analizadas como, por ejemplo, las ecocardiográficas.
CONCLUSIONESEn pacientes con IC y FANV en tratamiento con AVK, un valor de INR al ingreso fuera del rango óptimo, tanto infraterapéutico como supraterapéutico, en el contexto de una descompensación aguda de IC se asocia de manera independiente con un mayor riesgo de mortalidad en el seguimiento a largo plazo.
CONFLICTO DE INTERESESNo se declara ninguno.
- –
El valor pronóstico de la INR en las descompensaciones agudas de la IC de pacientes tratados con AVK es desconocido.
- –
El 81% de los pacientes con IC y FANV tratados con AVK presentan una INR fuera del rango terapéutico óptimo en el contexto de una descompensación aguda de la IC.
- –
Tanto un valor de la INR infraterapéutico como uno supraterapéutico se asocian de manera independiente con un mayor riesgo de mortalidad en el seguimiento.