A pesar de los avances introducidos en las últimas décadas en el manejo de la endocarditis infecciosa, esta continúa causando una elevada letalidad1. Los eventos embólicos (EE) son su complicación extracardiaca más frecuente, con una incidencia de EE sintomáticos de un 10-50%2, con predilección por el sistema nervioso central, cuya afección ensombrece más el pronóstico3.
Los EE también rigen la actitud terapéutica, ya que su prevención es indicación de cirugía; un reciente estudio demostró que la cirugía temprana los reduce significativamente4. Dado que son fenómenos precoces en la endocarditis infecciosa, resulta crucial cuantificar el riesgo embólico en el momento del diagnóstico para evitar esta complicación y ayudar en la toma de decisiones terapéuticas.
Recientemente se diseñaron dos sistemas predictivos del riesgo embólico en endocarditis infecciosa, uno francés5 y otro italiano6. Nuestro objetivo es probar y comparar la utilidad clínica de dichos sistemas.
Estudiamos a 153 pacientes consecutivos ingresados en un centro terciario entre enero de 2009 y abril de 2014 con diagnóstico de endocarditis infecciosa basado en los criterios modificados de Duke. En las primeras 24 h del ingreso se practicó un ecocardiograma transtorácico a todos los pacientes y transesofágico al 90%.
Calculamos el riesgo embólico estimado por el sistema francés, que adjudica 1 punto a cada una de las siguientes covariables: diabetes mellitus, fibrilación auricular, vegetación > 10 mm, embolia previa a antibioterapia y Staphylococcus aureus. A la suma de la puntuación previa, añadimos la edad como variable continua, tal y como considera el sistema francés, para generar las estimaciones de sufrir un EE5. También calculamos el riesgo según el sistema italiano asignando 1 punto a vegetación ≥ 13 mm y 1 punto a S. aureus. Se clasificó a los pacientes en alto riesgo embólico si tenían una probabilidad > 7,5% según el sistema francés o 2 puntos según el italiano.
El rendimiento de ambos sistemas en la predicción de EE desde el diagnóstico e iniciada la antibioterapia se evaluó con regresión de Cox. No consideramos EE los basados exclusivamente en sospecha clínica o manifestaciones cutáneas.
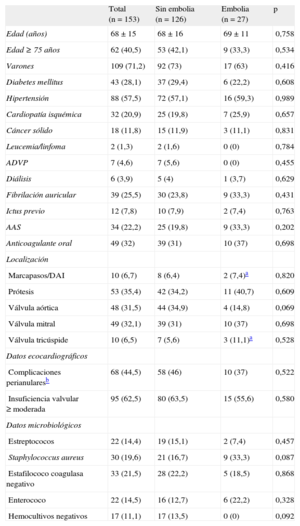
La tabla recoge los datos clínicos, ecocardiográficos y microbiológicos. El índice de Charlson fue 4 ± 2. La longitud de la vegetación en ecocardiograma transtorácico fue 8 ± 7 mm y 10 ± 7 mm en el transesofágico. Durante la hospitalización, se registraron 27 (17,6%) EE, 16 (59,9%) en el sistema nervioso central. La mortalidad hospitalaria fue 3 veces mayor (12/27; 44,4%) en pacientes con EE que en los pacientes sin EE (11,9%).
Características basales
| Total (n = 153) | Sin embolia (n = 126) | Embolia (n = 27) | p | |
| Edad (años) | 68 ± 15 | 68 ± 16 | 69 ± 11 | 0,758 |
| Edad ≥ 75 años | 62 (40,5) | 53 (42,1) | 9 (33,3) | 0,534 |
| Varones | 109 (71,2) | 92 (73) | 17 (63) | 0,416 |
| Diabetes mellitus | 43 (28,1) | 37 (29,4) | 6 (22,2) | 0,608 |
| Hipertensión | 88 (57,5) | 72 (57,1) | 16 (59,3) | 0,989 |
| Cardiopatía isquémica | 32 (20,9) | 25 (19,8) | 7 (25,9) | 0,657 |
| Cáncer sólido | 18 (11,8) | 15 (11,9) | 3 (11,1) | 0,831 |
| Leucemia/linfoma | 2 (1,3) | 2 (1,6) | 0 (0) | 0,784 |
| ADVP | 7 (4,6) | 7 (5,6) | 0 (0) | 0,455 |
| Diálisis | 6 (3,9) | 5 (4) | 1 (3,7) | 0,629 |
| Fibrilación auricular | 39 (25,5) | 30 (23,8) | 9 (33,3) | 0,431 |
| Ictus previo | 12 (7,8) | 10 (7,9) | 2 (7,4) | 0,763 |
| AAS | 34 (22,2) | 25 (19,8) | 9 (33,3) | 0,202 |
| Anticoagulante oral | 49 (32) | 39 (31) | 10 (37) | 0,698 |
| Localización | ||||
| Marcapasos/DAI | 10 (6,7) | 8 (6,4) | 2 (7,4)a | 0,820 |
| Prótesis | 53 (35,4) | 42 (34,2) | 11 (40,7) | 0,609 |
| Válvula aórtica | 48 (31,5) | 44 (34,9) | 4 (14,8) | 0,069 |
| Válvula mitral | 49 (32,1) | 39 (31) | 10 (37) | 0,698 |
| Válvula tricúspide | 10 (6,5) | 7 (5,6) | 3 (11,1)a | 0,528 |
| Datos ecocardiográficos | ||||
| Complicaciones perianularesb | 68 (44,5) | 58 (46) | 10 (37) | 0,522 |
| Insuficiencia valvular ≥ moderada | 95 (62,5) | 80 (63,5) | 15 (55,6) | 0,580 |
| Datos microbiológicos | ||||
| Estreptococos | 22 (14,4) | 19 (15,1) | 2 (7,4) | 0,457 |
| Staphylococcus aureus | 30 (19,6) | 21 (16,7) | 9 (33,3) | 0,087 |
| Estafilococo coagulasa negativo | 33 (21,5) | 28 (22,2) | 5 (18,5) | 0,868 |
| Enterococo | 22 (14,5) | 16 (12,7) | 6 (22,2) | 0,328 |
| Hemocultivos negativos | 17 (11,1) | 17 (13,5) | 0 (0) | 0,092 |
AAS: ácido acetilsalicílico; ADVP: adicto a drogas por vía parenteral; DAI: desfibrilador automático implantable.
Las estimaciones generadas por el sistema francés mostraron una asociación significativa con el riesgo embólico (hazard ratio [HR]= 2,7; intervalo de confianza del 95% [IC95%], 1,37-5,46). Sin embargo, de los 27 pacientes que sufrieron EE, 12 (44,4%) habían sido clasificados de bajo riesgo. La ocurrencia de EE se predijo mejor por este sistema que por el azar (p = 0,03), aunque su discriminación fue moderada (estadístico c = 0,66; IC95%, 0,54-0,77).
Las estimaciones del modelo italiano también se asociaron con el riesgo embólico: HR = 2,2 (IC95%, 1,28-3,92) y c = 0,62 (IC95%, 0,49-0,74; p = 0,05). En este modelo, el 85,2% (n = 23) de los pacientes que sufrieron un EE habían sido clasificados de bajo riesgo.
La calibración de ambos modelos fue adecuada (p≥0,2). Comparado con el sistema italiano, el francés mostró un índice de mejora neta de la reclasificación del 7,4% (p = 0,5).
Así, aunque ambos modelos tienen una potencia predictiva similar, el francés clasifica de modo menos erróneo que el italiano a los pacientes verdaderamente de bajo riesgo embólico. La principal ventaja de este último sería su mayor facilidad de uso, dado que requiere el empleo de dos variables, mientras que el esquema francés, además de requerir mayor número de variables, hace necesario el uso de un software para su cálculo5. En nuestra cohorte, solo un paciente sufrió embolia derecha. Excluirla del análisis no modificó los resultados generales. Así, nuestros resultados se refieren en esencia a las embolias izquierdas.
En conclusión, en esta serie contemporánea de endocarditis infecciosa, aproximadamente 1/6 pacientes sufren EE desde el diagnóstico o inicio de antibioterapia. El exceso de riesgo bruto de muerte hospitalaria de los pacientes con EE ronda el 30%. Se antoja posible predecir el riesgo embólico con una simple herramienta clínica. En nuestra población, el sistema francés se demostró más útil, por lo que su empleo (integrado en el juicio clínico) ayudaría a mejorar el proceso de toma de decisiones terapéuticas haciéndolo más ágil e individualizado. Gracias a ello, se reduciría la tasa de una complicación devastadora como la embolia séptica cerebral. Es deseable desarrollar una herramienta clínica de mayor rendimiento que las actualmente disponibles.