La nefropatía aguda inducida por contraste es una causa importante de insuficiencia renal aguda (IRA-IC) en los pacientes hospitalizados y conlleva un peor pronóstico. La creatinina sérica presenta limitaciones para evaluarla, ya que su elevación es relativamente lenta y se ve influida por factores extrarrenales1. Recientemente se ha introducido el uso de la lipocalina asociada a la gelatinasa neutrófila (NGAL, neutrophil gelatinase-associated lipocalin) como biomarcador no invasivo sensible y temprano para predecir la IRA-IC en diferentes trastornos cardiovasculares2,3. Sin embargo, aún no se ha definido el papel que pueden desempeñar las determinaciones tempranas de la NGAL en la predicción de los cambios de la creatinina sérica en pacientes no seleccionados con síndrome coronario agudo a quienes se administra iodixanol, un medio de contraste no iónico isoosmolar. El objetivo de este estudio fue evaluar la utilidad de las determinaciones tempranas de la NGAL para predecir los cambios de la creatinina sérica en un plazo de 48 horas tras la angiografía coronaria (ΔCr-48 h) en pacientes con síndrome coronario agudo que reciben iodixanol.
Se incluyeron 105 pacientes consecutivos con síndrome coronario agudo a quienes se practicó una coronariografía con iodixanol (Visipaque®). Se determinó la creatinina sérica antes de la angiografía y pasadas 24 y 48 horas, y la NGAL en suero antes y a las 4, 8 y 24 horas de la intervención. Según lo establecido en el protocolo aplicado, se utilizó iodixanol en todos los pacientes. Las demás medidas destinadas a la prevención de la IRA-IC se individualizaron según el criterio del médico que atendía al paciente. La IRA-IC se definió por un aumento de la creatinina sérica > 25% o > 0,5 mg/dl respecto al valor basal en las 48 horas siguientes a la intervención. La determinación de la NGAL se llevó a cabo mediante inmunoensayo de fluorescencia. Se determinó la filtración glomerular estimada aplicando la fórmula de cuatro variables de Modification of Diet in Renal Disease (MDRD). El objetivo principal fue determinar la asociación entre las determinaciones de la NGAL realizadas en las primeras 24 horas y el ΔCr-48 h absoluto máximo. Los objetivos secundarios consistieron en establecer: a) si las determinaciones de la NGAL se asociaban al riesgo de IRA-IC y b) la asociación entre el volumen de contraste y el ΔCr-48 h. Las variables continuas se expresaron como media ± desviación estándar (DE) o mediana [rango intercuartiles (RIC)], según fuera apropiado, y las variables discretas se presentaron en forma de porcentajes. Para determinar la asociación entre las determinaciones de la NGAL y las del ΔCr-48 h se utilizó un análisis de regresión lineal. El riesgo de IRA-IC se evaluó con un modelo de regresión logística. Se consideró que un valor de p bilateral < 0,05 era estadísticamente significativo.
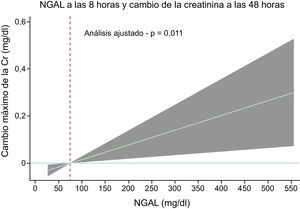
En la tabla se resumen las características basales de la muestra. Los valores de NGAL (mediana [RIC]) aumentaron en cada uno de los momentos de valoración: 63 (49, 112), 69 (56, 116), 75 (50, 114) y 77 (64, 174) ng/ml en las determinaciones realizadas en situación basal y a las 4, 8 y 24 horas, respectivamente. La media de la creatinina sérica al ingreso y el valor del ΔCr-48 h (mg/dl) fueron de 0,98 ± 0,35 y 0,06 ± 0,24, respectivamente. Seis pacientes (5,7%) presentaron una IRA-IC a las 48 horas. Hubo una asociación lineal positiva entre los valores de NGAL y los del ΔCr-48 h en el conjunto de la muestra, con independencia del momento de la valoración (p < 0,05 para todas las comparaciones), tal como se muestra en la tabla del material suplementario. En el análisis multivariante, en el cual se incluyeron la edad, la diabetes mellitus, la filtración glomerular estimada < 60 min/ml/1,73 m2, el tipo de síndrome coronario agudo y la clase de Killip > I al ingreso, el valor de la NGAL a las 8 horas continuó mostrando una asociación lineal positiva y significativa con el valor del ΔCr-48 h [coeficiente β por 100 ng/ml: 0,63; intervalo de confianza del 95% (IC95%), 0,15–1,11; p = 0,011]. En la figura se muestra el gradiente de riesgo de la determinación de la NGAL a las 8 horas respecto a la predicción del ΔCr-48 h. Este modelo explicaba un 33% de la variabilidad observada en el ΔCr-48 h. Por orden de importancia (reducción de R2), la NGAL a las 8 horas (40%), la filtración glomerular estimada < 60 min/ml/1,73 m2 (21,5%) y la diabetes mellitus (17,3%) fueron las covariables más importantes en la predicción del ΔCr-48 h. De igual modo, la NGAL a las 24 horas mostró una relación independiente con el ΔCr-48 h (coeficiente β por 100 ng/ml: 0,62; IC95%, 0,08-1,17; p = 0,026), mientras que el valor basal de la NGAL y el de la NGAL a las 4 horas se mantuvieron en el límite de la significación en cuanto a la asociación con el ΔCr-48 h (tabla del material suplementario). En un análisis univariante, los valores de NGAL basal y a las 4, 8 y 24 horas, por cada aumento de 10 ng/ml, estaban en el límite de la significación en su asociación con la IRA-IC. La curva de características operativas del receptor (ROC) correspondiente a los valores de NGAL a las 8 horas puso de manifiesto una gran capacidad de discriminación para predecir la IRA-IC (área bajo la curva de 0,788). Un valor ≥ 92 ng/ml mostró una sensibilidad del 100% y una especificidad del 60,6%. El volumen de contraste administrado (149,2 ± 66,4 ml) no mostró asociación alguna con el ΔCr-48 h en el análisis univariante (coeficiente β por 100 ml: 0,02; IC95%, −0,09- 0,07; p = 0,698) ni en el análisis multivariante (coeficiente β por 100 ml: 0,03; IC95%, −0,05-0,10; p = 0,451).
Características basales
| Muestra total (n = 105) | |
|---|---|
| Edad (años) | 65 ± 11 |
| Varones | 69 (66) |
| Peso (kg) | 78,7 ± 22,5 |
| Altura (cm) | 160,9 ± 17 |
| Hipertensión | 78 (74) |
| Diabetes mellitus | 24 (23) |
| Diabetes mellitus dependiente de insulina | 6 (6) |
| Dislipidemia | 63 (60) |
| Fumadores actuales | 60 (57) |
| Ex fumadores | 12 (11) |
| Antecedentes de IM | 24 (23) |
| Enfermedad renal crónica previa | 6 (5,7) |
| Clase de Killip > I al ingreso | 24 (23) |
| Presión arterial sistólica (mmHg) | 135 ± 31 |
| Presión arterial diastólica (mm Hg) | 74 ± 14 |
| Antecedentes previos de ICP | 21 (20) |
| Indicación para la ICP en el ingreso de cualificación para el estudio | |
| IAMCEST | 66 (63) |
| IAMSEST | 39 (37) |
| Número de vasos coronarios afectados | |
| 0 | 6 (6) |
| 1 | 60 (57) |
| 2 | 24 (23) |
| 3 | 18 (17) |
| ICP, n (%) | 87 (83) |
| Creatinina sérica al ingreso (mg/dl) | 0,98 ± 0,34 |
| FGeaal ingreso, ml/min/1,73 m2 | 83,6 ± 28,5 |
| FGeaal ingreso < 60 ml/min/1,73 m2 | 21 (20) |
| NGAL en suerobal ingreso (ng/mL) | 63 (49, 112) |
FGe: filtración glomerular estimada; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IAMSEST: infarto agudo de miocardio sin elevación del segmento ST; ICP: intervención coronaria percutánea; IM: infarto de miocardio; NGAL: lipocalina asociada a gelatinasa neutrófila.
Los datos expresan n (%), media ± desviación estándar o mediana [rango intercuartiles].
Gradiente de riesgo del valor de la lipocalina asociada a la gelatinasa neutrófila (NGAL) a las 8 horas de la intervención en la predicción del ΔCr-48 h absoluto máximo. ΔCr-48 h: cambio de la creatinina a las 48 horas; NGAL-8 h: lipocalina asociada a gelatinasa neutrófila a las 8 horas.
Este estudio muestra que las determinaciones de la NGAL, antes de la angiografía y tras realizarla, predicen los cambios absolutos de la creatinina sérica en pacientes con síndrome coronario agudo a los que se administra iodixanol como medio de contraste. No obstante, el valor de la NGAL 8 horas después de la intervención fue el que mostró el mejor rendimiento diagnóstico. Se demostró que la NGAL, en ausencia de aumentos diagnósticos de la creatinina sérica, permite detectar a los pacientes con una IRA-IC subclínica que tienen un mayor el riesgo de presentar una evolución clínica adversa2. En estudios previos se ha evidenciado la utilidad de la NGAL como biomarcador temprano de la IRA-IC en diferentes escenarios, sobre todo tras la administración de contraste3. Sin embargo, todavía no se había esclarecido por completo el momento óptimo para su determinación después de una angiografía coronaria. En este estudio, una comparación formal de diferentes momentos de valoración mostró que todos ellos tenían valor predictivo respecto al ΔCr-48 h. No obstante, el hecho de que del valor de la NGAL a las 8 horas sea el que obtiene un mayor rendimiento puede ser de utilidad para los clínicos al identificar aquellos pacientes con mayor riesgo de desarrollar una IRA-IC, en quienes podría ser beneficiosa la aplicación de estrategias preventivas4. A este respecto, y en consonancia con lo indicado por otros resultados recientes5, se observó que el volumen de iodixanol no mostró relación alguna con la IRA-IC.
Es preciso mencionar algunas limitaciones del estudio. Se trata de un estudio pequeño, llevado a cabo en un solo centro. La baja incidencia de IRA-IC impide obtener estimaciones robustas del riesgo respecto a este objetivo. No se registró de manera sistemática un factor de confusión como es el volumen de líquido administrado antes de la angiografía, lo que impide analizar su influencia. Por último, no se evaluó la IRA-IC después de las primeras 48 horas.
En conclusión, la determinación de la NGAL 8 horas después de la intervención predice los cambios de la creatinina en pacientes con síndrome coronario agudo a quienes se practica una coronariografía y reciben iodixanol como medio de contraste.
FINANCIACIÓNEste estudio contó con la financiación de una subvención no condicionada de GE Healthcare-Medical Diagnostics y de la Red de Investigación Cardiovascular; Programa 7 (RD12/0042/0010) FEDER.