Palabras clave
INTRODUCCION
Los objetivos en el tratamiento del infarto agudo de miocardio con elevación del segmento ST (IAMEST) se han centrado en la apertura de la arteria coronaria1-3. Sin embargo, la permeabilidad de la arteria no garantiza una adecuada perfusión tisular y, de hecho, hasta el 30% de los pacientes con flujo epicárdico aparentemente normal (Thrombolysis In Myocardial Infarction [TIMI] 3) tienen una perfusión tisular inadecuada como consecuencia de un daño en la microcirculación4-6.
Si bien la angiografía es de gran utilidad para identificar casos con microcirculación claramente dañada (TIMI < 3)7, para pacientes con TIMI 3 su utilidad es más controvertida. El blush miocárdico es un índice angiográfico creado para valorar el estado de la perfusión miocárdica, aunque hay reservas en cuanto a la fiabilidad y la variabilidad en sus medidas8.
El objetivo primario de este estudio fue determinar la variabilidad en las medidas del blush entre 2 laboratorios independientes: el laboratorio de hemodinámica de un hospital universitario y un laboratorio central. Como objetivos secundarios se evaluó la correlación del blush analizado en el laboratorio central con la perfusión miocárdica analizada mediante ecocardiografía miocárdica con inyección de contraste intracoronaria (EMC) y con la función ventricular a los 6 meses analizada mediante resonancia magnética cardiaca (RMC).
MÉTODOS
Grupo de estudio
Se estudió a 60 pacientes consecutivos con un primer IAMEST tratados con trombólisis dentro de las primeras 6 h desde el inicio del dolor. Los criterios de inclusión fueron los siguientes: a) enfermedad de un vaso con la arteria causante del infarto abierta, definida como flujo TIMI 3 y estenosis residual < 50% en la angiografía (y eventual angioplastia) realizada antes del alta; b) curso clínico estable y sin complicaciones durante los primeros 6 meses de seguimiento; c) persistencia de la arteria causante del infarto abierta (flujo TIMI 3 y estenosis residual < 50%) en la angiografía realizada al sexto mes, y d) ausencia de contraindicaciones para la realización de una RMC a los 6 meses. De los 60 pacientes iniciales se excluyó a 20 por enfermedad multivaso (9 casos), flujo TIMI < 3 (2 casos), deficiente calidad de la imagen angiográfica para valorar el blush (un caso), reinfarto durante el seguimiento (un caso), reestenosis a los 6 meses (5 casos) y claustrofobia (2 casos). Finalmente, el grupo de estudio definitivo estaba compuesto de 40 pacientes.
El protocolo del estudio cumple con la Declaración de Helsinki y fue aprobado por el comité ético de nuestro centro. Todos los participantes en el estudio firmaron consentimiento informado.
Cateterismo cardiaco
La angiografía se realizó en una mediana de 5 días tras el IAMEST (rango total, 3-7 días). En caso de estenosis > 50% u oclusión de la arteria relacionada con el infarto, se realizó angioplastia con implantación de stent (30 casos; 75%). En 3 casos (8%) se realizó angioplastia de rescate por la ausencia de criterios electrocardiográficos de reperfusión. En estos casos se repitió la angiografía antes del alta y los datos empleados en el estudio se tomaron del cateterismo prealta. En todos los casos quedó una estenosis residual < 50% y flujo TIMI 3 al finalizar el procedimiento.
La arteria relacionada con el infarto fue la descendente anterior en 28 casos (70%) y la arteria coronaria derecha en 12 casos (30%). En ningún caso con arteria circunfleja como causante del infarto se cumplieron los criterios de inclusión.
Para garantizar la homogeneidad de las medidas se empleó un protocolo estandarizado: todos los angiogramas se grabaron a 12,5 imágenes por segundo, se empleó una inyectora de contraste (Acist Medical Systems CMS2000, Estados Unidos) con velocidades de infusión constantes de 4 ml por segundo para la arteria coronaria izquierda (bolos de 8 ml) y 3 para la arteria coronaria derecha (bolos de 6 ml). Se utilizó la proyección caudal derecha como primera opción para la evaluación de la arteria coronaria izquierda, mientras que para la valoración de la arteria coronaria derecha se emplearon proyecciones izquierdas; en caso necesario se utilizaron otras proyecciones en las que el análisis individual de la arteria causante fuera óptimo. Se realizaron secuencias angiográficas largas (hasta la fase venosa). Se administró nitroglicerina intravenosa previamente a la proyección analizada salvo en caso de hipotensión arterial (presión arterial sistólica < 90 mmHg).
El blush miocárdico evalúa la microcirculación mediante la valoración de la densidad de contraste en el territorio de miocardio dependiente de la arteria causante. Los grados de blush se definieron de la siguiente manera: 0, ausencia de blush o densidad de contraste; 1, mínima densidad de contraste; 2, densidad de contraste moderada pero inferior a la obtenida durante la angiografía de una arteria contralateral o ipsolateral no relacionada con el infarto, y 3, densidad de contraste normal, comparable a la obtenida durante la angiografía de una arteria contralateral o ipsolateral no relacionada con el infarto; en caso de persistencia de densidad de contraste en la siguiente proyección se interpretó como escape del contraste al espacio extravascular, y se dio el valor de 09. La valoración del blush se realizó en todos los casos en fase subaguda (mediana 5 días, entre 3 y 7).
La valoración de las angiografías se realizó en 2 laboratorios independientes por cardiólogos intervencionistas experimentados en ambos casos. Los observadores desconocían el resto de la información clínica. El laboratorio 1 (Lab 1) es la institución en la que se llevó a cabo el estudio, el laboratorio de hemodinámica de un hospital universitario, y el laboratorio 2 (Lab 2), un laboratorio central independiente con amplia experiencia en la cuantificación de este índice. Se consideraron como perfusión normal los grados 2 y 310; también determinamos la variabilidad en caso de considerar como perfusión normal únicamente el grado blush 3. El análisis cuantitativo se llevó a cabo en el Lab 1 con el sistema digital Integris HM-3000 Philips (Holanda) y en el Lab 2 con el programa informático BlushPlus 2004 de Sanders Data System (Estados Unidos).
La variabilidad interobservador para la detección de blush 2-3 fue del 10%, y para blush 3 del 20% en el Lab 1, y del 13 y el 15%, respectivamente, en el Lab 2.
Ecografía miocárdica con inyección de contraste intracoronario
Inmediatamente tras el final de la toma de proyecciones angiográficas (del cateterismo prealta) se procedió a la realización de la EMC siguiendo el protocolo previamente descrito11-14. Se consideró una división en 17 segmentos15 y se asignó una puntuación de perfusión cuantitativa de los segmentos correspondientes al territorio del infarto (o zona de riesgo) mediante el programa informático MATLAB 6.511 (The Mathworks Inc., Natick, Massachusetts, Estados Unidos), con escala de videointensidad normalizada entre 0 (ausencia de perfusión) y 1 (perfusión normal). De acuerdo con nuestros datos previos12,13, se consideró un estudio normal cuando el score medio de perfusión en la zona del infarto era > 0,75. En función de nuestra experiencia11-14 y de datos previos16, la EMC se consideró como técnica de referencia para el análisis de la perfusión.
La variabilidad interobservador para detectar perfusión normal según los criterios definidos para EMC fue del 4%14.
Resonancia magnética cardiaca
La RMC (Sonata 1.5 T, Siemens, Alemania) se realizó a los 6 meses del infarto en todos los casos en un laboratorio independiente, sin ningún conocimiento de los datos clínicos o angiográficos. Se adquirieron las imágenes con una bobina de superficie, sincronismo cardiaco prospectivo y apnea respiratoria. Se adquirieron secuencias funcionales de cine (True Fast Imaging in Steady-state Precession) a lo largo del ventrículo izquierdo en diferentes proyecciones, y la fracción de eyección se calculó mediante el trazado manual de los contornos telediastólico y telesistólico en múltiples zonas del eje corto en las secuencias de cine (con un grosor por corte de 6 mm) con el software QMASS MR 6.1.5, Medis17.
La variabilidad interobservador para la fracción de eyección en términos absolutos fue del 3 ± 2%14.
Análisis estadístico
Las variables continuas se expresaron como media ± desviación estándar y se compararon mediante el test de la t de Student para datos no emparejados. Las variables categóricas se expresaron como porcentajes de la población a estudio y se compararon mediante el test de la χ².
Se calculó el coeficiente de correlación intraclase y el índice kappa entre los 2 laboratorios para determinaciones de blush. Se muestran las gráficas de Bland-Altman. Se calculó el índice de correlación de la perfusión valorada mediante blush en el laboratorio central con la perfusión por EMC y con la fracción de eyección al sexto mes del infarto mediante el cálculo del coeficiente de correlación de Spearman.
Todos los cálculos se realizaron utilizando el paquete estadístico SPSS 9.0 (Chicago, Estados Unidos). Se consideraron estadísticamente significativos los valores de p < 0,05.
RESULTADOS
En la tabla 1 se exponen las características basales de la muestra del estudio.
La elevación máxima del segmento ST en el primer ECG fue de 6 ± 3,4 mm y la elevación media, de 3,6 ± 2,2 mm. La elevación máxima a los 90 min de la trombólisis fue de 2,5 ± 1,9 mm (p < 0,0001 respecto al primer ECG) y la elevación media, de 1,6 ± 2 mm (p < 0,0001 respecto al primer ECG). El porcentaje de resolución de la elevación máxima del segmento ST a los 90 min fue del 52 ± 35% y el de la elevación media del ST fue del 49 ± 64%.
La fracción de eyección media en la primera semana fue del 48 ± 12% y en el sexto mes, del 52 ± 13% (p = 0,007 frente a la primera semana). La estenosis residual inicial fue del 87 ± 15% y al finalizar el cateterismo (y la angioplastia si se realizó), del 11 ± 26% (p < 0,0001 frente a la inicial).
Mediante blush se clasificó a 31 pacientes (78%) como perfusión normal para el criterio de normalidad de 2-3 en ambos laboratorios, mientras que para el criterio de normalidad de blush 3 se clasificó a 23 pacientes (57%) como perfusión normal en el Lab 1 y a 27 (67%) en el Lab 2 (tabla 2).
La media de valores obtenidos fue blush 2,2 ± 1,1 en el Lab 1 y 2,4 ± 1 en el Lab 2.
No hubo diferencias entre los infartos anteriores e inferiores en cuanto al blush (2,5 ± 0,9 frente a 2,2 ± 0,9; p = 0,3). Sin embargo, y de acuerdo con datos previos que indican una mejor perfusión en los infartos inferiores que en los anteriores, el MCE fue peor en los infartos anteriores (0,75 ± 0,27 frente a 0,96 ± 0,1; p = 0,01).
El TIMI frame count corregido fue de 20,5 ± 6,3 en el Lab 1 y 22,4 ± 9,7 en el Lab 2.
Variabilidad en la medición
La correlación detectada entre los resultados de los 2 laboratorios fue escasa (coeficiente de correlación intraclase, r = 0,38; p = 0,006). La concordancia en la valoración del blush miocárdico 2-3 fue del 80%, lo que se tradujo en un índice kappa de 0,43. En el caso de tomar como normal blush 3, la concordancia era del 55%, con un índice kappa de 0,1 (fig. 1; tabla 2). La variación media entre el grado blush del Lab 1 y el Lab 2 fue de 0,72 ± 0,88 (variación porcentual del 41 ± 57%).
Fig. 1. Gráfica de Bland-Altman que muestra la dispersión entre los dos laboratorios para la valoración de blush. DE: desviación estándar; Lab 1: laboratorio 1; Lab 2: laboratorio 2.
Correlación entre la perfusión valorada mediante blush y mediante ecocardiografía miocárdica con inyección de contraste intracoronario
Mediante EMC detectamos a 14 pacientes (34%) con ausencia de perfusión miocárdica adecuada. El blush miocárdico analizado en el laboratorio central no mostró correlación significativa con la perfusión valorada mediante EMC (r = 0,23; p = 0,2 para blush 2-3).
Implicaciones de los datos angiográficos en la función sistólica
Se observó una correlación positiva y significativa entre la fracción de eyección calculada mediante RMC al sexto mes y el grado de perfusión miocárdica calculado mediante EMC (r = 0,67; p < 0,0001); sin embargo, no se encontró dicha correlación con la perfusión calculada mediante blush en el laboratorio central (r = 0,20; p = 0,3 para blush 2-3) (fig. 2).
Fig. 2. Relación de perfusión miocárdica medida por EMC y blush (en el laboratorio central) con la fracción de eyección al sexto mes analizada mediante RMC. EMC: ecocardiografía miocárdica con inyección de contraste intracoronario; FE-6 m: fracción de eyección a los 6 meses; RMC: resonancia magnética cardiaca.
DISCUSION
Estudios previos han confirmado la relevancia pronóstica de la reperfusión en el contexto de IAMEST1-3. Aunque una arteria coronaria permeable con flujo TIMI 3 parece una condición indispensable para una perfusión adecuada, no la garantiza. Por tanto, se requieren métodos adicionales para determinar el estado de la microcirculación9,10.
En nuestra evaluación del blush miocárdico observamos: a) una variabilidad considerable en las mediciones entre un hospital universitario y un laboratorio central independiente para identificar blush 3; b) una baja correlación con la EMC, y c) una baja correlación con la fracción de eyección tardía.
Variabilidad en la medición
Al analizar a un grupo de pacientes con un primer IAMEST con arteria abierta, la correlación en la valoración de los 2 laboratorios fue significativa, aunque escasa.
Estos datos están en la línea de la sensación subjetiva detectada en muchos laboratorios de hemodinámica e indican que, aunque el análisis del blush es de gran interés para determinar el estado de la perfusión más allá del flujo TIMI (de probada utilidad en grandes estudios), se debe tener en consideración la importante variabilidad que hemos hallado en las medidas de un laboratorio periférico respecto a un laboratorio central.
Los valores de perfusión anormales se concentran de forma muy significativa en el grupo de pacientes con flujo TIMI < 39,16, lo que hace que en grandes series de pacientes que incluyan diferentes grados TIMI la correlación entre medidas de distintos observadores sea superior. En los trabajos publicados sobre el blush, la aparente facilidad para excluir la perfusión normal en pacientes con flujo TIMI 1 o 2 hace que la concordancia interobservador en grupos heterogéneos sea superior a la encontrada en grupos de pacientes exclusivamente con flujo TIMI 3. Tenemos el ejemplo del artículo de Van't Hof et al9, en cuya serie, hasta un 98% de los pacientes con blush 2 o 3 tenía flujo TIMI 3.
Nuestros resultados muestran una concordancia aceptable en la diferenciación de blush 2-3 de 0-1 (80%). Este fenómeno (mayor concordancia cuando se considera en conjunto grados moderados y severos) también se ha encontrado en otras estimaciones visuales, como en el caso de regurgitaciones valvulares mediante ecocardiografía o angiografía18. Sin embargo, para blush 3 --los pacientes con mejor pronóstico7--, la concordancia obtenida ha sido escasa (55%).
La escasa concordancia en las medidas de los índices angiográficos ha sido observada recientemente en otros parámetros angiográficos en apariencia más fáciles de cuantificar (porcentaje de estenosis)19.
En la actulalidad, el análisis del blush se centra sobre todo en estudios multicéntricos, que analizan los angiogramas en laboratorios centrales. La menor experiencia en el laboratorio periférico puede haber sido la causa de la baja concordancia en el presente estudio. Nuestros resultados refuerzan la necesidad de analizar el blush en laboratorios centrales independientes. Parece recomendable agrupar los niveles 2 y 3 como perfusión normal para reducir la variabilidad20.
Correlación con la ecocardiografía miocárdica con inyección intracoronaria de contraste
La EMC permite valorar de manera precisa el estado de la perfusión (fig. 3); su utilidad en la predicción del remodelado y la recuperación sistólica ha sido demostrada con anterioridad21. Esta técnica se ha indicado como de referencia para el estudio de la perfusión11,13,16, aunque su carácter invasivo ha limitado su uso y su popularidad entre los ecocardiografistas. Atribuimos la escasa correlación hallada entre blush y EMC a: a) falsos positivos por la difícil separación de los territorios irrigados por una arteria en diferentes segmentos en angiografía, ya que la opacificación de zonas con una perfusión adecuada puede enmascarar zonas con la perfusión alterada, mientras que el estudio de los segmentos mediante EMC es más fácil, y b) falsos negativos por la dificultad en la valoración visual, sobre todo en algunos casos en el territorio anterior. De hecho, nuestros resultados no mostraron diferencias en la perfusión cuantificada mediante blush entre infartos anteriores e inferiores, mientras que el análisis del MCE demostró una peor perfusión de los segmentos infartados del territorio anterior.
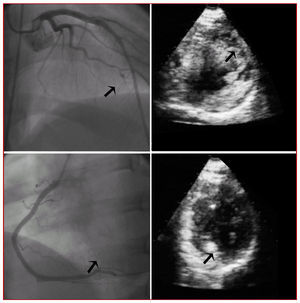
Fig. 3. Imágenes de angiografía y ecocardiografía miocárdica con inyección intracoronaria de contraste de 2 pacientes del grupo de estudio. En el panel superior se muestran imágenes de un paciente con un infarto anterior, flujo TIMI 3 en arteria descendente anterior (flecha) y déficit de perfusión en zona anterior mediante ecocardiografía (flecha). En el panel inferior un paciente con un infarto inferior, flujo TIMI 3 en arteria coronaria derecha (flecha) y perfusión normal en la zona del infarto (flecha).
Relación con la fracción de eyección a los 6 meses
El estado de la microcirculación miocárdica guarda una estrecha relación con la recuperación de la función sistólica en caso de integridad, o con el remodelado ventricular en caso de afección22. En nuestro estudio, la valoración de la perfusión mediante blush realizada inmediatamente tras la angioplastia (o al final del cateterismo en casos no terapéuticos) no se relacionó de forma significativa con la función sistólica tardía valorada de manera independiente mediante RMC. Quizá una estimación de la perfusión en fases más tardías del infarto podría mejorar esta correlación23, aunque en este sentido debemos recordar que la EMC se realizó simultáneamente con el cateterismo, y sí constituyó un buen predictor de la fracción de eyección.
Estos datos podrían indicar que en un paciente con flujo TIMI 3 claro deberíamos buscar índices alternativos (o complementarios) al blush miocárdico como patrón de referencia de perfusión.
Limitaciones
1. La principal limitación es el escaso número de pacientes incluidos en el estudio, que se ve dificultado por los estrictos criterios de selección de los pacientes y por la necesidad de realizar pruebas adicionales a las empleadas en la práctica clínica diaria.
2. Otro aspecto que cabe señalar es el hecho de que nuestro estudio no se centre en la valoración de la perfusión tras una angioplastia primaria sino en fase subaguda, mientras que en la mayoría de los estudios que analizan perfusión miocárdica la angiografía se realizó entre 60 y 90 min tras la administración del trombolítico. Sin embargo, estas diferencias no deberían afectar a la variabilidad en las mediciones entre diferentes observadores. Como ya se ha mencionado, este factor tampoco afectó a la predicción de la fracción de eyección tardía mediante EMC.
3. El uso de diferente software al realizar las mediciones probablemente ejerció una influencia en los resultados finales; en cualquier caso, este hecho es inevitable en la práctica diaria a la hora de comparar resultados entre diferentes laboratorios.
4. Para la valoración cuantitativa de los parámetros angiográficos hubiera sido interesante la cuantifiación de la perfusión según el sistema TIMI myocardial perfusion, por tratarse de una medida ampliamente validada; nosotros realizamos una estimación cuantitativa mediante el TIMI frame count.
CONCLUSIONES
Tras un IAMEST, la angiografía mediante el índice TIMI constituye globalmente el mejor índice para el análisis de la perfusión. El índice blush ha mostrado su utilidad en múltiples estudios multicéntricos para una mejor definición del estado de la perfusión. Nuestros resultados indican que, en pacientes con TIMI 3 claro, hay una variabilidad conable entre un laboratorio periférico y uno central. La consideración de normalidad para los grados 2 y 3 reduce esta variabilidad, pero en cualquier caso parece aconsejable realizar este análisis en laboratorios centrales muy experimentados. La baja correlación detectada entre la función sistólica tardía y la perfusión analizada mediante EMC señala la necesidad de avanzar hacia una valoración angiográfica de la microcirculación mediante análisis cuantitativo, validada en laboratorios centrales independientes, o bien plantear el uso de métodos alternativos.
Trabajo financiado por la Sociedad Española de Cardiología con la beca Bayer 2004 y por la Generalitat Valenciana con la beca GRUPOS0442.
Correspondencia: Dr. V. Bodí Peris.
Hospital Clínico Universitario de Valencia. Servicio de Cardiología.
Blasco Ibáñez, 17. 46010 Valencia. España.
Correo electrónico: vicentbodi@hotmail.com
Recibido el 27 de octubre de 2005.
Aceptado para su publicación el 2 de marzo de 2006.