La terapia de resincronización cardiaca en pacientes con fibrilación auricular (FA) requiere un estricto control de la frecuencia ventricular para asegurar un porcentaje de estimulación biventricular lo más cercano posible al 100% y que permita una adecuada respuesta a la terapia1. Para ello se utilizan fármacos frenadores de la conducción auriculoventricular (AV) y, cuando estos fracasan, se indica la ablación del nódulo AV, lo cual conlleva que el paciente se haga dependiente de marcapasos. Se presenta el caso de un paciente en FA permanente portador de un resincronizador, en el que se utilizó ivabradina como alternativa a la ablación del nódulo AV para el control de la frecuencia cardiaca.
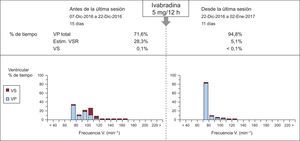
Se trata de un varón de 60 años portador de una prótesis mitral mecánica por una estenosis mitral reumática, en FA permanente conducida con bloqueo de rama izquierda. Durante su evolución presentó disfunción sistólica grave del ventrículo izquierdo e insuficiencia cardiaca en ausencia de lesiones coronarias, motivo por el cual se le implantó un desfibrilador-resincronizador. En las revisiones posteriores al implante, se comprobó un 74% de estimulación biventricular pese a haber escalado el bisoprolol a la dosis máxima tolerada (5 mg/12 h) y programar el dispositivo en VVIR con una frecuencia mínima de 70 lpm. No se añadió digoxina por antecedentes de intoxicación digitálica e insuficiencia renal. Se decidió realizar un intento terapéutico con ivabradina (5 mg/12 h) antes de plantear la ablación del nódulo AV. Once días después el dispositivo mostraba un porcentaje de estimulación biventricular del 95% (figura). En una nueva revisión realizada 1 mes después de iniciar la ivabradina, la estimulación se mantenía en el 96%, por lo que no fue necesario realizar la ablación.
Registro del resincronizador en 2 revisiones consecutivas del dispositivo (antes y después de iniciar ivabradina oral). Se observa que el porcentaje de estimulación biventricular asciende del 71,6 al 94,8% tras 11 días del tratamiento con ivabradina. El porcentaje de ritmo ventricular intrínseco (no resincronizado) se expresa como VS y Estim. VSR, que corresponde a un algoritmo de estimulación en respuesta a los latidos ventriculares detectados. Estim. VSR: ventricular sensing response (respuesta a la detección ventricular); VP: ventricular pacing (estimulación ventricular); VS: ventricular sensing (detección ventricular).
La ivabradina es un inhibidor de la corriente If, principal determinante de la frecuencia de descarga del nódulo sinusal. Su efecto beneficioso como fármaco bradicardizante en pacientes en ritmo sinusal está claramente demostrado, tanto en enfermedad coronaria como en insuficiencia cardiaca.
Sin embargo, el canal de sodio que determina la corriente If no se encuentra exclusivamente en el nódulo sinusal, sino que también está presente en altas concentraciones tanto en el nódulo AV compacto como en sus extensiones posteronodulares2. La corriente If, además de determinar el automatismo del marcapasos nodular subsidiario, al parecer también está directamente relacionada con las propiedades de conducción del nódulo AV (dromotropismo). En un ensayo clínico en el que se administró un inhibidor de la corriente If (zatebradina) o placebo a pacientes sin cardiopatía estructural, el fármaco produjo un alargamiento significativo de los parámetros electrofisiológicos de conducción nodular (intervalo AH, periodo refractario efectivo AV y longitud de ciclo de Wenckebach)3. Más recientemente, se ha comprobado que la ivabradina también tiene este efecto depresor de la conducción nodular. En un estudio experimental en modelo animal publicado por Verrier et al.4, la administración de ivabradina durante el ritmo auricular estimulado produjo un alargamiento de los intervalos PR y AH que fue más marcado a frecuencias de estimulación auricular rápidas (dependencia de uso), sin alterar la conducción en el sistema His-Purkinje ni el intervalo QT. Cuando se administró el fármaco durante la FA, se observó una reducción de la respuesta ventricular sin alterar las frecuencias dominantes en las aurículas.
Hay menos experiencia publicada con ivabradina como fármaco para el control de la respuesta ventricular durante FA en humanos. En una pequeña serie de casos, la administración oral de ivabradina mejoró el control de la respuesta ventricular y la capacidad funcional en 4 de 6 pacientes con FA rápida sintomática a pesar del tratamiento con bloqueadores beta5. Más recientemente, un ensayo clínico con 32 pacientes con FA mostró que la ivabradina produce una reducción estadísticamente significativa de las frecuencias cardiacas media y máxima frente a placebo, sin cambios relevantes en la frecuencia cardiaca mínima tras 1 mes de tratamiento6.
La disponibilidad de fármacos para el control de la frecuencia cardiaca para los pacientes con disfunción ventricular es muy escasa, lo que conlleva indicar la ablación del nódulo AV en muchos casos. La seguridad de ivabradina, demostrada en grandes ensayos clínicos con pacientes en riesgo (enfermedad coronaria e insuficiencia cardiaca), sumada a la ausencia de efectos vasodilatadores o depresores de la contractilidad miocárdica, la convierten en un fármaco prometedor para el control de la respuesta ventricular de los pacientes con FA. La inclusión de ivabradina en el arsenal de fármacos frenadores de la conducción nodular debería respaldarse en ensayos clínicos realizados ad hoc.