El drenaje venoso pulmonar anómalo total representa el 1,5% de todas las cardiopatías congénitas1. Aunque la mortalidad posquirúrgica total ha disminuido hasta un 10%, en los casos en que se produce una obstrucción venosa postoperatoria, la mortalidad aumenta hasta un 40-60%1,2. Dicha obstrucción puede producirse en la anastomosis del colector a la aurícula o en los ostium de las venas pulmonares.
Para su tratamiento se ha empleado la dilatación con balón o el implante de stents en los ostium de las venas pulmonares3,4, aunque actualmente la técnica quirúrgica sutureless se considera de elección5.
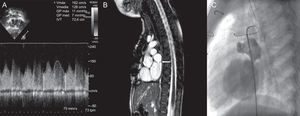
Presentamos el caso de un niño de 4 años, diagnosticado al mes de vida de drenaje venoso pulmonar anómalo total no obstructivo supradiafragmático, en el que las venas pulmonares confluían en un colector común que drenaba en la vena innominada. Se realizó cirugía correctora a los 2 meses anastomosando el colector al techo de la aurícula izquierda. El postoperatorio transcurrió sin complicaciones. Pasados 2 años, la ecocardiografía mostró una posible estenosis en la anastomosis (figura 1A), que se confirmó en la resonancia magnética (figura 1B).
A: ecocardiografía con Doppler pulsado en anastomosis, con pérdida del patrón bifásico en el flujo venoso pulmonar y gradiente medio de 7mmHg. B: plano sagital de resonancia magnética cardiaca; estenosis en la anastomosis, con diámetro de 6,6mm (flecha). C: angiografía (proyección lateral); colector dilatado conectado al techo de la aurícula izquierda a través de un orificio estenosado. GP: gradiente de presión; IVT: integral tiempo velocidad; lpm: latidos por minuto; Vmáx: velocidad máxima; Vmedia: velocidad media.
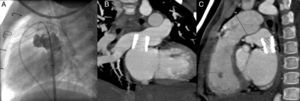
Se realizó un cateterismo cardiaco por vía venosa femoral, con perforación por radiofrecuencia del tabique interauricular. La presión pulmonar era 27/15 (25) mmHg; la presión aórtica, 63/40 (50) mmHg, y la de enclavamiento pulmonar, 18mmHg, con un gradiente entre el colector y la aurícula izquierda de 7mmHg. En la angiografía se objetivó dilatación de las venas pulmonares y del colector, con un diámetro en la anastomosis con la aurícula izquierda de 6,1mm (figura 1C). Se realizó angioplastia con un catéter balón Cristal Balloon de 15×25mm, que fue ineficaz, y se decidió implantar un stent en la anastomosis. Sobre una guía Amplatz Super-Stiff™ de 0,035” y una vaina de Mullins de 9 Fr, se avanzó un IntraStent® LD Mega™ de 16mm montado sobre un BIB® (balloon-in-balloon) catheter de 14×35mm, que se implantó en la anastomosis (figura 2A). El gradiente entre el colector y la aurícula izquierda bajó hasta 2mmHg. No hubo complicaciones y se inició tratamiento con ácido acetilsalicílico y clopidogrel.
En los ecocardiogramas de control persistía la dilatación de las venas pulmonares, con un leve aumento en la velocidad, pero se mantenía el patrón bifásico en el flujo de las venas pulmonares. A los 2 años del procedimiento, se realizó una angiografía por tomografía computarizada de control, en la que se sospechó una estenosis por el ángulo del stent con las venas pulmonares derechas (figuras 2B y C), por lo que se realizó un nuevo cateterismo cardiaco. La presión media pulmonar era de 15mmHg; la presión media aórtica, 54mmHg, y la presión de enclavamiento pulmonar, 11mmHg, igual a la telediastólica del ventrículo izquierdo. Se realizó un ecocardiograma transesofágico, que mostró un flujo laminar a través del stent y entre las celdillas, sin proliferación endotelial. Ante la ausencia de datos objetivos de estenosis, se decidió mantenerse a la espera y continuar a largo plazo la doble antiagregación para evitar el riesgo de tromboembolias.
La obstrucción venosa postoperatoria tras la corrección quirúrgica del drenaje venoso pulmonar anómalo total es una grave complicación, sobre todo en los casos en que se presenta precozmente, es bilateral y afecta a los ostium de las venas pulmonares1,2. En estos casos se produce una proliferación endotelial que estrecha la luz de las venas pulmonares y suele recurrir tras el implante de stents o cirugía reparativa clásica2–4. Nuestro paciente está en el espectro de mejor pronóstico de este cuadro, ya que la obstrucción venosa postoperatoria se desarrolló a los 2 años de la cirugía y afectaba solo a la anastomosis, por lo que pensamos que la implantación de un stent de gran tamaño lejos de los ostium de las venas pulmonares no promovería la proliferación endotelial. En la evolución, la luz del stent y sus celdillas laterales se han mantenido permeables, lo que respalda nuestra hipótesis.
Hasta nuestro conocimiento se trata del primer caso de implantación con éxito de un stent para la resolución de una obstrucción venosa postoperatoria a nivel de la anastomosis. El seguimiento es corto, por lo que en el futuro podría desarrollarse una estenosis en el stent, pero la posibilidad de dilatarlo hasta los 22mm permite un amplio margen de intervención y, si en algún momento se considerase la cirugía, retirar el stent no debería plantear dificultades.
En conclusión, planteamos que en las obstrucciones venosas postoperatorias de tipo anastomótico tras la cirugía de drenaje venoso pulmonar anómalo total, implantar stents puede ser de utilidad para evitar la reoperación, al menos a corto y medio plazo.