Palabras clave
INTRODUCCIÓN
El estudio clínico de la fibrilación ventricular (FV) siempre ha encontrado el obstáculo de su aparición imprevista y el corto tiempo que el organismo es capaz de soportarla; por todo ello, el registro de la señal de la FV es complicado y difícil de obtener, y se dispone únicamente de escasas referencias en la literatura de FV espontáneas con registro electro-cardiográfico1. Recientemente se han descrito casos de ablación con éxito de las extrasístoles ventriculares que desencadenan los episodios de FV en situaciones de tormentas arrítmicas2-7, lo que aumenta el interés en conocer el modo de inicio de la FV. Los desfibriladores implantables (DAI) permiten almacenar los episodios arrítmicos, y su análisis permite avanzar en el estudio de los mecanismos de inicio de la FV. Con el objetivo de estudiar el modo de inicio de la FV que aparece de modo aislado o cuando lo hace de modo repetido en el transcurso de las tormentas arrítmicas, hemos analizado los episodios de FV espontáneas almacenados en pacientes portadores de un DAI.
MÉTODOS
Hemos analizado los registros (campo cercano y lejano) de FV en 250 pacientes portadores de DAI pertenecientes a un hospital terciario, en el periodo comprendido entre los años 1997 y 2008. De los 250 pacientes, 13 presentaron al menos un episodio de FV. Los modelos de DAI analizados pertenecen a las series MINI y PRIZM de Guidant y GEM de Medtronic. En todos ellos estaba programada la opción de almacenar la señal previa al episodio de FV declarada. Hemos considerado FV los episodios con electrogramas sinusoidales, con morfología, ciclo y amplitud cambiantes, en los que no fue posible distinguir complejos QRS definidos y con registro bipolar verdadero o seudobipolar con señal característicamente fragmentada. Todos los episodios precisaron descarga eléctrica para su finalización, y se desechó los que se autolimitaron, que consideramos taquicardias ventriculares polimorfas y no se incluyeron en el estudio. Hemos definido ciclo corto-largo-corto cuando aparece en el ritmo de base una extrasístole (corto), seguida de una pausa (con intervalo de acoplamiento > 1,2 veces el intervalo precedente) y una despolarización prematura con acoplamiento corto (corto) que inicia la FV.
Hemos analizado la morfología en el canal de campo lejano y cercano, el intervalo de acoplamiento, el ciclo del latido sinusal precedente y la presencia de secuencia corto-largo-corto precediendo tanto a las extrasístoles que desencadenaron la FV (EV fibrilatoria) como las que no (EV no fibrilatorias). Hemos comparado el intervalo de acoplamiento y la longitud de ciclo del latido sinusal precedente de ambas extrasístoles mediante análisis estadístico de la t de Student para datos apareados.
RESULTADOS
En 13 pacientes (10 varones y 3 mujeres; edad, 49 ± 22 años) —diagnosticados 4 de ellos de síndrome de Brugada, 3 con cardiopatía isquémica, 1 con miocardiopatía hipertrófica, 2 miocardiopatía dilatada, 1 con torsades de pointes por EV con acoplamiento corto, 1 con fibroelastosis cardiaca y 1 con FV idiopática—, se registraron en total 31 episodios de FV espontáneas. En 7 pacientes la FV fue el motivo del implante; de ellos, 2 con cardiopatía isquémica, 2 con síndrome de Brugada, 1 con miocardiopatía hipertrófica, 1 con fibroelastosis cardiaca y 1 con torsades de pointes por EV con acoplamiento corto. La media de episodios por paciente fue de 2,5 (1-12). De los 31 episodios de FV, 14 fueron episodios aislados, y los demás estaban relacionados con una tormenta arrítmica. Tres pacientes presentaron tormentas arrítmicas. Todos los episodios analizados comenzaron con extrasístole ventricular, la cual fue de la misma morfología y similar intervalo de acoplamiento en los 7 pacientes que tuvieron más de un episodio (tiempo entre episodios: desde minutos hasta 3 años) (figs. 1 y 2). El intervalo de acoplamiento de la extrasístole osciló en torno a 409 ± 121 ms y el ciclo del latido sinusal precedente fue de 801 ± 233 ms. La presencia de ciclo largocorto en relación con el inicio de la FV sólo se observó en 2 casos de FV (9%). En 21 episodios, la FV estuvo precedida por EV en ritmo sinusal que no indujeron la FV. La morfología, el intervalo de acoplamiento (411 ± 123 ms) y el ciclo del latido sinusal precedente (793 ± 230 ms) no presentaron diferencias significativas con respecto a la EV inductora de FV.
Fig. 1. Inicio de un episodio de fibrilación ventricular en un paciente con torsades de pointes por extrasístole ventricular con acoplamiento corto.
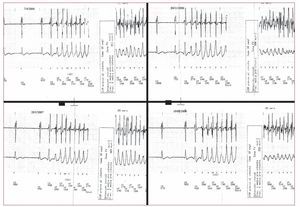
Fig. 2. Inicio de cuatro episodios de fibrilación ventricular en diferentes días correspondientes a un paciente con síndrome de Brugada. Obsérvese la morfología similar del extrasístole ventricular que desencadena la fibrilación ventricular.
DISCUSIÓN
La EV que precede al inicio de la FV se conoce desde hace tiempo, y se han descrito en casos de FV primaria en infarto agudo de miocardio8. Más recientemente se la ha considerado desencadenante de los episodios de FV en el marco de tormentas arrítmicas, y eliminarla mediante ablación ha evitado las recurrencias2-7.
En los trabajos pioneros en el estudio de las causas de muerte súbita ambulatoria1, los casos de FV precedida de EV supusieron únicamente el 8,28% y la gran mayoría de las FV (83,4%) se desencadenaron a partir de una taquicardia ventricular. El motivo de resultados tan dispares con los obtenidos por nosotros podría explicarse por el diferente modo de registro, Holter en los casos del estudio al que nos referimos y desde un DAI en los nuestros; suponemos que los posibles episodios de taquicardia ventricular que hubiesen degenerado en FV en nuestros pacientes fueron tratados con éxito mediante la terapia antitaquicárdica del DAI, la cual se ha demostrado efectiva en un elevado porcentaje de taquicardias ventriculares9,10.
A diferencia del inicio de las TV monomórficas, que sí se ha estudiado ampliamente en pacientes portadores de DAI11, existen escasos estudios que hayan analizado el inicio de la FV12,13. Entre ellos destaca el que ha estudiado este aspecto en pacientes tipo MADIT II (estudio de prevención primaria en pacientes con cardiopatía isquémica y disfunción ventricular)12. En ese estudio se observó que una EV inició el 77% de los episodios de FV, mientras que había secuencia corto-largo-corto en el 23% de los pacientes (14 episodios de un total de 60).
En pacientes con síndrome de Brugada, Kakishita et al14 describen el inicio de la FV con EV e incluyen una figura en su artículo que de modo característico presenta tres episodios de FV en diferentes momentos con EV similares en su morfología; esta constancia en las características de la EV inductora de FV también la hemos observado en nuestros pacientes.
Aunque el tiempo almacenado del registro previo a la FV es corto, a menudo se observaron durante EV que no indujeron la FV y presentaron características morfológicas y eléctricas similares en cuanto a su intervalo de acoplamiento, por lo que se puede hablar del concepto de extrasistolia fibrilatoria y no fibrilatoria, coincidentes en un corto lapso. En el registro de muerte súbita ambulatoria se decribe también un aumento significativo del número de EV en la hora previa a la FV1.
Se desconoce el motivo por el que unas extrasístoles desencadenan la FV y otras no sin que aparentemente tengan características electrofisiológicas diferentes. El hecho de que la extrasistolia ventricular que desencadena la FV en diferentes etapas de la historia natural de un paciente tenga la misma morfología indica que en cada paciente las extrasístoles inductoras de FV tienen el mismo origen, lo cual podría ser de interés para planear el procedimiento de ablación de la FV de modo diferido, siempre y cuando se pudieran inducir.
Limitaciones
La limitación más importante del estudio es el escaso número de pacientes incluidos, en parte porque la incidencia de episodios espontáneos de FV es también baja.
Del mismo modo, al disponer únicamente de dos canales (campo cercano y lejano) para el análisis de los episodios, podría haber dificultades en algunos episodios para diferenciar la fibrilación de la taquicardia ventricular con ciclos muy rápidos. El pequeño número de episodios iniciados con secuencia largo-corto impide comparar las características de los dos tipos de inicio (acoplamiento, intervalo QT precedente, amplitud de onda T y de la frecuencia cardiaca previa).
Asimismo, la capacidad de discriminación morfológica de los canales de memoria almacenada del DAI no nos permite excluir que la EV inductora de la FV sea ligeramente diferente en los episodios en que se repitió la FV.
CONCLUSIONES
La FV espontánea se desencadena por EVs tanto en los casos de tormentas arrítmicas como en episodios aislados. En muchas ocasiones las extrasístoles preceden a la FV pero no la inducen. Todo ello indica que en cada paciente hay características específicas en el mecanismo desencadenante de la FV.
ABREVIATURAS
DAI: desfibrilador implantable.
EV: extrasístole ventricular.
FV: fibrilación ventricular.
Full English text available from: www.revespcardiol.org
Este manuscrito ha sido parcialmente financiado por el proyecto de investigación TEC2007-68096-C02-TCM del MEC.
Los resultados de este trabajo fueron presentados en parte en el XIII World Congress on Cardiac Pacing and Electrophysiology, Rome, Italy 2007 y publicados como abstract en Giornale Italiano di Aritmologia e Cardiostimulazione. 2007;10(3):109.
Correspondencia: Dr. J.J. Sánchez-Muñoz.
Unidad de Arritmias. Servicio de Cardiología. Hospital Universitario Virgen de la Arrixaca.
Ctra. Madrid-Cartagena, s/n. 30120 El Palmar. Murcia. España.
Correo electrónico: juanjosanchezmunoz@me.com
Recibido el 14 de diciembre de 2009.
Aceptado para su publicación el 25 de enero de 2010.