Los estudios económicos pueden ayudar a tomar decisiones en el tratamiento de la enfermedad multivaso en el infarto. Se planteó realizar una evaluación económica del ensayo clínico CROSS-AMI (Complete Revascularization or Stress Echocardiography in Patients With Multivessel Disease and ST-Segment Elevation Acute Myocardial Infarction).
MétodosSe realizó un análisis de comparación de costes económicos de las estrategias (revascularización angiográfica completa [RCom] y revascularización selectiva guiada por isquemia en ecocardiograma de estrés [RSel]) comparadas en el ensayo clínico CROSS-AMI (N=306), derivados de la hospitalización inicial y del primer año de seguimiento, según las tarifas oficiales vigentes en nuestro sistema de salud.
ResultadosEl coste de la hospitalización inicial resultó superior en el grupo de RCom que en la rama de RSel (19.657,9±6.236,8 frente a 14.038,7±4.958,5 euros; p <0,001). No hubo diferencias entre ambos grupos en el coste del primer año de seguimiento (RCom, 2.423,5±4.568,0 euros; Rsel, 2.653,9±5.709,1 euros; p=0,697). El coste total fue 22.081,3±7.505,6 euros en la rama de RCom y 16.692,6±7.669,9 euros en la rama de RSel (p <0,001).
ConclusionesEn el ensayo clínico CROSS-AMI, el sobrecoste inicial de la RCom frente a la RSel no se vio compensado por un ahorro significativo en el seguimiento. La RSel parece ser una estrategia más eficiente que la RCom para los pacientes con síndrome coronario agudo con elevación del segmento ST y enfermedad multivaso tratados mediante angioplastia emergente.
Estudio registrado en ClinicalTrials.gov (Identificador: NCT01179126).
Palabras clave
Las enfermedades cardiovasculares, con el infarto agudo de miocardio a la cabeza, son la principal causa de mortalidad en los países occidentales1,2. La intervención coronaria percutánea (ICP) es el método de reperfusión de elección en el síndrome coronario agudo con elevación persistente del segmento ST (SCACEST)3. Aproximadamente un 40-60% de los pacientes con SCACEST presentan enfermedad coronaria multivaso y tienen un peor pronóstico clínico4,5.
Actualmente se recomienda considerar la revascularización de las lesiones coronarias no culpables, sobre todo por la reducción del riesgo de revascularizaciones, muerte e infarto tras el alta hospitalaria3,6. No obstante, en estos ensayos clínicos la rama conservadora lo es excesivamente, pues se revasculariza únicamente la lesión culpable del evento sin tener en cuenta la posible repercusión funcional de las lesiones no culpables. De hecho, esto podría sobrestimar el beneficio real de la revascularización completa7.
Si bien la toma de decisiones se debe basar en el perfil clínico de los pacientes y la eficacia y la seguridad de las intervenciones, los estudios de evaluación económica, al incorporar la valoración de los costes a dicho proceso, resultan útiles en situaciones complejas, especialmente cuando los recursos son limitados8,9.
El tratamiento de la enfermedad multivaso en el SCACEST presenta la situación idónea para la evaluación económica sanitaria, pues es complejo y costoso y aún hay aspectos por aclarar antes de recomendar la revascularización completa sistemática, como la forma óptima de seleccionar lesiones no culpables7.
Se plantea realizar una evaluación económica dentro del ensayo clínico CROSS-AMI (Complete Revascularization or Stress Echocardiography in Patients With Multivessel Disease and ST-Segment Elevation Acute Myocardial Infarction).
MÉTODOSDiseño del estudio CROSS-AMIComo se ha descrito anteriormente10, el estudio clínico CROSS-AMI fue un ensayo clínico multicéntrico aleatorizado que comparó una estrategia de revascularización anatómica completa de todas las lesiones coronarias no culpables durante el ingreso inicial (RCom) con una estrategia de revascularización guiada por isquemia detectada mediante ecocardiografía de estrés (RSel) en pacientes con SCACEST y enfermedad multivaso10. El Comité de Ética aprobó el estudio, que siguió las directrices de la Declaración de Helsinki (referencia 2010/160) y se registró en ClinicalTrials.gov con el identificador NCT01179126.
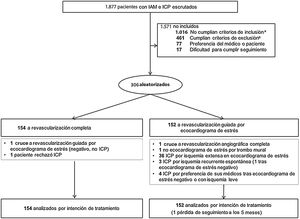
Entre octubre de 2010 y octubre de 2015, se incluyó a 306 pacientes en nuestro centro. Todos los pacientes firmaron el consentimiento informado. Brevemente, los pacientes con SCACEST tratados mediante ICP urgente de la lesión culpable del infarto eran elegibles si presentaban una estenosis significativa (del 70% por estimación visual) en al menos otra arteria coronaria diferente de la oclusión culpable del evento (criterios de inclusión y exclusión del material adicional) y se los aleatorizó mediante un sistema de números seudoaleatorios en las primeras 48 h tras la ICP inicial. En la RCom (n=154), se programó un segundo procedimiento de ICP para tratar todas las lesiones coronarias significativas antes del alta. No se empleó la guía de presión para seleccionar qué lesiones tratar. A los pacientes de la estrategia RSel (n=152) se les realizó un ecocardiograma de estrés (en esfuerzo o con dobutamina) durante la hospitalización inicial. Dentro del protocolo, se indicaba la realización de ICP de lesiones en arteria no culpable del infarto en caso de isquemia recurrente espontánea, así como de las lesiones coronarias con evidencia de isquemia a bajas cargas (< 120 lpm) o en más de 2 segmentos coronarios (figura 1).
Diagrama de flujo del ensayo clínico CROSS-AMI. ARI: arteria responsable del infarto; IAM: infarto agudo de miocardio; ICP: intervención coronaria percutánea. aPor enfermedad coronaria de 1 vaso (n=904), ICP multivaso inicial (n=82) e ICP inicial subóptima (n=30). bAnatomía inadecuada para ICP de lesiones distintas de la ARI (n=245), enfermedad significativa del tronco común izquierdo (n=70), shock cardiogénico (n=73), comorbilidad grave (n=57), cirugía de revascularización coronaria previa (n=4) y trombosis de stent coronario como causa del IAM (n=12).
Se realizó un análisis de minimización o comparación de costes económicos de las 2 estrategias estudiadas en el ensayo clínico CROSS-AMI. En este tipo de análisis, se parte de la base de que ambas estrategias tienen una eficacia similar y se estiman y comparan sus respectivos costes económicos.
En primer lugar, desde la perspectiva del sistema público de salud de nuestra comunidad autónoma, se estimó el coste económico de la hospitalización inicial, que se definió como la suma de los costes de la estancia hospitalaria, la ICP urgente, la coronariografía, los nuevos procedimientos percutáneos de revascularización y las pruebas diagnósticas cardiológicas realizadas durante dicho ingreso. Se estimó el coste del seguimiento, que se definió como la suma de los costes de la estancia hospitalaria, la realización de pruebas diagnósticas cardiológicas y los nuevos procedimientos de revascularización durante los reingresos hospitalarios (por causa cardiovascular y no cardiovascular) durante el primer año de seguimiento.
Para ello, se determinaron las duraciones de las estancias hospitalarias del ingreso índice y los reingresos en los primeros 12 meses. Se cuantificaron los procedimientos diagnósticos y terapéuticos cardiológicos realizados tanto durante la hospitalización inicial como en los reingresos. La imputación de costes se basó en el decreto que establece las tarifas de los servicios sanitarios prestados por los centros dependientes de nuestro sistema de salud11 (tabla 1).
Costes económicos de la hospitalización y los procedimientos cardiológicos11
| Coste (euros) | |
|---|---|
| Hospitalización | |
| Estancia en unidad coronaria o unidad de cuidados intensivos (por día) | 1.142,47 |
| Estancia en unidad de hospitalización (por día) | 528,95 |
| Procedimientos no invasivos | |
| Ecocardiograma | 321,64 |
| Ergometría | 310,76 |
| Ecocardiograma de estrés con ejercicio o farmacológico | 377,67 |
| SPECT de perfusión miocárdica | 294,32 |
| Procedimientos invasivos | |
| Coronariografía | 1.055,38 |
| Coronariografía y angioplastia con balón | 3.325,31 |
| Coronariografía, angioplastia con balón e implante de stent | 6.856,31 |
SPECT: tomografía computarizada por emisión monofotónica.
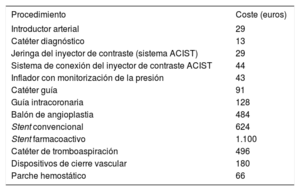
De modo complementario, se realizó un análisis detallado del consumo de material fungible. El sistema de tarifas que aplica nuestro servicio de salud es genérico, tiene en cuenta el gasto en personal, el mantenimiento de las instalaciones y un coste promediado del material. No computa exhaustivamente el coste de los dispositivos empleados en la ICP (introductores, catéteres, guías, balones, stents, etc.). Durante el ensayo, se recogió prospectivamente el material empleado en las diferentes ICP realizadas en el ingreso inicial como parte del protocolo del estudio. Se determinó su coste en función de los precios pagados por nuestro centro, facilitados por el servicio de compras (tabla 2).
Coste del material fungible
| Procedimiento | Coste (euros) |
|---|---|
| Introductor arterial | 29 |
| Catéter diagnóstico | 13 |
| Jeringa del inyector de contraste (sistema ACIST) | 29 |
| Sistema de conexión del inyector de contraste ACIST | 44 |
| Inflador con monitorización de la presión | 43 |
| Catéter guía | 91 |
| Guía intracoronaria | 128 |
| Balón de angioplastia | 484 |
| Stent convencional | 624 |
| Stent farmacoactivo | 1.100 |
| Catéter de tromboaspiración | 496 |
| Dispositivos de cierre vascular | 180 |
| Parche hemostático | 66 |
Las variables continuas se presentan como media±desviación típica. Las variables categóricas se expresan en frecuencia absoluta y relativa. Específicamente, los costes se expresan en valor medio por paciente, con su desviación típica. Las variables categóricas se compararon mediante la prueba de la χ2 o el test exacto de Fisher y las variables cuantitativas, mediante la t de Student o la U de Mann-Whitney si su distribución no era normal. Para el análisis estadístico se empleó el programa SPSS (versión 24.0, IBM). Se consideró como resultado estadísticamente significativo p <0,05 para un contraste bilateral.
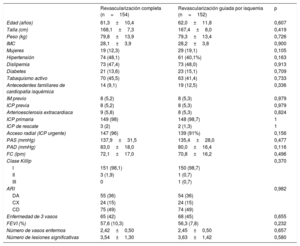
RESULTADOSParticipantesSe aleatorizó en total a 306 pacientes, cuyas características basales se presentan en la tabla 3. No hubo diferencias significativas entre los 2 grupos del estudio en factores de riesgo cardiovascular, antecedentes médicos o presentación clínica del infarto.
Características basales de la población
| Revascularización completa (n=154) | Revascularización guiada por isquemia (n=152) | p | |
|---|---|---|---|
| Edad (años) | 61,3±10,4 | 62,0±11,8 | 0,607 |
| Talla (cm) | 168,1±7,3 | 167,4±8,0 | 0,419 |
| Peso (kg) | 79,8±13,9 | 79,3±13,4 | 0,726 |
| IMC | 28,1±3,9 | 28,2±3,8 | 0,900 |
| Mujeres | 19 (12,3) | 29 (19,1) | 0,105 |
| Hipertensión | 74 (48,1) | 61 (40,1%) | 0,163 |
| Dislipemia | 73 (47,4) | 73 (48,0) | 0,913 |
| Diabetes | 21 (13,6) | 23 (15,1) | 0,709 |
| Tabaquismo activo | 70 (45,5) | 63 (41,4) | 0,733 |
| Antecedentes familiares de cardiopatía isquémica | 14 (9,1) | 19 (12,5) | 0,336 |
| IM previo | 8 (5,2) | 8 (5,3) | 0,979 |
| ICP previa | 8 (5,2) | 8 (5,3) | 0,979 |
| Arterioesclerosis extracardiaca | 9 (5,8) | 8 (5,3) | 0,824 |
| ICP primaria | 149 (98) | 148 (98,7) | 1 |
| ICP de rescate | 3 (2) | 2 (1,3) | 1 |
| Acceso radial (ICP urgente) | 147 (96) | 139 (91%) | 0,156 |
| PAS (mmHg) | 137,9±31,5 | 135,4±28,0 | 0,477 |
| PAD (mmHg) | 83,0±18,0 | 80,0±16,4 | 0,116 |
| FC (lpm) | 72,1±17,0 | 70,8±16,2 | 0,496 |
| Clase Killip | 0,370 | ||
| I | 151 (98,1) | 150 (98,7) | |
| II | 3 (1,9) | 1 (0,7) | |
| III | 0 | 1 (0,7) | |
| ARI | 0,982 | ||
| DA | 55 (36) | 54 (36) | |
| CX | 24 (15) | 24 (15) | |
| CD | 75 (49) | 74 (49) | |
| Enfermedad de 3 vasos | 65 (42) | 68 (45) | 0,655 |
| FEVI (%) | 57,6 (10,3) | 56,3 (7,8) | 0,232 |
| Número de vasos enfermos | 2,42±0,50 | 2,45±0,50 | 0,657 |
| Número de lesiones significativas | 3,54±1,30 | 3,63±1,42 | 0,580 |
ARI: arteria responsable del infarto; CD: arteria coronaria derecha; CX: arteria circunfleja; DA: arteria descendente anterior; FC: frecuencia cardiaca; FEVI: fracción de eyección del ventrículo izquierdo; ICP: intervención coronaria percutánea; IM: infarto de miocardio; IMC: índice de masa corporal; PAD: presión arterial diastólica; PAS: presión arterial sistólica.
Los valores expresan n (%) o media±desviación estándar.
Del total de los 154 pacientes asignados a la RCom, se trató a 152 (99%) con ICP de las lesiones coronarias no culpables (en 147 pacientes fue preciso solo 1 procedimiento y otros 5 necesitaron 2 procedimientos adicionales). Se produjo 1 cruce a la rama de RSel por preferencia del paciente (se realizó ecocardiograma de estrés —negativo— y fue dado de alta sin ICP). Otro paciente rechazó la ICP (figura 1).
De los 152 pacientes incluidos en la RSel, se produjo 1 cruce a la RCom (se trató con ICP) y a 1 paciente no se le realizó ecocardiograma de estrés por un trombo mural. Dos pacientes presentaron isquemia recurrente espontánea antes del ecocardiograma de estrés y se los trató con ICP, de acuerdo con el protocolo del estudio. Se realizó el ecocardiograma de estrés a 148 pacientes, de los que 36 presentaron criterios de positividad extensa, por lo que se indicó ICP. Entre los demás pacientes (n=64 con ecocardiograma de estrés negativo, n=25 con prueba no concluyente y n=23 con prueba sugestiva de isquemia leve), 1 precisó ICP antes del alta por isquemia recurrente espontánea y se remitió a otros 4 para ICP por preferencia de sus médicos (figura 1).
EventosEl evento principal del estudio original, un combinado de muerte cardiovascular, infarto agudo de miocardio, revascularización coronaria y reingreso por insuficiencia cardiaca, ocurrió en 22 pacientes (14%) asignados a la RCom y 21 (14%) de la rama de RSel (hazard ratio=0,95; intervalo de confianza del 95% [IC95%], 0,52-1,72; p=0,85). No hubo diferencias en cuanto al riesgo de cada uno de los componentes individuales del evento principal (tabla 1 del material adicional)10.
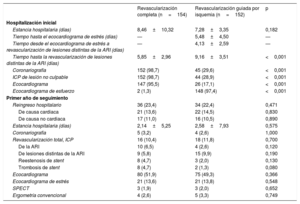
Análisis de comparación de costesLa tabla 4 recoge la estancia hospitalaria, los procedimientos y las pruebas realizadas en cada grupo al alta del ingreso índice y en el primer año de seguimiento. En la tabla 5 se muestran los costes económicos.
Procedimientos realizados en el ingreso hospitalario inicial y en el primer año de seguimiento
| Revascularización completa (n=154) | Revascularización guiada por isquemia (n=152) | p | |
|---|---|---|---|
| Hospitalización inicial | |||
| Estancia hospitalaria (días) | 8,46±10,32 | 7,28±3,35 | 0,182 |
| Tiempo hasta el ecocardiograma de estrés (días) | — | 5,48±4,50 | — |
| Tiempo desde el ecocardiograma de estrés a revascularización de lesiones distintas de la ARI (días) | — | 4,13±2,59 | — |
| Tiempo hasta la revascularización de lesiones distintas de la ARI (días) | 5,85±2,96 | 9,16±3,51 | <0,001 |
| Coronariografía | 152 (98,7) | 45 (29,6) | <0,001 |
| ICP de lesión no culpable | 152 (98,7) | 44 (28,9) | <0,001 |
| Ecocardiograma | 147 (95,5) | 26 (17,1) | <0,001 |
| Ecocardiograma de esfuerzo | 2 (1,3) | 148 (97,4) | <0,001 |
| Primer año de seguimiento | |||
| Reingreso hospitalario | 36 (23,4) | 34 (22,4) | 0,471 |
| De causa cardiaca | 21 (13,6) | 22 (14,5) | 0,830 |
| De causa no cardiaca | 17 (11,0) | 16 (10,5) | 0,890 |
| Estancia hospitalaria (días) | 2,14±5,25 | 2,58±7,93 | 0,575 |
| Coronariografía | 5 (3,2) | 4 (2,6) | 1,000 |
| Revascularización total, ICP | 16 (10,4) | 18 (11,8) | 0,700 |
| De la ARI | 10 (6,5) | 4 (2,6) | 0,120 |
| De lesiones distintas de la ARI | 9 (5,8) | 15 (9,9) | 0,190 |
| Reestenosis de stent | 8 (4,7) | 3 (2,0) | 0,130 |
| Trombosis de stent | 8 (4,7) | 2 (1,3) | 0,080 |
| Ecocardiograma | 80 (51,9) | 75 (49,3) | 0,366 |
| Ecocardiograma de estrés | 21 (13,6) | 21 (13,8) | 0,548 |
| SPECT | 3 (1,9) | 3 (2,0) | 0,652 |
| Ergometría convencional | 4 (2,6) | 5 (3,3) | 0,749 |
ARI: arteria responsable del infarto; ICP: intervención coronaria percutánea; SPECT: tomografía computarizada por emisión monofotónica.
Los valores expresan n (%) o media±desviación estándar.
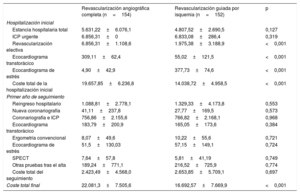
Costes económicos (euros) durante la hospitalización inicial y el primer año de seguimiento
| Revascularización angiográfica completa (n=154) | Revascularización guiada por isquemia (n=152) | p | |
|---|---|---|---|
| Hospitalización inicial | |||
| Estancia hospitalaria total | 5.631,22±6.076,1 | 4.807,52±2.690,5 | 0,127 |
| ICP urgente | 6.856,31±0 | 6.833,08±286,4 | 0,319 |
| Revascularización electiva | 6.856,31±1.108,6 | 1.975,38±3.188,9 | <0,001 |
| Ecocardiograma transtorácico | 309,11±62,4 | 55,02±121,5 | <0,001 |
| Ecocardiograma de estrés | 4,90±42,9 | 377,73±74,6 | <0,001 |
| Coste total de la hospitalización inicial | 19.657,85±6.236,8 | 14.038,72±4.958,5 | <0,001 |
| Primer año de seguimiento | |||
| Reingreso hospitalario | 1.088,81±2.778,1 | 1.329,33±4.173,8 | 0,553 |
| Nueva coronariografía | 41,11±237,8 | 27,77±169,5 | 0,573 |
| Coronariografía e ICP | 756,86±2.155,6 | 766,82±2.168,1 | 0,968 |
| Ecocardiograma transtorácico | 183,79±200,9 | 165,05±173,6 | 0,384 |
| Ergometría convencional | 8,07±49,6 | 10,22±55,6 | 0,721 |
| Ecocardiograma de estrés | 51,5±130,03 | 57,15±149,1 | 0,724 |
| SPECT | 7,64±57,8 | 5,81±41,19 | 0,749 |
| Otras pruebas tras el alta | 189,24±771,1 | 216,52±725,9 | 0,774 |
| Coste total del seguimiento | 2.423,49±4.568,0 | 2.653,85±5.709,1 | 0,697 |
| Coste total final | 22.081,3±7.505,6 | 16.692,57±7.669,9 | <0,001 |
ICP: intervención coronaria percutánea; SPECT: tomografía computarizada por emisión monofotónica.
Los valores expresan media±desviación estándar.
No hubo diferencias significativas en la duración de la estancia hospitalaria entre la RCom y la RSel (8,46±10,32 frente a 7,28±3,35 días; p=0,182). El tiempo hasta la revascularización de las lesiones no culpables en la RCom resultó menor que en la RSel (5,9 frente a 9,1 días; p <0,001). En la RSel, el tiempo medio hasta la realización del ecocardiograma de estrés fue de 5,5 días y el tiempo desde dicha prueba hasta la ICP, 4,13 días.
Como ya se ha detallado, se trató con ICP electiva de lesiones no culpables al 98,7% de los pacientes aleatorizados a la rama RCom, frente al 28,9% de los de RSel (p <0,001). En cambio, se realizó ecocardiograma de estrés a la inmensa mayoría de los pacientes asignados a la RSel (97,4%), pero solo al 1,3% del grupo de RCom (p <0,001).
Se practicó un ecocardiograma transtorácico al 95,5% de los pacientes de la RCom, pero solo al 17,1% de la RSel (p <0,001).
Si bien el coste de la ICP urgente inicial resultó similar con ambas estrategias (RCom frente a RSel, 6.856,3 frente a 6.833 euros; p=0,319), el coste de las ICP electivas fue significativamente superior en la RCom que en la RSel (6.856,3 frente a 1.975,4 euros; p <0,001). En cambio, el coste atribuible al ecocardiograma de estrés fue superior en la RSel (377,7 frente a 4,9 euros; p <0,001).
El coste de la hospitalización inicial se cifró en 19.657,9 euros en la RCom y 14.038,7 euros en la RSel (p <0,001), con lo que la RSel permitió un ahorro estimado de 5.619,13 (IC95%, 4.350,6-6.887,7) euros.
En el primer año de seguimientoLas tasas de reingreso hospitalario en el primer año fueron similares entre los grupos de tratamiento (el 23,4% en la RCom y el 22,4% en la RSel; p=0,471), tanto por causa cardiaca (el 13,6 y el 14,5%; p=0,830) como no cardiaca (el 11,0 y el 10,5%; p=0,890. No hubo diferencias en la duración de la estancia hospitalaria de dichos reingresos (2,14 frente a 2,58 días; p=0,575).
Tampoco se observaron diferencias entre ambos grupos en la realización de las pruebas cardiológicas no invasivas, como el ecocardiograma transtorácico (el 51,9 frente al 49,3%; p=0,366) o el ecocardiograma de estrés (el 13,6 frente al 13,8%; p=0,548) y los procedimientos de revascularización coronaria (el 10,4 frente al 11,8%; p=0,700).
Los costes atribuibles a la estancia por reingresos hospitalarios (1.088,8 frente a 1.329,3 euros; p=0,553), la realización de pruebas complementarias como ecocardiogramas, ecocardiogramas de estrés y coronariografías o derivados de nuevos procedimientos de ICP no mostraron diferencias entre ambos grupos de tratamiento.
El coste económico de los reingresos en el primer año de seguimiento se cifró en 2.423,5 euros en la rama de RCom y 2.653,9 euros en la rama de RSel (p=0,697). Así, el coste total final resultó significativamente superior en la RCom que en la RSel (22.081,3 y 16.692,6 euros; p <0,001).
Coste del material fungibleNo se observaron diferencias en el coste de los fungibles para la ICP índice entre ambas ramas de tratamiento (1.643 euros en la RCom frente a 1.687 euros en la RSel) (tabla 6). En cambio, el coste del material empleado durante las ICP electivas fue significativamente superior en el grupo de RCom (3.166 frente a 896 euros; p <0,001). Así, el coste total del material fungible fue 4.810,4 euros en la rama de RCom y 2.557,0 en la de RSel, lo cual supuso un incremento por paciente de 2.253 (IC95%, 1.794,2-2.712,2) euros en la RCom respecto a la RSel.
Costes del material fungible
| Revascularización angiográfica completa (n=154) | Revascularización guiada por eco de estrés (n=152) | p | |
|---|---|---|---|
| Coste de fungibles en la primera ICP | 1.643,76±931,9 | 1.687,59±924,3 | 0,680 |
| Coste de fungibles en la segunda ICP durante el ingreso inicial | 3.166,68±1.771,2 | 869,38±1.617,0 | <0,001 |
| Coste total de material fungible | 4.810,44±2.026,1 | 2.556,96±2.051,7 | <0,001 |
ICP: intervención coronaria percutánea.
Los valores expresan media±desviación estándar.
En la presente evaluación económica del ensayo clínico CROSS-AMI, el coste del ingreso inicial, desde la perspectiva de nuestro servicio de salud, resultó significativamente superior en la RCom que en la RSel (coste medio, 19.658 frente a 14.039 euros). La RSel permitió ahorrar durante el ingreso inicial aproximadamente 5.619 euros por paciente frente a la RCom, debido al menor número de revascularizaciones electivas. En cambio, no se observaron diferencias entre ambas estrategias en los costes del primer año de seguimiento tras el alta hospitalaria. Así, el coste del ingreso inicial y el seguimiento resultó aproximadamente 5.388 euros superior en la rama de RCom que en la de RSel.
Las diferencias económicas entre ambas estrategias se deben, principalmente, a las ICP electivas de las lesiones no culpables practicadas durante el ingreso inicial. Solo un 29% de los pacientes de la RSel precisaron ICP, frente al 99% con la RCom. Esto se ve refrendado por el análisis complementario sobre el material fungible: el coste del fungible de las ICP electivas de lesiones no culpables resultó significativamente mayor en la RCom que en la RSel (3.166 frente a 869 euros; p <0,001), sin diferencias en la ICP urgente.
Uno de los principales beneficios de la revascularización completa en el SCACEST con enfermedad multivaso radica en reducir los eventos clínicos, lo cual compensa el sobrecoste económico inicial de los procedimientos de revascularización4. En el ensayo clínico CROSS-AMI no se observaron diferencias significativas entre la RCom y la RSel en eventos clínicos al año de seguimiento10. Esto explica que el coste del seguimiento clínico sea similar entre ambas estrategias y juega a favor de la RSel y en contra de la RCom, debido al elevado coste de la ICP frente a las pruebas de detección de isquemia. Así, el sobrecoste económico del ingreso inicial en el grupo de la RCom frente a la RSel no se vio rentabilizado por esa anticipada necesidad de reducir eventos clínicos.
Los retrasos hasta el ecocardiograma de estrés y la revascularización resultaron claramente mejorables, y pueden haber influido en los resultados que se presentan. El CROSS-AMI10 fue un ensayo clínico pragmático, integrado en nuestra práctica clínica habitual, que se ve afectado por las demoras hospitalarias, en las que influyen múltiples factores no controlables por los investigadores. El tiempo medio hasta la revascularización en la RCom fue de 5,85 días, significativamente menor que en la RSel (9,1 días; p <0,001). Sin embargo, la duración de la estancia hospitalaria y su coste no difirieron estadísticamente entre ambos grupos. Además, su posible impacto en el coste se minimizó porque el tiempo medio desde la aleatorización hasta el ecocardiograma de estrés en la RSel fue 5,5 días (similar al tiempo hasta la revascularización en la RCom) y precisaron una segunda revascularización solo el 29% de estos pacientes.
Numerosos estudios han abordado el tratamiento de la enfermedad multivaso en el SCACEST12,13, pero únicamente el CvLPRIT14 cuenta con un estudio económico15. Resulta extraordinariamente complejo compararlo con el presente análisis, pues las estrategias de revascularización, los resultados y los análisis económicos fueron diferentes. Entra dentro del terreno especulativo si la realización de una prueba de isquemia a los pacientes de la rama conservadora del CvLPRIT podría haber modificado sus resultados. Por otra parte, dicho subestudio económico genera numerosas dudas. Se estimó una probabilidad de que la revascularización completa resultase coste-efectiva del 72%, con un umbral de disposición a pagar 20.000 libras por QUALY, lo cual cuestiona su efectividad para casi un tercio de los pacientes. La medición de los QUALY se basó en una encuesta indirecta (EQ-5D) que solo se realizó al 70% de los pacientes. Además, lo penaliza el amplio porcentaje de valores perdidos y la necesidad de tratarlos mediante imputación múltiple, lo cual produce sesgos y falta de precisión16. No se observaron diferencias significativas en los costes económicos de ambas estrategias de tratamiento durante la hospitalización inicial (4.890 libras en la rama de revascularización completa frente a 4.668 libras en la de revascularización de la lesión culpable; p=0,654), cuando resultaría más lógico un sobrecoste económico inicial para la revascularización completa, como en nuestro análisis.
En el CROSS-AMI no se realizó una valoración invasiva de las lesiones no culpables mediante guía de presión, como en el Compare-Acute17 o en el DANAMI-3-PRIMULTI18. No se pudo confrontar nuestros hallazgos con dichos estudios, pues no se han publicado los análisis económicos. Esto resultaría muy interesante, pues la guía de presión se ha demostrado coste-efectiva en la enfermedad coronaria estable19,20. La valoración invasiva mediante reserva de flujo coronario no solo es un procedimiento más costoso que la evaluación no invasiva mediante ecocardiograma de esfuerzo, sino que habría que añadirle el coste de la revascularización si fuese necesaria. En el Compare-Acute se trató un 55% de las lesiones no culpables17, frente al 28% de los pacientes incluidos en la rama RSel del CROSS-AMI.
Si bien la revascularización completa ha resultado superior al tratamiento de la lesión culpable12, en cuanto a revascularizaciones y eventos «duros» (muerte e infarto6), se puede haber sobrestimado su efecto real por el tratamiento demasiado conservador de las lesiones no culpables7. Recientemente se ha propuesto emplear un enfoque individualizado en la toma de decisiones para los pacientes con un SCACEST y enfermedad multivaso, teniendo en cuenta el perfil clínico de los pacientes (edad, fragilidad, comorbilidades) y la gravedad, la complejidad y la relevancia de las lesiones no culpables. Otro aspecto que tener en cuenta en la toma de decisiones es el económico21. Nuestros resultados ponen de manifiesto que la RSel resulta más rentable económicamente que la RCom, pues permite seleccionar qué lesiones es necesario revascularizar, con lo que se reduce el sobrecoste inicial de la ICP, sin que esto resulte penalizado en el seguimiento como consecuencia de un exceso de eventos clínicos.
Es controvertido en qué momento valorar y revascularizar las lesiones no culpables7. En el CROSS-AMI, el ecocardiograma de estrés y las revascularizaciones percutáneas se realizaron durante el ingreso inicial. Realizar la valoración no invasiva y la revascularización en las 4-6 semanas tras el alta es una alternativa válida para la mayoría de los pacientes con infartos no complicados, máxime teniendo en cuenta los cambios que se producen en la fisiología de la circulación coronaria tras un infarto22. De hecho, en el estudio COMPLETE el beneficio de la revascularización resultó independiente del momento en que se realizase23.
LimitacionesUna de las principales limitaciones del estudio original radica en la interrupción precoz de la inclusión del ensayo CROSS-AMI con un total de 306 pacientes aleatorizados (un 77% del tamaño muestral estimado inicialmente) por baja tasa de inclusión10. Con base en los análisis de sensibilidad realizados, asumiendo una tasa de eventos similar, incluso si todos se concentrasen en el mismo grupo, la probabilidad de obtener una diferencia significativa en el evento principal completando el tamaño muestral es remota10.
No se puede excluir que haya habido sesgo de selección por los criterios de exclusión o el análisis de las características basales de la población (p. ej., alta frecuencia de Killip I). La proporción de pacientes incluidos en el estudio fue del 31% de los valorados como candidatos. Si bien esto puede afectar a su validez externa, dicha proporción es similar a la de los principales ensayos clínicos realizados13.
Si bien el ecocardiograma de estrés proporciona información pronóstica adicional frente a la ergometría24, su interpretación puede ser difícil y depende del operador. Los centros hospitalarios participantes en el CROSS-AMI cuentan con amplia experiencia en la ecocardiografía de estrés25.
Los resultados podrían haber sido diferentes con un seguimiento más prolongado. Dado que tampoco hubo diferencias entre ambas estrategias de revascularización a 3 años, esto parece poco probable, aunque no se puede descartar definitivamente que las hubiera tras seguimientos incluso mayores (> 5 años).
Para el presente análisis económico se han empleado las tarifas vigentes en nuestro sistema de salud, lo cual limita su aplicación a los sistemas sanitarios en que los cómputos de los costes resulten comparables en cuantía. No se puede perder de vista que, en nuestro país, cada comunidad autónoma cuenta con su sistema de tarifas, lo cual dificulta realizar comparaciones. También se debe tener en cuenta que los costes podrían variar en el futuro, lo que afectaría al balance económico que se presenta.
En el cálculo de los costes durante el seguimiento, se contabilizaron los procedimientos o tratamientos realizados durante los reingresos hospitalarios, y no se incluyeron las consultas al médico de atención primaria, las asistencias a urgencias u otras pruebas complementarias ambulatorias. En el análisis económico del CvLPRIT15, en cambio, el coste de las visitas médicas supuso menos del 10% del coste total, por lo que no parece que sea un factor económico de relevancia.
CONCLUSIONESEn el análisis económico del ensayo clínico CROSS-AMI, los costes de la hospitalización inicial, según la perspectiva de nuestro servicio de salud, resultaron significativamente mayores en el grupo de RCom que en el de la RSel. No hubo diferencias significativas entre las 2 estrategias de tratamiento en los costes atribuibles a procedimientos diagnósticos y terapéuticos realizados durante los reingresos hospitalarios en el primer año de seguimiento.
Así, el sobrecoste económico inicial de la RCom no se vio compensado por un ahorro significativo durante el primer año de seguimiento, probablemente por la similar incidencia de eventos clínicos en ambos grupos.
Por lo tanto, la RSel en los pacientes con SCACEST y enfermedad coronaria multivaso tratados mediante angioplastia urgente de la lesión culpable, parece ser una estrategia más eficiente que la RCom de todas las lesiones no culpables durante el primer año de seguimiento, pues en dicha ventana temporal consigue resultados clínicos similares con un menor coste económico.
FINANCIACIÓNR. Estévez-Loureiro recibió un Contrato Rio Hortega del Instituto de Salud Carlos III durante su participación en este proyecto. El Instituto de Salud Carlos III no tuvo participación en el diseño o desarrollo de este estudio.
CONFLICTO DE INTERESESLos autores no presentan conflictos de intereses relativos a esta publicación.
- –
La enfermedad coronaria multivaso es frecuente en el SCACEST, entraña peor pronóstico y su tratamiento es complejo.
- –
Actualmente se aconseja considerar la revascularización completa de las lesiones no culpables con base en estudios que la han comparado frente a una actitud conservadora (revascularización de la lesión culpable).
- –
Sin embargo, hasta la fecha, solo el ensayo clínico CROSS-AMI ha comparado 2 estrategias de revascularización diferentes en esta situación.
- –
Los estudios de evaluación económica resultan útiles en situaciones complejas como esta, especialmente cuando los recursos son limitados.
- –
Dentro del ensayo CROSS-AMI, el mayor coste económico de la hospitalización inicial en la revascularización completa no se compensó con un ahorro significativo frente a la revascularización selectiva guiada por isquemia en ecocardiografía de estrés durante el primer año de seguimiento, debido a la similar incidencia de eventos clínicos.
- –
La revascularización selectiva guiada por isquemia en pacientes con SCACEST y enfermedad multivaso tratados mediante angioplastia urgente de la lesión culpable parece ser una estrategia más eficiente que la revascularización completa durante el primer año de seguimiento, pues consigue resultados clínicos similares con menor coste económico.