La detección precoz de la fibrilación auricular (FA) es prioritaria para reducir su riesgo embólico mediante la instauración del tratamiento anticoagulante. El objetivo de este estudio es evaluar la capacidad diagnóstica de un dispositivo de muñeca diseñado para la monitorización del ritmo cardiaco y la detección automática de la FA.
MétodosEl RITHMI es un estudio prospectivo, comparativo y observacional, realizado en 167 pacientes remitidos a una consulta cardiológica o para cardioversión eléctrica, en el que se comparó la capacidad de detección automática de FA de un monitor de pulsera que emplea la señal de fotopletismografía (PPG) frente a una derivación electrocardiográfica con el diagnóstico realizado por 2 cardiólogos con un ECG de 12 derivaciones.
ResultadosEl algoritmo de detección de FA basado en la señal de PPG mostró una sensibilidad del 91% y una especificidad del 96% (exactitud diagnóstica del 93%). El algoritmo automático basado en la señal del ECG mostró una sensibilidad del 94% y una especificidad del 96% (exactitud diagnóstica: 95%). Ambos algoritmos coincidieron en el diagnóstico en el 96% de los casos. El monitor, en general, mostró una sensibilidad y una especificidad del 95% (exactitud diagnóstica del 95% y κ = 0,98).
ConclusionesEl estudio RHITMI mostró que la detección automática de FA mediante un monitor que incorpora detectores y algoritmos que analizan la señal de PPG y la señal electrocardiográfica correspondiente a la derivación I es factible y presenta una gran exactitud diagnóstica.
Palabras clave
La fibrilación auricular (FA) es el trastorno arrítmico más frecuente en la población general, y afecta a un 3-4% de los adultos mayores de 20 años1. La FA se asocia con un incremento de los riesgos de muerte e insuficiencia cardiaca que afecta tanto a varones como a mujeres, un mayor riesgo de ictus, un deterioro cognitivo y un deterioro de la calidad de vida. Como consecuencia, la identificación precoz de la FA es fundamental porque se ha demostrado que la instauración del tratamiento anticoagulante reduce la mortalidad entre los pacientes con mayor riesgo2.
La presentación clínica de la FA es muy heterogénea, de forma que los pacientes pueden tener síntomas limitantes o, por el contrario, encontrarse completamente asintomáticos (FA silente). La FA silente es una manifestación frecuente de la arritmia, especialmente entre los ancianos, y se asocia con mayores riesgos de ictus y de insuficiencia cardiaca3. La prevalencia de la FA silente es por definición desconocida; no obstante, de los pacientes a los que se diagnostica FA, un tercio no presenta síntomas3. Además, en los pacientes ingresados por un ictus isquémico en presencia de FA, la arritmia no se conocía antes en un 25-50% de todos los casos4. Estos hallazgos indican que la prevalencia real de la FA silente es mayor de lo esperado e inciden en la importancia de un diagnóstico precoz con el objetivo principal de prevenir los ictus mediante un tratamiento anticoagulante.
La detección de la FA ha evolucionado en los últimos años con el desarrollo de sistemas de monitorización electrocardiográfica más allá del electrocardiograma (ECG) de 12 derivaciones. Actualmente se dispone de varios sistemas diagnósticos de FA validados y aprobados para su uso clínico, que bien exigen la participación del paciente en la grabación del ritmo cardiaco, bien son sistemas de monitorización electrocardiográfica prolongada que emplean parches cutáneos o dispositivos subcutáneos insertables2. Por último, se ha demostrado que las nuevas tecnologías, como carcasas de teléfono móvil con electrodos de ECG incorporados, tienen mayor capacidad de detección de FA que un seguimiento clínico convencional5. El hallazgo común en todos estos trabajos es el incremento en la detección de FA en paralelo al incremento de la intensidad y la duración de la monitorización electrocardiográfica.
El instrumento ideal de detección de FA debería ser no invasivo, exacto, sin necesidad de que el paciente participe en el registro de la arritmia (detección pasiva), no limitado a registros puntuales en el tiempo y con capacidad para mostrar en tiempo real que se está produciendo una FA. La tecnología «vestible» (wearable), especialmente los relojes o pulseras inteligentes, estaría bien posicionada para lograr estos objetivos de modo coste-eficiente6. Las generaciones actuales de relojes inteligentes están equipadas con pletismógrafos que son capaces de determinar continuamente la frecuencia cardiaca. La aplicabilidad de esta tecnología es grande y permitiría una monitorización prolongada y no invasiva del ritmo cardiaco y se podría emplear para la detección de FA.
El objetivo de este estudio es evaluar la capacidad diagnóstica de un dispositivo de muñeca diseñado para la monitorización del ritmo cardiaco y la detección automática de la FA basado en un sistema doble de detección: señales del ritmo cardiaco detectadas por fotopletismografía (PPG) y la señal del ECG.
MÉTODOSDiseño del estudio y pacientesEl RITHMI es un estudio prospectivo y no aleatorizado, realizado en el Hospital Universitario y Politécnico La Fe durante los meses de enero a junio de 2019, en el que se analizó la capacidad diagnóstica del monitor de pulsera RITHMI para la detección de FA en una población de pacientes con edad> 18 años remitidos a una consulta general de cardiología, independientemente de que se encontraran en ritmo sinusal o en FA, así como pacientes remitidos para cardioversión eléctrica (CVE) de FA. Se excluyó a los pacientes que se encontraban en aleteo auricular y los pacientes estimulados por marcapasos.
El estudio se llevó a cabo siguiendo los principios de la Declaración de Helsinki y fue aprobado por el comité ético del hospital. Todos los pacientes aceptaron participar en el estudio mediante la firma de un consentimiento informado. Se obtuvo de todos los pacientes 1 ECG de 12 derivaciones, que fue analizado por 2 cardiólogos electrofisiólogos para determinar el ritmo del paciente y se empleó como referencia para la determinación del ritmo cardiaco. Los ECG se clasificaron como ritmo sinusal o FA.
Tras la obtención del ECG de 12 derivaciones, se colocó el monitor de ritmo de pulsera, lo que permitió el registro del ritmo cardiaco durante 3min mientras el paciente se encontraba sentado. A la finalización del registro, los pacientes que acudían a la consulta cardiológica siguieron con ella, mientras que en el segundo grupo de pacientes se llevó a cabo la CVE.
Monitor de ritmo RITHMIEl monitor del ritmo cardiaco RITHMI es un prototipo aún no comercializado que presenta un sistema doble de detección: señales del ritmo cardiaco detectadas por PPG en la región distal del antebrazo/muñeca y la señal del ECG de 1 derivación incorporado en el dispositivo y equivalente a la derivación I del ECG de 12 derivaciones. El sensor de PPG (ADPD107) se compone de 2 fotodiodos emisores y 1 receptor que se encuentran en la parte inferior del dispositivo. El sensor de electrocardiografía (AD8233) se compone de 3 electrodos, 2 de ellos en la parte superior, donde se colocarán el índice y el pulgar y el tercero en la parte inferior que estará en contacto con la superficie de la piel. Así pues, la disposición del sujeto descrita cierra un circuito eléctrico entre los brazos y proporciona una derivación equivalente a la derivación I del ECG estándar (figura 1). Uno de los electrodos dispuestos en la parte superior del sensor de electrocardiografía se comporta como toma de tierra y ayuda a eliminar interferencias eléctricas. El sistema dispone de un microcontrolador de bajo consumo dotado de comunicación Bluetooth y de una memoria para el almacenamiento de los datos.
El monitor del ritmo cardiaco RITHMI presenta un doble algoritmo automático para el diagnóstico de FA, uno diseñado para el análisis de la señal identificada por el detector de PPG y otro basado en el ECG. El algoritmo automático de diagnóstico de FA se basa en la irregularidad estadística de la señal para diagnosticar la posible presencia de la arritmia. El diseño del monitor de ritmo permite una monitorización del ritmo cardiaco continua, pasiva e independiente del paciente a través del sensor de PPG, mientras que la detección de la señal electrocardiográfica permitiría confirmar la presencia de la arritmia además de generar un registro gráfico exportable para un posterior análisis.
Análisis estadísticoLas variables continuas se expresan como media±desviación estándar y las categóricas, como valores absolutos y porcentajes. Se empleó el test de la χ2 para comparar las variables categóricas y el test de la t de Student para comparar las variables cuantitativas continuas.
El objetivo principal del estudio es evaluar la capacidad diagnóstica del monitor RITHMI en la detección automática de FA mediante la comparación del diagnóstico establecido por cada uno de los algoritmos que incluye el monitor y el diagnóstico realizado por 2 electrofisiólogos mediante el ECG de 12 derivaciones. La evaluación se efectuó mediante un doble enmascaramiento: los electrofisiólogos no conocían la clasificación del ritmo establecido por el monitor de ritmo cardiaco, mientras que los resultados ofrecidos por el monitor de ritmo cardiaco se incluyeron en una base de datos cumplimentada por un ingeniero que desconocía el rimo electrocardiográfico del paciente. A la finalización del estudio, se comparó el diagnóstico establecido por el monitor de ritmo cardiaco, en cada uno de sus 2 algoritmos, con el ofrecido por el análisis del ECG realizado por los electrofisiólogos, que se empleó como referencia.
Para cada uno de los 2 algoritmos automáticos (PPG y ECG), se calcularon las siguientes medidas para determinar su capacidad diagnóstica: en primer lugar se evaluaron la sensibilidad y la especificidad; en segundo lugar, se determinaron los valores predictivo positivo y predictivo negativo; en tercer lugar, la razón de verosimilitud positiva=sensibilidad / (1 – especificidad) y la razón de verosimilitud negativa=(1 – sensibilidad) / especificidad; finalmente, se calculó el porcentaje de casos correctamente diagnosticados como el cociente entre (n casos correctamente diagnosticados de FA + n casos correctamente diagnosticados como ritmo sinusal) / N total de casos×100.
Se calculó el índice de correlación kappa (κ) para determinar el grado de concordancia entre los 2 sistemas automáticos de detección de la FA (PPG y ECG), así como cada uno de ellos con la interpretación del ECG de 12 derivaciones realizada por los electrofisiólogos.
RESULTADOSSe evaluó el monitor de ritmo cardiaco en un total de 167 pacientes, de los que 109 formaban parte del grupo que acudió para CVE y 58 del grupo atendido en la consulta de cardiología. Se estableció el ritmo cardiaco de todos ellos mediante el análisis del ECG de 12 derivaciones, y se determinó FA en 98 pacientes y ritmo sinusal en 69.
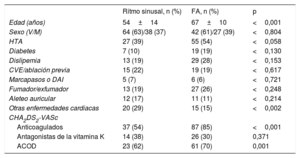
Las características basales de la población evaluada en el estudio se muestran en la tabla 1. Los pacientes que se encontraban en FA en el momento del análisis mostraban una mayor prevalencia de hipertensión arterial, diabetes, dislipemia y antecedentes de tabaquismo. La media de edad, el sexo y la presencia de cardiopatía estructural resultaron similares entre ambos grupos de pacientes. Los pacientes con FA presentaron una frecuencia cardiaca media de 81 (49-153) lpm.
Características de la población evaluada
| Ritmo sinusal, n (%) | FA, n (%) | p | |
|---|---|---|---|
| Edad (años) | 54±14 | 67±10 | <0,001 |
| Sexo (V/M) | 64 (63)/38 (37) | 42 (61)/27 (39) | <0,804 |
| HTA | 27 (39) | 55 (54) | <0,058 |
| Diabetes | 7 (10) | 19 (19) | <0,130 |
| Dislipemia | 13 (19) | 29 (28) | <0,153 |
| CVE/ablación previa | 15 (22) | 19 (19) | <0,617 |
| Marcapasos o DAI | 5 (7) | 6 (6) | <0,721 |
| Fumador/exfumador | 13 (19) | 27 (26) | <0,248 |
| Aleteo auricular | 12 (17) | 11 (11) | <0,214 |
| Otras enfermedades cardiacas | 20 (29) | 15 (15) | <0,002 |
| CHA2DS2-VASc | |||
| Anticoagulados | 37 (54) | 87 (85) | <0,001 |
| Antagonistas de la vitamina K | 14 (38) | 26 (30) | 0,371 |
| ACOD | 23 (62) | 61 (70) | 0,001 |
ACOD: anticoagulantes orales de acción directa; CVE: cardioversión eléctrica; DAI: desfibrilador automático implantable; HTA: hipertensión arterial; M: mujer; V: varón.
Los valores expresan n (%) o media±desviación estándar.
En 167 pacientes se evaluó el algoritmo automático de detección de FA basado en el análisis de la señal de PPG, mientras que en 133 se analizó el algoritmo automático basado en el ECG.
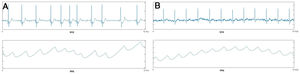
Capacidad diagnóstica del algoritmo de detección de FA basado en la señal de PPGDe los 167 pacientes en los que se evaluó el algoritmo basado en la señal de PPG, esta no se pudo analizar en 5 pacientes por una señal de mala calidad, lo que resulta en una muestra total de 162 pacientes, 95 en FA (figura 2A) y 67 en ritmo sinusal (figura 2B).
El algoritmo de detección de FA basado en la señal de PPG mostró una sensibilidad del 91% y una especificidad del 96% respecto al ritmo determinado por el ECG de 12 derivaciones. El valor predictivo positivo y el valor predictivo negativo del algoritmo evaluado fueron del 97 y el 88% respectivamente, mientras que la exactitud diagnóstica fue del 93%. La detección de FA basada en la señal de PPG mostró unas razones de verosimilitud positiva y negativa de 20,22 y 0,05. Se observó un 3% de falsos positivos y un 9% de falsos negativos. El análisis posterior reveló que los falsos positivos se explicarían por una mala calidad de la señal, con artefactos debidos a movimientos bruscos. Por otro lado, los falsos negativos se motivaron por una variabilidad de los latidos durante la arritmia inferior al umbral que los clasifica como pulso arrítmico, secundario en la mayoría de los casos a una frecuencia cardiaca elevada, de media 121±32 frente a 68±14 lpm entre los pacientes con FA correctamente identificados por el dispositivo (p=0,015).
Capacidad diagnóstica del algoritmo de detección de FA basado en el ECGEl algoritmo automático basado en la señal del ECG se evaluó en un total de 133 pacientes, 87 en FA y 46 en ritmo sinusal. El algoritmo evaluado mostró una sensibilidad del 94% y una especificidad del 96% respecto al ritmo determinado por el ECG de 12 derivaciones. El valor predictivo positivo y el valor predictivo negativo del algoritmo automático electrocardiográfico fueron del 98 y el 90% respectivamente, mientras que la exactitud diagnóstica fue del 95%. La detección de FA basada en el ECG mostró unas razones de verosimilitud positiva y negativa de 21,68 y 0,01. Se observó un 2% de falsos positivos y un 6% de falsos negativos. El análisis posterior reveló que los falsos positivos se explicarían por artefactos en la señal debidos a un mal contacto de los electrodos con la piel que produjo saltos brucos en la señal eléctrica registrada, mientras que los falsos negativos se motivaron igualmente por una variabilidad de los latidos durante la arritmia inferior al umbral que los clasifica como pulso arrítmico.
Capacidad diagnóstica conjunta de ambos algoritmosEn general, ambos algoritmos coincidieron en detectar FA o ritmo sinusal en el 96% de los casos, con un índice de correlación entre ellos de κ=0,91. Ambos algoritmos discreparon en la presencia de FA o ritmo sinusal en 5 casos, debido a que una de las 2 señales presentaba artefactos, bien por movimiento del paciente durante el registro de PPG, bien por un contacto deficiente del detector del ECG.
En conjunto (ambos algoritmos coincidieron en el diagnóstico), el monitor de ritmo evaluado mostró una sensibilidad y una especificidad para detectar la presencia de FA del 95%, un valor predictivo positivo del 99% y un valor predictivo negativo del 100%. La exactitud diagnóstica del monitor fue del 95%. Las razones de verosimilitud positiva y negativa fueron 19,09 y <0,1 respectivamente. El índice de correlación entre el monitor y el diagnóstico establecido por el electrofisiólogo fue κ=0,98.
DISCUSIÓNEl estudio RITHMI evaluó la capacidad diagnóstica de un nuevo monitor de pulsera para la detección de FA que incluye 2 algoritmos automáticos de detección del ritmo cardiaco, uno que emplea la señal de PPG y otro basado en la derivación electrocardiográfica registrada por el monitor y que sería equivalente a la derivación I del ECG. El resultado de ambos algoritmos se comparó con el diagnóstico establecido por 2 electrofisiólogos mediante el análisis del ECG de 12 derivaciones. El estudio mostró que la detección de FA por el monitor fue posible con una exactitud diagnóstica total del 95% (sensibilidad y especificidad del 95%) en una muestra de 167 pacientes que acudían a la consulta de cardiología o a la realización de una CVE, de los que 98 se encontraban en FA. Estos resultados superan a los mostrados por diferentes métodos propuestos para la detección de la FA, como la palpación del pulso (especificidad del 72%)7 o el uso de esfigmomanómetros (especificidad entre el 89 y el 91%)8,9.
Al compararse con el ritmo establecido por los electrofisiólogos mediante análisis del ECG de 12 derivaciones, el algoritmo basado en el análisis de la señal de PPG se asoció con una exactitud diagnóstica del 93% (sensibilidad del 91% y especificidad del 96%) y un 9% de falsos negativos como consecuencia de que la FA presentaba una frecuencia cardiaca elevada (121±32 lpm de media) en el momento de la monitorización. Estos resultados son similares a los mostrados por otros estudios que han analizado algoritmos de detección de FA disponibles en teléfonos móviles que emplean la señal de PPG. Conjuntamente, estos estudios mostrarían una sensibilidad entre el 90 y el 96% y una especificidad entre el 85 y el 99% para la detección de FA10–12. Sin embargo, el único estudio comparable al RITHMI es el Watch AF13, que también evaluó la capacidad diagnóstica de un algoritmo de detección de FA basado en la señal de PPG detectada por diversos relojes inteligentes disponibles en el mercado. Los resultados del algoritmo evaluado en el Watch AF se compararon con la lectura del ECG de 1 derivación obtenida con el sistema AliveCor Kardia (AliveCor Inc.; Estados Unidos) realizada por 2 cardiólogos con resultado del algoritmo enmascarado. El estudio incluyó a 508 pacientes, de los que 237 se encontraban en FA. En este estudio el algoritmo evaluado mostró una sensibilidad del 93,7% y una especificidad del 98,2%, con una exactitud diagnóstica del 96,1%. En ambos estudios se confirmó la presencia de FA mediante análisis del ECG (1 derivación en el Watch AF y 12 derivaciones en el RITHMI) y ambos estudios mostraron una capacidad similar para detectar la presencia de FA mediante el algoritmo basado en la señal de PPG. En el estudio Watch AF no se pudo analizar la señal de PPG en el 21,8% de los registros por mala calidad de la señal. Este valor es claramente superior al hallado en nuestro estudio, en el que solo hubo un 3% de registros inclasificables, lo que refuerza la capacidad del monitor RITHMI para detectar una señal de PPG con la calidad suficiente para analizarla. La obtención de una señal adecuada de PPG en la muñeca representa la principal limitación técnica para estos sistemas y hace deseable la combinación con otro sistema de detección de FA a través de una señal biológica diferente.
En este sentido, el estudio RITHMI también evaluó la utilidad de un algoritmo de detección de FA basado en el análisis automático de la señal electrocardiográfica registrada por el monitor. Comparado con el ritmo presente en el ECG de 12 derivaciones, el algoritmo basado en el análisis de la señal ECG se asoció con una exactitud diagnóstica del 95% (sensibilidad y especificidad del 94 y el 96% respectivamente). Estos resultados se pueden comparar con los obtenidos en un estudio en el que se evaluó el algoritmo automático de análisis del ECG ofrecido por el sistema AliveCor Kardia en una serie consecutiva de pacientes remitidos para CVE14. El estudio incluyó a 100 pacientes, en los que se realizaron 169 registros simultáneos entre el ECG y el registro del sistema AliveCor Kardia. El algoritmo automático detectó 57 registros (33,7%) como inclasificables por diversas razones (artefactos, señales de baja amplitud, frecuencia cardiaca anormalmente elevada o reducida u otras razones). En los 112 registros restantes, el algoritmo mostró una sensibilidad y una especificidad para detectar FA del 93 y el 84% respectivamente. Estos valores son inferiores a los mostrados por el algoritmo automático de detección de FA que emplea la señal electrocardiográfica del monitor RITHMI. Por otro lado, el algoritmo electrocardiográfico del monitor RITHMI ofrecería unos resultados comparables con los de los algoritmos que emplean los Holter insertables para detectar FA. De esta forma, el estudio XPECT evaluó la utilidad del algoritmo que emplea el Reveal LINQ (Medtronic; Estados Unidos) y mostró una sensibilidad y una especificidad para la detección de FA del 96,1 y el 85,4%15.
El monitor de RITHMI muestra un sistema doble de detección de FA con una sensibilidad y una especificidad total del 95%. La información ofrecida por la señal de PPG y del ECG son complementarias, de modo que el sistema doble de detección y los resultados que cada uno de los algoritmos evaluados muestra por separado hacen que el sistema sea especialmente atractivo como herramienta de detección de FA. La monitorización que ofrece la detección de la señal de PPG permitiría una monitorización continua del paciente, sin necesidad de una participación activa, a diferencia de otros sistemas de monitorización. En caso de que se detecte FA, esta podría corroborase mediante el algoritmo basado en la detección de la señal electrocardiográfica, que además permite la obtención de un registro gráfico para su posterior análisis.
Detección de FA y perspectivas futurasLa guía de la Sociedad Europea de Cardiología aconseja la detección oportunista de la FA silente en mayores de 65 años mediante la palpación del pulso (recomendación de clase I y nivel de evidencia B), así como una detección sistemática de FA mediante ECG en mayores de 75 años o con un alto riesgo de ictus (recomendación de clase IIa, nivel de evidencia B)1.
La tecnología mostrada en este trabajo permitiría una monitorización continua y pasiva de la persona portadora del dispositivo, lo que podría facilitar el diagnóstico de FA en población de riesgo. Sin embargo, para generalizar su utilización es necesario superar las limitaciones impuestas por la calidad de los registros (reducción de ruido, limitaciones que ofrece el análisis de una derivación electrocardiográfica única) y, sobre todo, confirmar los resultados en población general, en la que la prevalencia de la enfermedad es menor, con mayor posibilidad de falsos positivos. En un reciente estudio que incluyó a más de 400.000 personas sin antecedentes de FA y portadoras de un teléfono y reloj inteligentes con una aplicación dedicada a la detección de FA, se detectó un ritmo compatible con FA en el 0,52% de las personas incluidas y en el 3,2% de los mayores de 65 años. En estas personas, el ECG realizado una media de 13 días tras la detección mostró FA en el 34% de los casos16.
La posibilidad de detectar la FA mediante la tecnología que ofrecen los teléfonos móviles o los relojes inteligentes puede suponer un gran cambio en el modelo convencional de detección de la FA, difumina la distinción entre paciente y consumidor, sin duda generará un incremento en la demanda asistencial y probablemente aumentará el número de personas diagnosticadas de FA. Al mismo tiempo, la accesibilidad de la tecnología hace difícil de prever cuál puede ser su papel en el futuro y modificará el perfil de la población sujeta a monitorización. Por último, será necesario determinar la utilidad del tratamiento anticoagulante en pacientes en los que se detecte una FA por estos métodos.
LimitacionesLa principal limitación del estudio son las condiciones en que se obtuvieron los registros de las señales de PPG y ECG, ya que el paciente se encontraba en reposo y libre de estímulos externos, lo que facilita la obtención de una señal adecuada, sobre todo de PPG. Las limitaciones de la determinación del ritmo eléctrico por el análisis de la señal de PPG están descritas en la literatura, como la influencia del temblor o el movimiento en la relación entre la señal y el ruido captados por el detector10–13. Todos los pacientes incluidos en el estudio son de raza blanca, por lo que no se ha podido evaluar el impacto de la pigmentación cutánea en la calidad de la señal y la exactitud del algoritmo. El algoritmo basado en la señal de PPG mostró un 9% de falsos negativos, en muchos casos consecuencia de una frecuencia cardiaca elevada. Otros trabajos no describen la frecuencia cardiaca de los pacientes o han excluido a los pacientes con frecuencias cardiacas más altas13,14 por el impacto en los algoritmos automáticos de detección de la FA.
En conjunto, en el 3% de los pacientes no se pudo evaluar el algoritmo basado en la señal de PPG por falta de calidad, y no se puede excluir que este valor sea incluso superior en condiciones menos controladas. Se excluyó a los pacientes que se encontraban en aleteo auricular y a los estimulados por marcapasos, ya que estos pacientes pueden presentar un ritmo cardiaco regular, lo que imposibilita la detección de la FA por un algoritmo que analiza la irregularidad del ritmo cardiaco.
El algoritmo basado en la señal del ECG estuvo disponible más tardíamente, por lo que solo se pudo analizar en 133 pacientes. Sin embargo, parece poco probable que los resultados hubieran cambiado de manera significativa de haber estado disponible desde el principio del estudio.
Otra limitación del estudio es el número de pacientes incluidos, ya que sería deseable confirmar estos resultados en una muestra de mayor tamaño, en condiciones de determinación variables, no solo en reposo y en un entorno menos controlado. No se puede concluir que sea un sistema validado para realizar una campaña de detección de FA y son necesarios nuevos estudios que confirmen este punto. Sin embargo, los resultados del estudio confirman la «prueba de concepto» y sirven de punto de partida para diseñar un estudio que evalúe su utilidad a escala poblacional.
CONCLUSIONESLos resultados del estudio RITHMI muestran que la detección continua y automática de FA mediante un monitor del ritmo cardiaco que incorpora un detector y algoritmos que analizan la señal de PPG y la señal electrocardiográfica correspondiente a la derivación I es factible y muestra una exactitud diagnóstica elevada.
CONFLICTO DE INTERESESC. Planells Palop es ingeniero en procesamiento de señal de Arrythmia Algorithm S.L. y J. Osca Asensi es asesor médico de Arrhythmia Algorithm S.L.
- –
La detección de la FA ha evolucionado en los últimos años con el desarrollo de sistemas de monitorización electrocardiográfica más allá del ECG de 12 derivaciones.
- –
La detección de la FA mediante nuevas tecnologías, especialmente los teléfonos, relojes o pulseras inteligentes, podría servir como sistema de monitorización no invasivo, continuo y con capacidad para demostrar la presencia de FA en tiempo real.
- –
El estudio RITHMI muestra la utilidad de un nuevo monitor del ritmo cardiaco que incluye 2 algoritmos automáticos de detección de FA, uno basado en el análisis de la señal de PPG y otro basado en el análisis de la señal electrocardiográfica.
- –
El estudio mostró una buena exactitud diagnóstica de cada uno de los algoritmos evaluados.
- –
En conjunto, el monitor permitiría una monitorización del ritmo cardiaco continua, pasiva y sin ayuda del paciente mediante el análisis de la señal de PPG con la posibilidad de emplear el análisis del ECG para confirmar la presencia de FA.