No está claro si es necesaria la predilatación de la rama lateral antes de implantar stents en el vaso principal. Se ha evaluado el efecto de la predilatación de la rama lateral en los resultados obtenidos con la intervención coronaria percutánea en una lesión en bifurcación verdadera, no situada en el tronco principal izquierdo según la clasificación de Medina, empleando la técnica de stent condicional.
MétodosSe compararon los fallos en el vaso diana (objetivo combinado de muerte cardiaca, infarto de miocardio o revascularización del vaso diana) entre los pacientes a los que se predilató la rama lateral (grupo de predilatación, n = 175) y los que no (grupo sin predilatación, n = 662).
ResultadosEn el grupo de predilatación el hinchado del kissing-balloon final (el 57,1 frente al 35,8%; p < 0,001) se realizó con mayor frecuencia y el porcentaje de cambio a una técnica de dos stents fue mayor (el 14,9 frente al 5,1%; p < 0,001). Durante una mediana de seguimiento de 21 meses, el grupo de predilatación presentó incidencias de fallos en el vaso diana (el 14,3 frente al 6,8%; p = 0,002) y de revascularización del vaso diana (el 12,0 frente al 5,6%; p = 0,003) superiores que el grupo sin predilatación, pero no de muerte cardiaca e infarto de miocardio. En el análisis multivariable, la predilatación la rama lateral se asoció con mayor frecuencia de fallos en el vaso diana (razón de riesgos ajustada = 2,11; intervalo de confianza del 95%, 1,27-3,50; p = 0,004). Estos resultados se mantuvieron constantes después de aplicar un análisis de la población igualada por puntuaciones de propensión (para los fallos en el vaso diana, razón de riesgos ajustada = 2,63; intervalo de confianza del 95%, 1,09-6,34; p = 0,0031) y fueron uniformes también en los diversos subgrupos definidos según el ángulo de la bifurcación, la calcificación y la estenosis diametral de la rama lateral.
ConclusionesLa predilatación de la rama lateral antes del implante de stent en el vaso principal puede asociarse con un aumento del riesgo de nueva revascularización para los pacientes con una lesión coronaria en bifurcación verdadera no situada en el tronco principal izquierdo tratados con la técnica de stent condicional.
Registro del ensayo: ClinicalTrials.gov número: NCT00851526.
Palabras clave
A la vista de los resultados obtenidos en numerosos ensayos aleatorizados, actualmente se considera que la técnica de stent condicional de intervención selectiva en la rama lateral (RL) después del implante de stent en el vaso principal es el tratamiento de primera línea para la mayoría de las lesiones en bifurcación1–5. Sin embargo, no está claro que la predilatación de una RL antes de implantar el stent en el vaso principal pueda mejorar los resultados de la intervención y los resultados clínicos de la intervención coronaria percutánea (ICP) en una lesión en bifurcación utilizando la técnica de stent condicional. El objetivo del presente estudio es evaluar el efecto de la predilatación de la RL antes del implante de stent en el vaso principal en los resultados de la intervención y los resultados clínicos a largo plazo de pacientes con lesiones coronarias en bifurcación verdaderas, no situadas en el tronco principal izquierdo, utilizando los datos de un amplio registro específico de lesiones en bifurcación.
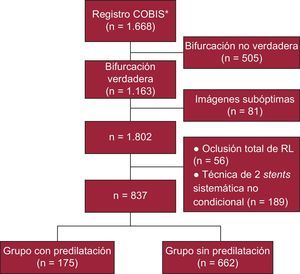
MÉTODOSPoblación en estudioEl COBIS6,7 es un registro multicéntrico retrospectivo de pacientes con lesiones coronarias en bifurcación tratados por ICP con stents farmacoactivos. Se incluyó a un total de 1.668 pacientes consecutivos de 16 centros de intervención coronaria de referencia de Corea del Sur entre enero de 2004 y junio de 2006. Anteriormente se ha publicado información detallada del registro COBIS que se ha empleado ya para otros análisis retrospectivos6,7.
Con objeto de evaluar el efecto de predilatar la RL antes del implante de stent en el vaso principal en los resultados de la intervención y los resultados clínicos, seleccionamos a 1.163 pacientes con lesiones en bifurcación verdaderas no situadas en el tronco principal izquierdo, según lo determinado por la clasificación de Medina8. Se excluyó a un total de 81 pacientes porque las imágenes eran subóptimas e insuficientes para evaluar la predilatación de la RL. De los demás pacientes (n = 1.082), se excluyó a 245; 56 debido a oclusión total de la RL en la evaluación realizada antes de la intervención y 189 pacientes sometidos a intervenciones de implante de 22 stents no condicionales en la RL. Finalmente se incluyó en el estudio a 837 pacientes (figura 1).
Intervención coronaria percutáneaA todos los pacientes se les prescribió ácido acetilsalicílico (300 mg) y clopidogrel (300 o 600 mg), a no ser que se les hubiera administrado previamente esos antiagregantes plaquetarios. Cada operador individual tomó las decisiones de predilatar la RL, llevar a cabo intervención con dos stents o realizar el hinchado final del kissing-ballon.
Obtención de los datos y análisis angiográficoSe obtuvieron datos demográficos, clínicos, angiográficos, de la intervención y de los resultados clínicos empleando un sistema de notificación a través de internet. Se obtuvo información adicional a partir de las historias clínicas o mediante contacto telefónico en caso necesario. Todos los datos de resultados clínicos comunicados por el centro participante fueron verificados por un comité independiente de validación de los eventos clínicos. Las características angiográficas y de la intervención correspondientes a todas las cineangiografías se examinaron y se analizaron en el laboratorio central de angiografía (Cardiac and Vascular Center, Samsung Medical Center, Seúl, Corea del Sur) con un sistema automático de detección de bordes (Centricity CA1000, GE; Waukesha, Wisconsin, Estados Unidos) aplicando definiciones estándares9,10.
Las lesiones en bifurcación se clasificaron según la clasificación de Medina8. Las lesiones con clasificación de Medina (1,1,1), (1,0,1) o (0,1,1) se consideraron lesiones en bifurcación verdaderas. Para el análisis angiográfico coronario cuantitativo, las lesiones en bifurcación se dividieron en ocho segmentos (figura 1 del material suplementario)11. Para el vaso principal, el diámetro de referencia se definió como la media de los diámetros luminales de referencia proximal y distal. Para la RL, el diámetro de referencia fue el diámetro luminal de referencia distal.
Variables de valoración del estudio y definicionesEl objetivo principal de este estudio es comparar la incidencia del fallo en el vaso diana (FVD) entre los pacientes tratados con y sin predilatación de la RL antes de implantar stent en el vaso principal. El FVD se definió mediante la variable de valoración combinada de muerte cardiaca, infarto de miocardio o revascularización del vaso diana (RVD). Los eventos clínicos se definieron según las recomendaciones del Academic Research Consortium12. El ángulo de bifurcación se definió como el formado por el eje del vaso principal con el eje de la RL en su origen. El diámetro de la estenosis en el ostium de la RL se calculó con la siguiente fórmula: 100 × (diámetro de referencia de la RL distal – diámetro luminal mínimo del ostium de la RL) / diámetro de referencia de la RL distal. Se identificaron las calcificaciones como radioopacidades manifiestas dentro de la pared vascular en el lugar de la estenosis, y se clasificaron como moderadas (radioopacidades observadas tan solo durante el ciclo cardiaco anterior a la inyección de contraste) o graves (radioopacidades observadas sin movimiento cardiaco antes de la inyección de contraste y que generalmente comprometían ambos lados de la luz arterial)13. Se definió la oclusión aguda relacionada con la ICP como la aparición de un flujo de grado < 3 de Thrombolysis In Myocardial Infarction durante la intervención de cualificación para el estudio. El éxito angiográfico se definió por la obtención de un flujo Thrombolysis In Myocardial Infarction 3 con una estenosis residual final < 30% en el vaso principal o < 50% en la RL. El éxito de la intervención se definió como el éxito angiográfico sin eventos cardiacos adversos mayores durante la estancia en el hospital. El infarto de miocardio periintervención se definió como una elevación de la banda miocárdica de la creatincinasa ≥ 3 veces el límite superior de la normalidad después de la ICP de cualificación. El periodo periintervención incluyó las primeras 48 h siguientes a la ICP, y el infarto de miocardio periintervención no se consideró objetivo principal en este estudio.
Análisis estadísticoLas variables continuas se presentan como media ± desviación estándar o mediana [intervalo intercuartílico]. Las variables categóricas se presentan en forma de frecuencias y porcentajes. Las variables continuas se analizaron con la prueba de la t de Student para muestras independientes o con la prueba de Mann-Whitney, y las variables categóricas se analizaron con la prueba de la χ2 o la exacta de Fisher. Las tasas acumulativas de eventos se estimaron con los métodos de Kaplan-Meier y se compararon mediante log rank test. Se utilizó el modelo de riesgos proporcionales de Cox para identificar los factores independientes predictivos de los resultados clínicos individuales. Las covariables estadísticamente significativas en el análisis univariable (p < 0,05) o las que se consideraron clínicamente relevantes se tomaron como variables candidatas para los modelos multivariable. Se seleccionaron las siguientes variables para el análisis del FVD con el modelo de riesgos proporcionales de Cox: diabetes mellitus, síndrome coronario agudo como forma de presentación, creatinina, ángulo de la bifurcación, estenosis del diámetro del ostium de la RL, longitud de la lesión de la RL, calcificación moderada o grave en la RL, tipo de stent farmacoactivo, longitud total del stent en el vaso principal, hinchado final del kissing-balloon y predilatación de la RL antes del implante de stent en el vaso principal.
Con objeto de reducir el sesgo de selección del tratamiento para la predilatación de la RL y los posibles factores de confusión, llevamos a cabo ajustes rigurosos respecto a las características basales de los pacientes utilizando sus puntuaciones de propensión. Las puntuaciones de propensión se estimaron empleando análisis de regresión logística múltiple. Se elaboró un modelo completo no restringido, que incluía casi todas las variables de las tablas 1 y 2, y los datos angiográficos coronarios cuantitativos basales de la tabla 3. Se determinó la capacidad de discriminación y la calibración del modelo de puntuación de propensión mediante el estadístico c y el estadístico de Hosmer-Lemeshow. Se evaluó el equilibrio de las covariables basales en los dos grupos en una población igualada por la puntuación de propensión. Se compararon las variables continuas con la prueba de la t de Student para datos apareados o con la prueba de Mann-Whitney según fuera apropiado y las variables categóricas, con las pruebas de McNemar o Bhapkar de simetría según correspondiese. En la población igualada por la puntuación de propensión, se compararon las razones de riesgos (HR) de los resultados clínicos mediante un modelo de regresión de Cox estratificado. Se aceptó como significación estadística un valor de p bilateral < 0,05. Todos los análisis se llevaron a cabo con el programa informático SAS (Statistical Analysis System) versión 9.1. (SAS Institute; Cary, North Carolina, Estados Unidos).
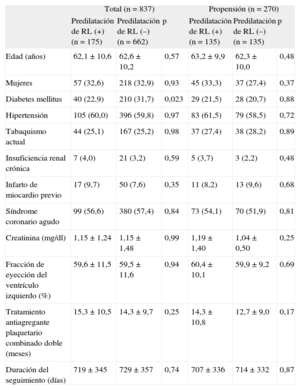
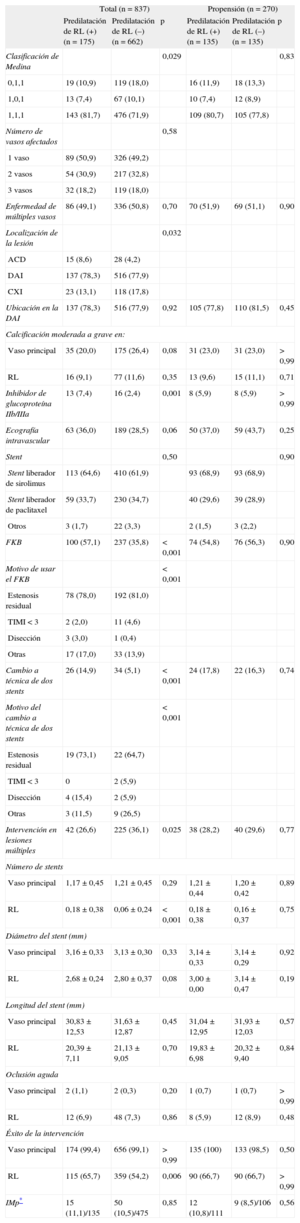
Características clínicas basales
| Total (n = 837) | Propensión (n = 270) | |||||
| Predilatación de RL (+) (n = 175) | Predilatación de RL (–) (n = 662) | p | Predilatación de RL (+) (n = 135) | Predilatación de RL (–) (n = 135) | p | |
| Edad (años) | 62,1 ± 10,6 | 62,6 ± 10,2 | 0,57 | 63,2 ± 9,9 | 62,3 ± 10,0 | 0,48 |
| Mujeres | 57 (32,6) | 218 (32,9) | 0,93 | 45 (33,3) | 37 (27,4) | 0,37 |
| Diabetes mellitus | 40 (22,9) | 210 (31,7) | 0,023 | 29 (21,5) | 28 (20,7) | 0,88 |
| Hipertensión | 105 (60,0) | 396 (59,8) | 0,97 | 83 (61,5) | 79 (58,5) | 0,72 |
| Tabaquismo actual | 44 (25,1) | 167 (25,2) | 0,98 | 37 (27,4) | 38 (28,2) | 0,89 |
| Insuficiencia renal crónica | 7 (4,0) | 21 (3,2) | 0,59 | 5 (3,7) | 3 (2,2) | 0,48 |
| Infarto de miocardio previo | 17 (9,7) | 50 (7,6) | 0,35 | 11 (8,2) | 13 (9,6) | 0,68 |
| Síndrome coronario agudo | 99 (56,6) | 380 (57,4) | 0,84 | 73 (54,1) | 70 (51,9) | 0,81 |
| Creatinina (mg/dl) | 1,15 ± 1,24 | 1,15 ± 1,48 | 0,99 | 1,19 ± 1,40 | 1,04 ± 0,50 | 0,25 |
| Fracción de eyección del ventrículo izquierdo (%) | 59,6 ± 11,5 | 59,5 ± 11,6 | 0,94 | 60,4 ± 10,1 | 59,9 ± 9,2 | 0,69 |
| Tratamiento antiagregante plaquetario combinado doble (meses) | 15,3 ± 10,5 | 14,3 ± 9,7 | 0,25 | 14,3 ± 10,8 | 12,7 ± 9,0 | 0,17 |
| Duración del seguimiento (días) | 719 ± 345 | 729 ± 357 | 0,74 | 707 ± 336 | 714 ± 332 | 0,87 |
RL: rama lateral.
Los datos expresan n (%) o media ± desviación estándar.
Datos basales angiográficos y periintervención
| Total (n = 837) | Propensión (n = 270) | |||||
| Predilatación de RL (+) (n = 175) | Predilatación de RL (–) (n = 662) | p | Predilatación de RL (+) (n = 135) | Predilatación de RL (–) (n = 135) | p | |
| Clasificación de Medina | 0,029 | 0,83 | ||||
| 0,1,1 | 19 (10,9) | 119 (18,0) | 16 (11,9) | 18 (13,3) | ||
| 1,0,1 | 13 (7,4) | 67 (10,1) | 10 (7,4) | 12 (8,9) | ||
| 1,1,1 | 143 (81,7) | 476 (71,9) | 109 (80,7) | 105 (77,8) | ||
| Número de vasos afectados | 0,58 | |||||
| 1 vaso | 89 (50,9) | 326 (49,2) | ||||
| 2 vasos | 54 (30,9) | 217 (32,8) | ||||
| 3 vasos | 32 (18,2) | 119 (18,0) | ||||
| Enfermedad de múltiples vasos | 86 (49,1) | 336 (50,8) | 0,70 | 70 (51,9) | 69 (51,1) | 0,90 |
| Localización de la lesión | 0,032 | |||||
| ACD | 15 (8,6) | 28 (4,2) | ||||
| DAI | 137 (78,3) | 516 (77,9) | ||||
| CXI | 23 (13,1) | 118 (17,8) | ||||
| Ubicación en la DAI | 137 (78,3) | 516 (77,9) | 0,92 | 105 (77,8) | 110 (81,5) | 0,45 |
| Calcificación moderada a grave en: | ||||||
| Vaso principal | 35 (20,0) | 175 (26,4) | 0,08 | 31 (23,0) | 31 (23,0) | > 0,99 |
| RL | 16 (9,1) | 77 (11,6) | 0,35 | 13 (9,6) | 15 (11,1) | 0,71 |
| Inhibidor de glucoproteína IIb/IIIa | 13 (7,4) | 16 (2,4) | 0,001 | 8 (5,9) | 8 (5,9) | > 0,99 |
| Ecografía intravascular | 63 (36,0) | 189 (28,5) | 0,06 | 50 (37,0) | 59 (43,7) | 0,25 |
| Stent | 0,50 | 0,90 | ||||
| Stent liberador de sirolimus | 113 (64,6) | 410 (61,9) | 93 (68,9) | 93 (68,9) | ||
| Stent liberador de paclitaxel | 59 (33,7) | 230 (34,7) | 40 (29,6) | 39 (28,9) | ||
| Otros | 3 (1,7) | 22 (3,3) | 2 (1,5) | 3 (2,2) | ||
| FKB | 100 (57,1) | 237 (35,8) | < 0,001 | 74 (54,8) | 76 (56,3) | 0,90 |
| Motivo de usar el FKB | < 0,001 | |||||
| Estenosis residual | 78 (78,0) | 192 (81,0) | ||||
| TIMI < 3 | 2 (2,0) | 11 (4,6) | ||||
| Disección | 3 (3,0) | 1 (0,4) | ||||
| Otras | 17 (17,0) | 33 (13,9) | ||||
| Cambio a técnica de dos stents | 26 (14,9) | 34 (5,1) | < 0,001 | 24 (17,8) | 22 (16,3) | 0,74 |
| Motivo del cambio a técnica de dos stents | < 0,001 | |||||
| Estenosis residual | 19 (73,1) | 22 (64,7) | ||||
| TIMI < 3 | 0 | 2 (5,9) | ||||
| Disección | 4 (15,4) | 2 (5,9) | ||||
| Otras | 3 (11,5) | 9 (26,5) | ||||
| Intervención en lesiones múltiples | 42 (26,6) | 225 (36,1) | 0,025 | 38 (28,2) | 40 (29,6) | 0,77 |
| Número de stents | ||||||
| Vaso principal | 1,17 ± 0,45 | 1,21 ± 0,45 | 0,29 | 1,21 ± 0,44 | 1,20 ± 0,42 | 0,89 |
| RL | 0,18 ± 0,38 | 0,06 ± 0,24 | < 0,001 | 0,18 ± 0,38 | 0,16 ± 0,37 | 0,75 |
| Diámetro del stent (mm) | ||||||
| Vaso principal | 3,16 ± 0,33 | 3,13 ± 0,30 | 0,33 | 3,14 ± 0,33 | 3,14 ± 0,29 | 0,92 |
| RL | 2,68 ± 0,24 | 2,80 ± 0,37 | 0,08 | 3,00 ± 0,00 | 3,14 ± 0,47 | 0,19 |
| Longitud del stent (mm) | ||||||
| Vaso principal | 30,83 ± 12,53 | 31,63 ± 12,87 | 0,45 | 31,04 ± 12,95 | 31,93 ± 12,03 | 0,57 |
| RL | 20,39 ± 7,11 | 21,13 ± 9,05 | 0,70 | 19,83 ± 6,98 | 20,32 ± 9,40 | 0,84 |
| Oclusión aguda | ||||||
| Vaso principal | 2 (1,1) | 2 (0,3) | 0,20 | 1 (0,7) | 1 (0,7) | > 0,99 |
| RL | 12 (6,9) | 48 (7,3) | 0,86 | 8 (5,9) | 12 (8,9) | 0,48 |
| Éxito de la intervención | ||||||
| Vaso principal | 174 (99,4) | 656 (99,1) | > 0,99 | 135 (100) | 133 (98,5) | 0,50 |
| RL | 115 (65,7) | 359 (54,2) | 0,006 | 90 (66,7) | 90 (66,7) | > 0,99 |
| IMp* | 15 (11,1)/135 | 50 (10,5)/475 | 0,85 | 12 (10,8)/111 | 9 (8,5)/106 | 0,56 |
ACD: arteria coronaria derecha; CXI: circunfleja izquierda; DAI: arteria coronaria descendente anterior izquierda; FKB: final kissing-ballooning; IMp: infarto de miocardio periintervención; RL: rama lateral; TIMI: Thrombolysis In Myocardial Infarction.
Los datos expresan n (%) o media ± desviación estándar
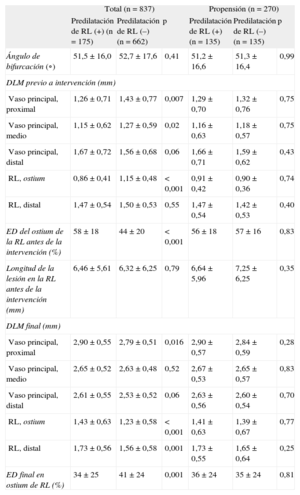
Datos cuantitativos de angiografía coronaria
| Total (n = 837) | Propensión (n = 270) | |||||
| Predilatación de RL (+) (n = 175) | Predilatación de RL (–) (n = 662) | p | Predilatación de RL (+) (n = 135) | Predilatación de RL (–) (n = 135) | p | |
| Ángulo de bifurcación (∘) | 51,5 ± 16,0 | 52,7 ± 17,6 | 0,41 | 51,2 ± 16,6 | 51,3 ± 16,4 | 0,99 |
| DLM previo a intervención (mm) | ||||||
| Vaso principal, proximal | 1,26 ± 0,71 | 1,43 ± 0,77 | 0,007 | 1,29 ± 0,70 | 1,32 ± 0,76 | 0,75 |
| Vaso principal, medio | 1,15 ± 0,62 | 1,27 ± 0,59 | 0,02 | 1,16 ± 0,63 | 1,18 ± 0,57 | 0,75 |
| Vaso principal, distal | 1,67 ± 0,72 | 1,56 ± 0,68 | 0,06 | 1,66 ± 0,71 | 1,59 ± 0,62 | 0,43 |
| RL, ostium | 0,86 ± 0,41 | 1,15 ± 0,48 | < 0,001 | 0,91 ± 0,42 | 0,90 ± 0,36 | 0,74 |
| RL, distal | 1,47 ± 0,54 | 1,50 ± 0,53 | 0,55 | 1,47 ± 0,54 | 1,42 ± 0,53 | 0,40 |
| ED del ostium de la RL antes de la intervención (%) | 58 ± 18 | 44 ± 20 | < 0,001 | 56 ± 18 | 57 ± 16 | 0,83 |
| Longitud de la lesión en la RL antes de la intervención (mm) | 6,46 ± 5,61 | 6,32 ± 6,25 | 0,79 | 6,64 ± 5,96 | 7,25 ± 6,25 | 0,35 |
| DLM final (mm) | ||||||
| Vaso principal, proximal | 2,90 ± 0,55 | 2,79 ± 0,51 | 0,016 | 2,90 ± 0,57 | 2,84 ± 0,59 | 0,28 |
| Vaso principal, medio | 2,65 ± 0,52 | 2,63 ± 0,48 | 0,52 | 2,67 ± 0,53 | 2,65 ± 0,57 | 0,83 |
| Vaso principal, distal | 2,61 ± 0,55 | 2,53 ± 0,52 | 0,06 | 2,63 ± 0,56 | 2,60 ± 0,54 | 0,70 |
| RL, ostium | 1,43 ± 0,63 | 1,23 ± 0,58 | < 0,001 | 1,41 ± 0,63 | 1,39 ± 0,67 | 0,77 |
| RL, distal | 1,73 ± 0,56 | 1,56 ± 0,58 | 0,001 | 1,73 ± 0,55 | 1,65 ± 0,64 | 0,25 |
| ED final en ostium de RL (%) | 34 ± 25 | 41 ± 24 | 0,001 | 36 ± 24 | 35 ± 24 | 0,81 |
DLM: diámetro luminal mínimo; ED: estenosis diametral; RL: rama lateral.
Los datos expresan media ± desviación estándar.
La predilatación de la RL antes de implantar stent en el vaso principal se llevó a cabo en 175 (20,9%) pacientes. Entre los grupos no hubo diferencias significativas en las características clínicas basales, excepto el porcentaje de pacientes con diabetes mellitus (tabla 1). En la tabla 2 se presentan los datos angiográficos y periintervención. Había una diferencia significativa entre los grupos en cuanto a la clasificación de Medina (p = 0,029). En el grupo de predilatación, se realizó con mayor frecuencia el hinchado final del kissing-balloon y el porcentaje de cambio a una técnica de dos stents fue superior. Así pues, el porcentaje de éxitos de la intervención en la RL fue mayor en el grupo de predilatación, a pesar de que no hubo diferencias significativas en la frecuencia de oclusiones agudas del vaso principal o de la RL asociadas a la ICP. Además, la incidencia de infarto de miocardio periintervención tampoco se redujo en el grupo de predilatación (el 11,1 frente al 10,5%; odds ratio ajustada = 1,05; intervalo de confianza del 95% [IC95%], 0,42-2,60; p = 0,92).
Datos cuantitativos de angiografía coronariaLos datos cuantitativos de angiografía coronaria se presentan en la tabla 3.
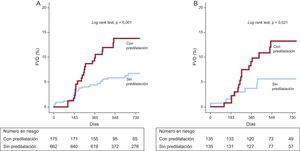
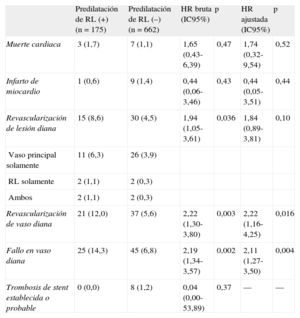
Resultados clínicosSe dispuso de datos de seguimiento clínico completos de todos los pacientes incluidos en este estudio. No hubo entre los grupos diferencias significativas en la duración del seguimiento (tabla 1). Durante una mediana de seguimiento de 21 [14-31] meses, se produjeron 45 (5,4%) casos de revascularización en la lesión diana y 70 (8,4%) casos de FVD. En total, el 82,2% (37 de 45) de las revascularización en la lesión diana se llevaron a cabo en el vaso principal; el 8,9%, en la RL, y el 8,9% restante, tanto en el vaso principal como en la RL. La incidencia de FVD fue significativamente superior en el grupo de predilatación, y la diferencia se debió principalmente a la mayor frecuencia de RVD en el grupo de predilatación (tabla 4 y figura 2A). Sin embargo, las tasas de muerte cardiaca, infarto de miocardio y trombosis de stent no mostraron diferencias significativas entre los grupos. En el análisis multivariable, el grupo de predilatación presentó probabilidades de FVD y RVD ajustadas significativamente mayores.
Resultados clínicos a largo plazo en la población total
| Predilatación de RL (+) (n = 175) | Predilatación de RL (–) (n = 662) | HR bruta (IC95%) | p | HR ajustada (IC95%) | p | |
| Muerte cardiaca | 3 (1,7) | 7 (1,1) | 1,65 (0,43-6,39) | 0,47 | 1,74 (0,32-9,54) | 0,52 |
| Infarto de miocardio | 1 (0,6) | 9 (1,4) | 0,44 (0,06-3,46) | 0,43 | 0,44 (0,05-3,51) | 0,44 |
| Revascularización de lesión diana | 15 (8,6) | 30 (4,5) | 1,94 (1,05-3,61) | 0,036 | 1,84 (0,89-3,81) | 0,10 |
| Vaso principal solamente | 11 (6,3) | 26 (3,9) | ||||
| RL solamente | 2 (1,1) | 2 (0,3) | ||||
| Ambos | 2 (1,1) | 2 (0,3) | ||||
| Revascularización de vaso diana | 21 (12,0) | 37 (5,6) | 2,22 (1,30-3,80) | 0,003 | 2,22 (1,16-4,25) | 0,016 |
| Fallo en vaso diana | 25 (14,3) | 45 (6,8) | 2,19 (1,34-3,57) | 0,002 | 2,11 (1,27-3,50) | 0,004 |
| Trombosis de stent establecida o probable | 0 (0,0) | 8 (1,2) | 0,04 (0,00-53,89) | 0,37 | — | — |
HR: razón de riesgos; IC95%: intervalo de confianza del 95%; RL: rama lateral.
Salvo otra indicación, los datos expresan n (%).
*Muerte cardiaca, infarto de miocardio y revascularización de vaso diana.
Tras aplicar una igualación por puntuación de propensión, se generó un total de 135 pares igualados. El estadístico c para el modelo de puntuación de propensión fue 0,790, lo cual indica una discriminación aceptable. No hubo diferencias significativas en las características clínicas, angiográficas y de la intervención basales de la población igualada por puntuación de propensión (tablas 1 y 2). La incidencia de infarto de miocardio periintervención fue similar en los dos grupos (OR ajustada = 1,71; IC95%, 0,16-18,26; p = 0,66). En la tabla 3 se presentan los datos cuantitativos de angiografía coronaria correspondientes a la población igualada por puntuación de propensión.
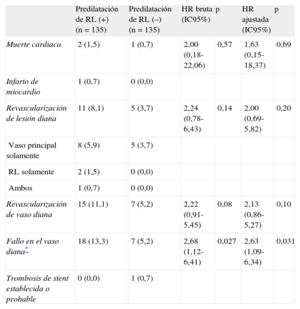
Se produjo un total de 25 FVD durante una mediana de seguimiento de la población igualada de 21 meses. En el grupo de predilatación, los resultados clínicos fueron significativamente peores en la población igualada (tabla 5 y figura 2B). Aunque no hubo diferencias significativas entre los grupos en cuanto a la incidencia de muerte cardiaca o infarto de miocardio, los pacientes del grupo de predilatación presentaron una tasa significativamente superior de revascularización en la lesión diana, RVD y FVD. En el análisis multivariable, empleando la estenosis basal del diámetro de la RL como covariable, el grupo de predilatación continuó mostrando una incidencia de FVD ajustada significativamente superior.
Resultados clínicos a largo plazo en la población igualada por puntuación de propensión
| Predilatación de RL (+) (n = 135) | Predilatación de RL (–) (n = 135) | HR bruta (IC95%) | p | HR ajustada (IC95%) | p | |
| Muerte cardiaca | 2 (1,5) | 1 (0,7) | 2,00 (0,18-22,06) | 0,57 | 1,63 (0,15-18,37) | 0,69 |
| Infarto de miocardio | 1 (0,7) | 0 (0,0) | ||||
| Revascularización de lesión diana | 11 (8,1) | 5 (3,7) | 2,24 (0,78-6,43) | 0,14 | 2,00 (0,69-5,82) | 0,20 |
| Vaso principal solamente | 8 (5,9) | 5 (3,7) | ||||
| RL solamente | 2 (1,5) | 0 (0,0) | ||||
| Ambos | 1 (0,7) | 0 (0,0) | ||||
| Revascularización de vaso diana | 15 (11,1) | 7 (5,2) | 2,22 (0,91-5,45) | 0,08 | 2,13 (0,86-5,27) | 0,10 |
| Fallo en el vaso diana* | 18 (13,3) | 7 (5,2) | 2,68 (1,12-6,41) | 0,027 | 2,63 (1,09-6,34) | 0,031 |
| Trombosis de stent establecida o probable | 0 (0,0) | 1 (0,7) |
IC95%: intervalo de confianza del 95%; HR: razón de riesgos; RL: rama lateral.
Salvo otra indicación, los datos expresan n (%).
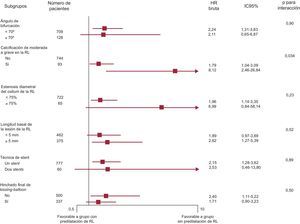
Con objeto de determinar si el aumento del riesgo de FVD observado con la predilatación de la RL en la población total es constante, comparamos la HR de la predilatación de la RL en cuanto al FVD en diversos subgrupos importantes (ángulo de bifurcación < 70° frente a ≥ 70°, calcificación en la RL de moderada a grave, diámetro de la estenosis del ostium de la RL < 75% frente a ≥ 75%, longitud basal de la lesión presente en la RL < 5 mm frente a ≥ 5 mm, técnica de un stent e hinchado final del kissing-balloon). La tasa de FVD fue uniformemente superior en todos los subgrupos especificados del grupo de predilatación (figura 3). Además, se observó una interacción significativa entre la predilatación de la RL y la calcificación de moderada a grave en la RL. En el grupo de predilatación, se observó una tasa de FVD muy superior tanto entre los pacientes con calcificación de moderada a grave como sin ella.
Además, se analizó también la HR ajustada de la predilatación de la RL en varias cohortes específicas. Entre los pacientes de la cohorte en que no se realizó el hinchado final del kissing-balloon, hubo una tendencia en el límite de la significación a mayor tasa de FVD ajustada en el grupo de predilatación (HR ajustada = 2,16; IC95%, 0,99-4,72; p = 0,054). Además, se observó que la predilatación de la RL seguía siendo un significativo factor de riesgo de FVD ajustado en la cohorte de pacientes tratados con técnica de un stent (HR ajustada = 2,02; IC95%, 1,18-3,44; p = 0,01).
DISCUSIÓNEl presente análisis es la primera investigación realizada sobre el efecto en los resultados de la intervención y clínicos a largo plazo de predilatar la RL antes del implante de stent en el vaso principal, empleando los datos de un amplio registro específico de lesiones en bifurcación. Se observó que en el grupo de predilatación el hinchado final del kissing-balloon se realizó con mayor frecuencia y que el porcentaje de cambios a una técnica de dos stents fue superior. Así pues, el porcentaje de éxitos de la intervención para la RL fue mayor en el grupo de predilatación que en el grupo sin predilatación, a pesar de que no hubo diferencias en la frecuencia de la oclusión aguda de la RL ni en la del infarto de miocardio periintervención entre los grupos con predilatación y si ella. Sin embargo, la predilatación de la RL aumentó el riesgo a largo plazo de FVD ajustado, principalmente como resultado de un aumento del riesgo de RVD. Además, no se observaron grandes diferencias intergrupales en las tasas de muerte cardiaca, infarto de miocardio o trombosis de stent.
Aunque la técnica de un stent con método de stent condicional en la RL es sencilla y actualmente se la considera el patrón de referencia para la mayoría de las lesiones en bifurcación1–5, no se ha establecido todavía un método óptimo y, por consiguiente, se han introducido nuevas técnicas14. Sin embargo, no hay ningún estudio específico que haya determinado si la predilatación de la RL antes de implantar stent en el vaso principal aporta un efecto beneficioso a los pacientes con lesiones en bifurcación verdaderas no situadas en el tronco principal izquierdo tratados con stents farmacoactivos. Teóricamente, la predilatación de la RL puede servir de andamiaje en el origen de la RL, con lo que se mantiene el acceso a la RL después de implantar stent en el vaso principal. En el presente estudio, el porcentaje de éxitos de la intervención para la RL fue superior en el grupo de predilatación, a pesar de que otros parámetros de valoración del resultado de la intervención fueron similares en los dos grupos. No obstante, los resultados clínicos a largo plazo fueron peores en el grupo de predilatación de la RL.
La predilatación de la RL puede conducir a una disección de esta y a un aumento del riesgo de volver a cruzar el strut más proximal a través de un plano de disección, lo cual aumentaría, a su vez, la probabilidad de un hinchado del kissing-balloon potencialmente innecesario y/o el implante de stent en la RL15. Debido a la segunda intervención, como el hinchado del kissing-balloon y/o el implante de stent en la RL después de implantar stent en el vaso principal, los resultados inmediatos tras la intervención fueron mejores en el grupo de predilatación que en el grupo sin predilatación. En el presente estudio, el porcentaje de éxitos de la intervención para la RL en el grupo de predilatación fue superior que en el grupo sin predilatación. Los resultados identificados en este análisis concuerdan con lo observado en un reciente ensayo aleatorizado presentado en EuroPCR 201316. Pan et al aleatorizaron a 372 pacientes con lesiones en bifurcación a tratamiento con stent condicional (n = 187) o sin predilatación de la RL (n = 185). El objetivo principal mostró mejor resultado en el grupo de predilatación. Es decir, la prevalencia de flujo Thrombolysis In Myocardial Infarction 0-1 con la predilatación fue inferior que sin ella (el 1 frente al 10%; p < 0,001) después de implantar stent en el vaso principal.
Sin embargo, la ventaja inmediata tras la intervención observada en el presente estudio no se tradujo en un resultado favorable a largo plazo. Estos resultados inesperados son algo sorprendentes, y continúan sin estar claras las razones subyacentes. Sin embargo, es posible que haya una explicación para la incidencia relativamente alta del FVD ajustado en los pacientes tratados con predilatación de la RL. En primer lugar, el hinchado final del kissing-balloon se realizó con mayor frecuencia en el grupo de predilatación. Gwon et al11 describieron que, en pacientes tratados con la técnica de un stent, el hinchado final del kissing-balloon aumentó el riesgo de eventos adversos cardiacos mayores a largo plazo. En segundo lugar, el porcentaje de cambios a una técnica de dos stents fue más alto en el grupo de predilatación. Un examen de los datos individuales de los pacientes de dos ensayos aleatorizados actuales puso de manifiesto que la técnica de stent en T condicional es superior a una técnica compleja17. Por consiguiente, los efectos desfavorables de predilatar la RL en los resultados clínicos pueden deberse a un aumento de la probabilidad de un hinchado final del kissing-balloon potencialmente innecesario o de un cambio a implante de stent en la RL. Sin embargo, en el presente estudio, la predilatación de la RL fue un factor independiente de riesgo de FVD ajustado incluso en los análisis multivariable, y la diferencia de resultados en función de la predilatación de la RL no variaba en los diversos subgrupos de pacientes. En el grupo de predilatación, se observó una tendencia en el límite de la significación a una frecuencia superior del FVD ajustado en la cohorte sin hinchado final del kissing-balloon, mientras que la predilatación de la RL fue un significativo factor de riesgo de FVD ajustado en la cohorte con la técnica de un stent. Estos resultados indican que la predilatación de la RL puede tener de por sí efectos negativos en los resultados clínicos.
Algunos expertos han recomendado que se emplee la predilatación de la RL cuando el acceso a la RL sea difícil o haya una lesión grave y calcificada en la RL18. Sin embargo, en el presente estudio, los análisis de subgrupos preespecificados (ángulo de bifurcación, diámetro de la estenosis en el ostium de la RL y grado de calcificación en la RL) no revelaron interacciones significativas con la predilatación. En cambio, la tasa de FVD fue muy superior entre los pacientes del grupo de predilatación con y sin calcificación de moderada a grave. A la vista de nuestros resultados, la aplicación sistemática de la predilatación de la RL antes de implantar stent en el vaso principal puede no ser apropiada en la técnica de stent condicional para una lesión coronaria en bifurcación verdadera no situada en el tronco principal izquierdo.
Limitaciones del estudioEl presente estudio tiene ciertas limitaciones. En primer lugar, no es un ensayo aleatorizado y, por consiguiente, hay factores de confusión que pueden haber afectado de manera significativa a los resultados. Por ejemplo, la predilatación de la RL se llevó a cabo por decisión de los operadores, con mayor frecuencia en pacientes con características de la lesión desfavorables. Así pues, inevitablemente, los grupos no eran iguales. Para abordar esta limitación, se realizó un análisis multivariable con el modelo de riesgos proporcionales de Cox, un análisis con igualación por puntuación de propensión y diversos análisis de subgrupos con objeto de introducir un ajuste respecto a las diferencias en las características de los pacientes. Sin embargo, sigue habiendo una probabilidad considerable de que haya otros factores no evaluados o no documentados que hayan introducido confusión en la relación entre las estrategias de tratamiento y los resultados, a pesar de los amplios ajustes realizados respecto a los factores de riesgo basales. Además, dado que este estudio es retrospectivo, es posible que algunos casos no hayan sido detectados a causa de un registro incompleto de la intervención o de unas imágenes subóptimas insuficientes para evaluar la predilatación de la RL. Sin embargo, investigamos si los operadores intentaron aplicar una técnica de stent condicional en la fase inicial de la obtención de datos en el registro COBIS. En segundo lugar, en este estudio la potencia estadística de la muestra igualada por puntuación de propensión no fue suficiente para predecir los eventos clínicos. Esto puede atribuirse al relativamente bajo número de pacientes del estudio. La revascularización en la lesión diana estaba aumentada en aproximadamente 2 veces antes del ajuste y después perdió la significación, mientras que la RVD y el FVD continuaron siendo significativos. Tal vez esta observación se debiera también al número relativamente bajo de pacientes con revascularización en la lesión diana. En consecuencia, los resultados deben considerarse generadores de hipótesis y se deberá confirmarlos en ensayos aleatorizados amplios. En tercer lugar, parece que el diámetro de la estenosis en el ostium de la RL no era grave. Para el presente análisis, se seleccionó a pacientes con una lesión en bifurcación verdadera no situada en el tronco principal izquierdo, según la clasificación de Medina. La clasificación de Medina se estableció por estimación visual, que tiende a sobrestimar la gravedad de la estenosis en la lesión arterial coronaria en mayor medida que el análisis cuantitativo de la angiografía coronaria. Así pues, en el presente análisis se habrían incluido lesiones de la RL con estenosis menos graves según la evaluación del análisis cuantitativo de la angiografía coronaria. En consecuencia, puede resultar difícil extraer las mismas conclusiones acerca de la RL con estenosis más graves, que son la razón de que los cardiólogos intervencionistas opten a menudo por predilatar la RL antes de implantar stent en el vaso principal. Sin embargo, importancia angiográfica no siempre equivale a importancia funcional. Koo et al19,20 observaron que la evaluación angiográfica sobrestima la gravedad funcional de las lesiones de RL enjauladas en cada paso de la estrategia de stent condicional para las lesiones en bifurcación. Por último, los datos cuantitativos de angiografía coronaria se obtuvieron con un análisis de angiografía coronaria cuantitativa bidimensional convencional. Sin embargo, en las lesiones en bifurcación, el análisis de angiografía coronaria cuantitativa bidimensional es menos exacto, preciso y reproducible que el análisis cuantitativo tridimensional. Esto también es una limitación del estudio.
CONCLUSIONESEmpleando un registro amplio específico de lesiones en bifurcación, se ha estudiado el efecto en los resultados de la intervención y clínicos a largo plazo de predilatar la RL antes del implante de stent en el vaso principal. La predilatación de la RL aumentó el riesgo a largo plazo de FVD, debido principalmente al aumento del riesgo de RVD. A la vista de estos resultados, el empleo sistemático de predilatación de la RL antes de implantar stent en el vaso principal puede no ser apropiado para las lesiones en bifurcación fuera del tronco principal izquierdo usando una técnica de stent condicional en la era actual de la ICP. Sin embargo, este estudio es tan solo generador de hipótesis y se deberá confirmar los resultados en estudios aleatorizados y controlados de mayor tamaño.
CONFLICTO DE INTERESESNinguno.
Este registro fue patrocinado por la Korean Society of Interventional Cardiology.
Se puede consultar material suplementario a este artículo en su versión electrónica disponible en doi:10.1016/j.recesp.2014.01.033.