La insuficiencia cardiaca izquierda es la manifestación final de cardiopatías de diversa etiología que cursan con disfunción del ventrículo izquierdo, entre las que destaca la cardiopatía isquémica1. Gracias a los avances en su tratamiento la prevalencia es creciente, pero su curso natural se asocia a una continua disminución de la calidad de vida y a rehospitalizaciones, con una mortalidad precoz2. Estudios previos han demostrado que un estricto control de la presión auricular izquierda se asocia a una mejoría en la función ventricular y la clase funcional, lo que indica un potencial de mejoría en el pronóstico mediante esta estrategia1. El dispositivo V-Wave (V-Wave Ltd, Or Akiva, Israel) se basa en este concepto y en experiencias anteriores en la creación de cortocircuitos interauriculares para el alivio de pacientes con cardiopatías congénitas o con sistemas de asistencia ventricular mecánica3–5. Está constituido por un marco de nitinol con forma de reloj de arena que tiene un recubrimiento de un polímero de politetrafluoroetileno en su lado izquierdo y una válvula con tres velos de pericardio bovino en el lado derecho, para prevenir embolias paradójicas y el cierre precoz del cortocircuito, lo que permite una disminución permanente de la presión auricular izquierda (figura).
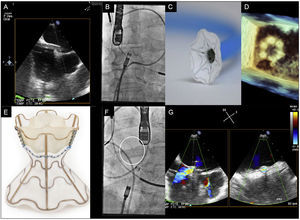
A: paso de la vaina hasta la aurícula izquierda por la fossa ovalis. B, C y D: imagen angiográfica (B), en banco de pruebas (C) y mediante ecocardiografía 3D (D) de la apertura de la parte izquierda del dispositivo en la aurícula izquierda. E, F y G: imágenes en banco de pruebas (E), angiográfica (F) y ecocardiográfica con Doppler color (G) del dispositivo V-Wave desplegado.
El primer caso se describió en Canadá6 y recientemente esta tecnología se ha introducido en Europa al realizar con éxito los dos primeros implantes bajo la aprobación de la Agencia Española de Medicamentos y Productos Sanitarios. Los criterios de selección para este estudio First-in-man aparecen resumidos en la tabla. Se ha realizado una detallada evaluación clínica (i.e., Kansas City Cardiomyopathy Questionnaire [KCCQ]) y funcional (test de los 6 minutos), se ha determinado la fracción aminoterminal del propéptido natriurético cerebral (NT-proBNP) y se ha realizado cateterismo cardiaco derecho.
Resumen de los criterios de inclusión y exclusión de pacientes candidatos a implante del dispositivo V-Wave en el estudio First-in-man
| Pacientes con miocardiopatía isquémica/no isquémica crónica en clase III de la New York Heart Association o bien en clase IV seguida de forma ambulatoria, estadio C del American College of Cardiology /American Heart Association; con los siguientes criterios de inclusión/exclusión: |
| Criterios de inclusión:1. Mayor dosis tolerada de fármacos indicados por las guías para el tratamiento de la insuficiencia cardiaca.2. Resincronización cardiaca (si indicada) al menos 90 días antes.3. Desfibrilador implantable (si indicado) al menos 30 días antes.4. Fracción de eyección ventricular izquierda > 15% y ≤ 40%.5. Los siguientes parámetros de cateterismo derecho: PCP ≥ 15 y ≤ 28mmHg, PAD > 4 y ≤ 11mmHg, gradiente medio PCP-PAD ≤ 16mmHg.6. NT-proBNP >1.500 pg/ml.7. Firma de consentimiento informado especificando riesgos (del acceso femoral, la punción transeptal, el propio dispositivo, la anestesia y la ecocardiografía transesofágica). |
| Criterios de exclusión:1. Disfunción ventricular derecha grave.2. Hipertensión pulmonar grave (PAP sistólica > 70 mmHg).3. Valvulopatía grave.4. Trasplante cardiaco previsto en los próximos 6 meses.5. Espesor del tabique a nivel de la fossa ovalis > 3mm.6. Enfermedad maligna activa.7. Bypass coronario, ICP o infarto agudo de miocardio en los 90 días previos.8. Alteración de la coagulación.9. Ictus en los 6 meses previos.10. Fibrilación auricular persistente/permanente.11. Trombo intraventricular.12. Acceso venoso femoral o vena cava inferior no permeable.13. Contraindicación para ecocardiografía transesofágica.14. Enfermedad ventilatoria pulmonar grave.15. Esperanza de vida menor de 1 año por causas no cardiovasculares. |
ICP: intervención coronaria percutánea; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; PAD: presión arterial diastólica; PAP: presión arterial pulmonar; PCP: presión capilar pulmonar.
El primer paciente fue un varón de 73 años de edad con cardiopatía isquémica crónica revascularizada parcialmente, portador de desfibrilador con terapia de resincronización. Presentaba disfunción ventricular izquierda grave (24%), insuficiencia mitral moderada (II/IV) y aceptable función ventricular derecha (desplazamiento sistólico del plano del anillo tricuspídeo [TAPSE, tricuspid annular plane systolic excursion] de 14mm). Recorrió 253 metros en el test de los 6 minutos, la puntuación del KCCQ fue de 35,42 y el cateterismo cardiaco derecho mostró un gasto cardiaco de 3,5 l/min, una presión capilar pulmonar de 26mmHg y una presión en la aurícula derecha de 10mmHg. El NT-proBNP fue de 3.341 pg/ml.
El segundo paciente fue un varón de 70 años de edad diagnosticado de miocardiopatía dilatada de origen isquémico revascularizada mediante cirugía y percutáneamente, portador de desfibrilador. Presentaba disfunción ventricular izquierda grave (28%), con insuficiencia mitral moderada (II/IV) y TAPSE de 19mm. En el test de los 6 minutos recorrió 236 metros, la puntuación del KCCQ fue de 42,45 y el cateterismo cardiaco derecho mostró un gasto cardiaco de 4,8 l/min, una presión capilar pulmonar de 16mmHg y una presión en la aurícula derecha de 5mmHg. El NT-proBNP fue de 1.526 pg/ml.
Ambos pacientes, a pesar de recibir un tratamiento médico óptimo y altas dosis de diuréticos (120mg y 80mg, respectivamente), presentaban disnea en clase funcional III de la New York Heart Association (NYHA) y ortopnea. De acuerdo con un comité de expertos en insuficiencia cardiaca y tras firmar el consentimiento informado, se decidió el implante del dispositivo V-Wave. El procedimiento se llevó a cabo bajo anestesia general para una mejor tolerancia del ecocardiograma transesofágico. A través de un abordaje venoso femoral se accedió a la aurícula derecha, se realizó punción transeptal a nivel de la fossa ovalis y se posicionó en la aurícula izquierda una vaina de 14 Fr (figura A-D). El dispositivo unido al catéter de liberación se empujó a través de la vaina hasta abrir su primera porción en la parte media de la aurícula izquierda. Tras comprobar la correcta aposición al tabique, el dispositivo se desenganchó del catéter de liberación y, tras una ligera tracción de la vaina, se produjo la apertura de la segunda parte del dispositivo en la aurícula derecha y se aseguró su correcta sujeción en el tabique interauricular (figura E-G; véase el vídeo del material suplementario). Tras el implante, el cortocircuito izquierda-derecha se evidenció inmediatamente por ecocardiograma transesofágico en ambos casos (figura G). Ambos pacientes fueron dados de alta a las 24 horas del procedimiento, sin complicaciones, bajo pauta de anticoagulación oral durante 3 meses, periodo durante el cual, por protocolo, no se realizaron otras modificaciones terapéuticas.
A los 3 meses de seguimiento, el dispositivo V-Wave estaba permeable y ambos pacientes se encontraban en clase funcional II de la NYHA, sin ortopnea y con una puntuación en el KCCQ de 62,5 y 63,54, respectivamente. Esta mejoría era evidente también en parámetros objetivos, como un aumento del 27,3% y el 19,0% en la distancia del test de los 6 minutos, unos valores de NT-proBNP de 2.663 pg/ml y 1.129 pg/ml, gasto cardiaco de 4,6 l/min y presión capilar pulmonar de 23mmHg para el primer paciente (Qp:Qs = 1,3) y de 5,2 l/min y 12mmHg para el segundo (Qp:Qs = 1,2). Los prometedores resultados de esta nueva línea terapéutica deberán ser validados a largo plazo.
CONFLICTO DE INTERESESJ. Rodés-Cabau es consultor para V-Wave Ltd.
A los doctores Gimeno, López, Arnold, de la Fuente, Urueña, Pastor y Mota, por su vital contribución al éxito de este proyecto.