El papel de la coronariografía urgente y angioplastia, si procede, en los pacientes con parada cardiaca extrahospitalaria (PCEH) recuperada que no presentan elevación del segmento ST es controvertido. Nuestro objetivo fue evaluar si la coronariografía urgente y la angioplastia mejoran la supervivencia con buen pronóstico neurológico en esta población.
MétodosEn este ensayo clínico multicéntrico, aleatorizado, abierto, incluimos 69 pacientes supervivientes a una PCEH sin elevación del ST y se aleatorizaron a recibir una coronariografía urgente (CU) o diferida (CD). El objetivo primario de eficacia fue el combinado de supervivencia hospitalaria libre de dependencia. El objetivo de seguridad fue un compuesto de eventos cardiacos mayores, incluyendo muerte, reinfarto, sangrado y arritmias ventriculares.
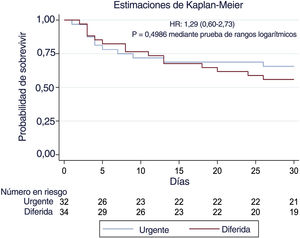
ResultadosSe incluyó a 66 pacientes en el análisis primario (95,7%). La supervivencia hospitalaria fue 62,5% en el grupo CU y 58,8% en el grupo CD (HR = 0,96; IC95%, 0,45-2,09; p=0,93). La supervivencia hospitalaria con buen pronóstico neurológico fue 59,4% en el grupo CU y 52,9% en el grupo CD (HR = 1,29; IC95%, 0,60-2,73; p=0,4986). No se encontraron diferencias en los objetivos secundarios, salvo por la incidencia de fracaso renal agudo, que fue más frecuente en el grupo CU (15,6 frente a 0%, p=0,002) y de infecciones, más prevalentes en el grupo CD (46,9 frente a 73,5%, p=0,003).
ConclusionesEn este estudio aleatorizado de pacientes con una PCEH sin elevación del ST, una CU no fue beneficiosa en términos de supervivencia con buen pronóstico neurológico comparada con una CD.
Identificador ClinicalTrials.gov:NCT02641626
Palabras clave
La parada cardiaca extrahospitalaria (PCEH) es un problema importante de salud pública que explica la mayor parte de la mortalidad en los pacientes con cardiopatía isquémica. A pesar de los avances en el campo de la reanimación y los cuidados intensivos cardiológicos, el pronóstico de estos pacientes sigue siendo malo y más del 70% de ellos fallecen o sobreviven con alteraciones neurológicas graves1.
Se ha observado que la implementación de un protocolo sobre el tratamiento habitual en los cuidados posteriores a la reanimación tras una PCEH, que incluye hipotermia terapéutica, una intervención coronaria de urgencia en los pacientes adecuados y la optimización del tratamiento de cuidados intensivos, mejoró la supervivencia comparado con los controles anteriores a la implementación de este protocolo2.
En varios estudios observacionales, la mayor parte de los cuales incluyen pacientes que han sufrido un infarto de miocardio con elevación del segmento ST (IAMCEST)3–6, se proporcionan indicios de que la coronariografía puede reducir la mortalidad en los pacientes que sufren una PCEH. Basándose en estos estudios, las guías recomiendan una estrategia de intervencionismo coronario primario (ICP) en los pacientes con una parada recuperada y un electrocardiograma compatible con IAMCEST (clase de recomendación I, nivel de evidencia B)7–10. Según las recomendaciones anteriores, debería contemplarse hacer una coronariografía de urgencia (CU) (y un ICP si está indicado) a los pacientes con PCEH y un electrocardiograma sin elevación del segmento ST, pero con una sospecha elevada de isquemia miocárdica en curso (clase de recomendación IIa, nivel de evidencia C)7,8,11. No obstante, recientemente se han publicado 2 ensayos clínicos controlados y aleatorizados con el objetivo de determinar la eficacia de la CU para reducir la mortalidad en los pacientes que han sufrido una PCEH sin IAMCEST. En ambos estudios se concluyó que hacer una CU no era beneficiosa comparada con la coronariografía diferida (CD) en términos de supervivencia. Según las recomendaciones recientes12–14, y basándose en los resultados del ensayo COACT15, debería contemplarse hacer una CD (en las primeras 24horas) en contraposición a la CU en los pacientes que han sufrido una PCEH, están hemodinámicamente estables y no presentan elevación del segmento ST. Sin embargo, en este ensayo, en el grupo tratado con CD, la coronariografía se llevó a cabo dentro de un periodo medio de 5 días. Por consiguiente, existe incertidumbre acerca de cuál es el momento ideal para hacer una angiografía en este grupo de pacientes.
El ensayo coronary angiography in out-of-hospital cardiac arrest patients without ST-segment elevation (COUPE) es un ensayo clínico aleatorizado que compara los efectos de una CU y la angioplastia, si procede con respecto a una CD, en los supervivientes de una PCEH que, tras la recuperación de la circulación espontánea (RCE), no satisfacen los criterios de un IAMCEST y no presentan una causa no isquémica evidente de la parada.
MÉTODOSDiseño del estudio y supervisiónEl COUPE es un ensayo clínico prospectivo, multicéntrico, aleatorizado y abierto, iniciado por investigadores, que compara la eficacia de una CU con una CD en supervivientes de una PCEH sin IAMCEST. El diseño del ensayo se ha publicado con anterioridad16. Los autores diseñaron el protocolo, que recibió la aprobación del comité de ética de cada centro participante..
Todos los investigadores de los centros que participaron en el ensayo avalan la integridad de los datos y la fidelidad del ensayo al protocolo. Un estadístico independiente aseguró la precisión del análisis de los datos.
Centros y pacientesEn el estudio participaron 15 hospitales terciarios de España. Todos estos hospitales son centros de gran volumen con servicio de ICP las 24 horas 7 días a la semana y con experiencia en el tratamiento de pacientes con PCEH en unidades de cuidados intensivos cardiológicos. A todos ellos se les realiza hipotermia terapéutica o control de la temperatura como parte de los cuidados posteriores a la reanimación.
Los pacientes se consideraron idóneos si presentaban RCE dentro de los 60minutos, si permanecían en coma y presentaban un electrocardiograma sin IAMCEST o bloqueo de la rama izquierda del haz de His. En el estudio se incluyeron pacientes tanto con ritmo desfibrilable como no desfibrilable. Antes de aleatorizarlos, se descartó la etiología no isquémica evidente del paro cardiaco como, por ejemplo, la sobredosis de drogas, la embolia pulmonar, el síndrome aórtico agudo, el ictus isquémico o la hemorragia intracraneal. Para ello, se realizaron un ecocardiograma y una tomografía computerizada craneal. En el las tablas 1 y 2 del material adicional, se presentan los criterios de inclusión y exclusión. Se obtuvo el consentimiento informado de todos los pacientes a través de sus familiares más próximos. A todos los pacientes que recuperaron la consciencia sin secuelas neurológicas graves, se les informó de su participación en el estudio y firmaron un consentimiento informado diferido sobre el uso de los datos del estudio en aquel momento. Dicho consentimiento informado podía anularse en cualquier momento y por cualquier motivo.
Aleatorización y tratamientoLos pacientes se asignaron de manera aleatoria y en una proporción 1:1 a una CU (y una ICP en caso de necesidad) o a una CD (y una ICP si era necesario). En el la figura 1, del material adicional, se muestra el esquema del ensayo COUPE. La asignación al grupo de estudio se hizo por aleatorización por bloques, en bloques de 6 pacientes, estratificándola según el ritmo inicial de la parada cardiaca (desfibrilable y no desfibrilable).
En el grupo asignado a CU, la coronariografía se hizo lo antes posible dentro de las 2 primeras horas de haber ingresado en el hospital y tras la aleatorización. En el grupo asignado a CD, la coronariografía se hizo tras la recuperación neurológica, después de extubar al paciente, en general antes de darle el alta de la unidad cuidados intensivos cardiológicos.
Ambos grupos recibieron cuidados sistemáticos en la unidad de cuidados intensivos cardiológicos, como la hipotermia terapéutica, con una temperatura objetivo de 33°C durante 24horas. El tratamiento de soporte, como la ventilación mecánica, la sedación y cualquier otro tratamiento médico, se administró siguiendo la práctica clínica habitual y a criterio de los médicos responsables del paciente en cada caso. Se obtuvieron muestras de sangre para la determinación de troponina en el momento del ingreso y a las 6, 12, 24, 48 y 72 horas. Se registró el tipo de troponina (T, I y ultrasensible dependiendo de los equipos de laboratorio del hospital). El hemograma y la bioquímica (con magnesio, lactato, proteína C reactiva, procalcitonina y enolasa neuronal específica) se obtuvieron en el ingreso y al cabo de 24, 48 y 72horas. Se realizaron un electrocardiograma y un ecocardiograma en el momento del ingreso, cuando el paciente alcanzó la temperatura objetivo y tras el recalentamiento.
La coronariografía se llevó a cabo según el protocolo local. El punto de acceso, el tratamiento con antiagregantes y anticoagulantes y la estrategia de revascularización se dejaron a criterio de los médicos al cargo del tratamiento. En los casos de que el paciente presentara enfermedad multivaso, la estrategia de revascularización se discutió en el equipo multidisciplinar (heart team) de cada centro. Si el tratamiento de elección para un paciente del grupo asignado a CU era la revascularización quirúrgica, dicha intervención se posponía hasta la recuperación neurológica. Si los pacientes inicialmente aleatorizados a la estrategia de CD mostraban signos de shock cardiogénico o arritmias ventriculares recurrentes durante la hospitalización, se les hacía una CU (crossover).
Criterios de valoración y seguimientoLa duración estimada del estudio fue de 3 años, con un seguimiento de 6 meses. Debido a la pandemia causada por el coronavirus, la selección de los participantes fue más lenta de lo que se esperaba. En el seguimiento clínico se evaluaron la supervivencia, el estado neurológico y la fracción de eyección del ventrículo izquierdo (FEVI).
El criterio combinado de valoración principal de eficacia fue la supervivencia hospitalaria sin dependencia grave, evaluada con la escala Cerebral Performance Category (CPC)17, donde las categorías 1 y 2 representan un buen pronóstico. El criterio combinado de valoración de la seguridad fueron las complicaciones cardiacas graves, como la muerte, el reinfarto, la hemorragia y las arritmias ventriculares. Entre los criterios secundarios de valoración se incluyeron la supervivencia hospitalaria y a los 6 meses, el pronóstico neurológico al alta del hospital y a los 6 meses, evaluado por la escala CPC, la FEVI al alta y a los 6 meses, el tamaño del infarto, determinado con marcadores cardiacos, complicaciones vasculares, hemorragias, arritmias ventriculares, insuficiencia renal aguda, trombosis del stent, infecciones, duración de la intubación y de la estancia hospitalaria (tablas 3 y 4 del material adicional).
Análisis estadísticoEn un metaanálisis previo de 55 estudios no aleatorizados, se observó una mejoría de la supervivencia con la CU frente al tratamiento convencional: 58,8% frente al 30,9% con una odds ratio de 2,77 (IC95%; 2,06-3,72)18. Basándonos en estudios previos, se calculó que se requeriría un tamaño muestral de 92 pacientes para detectar un aumento absoluto del 28% en la tasa de supervivencia del grupo a estudio (CU) con una potencia estadística del 80%. Considerando una pérdida de pacientes del 10% durante el seguimiento, se requeriría una muestra de 102 pacientes (51 en cada grupo) para comprobar la hipótesis de superioridad.
Lamentablemente, el tamaño de la muestra fue inferior al esperado debido a la pandemia causada por el coronavirus, que hizo que la inclusión de pacientes fuera enormemente complicada. Por este motivo, el estudio no tuvo suficiente potencia estadística para el criterio de valoración principal y los resultados deberían considerarse exploratorios.
Se analizaron los criterios de valoración de todos los pacientes seleccionados para el análisis con intención de tratar.
El análisis estadístico lo llevó a cabo un investigador independiente, que desconocía la asignación del grupo a estudio.
Las variables continuas se expresan mediante la mediana y el intervalo intercuartílico y la comparación entre grupos se llevó a cabo con el estimador Hodges-Lehmann para grupos independientes. Las variables categóricas se expresan con totales y porcentajes y los grupos se compararon con la prueba de la χ2. El análisis de supervivencia se hizo con el análisis de Kaplan-Meier y las diferencias entre grupos se evaluaron mediante la prueba de rangos logarítmicos. En el caso del criterio de valoración principal, la supervivencia entre grupos se comparó con el análisis univariante de riesgos proporcionales de Cox. Con respecto a las complicaciones cardiacas graves, las diferencias entre grupos se evaluaron con la prueba de la χ2, y la magnitud del efecto se expresó con la proporción de riesgo y la diferencia de riesgo. Se consideró que había significación estadística para los valores bilaterales de p <0,05. La gestión de todos los datos y el análisis subsiguiente se hicieron con el software de estadística STATA 17 (StataCorp. 2021: versión 17. College Station, TX: StataCorp LLC).
RESULTADOSPacientesEntre febrero del 2016 y diciembre del 2020, se seleccionó un total de 69 supervivientes de PCEH sin IAMCEST en los 15 centros participantes de España. A tres de estos pacientes se les excluyó del análisis, porque no completaron el proceso de aleatorización. Finalmente, 66 pacientes se asignaron de manera aleatoria al grupo de CU (32 pacientes) o de CD (34 pacientes). Las características iniciales de los pacientes estaban equilibradas en los dos grupos (tabla 1). La media de edad fue de 63 años (intervalo intercuartílico [IQR], [56-72]) y el 22,7% de los pacientes eran mujeres. En el 81,8% el ritmo inicial fue desfibrilable (fibrilación ventricular o taquicardia ventricular sin pulso), y en el 18,2% restante se constató un ritmo inicial no desfibrilable. El tiempo medio transcurrido entre la parada cardiaca y la RCE fue de 21,5minutos.
Características iniciales de los pacientes
| Coronariografía urgente(n=32) | Coronariografía diferida(n=34) | p | |
|---|---|---|---|
| Edad, años | 66,5 [60-73,5] | 60,5 [55-71] | 0,086 |
| Sexo masculino | 26 (81,3) | 25 (73,6) | |
| Índice de masa corporal* | 26,8 [25,5-29] | 26 [24,5-8,7] | 0,139 |
| Factores de riesgo o enfermedad cardiovascular | |||
| Diabetes | 5 (15,6) | 10 (30,3) | 0,1603 |
| Hipertensión | 22 (68,8) | 22 (66,7) | 0,8575 |
| Dislipidemia | 21 (65,6) | 15 (46,9) | 0,1306 |
| Fumador en el momento del estudio | 7 (21,9) | 10 (29,4) | 0,527 |
| Abuso de alcohol | 4 (12,5) | 7 (20,6) | 0,3782 |
| Abuso de drogas | 2 (6,3) | 3 (8,8) | 0,664 |
| Enfermedad coronaria | 7 (21,9) | 8 (23,5) | 0,928 |
| Arteriopatía periférica | 4 (12,5) | 4 (11,8) | 0,999 |
| Tratamiento previo con anticoagulantes | 7 (21,9) | 5 (14,7) | 0,578 |
| Ritmo inicial desfibrilable | 27/32 (84,4) | 27/34 (79,4) | 0,5986 |
| Antes de ingresar en el hospital | |||
| Tiempo transcurrido entre el paro cardiaco y el la recuperación de la circulación espontánea min | 20 [15-25] | 23 [15-32] | 0,445 |
| pH sanguíneo | 7,22 [7,1-7,3] | 7,17 [7,0-7,3] | 0,453 |
| Lactato, mmol/l | 6,28 [4,17-9,80] | 5,90 [2,5-13,10] | 0,611 |
| Después de ingresar en el hospital | |||
| Presión arterial sistólica, mmHg | 126 [110-140] | 120 [100-140] | 0,250 |
| Fracción de eyección del ventrículo izquierdo | 47 [40-60] | 49 [40-60] | 0,034 |
| Datos de pruebas analíticas | |||
| Saturación de oxígeno | 99 [97-100] | 99 [98-100] | 0,821 |
| pH sanguíneo | 7,32 [7,27-7,35] | 7,31 [7,22-7,39] | 0,818 |
| Lactato, mmol/l | 3,1 [1,62-6,10] | 3,1 [1,60-6,60] | 0,611 |
| Bicarbonato, mmol/l | 21 [18,8-23,3] | 23,1 [21-25] | 0,094 |
Los detalles sobre los procedimientos y tratamientos se muestran en la tabla 2. Se realizó una coronariografía a todos los pacientes del grupo de CU y a 20 (58,9%) del grupo de CD. El tiempo medio transcurrido entre la parada cardiaca y la coronariografía fue de 3,8 horas [IQR: 2,9-4,3] en el grupo asignado a CU y de 129 horas (5,4 días) en el grupo asignado a CD [IQR: 89-187 horas]. Se constató una prevalencia de enfermedad coronaria del 53,1% entre los pacientes a los que se hizo un CU y del 40% entre los pacientes del grupo asignado a CD. En el 37,5% de los pacientes del grupo asignado a CU y en el 25% de los del grupo asignado a CD, se observó que había una lesión responsable. Se llevó a cabo un ICP en el 31,3% de los pacientes del grupo asignado a CU y en tan solo el 10% de los pacientes del grupo asignado a CD, aunque al 15% de los pacientes de este último grupo se les revascularizó de forma quirúrgica durante la hospitalización. Todos los pacientes recibieron hipotermia terapéutica con una temperatura objetivo de 33°C. El tiempo medio transcurrido entre la parada cardiaca y el inicio de la hipotermia fue considerablemente mayor en el grupo tratado con CU (4,4 horas [IQR: 3-5,4 horas] comparado con 2,9 horas en el grupo tratado con CD [IQR: 1,2-3,4 horas], p=0,006).
Prevalencia, características y tratamiento de la enfermedad coronaria
| Coronariografía urgente(n=32) | Coronariografía diferida(n=34) | p | |
|---|---|---|---|
| Coronariografía | 32 (100) | 20 (58,8) | <0,001 |
| Tiempo medio transcurrido entre el paro cardíaco y la coronariografía, h | 2,7 [1,6-3,4] | 129 [87-186] | <0,001 |
| Acceso del cateterismo | 0,262 | ||
| Femoral | 5 (15,6) | 1 (5) | |
| Radial | 26 (81,2) | 18 (90) | |
| Braquial | 1 (3,1) | 1 (5) | |
| Gravedad de la enfermedad coronaria | 0,073 | ||
| Sin enfermedad clínicamente significativa | 16 (50) | 12 (60) | |
| Enfermedad de un vaso | 10 (31,3) | 2 (10) | |
| Enfermedad de dos vasos | 1 (3,1) | 1 (5) | |
| Enfermedad de tres vasos | 5 (15,6) | 5 (25) | |
| Lesión aguda inestable (lesión responsable)* | 12 (37,5) | 5 (25) | 0,3499 |
| Tratamiento de revascularización | |||
| ICP | 10 (31,3) | 2 (10) | 0,0768 |
| CABG | 0 (0,0) | 3 (15) | 0,0240 |
| Cantidad de contraste, ml | 100 [60-180] | 90,5 [52-140] | 0,9999 |
CABG: cirugía de revascularización coronaria; ICP: intervención coronaria percutánea; IQR: intervalo intercuartílico.
Los datos expresan n (%), media±desviación estándar o mediana [intervalo intercuartílico].
En el análisis principal se incluyó un total de 66 pacientes (95,7%). Los resultados clínicos se muestran en la tabla 3. La supervivencia hospitalaria sin dependencia grave (el criterio de valoración principal) fue del 59,4% en el grupo asignado a CU y del 52,9% en el grupo asignado a CD (HR: 1,29; IC95%, 0,60-2,73; p=0,4986) (figura 1). Tampoco hubo diferencias relacionadas con complicaciones cardiacas graves, como la muerte, el reinfarto, la hemorragias y las arritmias ventriculares (criterio de valoración principal de seguridad) entre ambos grupos. La supervivencia hospitalaria fue del 62,5% en el grupo asignado a CU y del 58,8% en el grupo asignado a CD (HR: 0,96; IC95%, 0,45-2,09; p=0,93). No se observaron diferencias en los criterios de valoración secundarios excepto por la incidencia de insuficiencia renal aguda, que fue más frecuente en el grupo asignado a CU (15,6% frente al 0%, p=0,002), y las infecciones, que fueron mayores en el grupo asignado a CD (46,9% frente al 73,5%, p=0,003). En la tabla 3 se proporcionan más resultados clínicos.
Resultados clínicos
| Coronariografía urgente(n=32) | Coronariografía diferidaa(n=34) | Magnitud del efectoHR (IC95%) | |
|---|---|---|---|
| Criterio de valoración principal | |||
| Supervivencia con buen pronóstico neurológico (CPC 1 y 2) | 19 (59,4) | 18 (52,9) | HR: 1,29 (0,60-2,73) |
| Complicaciones cardiacas graves, n.°/total | |||
| Muerte | 12/32 (37,5) | 14/34 (41,2) | RR: 0,91 (0,5-1,66) |
| Infarto de miocardio (reinfarto) | 0/32 | 1/34 (2,9) | DR: –0,03 (–0,086 a –0,027) |
| Hemorragia clínicamente evidente (BARC ≥ 2) | 3/32 (9,4) | 3/34 (8,8) | RR: 1.062 (0,231-4,88) |
| Arritmias ventriculares | 3/32 (9,4) | 9/34 (26,5) | RR: 0,354 [0,105-1,192) |
| Criterios de valoración secundarios | |||
| Supervivencia hospitalaria | 20 (62,5) | 20 (58,8) | HR: 1,06 [0,72-1,57] |
| Pronóstico neurológico evaluado por la puntuación de la escala CPC en el momento del altab | |||
| CPC 1 | 17/32 | 16/34 | RR: 1,13 [0,07-1,83] |
| CPC 2 | 2/32 | 2/34 | - |
| CPC 3 | 1/32 | 1/34 | - |
| CPC 4 | 0/32 | 1/34 | - |
| CPC 5 | 12/32 | 14/34 | RR: 0,91 [0,5-1,66] |
| Concentración máxima de enolasa neuronal específica | 25,6 [15,8-34] | 20,0 [15-35,8] | DM: 2,8 [−5,5-12,1] |
| Fracción de eyección del ventrículo izquierdo en el momento del alta | 51 [45-60] | 52 [45-60] | DM: 0 [−5-5] |
| Fracción de eyección del ventrículo izquierdo a los 6 meses | 61,1 [57-62] | 52,3 [45-60] | DM: 5 [0-20] |
| Tamaño del infarto (CPK máxima) | 293 [72-689] | 514 [272-1.824] | DM: –252 [–628 a –1,35)] |
| Hemorragia clínicamente evidente: BARC ≥ 2 | 3/32 (9,38%) | 3/34 (8,82%) | RR: 1.062 [0,231-4,88] |
| Insuficiencia renal aguda | 5/32 (15,6%) | 0/34 (0) | DR: 0,156 [0,03-0,282] |
| Infecciones / uso de antibióticos | 15/32 (46,9) | 25/34 (73,5) | RR: 0,64 [0,42-0,97] |
| Duración de la intubación, días | 3 [2-7] | 5 [3-12] | DM: –2 [–4-0] |
| Uso de dobutamina | 9 (28,1) | 5 (14,7) | RR: 1,91 (0,72-5,1) |
| Uso de noradrenalina | 17 (53,1) | 20 (58,2) | RR: 0,9 (0,59-1,39) |
| Duración de la estancia hospitalaria, días | 15 [6,5-23] | 18 [14-29] | DM: –5 [–12-2] |
| Resultado | |||
| Tiempo transcurrido entre el paro cardiaco y el comienzo de la hipotermia, h | 4,4 [3-5,4] | 2,9 [1,2-3,4] | DM: 1,5 [0,53-2,37] |
| Tiempo transcurrido entre el paro cardiaco y la temperatura objetivo, h | 8,3 [6,3-9,3] | 7 [5-9,9] | DM: 0,93 [–0,83-2,68] |
| Tratamiento en el momento del alta | |||
| Inhibidores de la enzima de conversión de la angiotensina | 13/32 (40,6) | 5/34 (14,7) | RR: 2,76 [1,11-6,87] |
| Bloqueantes β | 16/32 (50) | 9/34 (26,5) | RR: 1,89 [0,98-3,65] |
| Antagonistas de la aldosterona | 4/32 (12,5) | 1/34 (2,9) | RR: 4,25 [0,50-36,0] |
BARC: Bleeding Academic Research Consortium; CPC: Cerebral Performance Category; DM: diferencia media; DR: diferencia de riesgo; HR: hazard ratio; IC: intervalo de confianza; IQR: intervalo intercuartílico; RR: riesgo relativo o cociente de riesgos.
Los datos expresan n (%), media±desviación estándar o mediana [intervalo intercuartílico].
La coronariografía diferida se utilizó como grupo de referencia para calcular la HR, el RR y la DR.
Se consideró un buen pronóstico neurológico una puntuación de 1 o 2 en la escala Cerebral Performance Category, cuyos valores son del 1 al 5. Se definió como déficit neurológico grave la puntuación de 3, 4 o 5 en la misma escala (que corresponden a discapacidad neurológica grave, estado vegetativo persistente, o muerte cerebral).
Estimaciones de Kaplan-Meier de la supervivencia hospitalaria sin dependencia grave. No se observaron diferencias significativas en la supervivencia sin discapacidad neurológica (criterio de valoración principal) entre los pacientes reanimados tras sufrir una PCEH sin elevación del segmento ST a los que se hizo una coronariografía urgente o una diferida.
En el ensayo COUPE se observó que entre los pacientes reanimados tras sufrir una PCEH sin elevación del segmento ST, la CU no proporcionaba ningún beneficio en cuanto a supervivencia con buen pronóstico neurológico comparada con la CD. Estos hallazgos apoyan los resultados de 2 ensayos aleatorizados previos en los que se demuestra que la CU no presenta beneficios en esta población15,19. En nuestro estudio, se incluyó a pacientes con ritmos desfibrilables y no desfibrilables, igual que en el ensayo TOMAHAWK. En otros ensayos piloto aleatorizados20,21 tampoco se observaron diferencias en los resultados clínicos de los pacientes con una PCEH tratados con una CU o una CD.
La ausencia de beneficio de la CU podría explicarse por varios motivos. Solo el 50% del grupo asignado a CU presentaba enfermedad coronaria significativa (en el 37,5% se encontró una lesión aguda inestable que se consideró responsable de desencadenar la parada cardiaca). En el grupo asignado a CD fueron aún menos (40%) los que presentaban enfermedad coronaria, y solo en el 25% de ellos se observó una lesión coronaria responsable. En esta población, con una baja prevalencia de enfermedad coronaria, la CU podría aumentar el riesgo de complicaciones, tales como la nefropatía inducida por contraste o las hemorragias, sin ningún benefició en lo que respecta a supervivencia o pronóstico neurológico. De hecho, el 15,6% de los pacientes del grupo asignado a CU sufrieron insuficiencia renal aguda comparado con ninguno de los pacientes del grupo asignado a CD. En cambio, en el grupo asignado a CD fueron más los pacientes con infecciones (75,5% frente al 46,9%), lo que posiblemente se debió a que el periodo de intubación fue mayor (3 días en grupo asignado a CU frente a 5 días en el grupo asignado a CD).
Otra posible explicación de la ausencia de beneficio de la CU es que la mayoría de los pacientes que fallecieron fue debido a complicaciones no cardiovasculares, fundamentalmente encefalopatía hipóxico-isquémica (66,7% en el grupo asignado a CU y 92,9% en el grupo asignado a CD). Este resultado concuerda con los hallazgos de los estudios mencionados anteriormente15,19.
Todos los pacientes de ambos grupos recibieron hipotermia terapéutica con una temperatura objetivo de 33°C. Este era el protocolo habitual en la mayoría de los centros, si bien en algunos tenían protocolos locales de control de temperatura, con temperaturas entre 32°C y 36°C, siguiendo las recomendaciones de las guías internacionales13,14. Para este estudio se estableció este nivel de temperatura para evitar un posible factor de confusión de las distintas temperaturas, que podrían influir en los resultados de la CU o la CD. No se observaron diferencias en el pronóstico neurológico de ambos grupos (el 59,4% del grupo asignado a CU presentó buen pronóstico neurológico frente al 53% del grupo asignado a CD). En el ensayo COACT, los pacientes asignados al grupo de CU alcanzaron la temperatura objetivo más tarde que los del grupo asignado a CD. No obstante, en el presente estudio no se observaron diferencias significativas en el tiempo necesario para alcanzar la temperatura objetivo (8,3horas en el grupo asignado a CU y 7horas en el grupo de CD). Esta ausencia de beneficio de la CU fue independiente tanto del nivel de temperatura como de la velocidad de consecución de esta.
En nuestro estudio, el tiempo medio transcurrido desde la parada cardiaca hasta la RCE fue de 21,5minutos, mayor que en los ensayos COACT y TOMAHAWK, donde este tiempo fue de 15minutos. De manera concordante con lo anterior, el primer lactato objetivado fue de 6,22 mmol/l mientras que en los ensayos mencionados anteriormente fue en torno a 5 mmol/l.
El primer eslabón en la cadena de supervivencia es la identificación temprana del paro cardiaco, la rápida activación de los sistemas médicos de urgencias y el inicio inmediato de la reanimación cardiopulmonar (RCP) por parte del testigo. Identificar una parada cardíaca puede ser complejo. La enseñanza obligatoria de RCP a nivel nacional en las escuelas tiene el impacto más importante a largo plazo para mejorar la tasa de reanimación por testigo22,23. A la larga, esta parece ser la mejor forma de llegar a toda la población24. A pesar de que el tiempo transcurrido entre el paro cardiaco y la RCE de nuestro estudio es mayor, la supervivencia sin dependencia grave fue del 59,4% en el grupo asignado a CU y del 52,9% en el grupo asignado a CD. Este resultado razonablemente bueno pone de manifiesto la necesidad de tratar a los pacientes que sufren una PCEH en centros de referencia en paro cardiaco25.
En un esfuerzo por identificar otro posible beneficio de la CU, se analizó la FEVI, que era uno de los criterios de valoración secundarios preespecificados. No se observaron diferencias en la FEVI media al alta hospitalaria pero, curiosamente, a los 6 meses de seguimiento, la FEVI media fue del 61,1% en el grupo asignado a CU comparado con el 52,3% en el grupo asignado a CD, y casi se alcanzó la significación estadística (p=0,058). La revascularización urgente podría haber tenido algún beneficio en lo que respecta a índices funcionales, tales como la FEVI. Otra explicación de esta mejora en la FEVI podría ser el mayor número de pacientes tratados al alta con inhibidores de la enzima convertidora de angiotensina, bloqueadores beta y antagonistas de la aldosterona en el grupo asignado a CU comparado con el grupo de CD. Este hallazgo debe interpretarse con cautela dado el tamaño muestral del estudio y necesita investigarse en futuros ensayos diseñados para contestar a esta cuestión.
Este estudio tiene varias limitaciones. En primer lugar, el tamaño de la muestra fue inferior al esperado por varios motivos. Algunos pacientes se encontraban solos cuando sufrieron el paro cardiaco y no pudo identificarse con suficiente inmediatez a sus familiares más próximos para poder obtener el consentimiento informado. Además, algunos médicos de los centros participantes tenían el convencimiento de que hacer una CU era la estrategia terapéutica correcta en este subgrupo de pacientes que había sufrido una PCEH sin elevación del segmento ST y fueron más reticentes a seleccionar pacientes. Por último, la pandemia causada por la COVID-19 complicó la selección e hizo imposible completar la inclusión del número estimado de pacientes. Puesto que no se alcanzó el tamaño deseado de la muestra, la potencia estadística fue del 63,3% y, por lo tanto, todos los resultados deberían considerarse exploratorios. En segundo lugar, los médicos conocían la asignación aleatoria del tratamiento, aunque no intervinieron en el proceso de análisis. En tercer lugar, aunque se incluyó a pacientes con ritmos desfibrilables y no desfibrilables, los resultados no son aplicables a los pacientes que sufrieron un paro cardiaco en el hospital, con elevación del segmento ST, con bloqueo de la rama izquierda del haz de His o hemodinámicamente inestables, puesto que se excluyeron del estudio. Actualmente, son varios los ensayos aleatorizados en curso que proporcionarán datos más exhaustivos para seleccionar a los candidatos apropiados para una CU26,27.
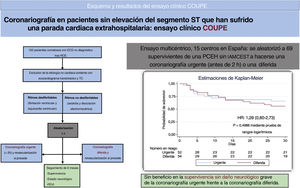
CONCLUSIONESEn conclusión, en este estudio aleatorizado de pacientes reanimados tras una PCEH sin elevación del ST, una CU no fue beneficiosa en términos de supervivencia con buen pronóstico neurológico comparada con una CD (figura 2).
Figura central. Esquema y resultados del ensayo clínico COUPE. ECG: electrocardiograma; FEVI: fracción de eyección del ventrículo izquierdo; HR: hazard ratio; IAMCEST: infarto de miocardio con elevación del segmento ST; PCEH: parada cardiaca extrahospitalaria; RCE: recuperación de la circulación espontánea.
El ensayo fue financiado por el Instituto de Salud Carlos III (proyecto PT13/0002/0003 y PT17/0017/0018) y cofinanciado por el Fondo Europeo de Desarrollo Regional (FEDER).
CONTRIBUCIÓN DE LOS AUTORESEl autor para correspondencia garantiza que todos los autores cumplen con cada una de las siguientes características definidas por el Comité Internacional de Editores de Revistas Médicas en los criterios de autoría de artículos científicos: a) contribuciones notables a la idea o el diseño del artículo; o la obtención, el análisis, o la interpretación de los datos para el artículo; b) redacción del artículo o revisión del mismo de manera crítica por su importante contenido intelectual; c) aprobación final de la versión que se publicará; y d) acuerdo de responsabilidad por todos los aspectos del artículo para garantizar que las cuestiones relacionadas con la precisión o integridad de cualquier parte del artículo se han investigado y resuelto de manera apropiada.
CONFLICTO DE INTERESESLos autores no declaran ninguno.
Pablo Salinas, Servicio de Cardiología, Hospital Clínico San Carlos, Instituto de Investigación Sanitaria Hospital Clínico San Carlos (IdISSC), Madrid,España.
Luis Nombela-Franco, Servicio de Cardiología, Hospital Clínico San Carlos, Instituto de Investigación Sanitaria Hospital Clínico San Carlos (IdISSC), Madrid,España.
Iván Núñez-Gil, Servicio de Cardiología. Hospital Clínico San Carlos, Instituto de Investigación Sanitaria Hospital Clínico San Carlos (IdISSC), Madrid, España.
Pedro Cepas Guillén, Instituto Cardiovascular, Hospital Clínic Barcelona, Universidad de Barcelona, Institut D́Investigacions Biomèdiques August Pi i Sunyer (IDIBAPS), Barcelona, España.
Gonzalo Luis Alonso-Salinas, Servicio de Cardiología, Hospital Universitario de Navarra, Pamplona, España.
Miriam Juárez, Servicio de Cardiología, Hospital General Universitario Gregorio Marañón, Madrid, España.
Iago Sousa, Servicio de Cardiología, Hospital General Universitario Gregorio Marañón, Madrid, España.
Carlos Tomás Querol, Servicio de Cardiología, Hospital Universitari Arnau de Vilanova, Lleida - IRBLL, Lleida, España.