Conocer la situación actual del control de la anticoagulación en pacientes con fibrilación auricular no valvular tratados con antagonistas de la vitamina K en atención primaria en España.
MétodosPAULA es un estudio observacional transversal/retrospectivo y multicéntrico de ámbito nacional. Se incluyó a pacientes con fibrilación auricular no valvular en tratamiento con antagonistas de la vitamina K durante el último año atendidos en las consultas de atención primaria. Se registraron los valores de la razón internacional nomalizada (INR) durante los últimos 12 meses. El grado de control de la anticoagulación se determinó mediante el tiempo en rango terapéutico, tanto por el método directo (mal control < 60%) como por el método de Rosendaal (mal control < 65%).
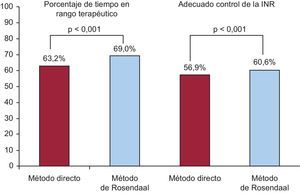
ResultadosSe evaluó a 1.524 pacientes (media de edad, 77,4 ± 8,7 años; el 48,6% mujeres; el 64,2% en fibrilación auricular permanente; media de CHADS2, 2,3 ± 1,2; de CHA2DS2-VASc, 3,9 ± 1,5, y de HAS-BLED, 1,6 ± 0,9). El número medio de determinaciones de la INR registradas por paciente fue 14,4±3,8. El 56,9% de los pacientes tenían un adecuado control por la INR según el método directo y el 60,6% según el método de Rosendaal. En el análisis multivariable, fueron predictores de mal control de la INR el sexo femenino, los hábitos dietéticos que pudieran afectar a la anticoagulación con antagonistas de la vitamina K, la polimedicación y los antecedentes de INR lábil.
ConclusionesAproximadamente el 40% de los pacientes (el 43,1% por el método directo y el 39,4% por el método de Rosendaal) con fibrilación auricular no valvular anticoagulados con antagonistas de la vitamina K en atención primaria en España presentan un control de la anticoagulación inadecuado durante los 12 meses previos.
Palabras clave
La fibrilación auricular (FA) es la arritmia más frecuente en la población general. Se estima que la prevalencia de FA es de aproximadamente el 2%, cifra que aumenta con la edad y las comorbilidades1. En España se han realizado recientemente algunos estudios dirigidos a conocer la situación de la FA en la práctica clínica. En el estudio VAL-FAAP2, que analizó a cerca de 120.000 sujetos asistidos en las consultas de atención primaria, la proporción de sujetos con FA alcanzó el 6,1%. En la población general mayor de 40 años, la prevalencia de FA en España fue del 4,4%3. De los hipertensos de 65 o más años de la Comunidad Valenciana, tenía FA el 10,3%4.
En comparación con los pacientes sin FA, los sujetos con FA tienen el doble de riesgo de muerte y hasta 5 veces más riesgo de presentar un ictus5. El ictus asociado a FA tiene mayores mortalidad y riesgo de recurrencias y produce más secuelas6. La anticoagulación oral crónica está indicada para la mayoría de los sujetos con FA para prevenir complicaciones tromboembólicas2. Los antagonistas de la vitamina K (AVK) se han utilizado ampliamente durante décadas para este fin, dado que son capaces de reducir aproximadamente un 64% el riesgo de ictus7.
Sin embargo, los AVK tienen importantes limitaciones, que habitualmente han condicionado su uso en la práctica clínica para la FA no valvular (FANV)2,8. Entre estas se encuentran la estrecha ventana terapéutica, las interacciones con otros fármacos y alimentos y su metabolismo variable, que obligan a la realización de controles periódicos de la anticoagulación y frecuentes ajustes de dosis9,10. Es crucial que la razón internacional normalizada (INR) del paciente en tratamiento con AVK se encuentre dentro del rango terapéutico para reducir el riesgo de complicaciones tanto tromboembólicas como hemorrágicas. De hecho, se ha demostrado que en pacientes con FANV y puntuación CHADS2 ≥ 2 tratados con warfarina, en comparación con los no tratados, se observó mejoría significativa en el tiempo hasta la aparición de un ictus solo en los sujetos que alcanzaron control por encima del 70% del tiempo en rango terapéutico11.
Por lo tanto, conocer el grado de control de la INR de los pacientes con FANV anticoagulados con AVK es un aspecto fundamental para el manejo adecuado de esta población. Aunque se han publicado algunos estudios que analizan el grado de control de la INR en España, se han realizado en una zona geográfica concreta del país o el número de valores de INR que han analizado era pequeño12,13. Con el fin de conocer la situación del control de la anticoagulación durante un periodo prolongado de los pacientes con FANV tratados con AVK en la práctica clínica de atención primaria en todo el territorio nacional, se realizó el estudio PAULA (Perspectiva Actual de la sitUación de la anticoaguLación en la práctica clínica de Atención primaria).
MÉTODOSEl estudio PAULA, de diseño observacional transversal/retrospectivo, multicéntrico y de ámbito nacional, tuvo como objetivo principal conocer el control de la anticoagulación de los pacientes con FANV anticoagulados con AVK en el ámbito de la atención primaria en España durante el último año. El estudio contó con el aval científico de las tres sociedades nacionales de atención primaria existentes en España (SEMERGEN, semFYC y SEMG).
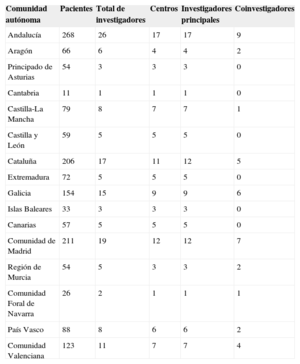
Para la realización del estudio, se constituyó un comité científico formado por dos cardiólogos, un bioestadístico y tres médicos de familia expertos en patología cardiovascular, en representación de las tres sociedades científicas nacionales de atención primaria. Los médicos de familia escogieron a nueve coordinadores regionales (anexo 1 del material suplementario), que a su vez seleccionaron a 139 investigadores (anexo 2 del material suplementario) provenientes de 99 centros de salud distribuidos por las diferentes comunidades autónomas (excepto La Rioja, por motivos logísticos), distribuidos de manera proporcional al número de habitantes de cada región, para que el número de pacientes fuese representativo del territorio nacional (tabla 1). Inicialmente el coordinador regional realizó la selección de los investigadores, en función de su capacidad clínica e investigadora. Posteriormente, el comité científico debía aprobar dicha elección. Cada investigador debía incluir al menos a los primeros 10 pacientes consecutivos que —cumpliendo todos los criterios de inclusión y ninguno de exclusión— acudieran sistemáticamente a realizarse el control de la anticoagulación y dieran su consentimiento para participar en el estudio. El reclutamiento se realizó entre febrero y junio de 2014.
Número de pacientes incluidos, investigadores y centros distribuidos por comunidad autónoma
| Comunidad autónoma | Pacientes | Total de investigadores | Centros | Investigadores principales | Coinvestigadores |
|---|---|---|---|---|---|
| Andalucía | 268 | 26 | 17 | 17 | 9 |
| Aragón | 66 | 6 | 4 | 4 | 2 |
| Principado de Asturias | 54 | 3 | 3 | 3 | 0 |
| Cantabria | 11 | 1 | 1 | 1 | 0 |
| Castilla-La Mancha | 79 | 8 | 7 | 7 | 1 |
| Castilla y León | 59 | 5 | 5 | 5 | 0 |
| Cataluña | 206 | 17 | 11 | 12 | 5 |
| Extremadura | 72 | 5 | 5 | 5 | 0 |
| Galicia | 154 | 15 | 9 | 9 | 6 |
| Islas Baleares | 33 | 3 | 3 | 3 | 0 |
| Canarias | 57 | 5 | 5 | 5 | 0 |
| Comunidad de Madrid | 211 | 19 | 12 | 12 | 7 |
| Región de Murcia | 54 | 5 | 3 | 3 | 2 |
| Comunidad Foral de Navarra | 26 | 2 | 1 | 1 | 1 |
| País Vasco | 88 | 8 | 6 | 6 | 2 |
| Comunidad Valenciana | 123 | 11 | 7 | 7 | 4 |
Los criterios de inclusión comprendieron a los pacientes: a) de ambos sexos y 18 o más años de edad; b) con FANV en tratamiento con AVK durante al menos el último año en el ámbito de atención primaria en condiciones de práctica clínica habitual; c) de los que se dispusiera al menos del 80% de la los controles de la INR del último año, y d) que hubiesen otorgado su consentimiento informado por escrito para participar en el estudio tras haber leído y comprendido la hoja de información al paciente. Se excluyó a los pacientes con un deterioro cognitivo que impidiese la comprensión correcta de la hoja de información al paciente y del consentimiento informado y los que hubieran participado en algún ensayo clínico durante los últimos 12 meses.
El estudio comprendía una única visita, que coincidía con cualquiera de las que realizase el paciente habitualmente para su seguimiento. Los datos se recogieron de la historia clínica y de la entrevista con el médico, sin aplicarse ningún tipo de intervención diagnóstica ni terapéutica específica para el estudio. Los datos se incluyeron en un cuaderno de recogida de datos electrónico. La información recogida electrónicamente fue monitorizada y revisada para velar por la calidad del registro, y la base de datos fue depurada para evitar la documentación de valores imposibles. El diseño del cuaderno de recogida de datos se realizó por una CRO (Contract Research Organization) —Dynamic Solutions— contratada específicamente, con la supervisión del comité científico. La CRO se encargó de garantizar la veracidad y calidad de los datos recogidos. Para ello, realizó un seguimiento especifíco telefónico y una monitorización presencial cuando se consideró necesario. Además se generaron listados de todos los datos que pudieran generar alguna duda y se enviaron a los centros y los investigadores resolvieron.
Las variables que se recogieron fueron: datos sociodemográficos, historia médica relevante, comorbilidades, eventos cardiovasculares presentados, incluyendo complicaciones tromboembólicas y eventos hemorrágicos mayores, exploración física, datos antropométricos, analítica sanguínea disponible en los 6 meses previos, datos sobre la FA (fecha del diagnóstico y tipo de FA), datos del tratamiento con AVK (fármaco y dosis total semanal), tratamientos concomitantes, puntuación de escalas CHADS2, CHA2DS2-VASc y HAS-BLED, determinaciones de la INR (incluyendo fecha y valor), opinión del investigador sobre la anticoagulación del paciente y posibles factores de riesgo asociados a un peor control de la INR. La mayoría de las variables analizadas se recogieron de la propia historia clínica del paciente. Sin embargo, algunas de ellas, como la presión arterial, la frecuencia cardiaca o el índice de masa corporal se midieron en la propia visita. Para conocer si el paciente presentaba hábitos dietéticos que pudieran afectar al control de la INR, se le preguntó específicamente si tomaba en exceso alguno de los siguientes alimentos: alimentos ricos en vitamina K (cereales, brécol, col, zanahorias, etc.), alcohol, zumo de grosella, ginseng, si era consumidor habitual de fitoterapia o si realizaba transgresiones dietéticas frecuentes. Se consideró consumo excesivo de alcohol cuando los pacientes consumían más de 8 bebidas alcohólicas por semana (considerando una bebida alcohólica como 10g de etanol puro)14.
Para valorar el control de la INR de los pacientes, se calculó de manera centralizada el tiempo en rango terapéutico en los últimos 12 meses tanto por el método directo (porcentaje de valores de la INR dentro de rango terapéutico) como por el método descrito por Rosendaal et al15. Se consideró INR lábil un tiempo en rango terapéutico < 60%, de acuerdo con la definición propuesta por Pisters et al16.
El estudio fue aprobado por el Comité Ético de Investigación Clínica del Hospital Universitario La Paz de Madrid. El paciente debía firmar el consentimiento informado por escrito antes de la inclusión, tras haber leído y comprendido perfectamente la hoja de información al paciente.
Análisis estadísticoEl cálculo del tamaño de la muestra se determinó en función del objetivo principal del estudio. Datos previos que habían evaluado el tiempo en rango terapéutico encontraron valores con un tiempo medio entre el 29 y el 75%17,18. En España, un estudio previo estimó el tiempo en rango terapéutico en el 64%19. De manera conservadora, se consideró para el cálculo del tamaño muestral un valor del 60%. Con ello, aceptando un riesgo alfa de 0,05, una precisión de ±3% y una tasa de pérdidas no superior al 5%, para estimar el tiempo en rango terapéutico en un 60%, con un contraste bilateral, se calculó finalmente que sería necesario incluir al menos a 1.100 pacientes.
Para el análisis descriptivo, las variables cuantitativas se describieron con medidas de centralización y de dispersión (media ± desviación típica) y las variables cualitativas, como frecuencias absolutas (n) y relativas (%). En el análisis bivariable para la comparación de dos medias, se realizaron tests estadísticos paramétricos (t de Student) o no paramétricos (U de Mann-Whitney) en función de la distribución muestral, y para comparar porcentajes, se usó la prueba de la χ2 o la de Fisher, en función del tamaño de la muestra. Se realizaron análisis bivariables para identificar qué factores estaban asociados individualmente con el control de la INR. Con los factores identificados individualmente, se realizó un análisis de regresión logística. Todos los análisis se realizaron con el paquete estadístico SPSS versión 18, Data Entry.
RESULTADOSEn el estudio se incluyó en total a 1.561 pacientes, de los que hubo que descartar 37 casos para el análisis final por diversos motivos. Las causas de exclusión fueron: tiempo desde la primera determinación de la INR hasta el inicio del estudio < 1 año (n = 34); tiempo de evolución de la FA < 1 año (n = 9), registro incorrecto en el cuaderno de recogida de datos electrónico (n = 6) y documentar un número insuficiente de determinaciones de la INR (n = 5). En algunos casos se dio más de una causa para la exclusión del estudio. Finalmente quedaron incluidos para su evaluación 1.524 pacientes.
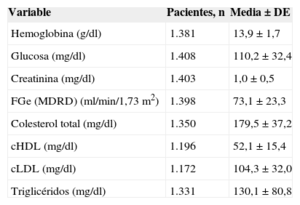
Las características basales de los pacientes se resumen en la tabla 2. Destaca el gran número de factores de riesgo cardiovascular asociados (el 80,2% tenía hipertensión arterial, el 63,5% era sedentario y el 57,2% tenía dislipemia) y factores que aumentan tanto el riesgo de complicaciones tromboembólicas (el 23,9% tenía antecedentes de insuficiencia cardiaca; el 13,7%, de ictus/accidente isquémico transitorio, y el 9,6%, de infarto de miocardio) como hemorrágicas (el 12,3% tenía antecedentes de INR lábil; el 8,8%, antecedentes de hemorragia, anemia o predisposición a la hemorragia, y el 6,0%, insuficiencia renal). El 18,4% de los pacientes tenían hábitos dietéticos que podían afectar al control de la anticoagulación con AVK, el 7,7% tomaba antiinflamatorios no esteroideos crónicamente y el 7,5%, otros fármacos antitrombóticos. El número medio total de comprimidos que tomaban los pacientes era 7,0 ± 3,8. En la tabla 3 se muestran los parámetros analíticos más relevantes.
Características basales de los pacientes incluidos en el estudio (n = 1.524)
| Características biodemográficas (media ± DE) | |
| Edad (años) | 77,4 ± 8,7 |
| Mujeres (%) | 48,6 |
| Exploración física (media ± DE) | |
| Presión arterial sistólica (mmHg) | 130,3 ± 14,6 |
| Presión arterial diastólica (mmHg) | 74,6 ± 9,8 |
| Frecuencia cardiaca (lpm) | 73,1 ± 11,6 |
| Índice de masa corporal | 30,0 ± 5,1 |
| Factores de riesgo cardiovascular (%) | |
| Hipertensión arterial | 80,2 |
| Sedentarismo | 63,5 |
| Dislipemia | 57,2 |
| Diabetes mellitus | 31,0 |
| Hábito tabáquico | |
| Fumadores | 5,1 |
| Ex fumadores < 1 año | 1,5 |
| Ex fumadores ≥ 1 año | 26,0 |
| No fumadores | 67,4 |
| Variables que afectan al riesgo tromboembólico y/o hemorrágico (%) | |
| Insuficiencia cardiaca | 23,9 |
| Ictus/AIT previo | 13,7 |
| Antecedentes de INR lábil | 12,3 |
| Infarto de miocardio previo | 9,6 |
| Hemorragia, anemia o predisposición a la hemorragia | 8,8 |
| Enfermedad arterial periférica | 6,5 |
| Insuficiencia renal | 6,0 |
| Consumo excesivo de alcohol | 4,3 |
| Antecedentes de tromboembolia | 3,9 |
| Placa aórtica diagnosticada | 2,3 |
| Insuficiencia hepática | 1,6 |
AIT: accidente isquémico transitorio; DE: desviación estándar; INR: razón internacional normalizada.
Parámetros analíticos (n = 1.524)
| Variable | Pacientes, n | Media ± DE |
|---|---|---|
| Hemoglobina (g/dl) | 1.381 | 13,9 ± 1,7 |
| Glucosa (mg/dl) | 1.408 | 110,2 ± 32,4 |
| Creatinina (mg/dl) | 1.403 | 1,0 ± 0,5 |
| FGe (MDRD) (ml/min/1,73 m2) | 1.398 | 73,1 ± 23,3 |
| Colesterol total (mg/dl) | 1.350 | 179,5 ± 37,2 |
| cHDL (mg/dl) | 1.196 | 52,1 ± 15,4 |
| cLDL (mg/dl) | 1.172 | 104,3 ± 32,0 |
| Triglicéridos (mg/dl) | 1.331 | 130,1 ± 80,8 |
cHDL: colesterol unido a lipoproteínas de alta densidad; cLDL: colesterol unido a lipoproteínas de baja densidad; DE: desviación estándar; FGe: tasa de filtrado glomerular estimada; MDRD: Modification of Diet in Renal Disease.
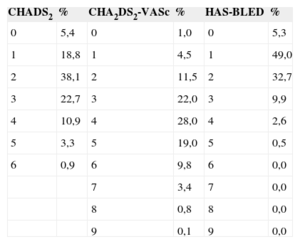
El tiempo medio desde que se identificó la FA hasta la fecha del estudio fue 6,0 ± 4,2 años. En cuanto al tipo de FA, el 20,1% tenía FA paroxística; el 13,6%, FA persistente y el 64,2%, FA permanente; en el 2,1% restante, no se documentó el tipo de FA. El 81,3% de los pacientes tenían un ecocardiograma. El 75,8% de los pacientes tenían una puntuación CHADS2 ≥ 2 (CHADS2 medio, 2,3 ± 1,2); el 94,5% tenía una puntuación CHA2DS2-VASc ≥ 2 (CHA2DS2-VASc medio, 3,9 ± 1,5), y el 13,0%, HAS-BLED ≥ 3 (HAS-BLED medio, 1,6 ± 0,9) (tabla 4).
Puntuaciones CHADS2, CHA2DS2-VASc y HAS-BLED de la población incluida en el estudio (n = 1.524)
| CHADS2 | % | CHA2DS2-VASc | % | HAS-BLED | % |
|---|---|---|---|---|---|
| 0 | 5,4 | 0 | 1,0 | 0 | 5,3 |
| 1 | 18,8 | 1 | 4,5 | 1 | 49,0 |
| 2 | 38,1 | 2 | 11,5 | 2 | 32,7 |
| 3 | 22,7 | 3 | 22,0 | 3 | 9,9 |
| 4 | 10,9 | 4 | 28,0 | 4 | 2,6 |
| 5 | 3,3 | 5 | 19,0 | 5 | 0,5 |
| 6 | 0,9 | 6 | 9,8 | 6 | 0,0 |
| 7 | 3,4 | 7 | 0,0 | ||
| 8 | 0,8 | 8 | 0,0 | ||
| 9 | 0,1 | 9 | 0,0 |
CHADS2: insuficiencia cardiaca, hipertensión, edad, diabetes, ictus [doble]; CHA2DS2-VASc, insuficiencia cardiaca congestiva, hipertensión, edad ≥ 75 años [doble], diabetes mellitus, ictus [doble], enfermedad vascular, edad 65-74 años y sexo [mujer]; HAS-BLED: hipertensión, función renal/hepática anormal, ictus, antecedentes de hemorragia o predisposición a ella, labilidad de la razón internacional normalizada, edad mayor 65 años y toma concomitante de fármacos o alcohol.
El 94,8% de los pacientes (n = 1.445) estaban tomando acenocumarol y el 5,2% (n = 79), warfarina. El control de la anticoagulación del 70,7% de los pacientes lo realizaba exclusivamente el médico de atención primaria; el del 8,1%, hematología; el del 20,9%, atención primaria y hematología en conjunto, y el del 0,3%, cardiología. El número total de registros de la INR en los 12 meses previos fue 21.982 y el número medio de determinaciones de la INR registradas por paciente en el último año, 14,4 ± 3,8. El porcentaje de tiempo en rango terapéutico fue del 63,2 ± 17,9% según el método directo y el 69,0 ± 17,7% según el método de Rosendaal. El 56,9% de los pacientes tenían un adecuado control de la INR según el método directo, y el 60,6% según el método de Rosendaal (figura). En el 65,0% de los casos, el médico consideraba que el paciente tenía un buen control de la INR. De los pacientes que tenían mal control de la INR calculada por el método directo, el 30,4% de las mediciones de la INR se encontraban por debajo de 2 y el 25,5%, por encima de 3. Por el método de Rosendaal, estos valores fueron del 30,2 y el 25,6% respectivamente. En el 30,5% de las determinaciones de la INR se modificó la dosis del anticoagulante. En el 46,4% el ajuste de dosis se realizó manualmente y en el resto, de manera automática/mixta (algún tipo de colaboración o ayuda).
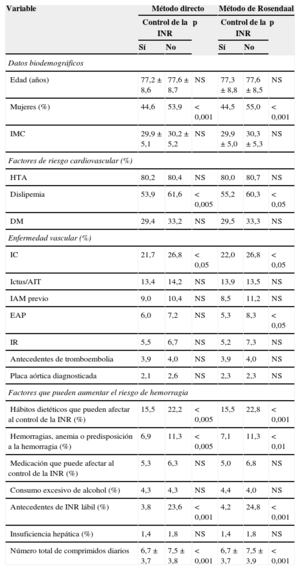
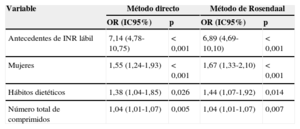
Las variables asociadas con el control de la INR se muestran en la tabla 5 (análisis bivariable) y la tabla 6 (análisis multivariable) según el método directo y el método de Rosendaal. En el análisis multivariable, tanto por el método directo como por el método de Rosendaal, se objetivó que los varones tenían mejor control que las mujeres, que los pacientes con hábitos dietéticos que pudieran afectar a la anticoagulación con AVK presentaban menor probabilidad de estar bien controlados, que los pacientes no controlados tomaban más comprimidos diarios que los controlados y que los pacientes con antecedentes de INR lábil presentaban menos probabilidad de estar controlados que quienes no tenían historia reconocida de INR lábil.
Variables asociadas con el control de la razón internacional normalizada (análisis bivariable) según el método directo y el método de Rosendaal (n = 1.524)
| Variable | Método directo | Método de Rosendaal | ||||
|---|---|---|---|---|---|---|
| Control de la INR | p | Control de la INR | p | |||
| Sí | No | Sí | No | |||
| Datos biodemográficos | ||||||
| Edad (años) | 77,2 ± 8,6 | 77,6 ± 8,7 | NS | 77,3 ± 8,8 | 77,6 ± 8,5 | NS |
| Mujeres (%) | 44,6 | 53,9 | < 0,001 | 44,5 | 55,0 | < 0,001 |
| IMC | 29,9 ± 5,1 | 30,2 ± 5,2 | NS | 29,9 ± 5,0 | 30,3 ± 5,3 | NS |
| Factores de riesgo cardiovascular (%) | ||||||
| HTA | 80,2 | 80,4 | NS | 80,0 | 80,7 | NS |
| Dislipemia | 53,9 | 61,6 | < 0,005 | 55,2 | 60,3 | < 0,05 |
| DM | 29,4 | 33,2 | NS | 29,5 | 33,3 | NS |
| Enfermedad vascular (%) | ||||||
| IC | 21,7 | 26,8 | < 0,05 | 22,0 | 26,8 | < 0,05 |
| Ictus/AIT | 13,4 | 14,2 | NS | 13,9 | 13,5 | NS |
| IAM previo | 9,0 | 10,4 | NS | 8,5 | 11,2 | NS |
| EAP | 6,0 | 7,2 | NS | 5,3 | 8,3 | < 0,05 |
| IR | 5,5 | 6,7 | NS | 5,2 | 7,3 | NS |
| Antecedentes de tromboembolia | 3,9 | 4,0 | NS | 3,9 | 4,0 | NS |
| Placa aórtica diagnosticada | 2,1 | 2,6 | NS | 2,3 | 2,3 | NS |
| Factores que pueden aumentar el riesgo de hemorragia | ||||||
| Hábitos dietéticos que pueden afectar al control de la INR (%) | 15,5 | 22,2 | < 0,005 | 15,5 | 22,8 | < 0,001 |
| Hemorragias, anemia o predisposición a la hemorragia (%) | 6,9 | 11,3 | < 0,005 | 7,1 | 11,3 | < 0,01 |
| Medicación que puede afectar al control de la INR (%) | 5,3 | 6,3 | NS | 5,0 | 6,8 | NS |
| Consumo excesivo de alcohol (%) | 4,3 | 4,3 | NS | 4,4 | 4,0 | NS |
| Antecedentes de INR lábil (%) | 3,8 | 23,6 | < 0,001 | 4,2 | 24,8 | < 0,001 |
| Insuficiencia hepática (%) | 1,4 | 1,8 | NS | 1,4 | 1,8 | NS |
| Número total de comprimidos diarios | 6,7 ± 3,7 | 7,5 ± 3,8 | < 0,001 | 6,7 ± 3,7 | 7,5 ± 3,9 | < 0,001 |
AIT: accidente isquémico transitorio; DM: diabetes mellitus; EAP: enfermedad arterial periférica; HTA: hipertensión arterial; IAM: infarto agudo de miocardio; IC: insuficiencia cardiaca; IMC: índice de masa corporal; INR: razón internacional normalizada; IR: insuficiencia renal; NS: no significativo.
Variables asociadas con mal control de la razón internacional normalizada (análisis multivariable) según el método directo y el método de Rosendaal
| Variable | Método directo | Método de Rosendaal | ||
|---|---|---|---|---|
| OR (IC95%) | p | OR (IC95%) | p | |
| Antecedentes de INR lábil | 7,14 (4,78-10,75) | < 0,001 | 6,89 (4,69-10,10) | < 0,001 |
| Mujeres | 1,55 (1,24-1,93) | < 0,001 | 1,67 (1,33-2,10) | < 0,001 |
| Hábitos dietéticos | 1,38 (1,04-1,85) | 0,026 | 1,44 (1,07-1,92) | 0,014 |
| Número total de comprimidos | 1,04 (1,01-1,07) | 0,005 | 1,04 (1,01-1,07) | 0,007 |
IC95%: intervalo de confianza del 95%; INR: razón internacional normalizada; OR: odds ratio.
Los resultados del estudio PAULA indican que el control de la INR en las consultas de atención primaria en España es claramente mejorable. Este estudio incluye una muestra amplia y representativa de toda la población española con FANV asistida en atención primaria, con un alto número de controles de la INR y un largo periodo de seguimiento. Es importante señalar que la monitorización de este trabajo fue muy meticulosa, aplicando un riguroso control que permitiera garantizar la calidad de los datos registrados. Por otra parte, entre los aspectos relevantes de este estudio, hay que destacar que no solamente es un ejemplo de trabajo conjunto entre médicos de atención primaria y cardiólogos, sino que, además, tiene el valor añadido de la colaboración entre sociedades científicas, al ser la primera vez en España que un estudio de estas características es avalado por las tres sociedades nacionales de atención primaria.
En cuanto a los datos recogidos en el estudio PAULA, se observa que la media de edad de los pacientes incluidos era 77 años; aproximadamente la mitad eran mujeres; el 80% tenía hipertensión arterial; el 24%, insuficiencia cardiaca; el 14%, antecedentes de ictus o accidente isquémico transitorio, y el 10%, infarto previo. Estos datos indican que el paciente con FANV anticoagulado en España tiene una edad relativamente avanzada y un gran número de comorbilidades asociadas. Sin embargo, en comparación con otras poblaciones con FA analizadas en España, sobre todo las atendidas en consultas de cardiología, la proporción de sujetos con algunas enfermedades como cardiopatía isquémica o insuficiencia renal fue algo menor en el estudio PAULA2,3,12,13,20. Resulta interesante destacar que el filtrado glomerular medio de los pacientes incluidos en el estudio PAULA fue 73,1ml/min/1,73 m2. Es probable que en poblaciones de mayor riesgo el control de la anticoagulación pudiera ser aún peor.
En cuanto al tipo de FA, diferentes estudios han puesto de manifiesto que la forma más frecuente en los pacientes asistidos en atención primaria es la FA permanente (el 45,3% en VAL-FAAP, el 77,5% en FIATE y el 64,2% en PAULA)2,13. Por lo tanto, para la mayoría de los pacientes con FANV en atención primaria, parece que los objetivos terapéuticos deberán dirigirse fundamentalmente al control de la frecuencia cardiaca y reducir el riesgo tromboembólico.
La evaluación del riesgo de ictus y de hemorragia en FANV es fundamental. En los últimos años se ha observado un incremento en el empleo de las escalas tanto de estratificación de riesgo tromboembólico (CHADS2 y CHA2DS2-VASc), como hemorrágico (HAS-BLED)21. En el estudio VAL-FAAP, el 67,4% tenía una puntuación CHADS2 ≥ 2 y el 85,7%, CHA2DS2-VASc ≥ 22,8. En el estudio ANFAGAL12, la puntuación CHADS2 fue 2,3; la CHA2DS2-VASc, 3,8 y HAS-BLED, 3,1. En el estudio PAULA, las cifras fueron 2,3 y 3,9 y 1,6 respectivamente. Por lo tanto, la indicación de anticoagulación parece muy adecuada. Respecto a la diferencia en la puntuación HAS-BLED observada entre los estudios ANFAGAL y PAULA, probablemente puede estar relacionada con la diferencia de edad entre los dos estudios, debido a que los criterios de inclusión fueron algo diferentes.
Las guías recomiendan la realización de un ecocardiograma dentro del estudio inicial del paciente con FA21. En el estudio FIATE, al 67,6% de los pacientes se les había realizado al menos un ecocardiograma13. En el estudio PAULA fueron el 81,3%. Este hallazgo es muy relevante, ya que indica que el manejo clínico del paciente con FA en atención primaria es cada vez mejor.
Con respecto a quién es el responsable del control habitual de la INR, en el estudio FIATE13, se objetivó que en el 72% de los casos el control se realizaba en atención primaria. En el estudio PAULA, el médico de atención primaria realizó el control de la anticoagulación del 70,7% de los pacientes, y conjuntamente atención primaria y hematología el del 20,9%. En consecuencia, en ambos estudios, el control de la INR se realizó, como es habitual en España, fundamentalmente en atención primaria. No obstante, es interesante destacar que el protagonismo de atención primaria fue aún mayor en el estudio PAULA. Este es un aspecto importante, ya que, aunque con algunas limitaciones metodológicas importantes, se ha señalado que los costes podrían ser menores cuando el control de la INR se realiza desde el primer nivel asistencial22.
Un control inadecuado de la INR incrementa bien el riesgo de ictus, bien el riesgo de hemorragias17,23,24. Por lo tanto, es imprescindible asegurar un control correcto. En los ensayos clínicos realizados con los nuevos anticoagulantes de acción directa, la media de tiempo en rango terapéutico varió del 55 al 68,4%25–28. Sin embargo, como los pacientes incluidos en los ensayos clínicos tienen unos criterios de inclusión y exclusión restrictivos y un seguimiento muy riguroso, sus resultados no son siempre extrapolables a la «vida real». En este contexto, los estudios realizados en condiciones de práctica clínica aportan una información muy relevante29,30.
En el estudio ANFAGAL12, con una media de 13,7 determinaciones por paciente, el 41,5% tenía menos del 60% de los controles en rango terapéutico y el 42,7% mostró un tiempo en rango terapéutico < 65% estimado según el método de Rosendaal. En el estudio FIATE13, de los pacientes en tratamiento con AVK en que solo se analizaban los últimos tres INR, el 66% presentaba en rango terapéutico su último INR y el 33%, los tres. Es importante tener presente que los resultados del estudio ANFAGAL se obtuvieron de una muestra de pacientes pequeña y solo de un área geográfica (Galicia), y en el estudio FIATE el número de determinaciones de la INR es realmente bajo. Por ello, la información del estudio PAULA ofrece datos de gran interés. En el estudio PAULA, el 43,1% de los pacientes tenían en rango terapéutico menos del 60% de los controles realizados en el último año y el 39,4% mostró un tiempo en rango terapéutico < 65%, con una media de 14,4 determinaciones por paciente. En un metanálisis de 95 artículos, los pacientes anticoagulados con AVK se mantuvieron el 61% del tiempo en rango terapéutico, y fue mejor el control observado en ensayos clínicos o en clínicas especializadas que en otros escenarios31. Por lo tanto, se puede decir que el control de la anticoagulación en España es malo, algo similar a lo que ocurre en otros países. A diferencia de lo que sucede con otras entidades crónicas, como la hipertensión, en las que uno de los motivos del mal control es una marcada percepción incorrecta de este, el estudio PAULA muestra que el mal control de la anticoagulación no parece deberse tanto a una percepción incorrecta del médico como a la dificultad inherente a mantener al paciente dentro del rango terapéutico adecuado32.
Distintos estudios han investigado qué factores se asocian con un peor control de la anticoagulación. En el estudio ANFAGAL se observó que era más frecuente el mal control de la INR en sujetos con valores de HAS-BLED elevados, diabetes mellitus, enfermedad renal e hipertensión12. En un estudio realizado en Estados Unidos, los predictores de mal control incluyeron el abuso de alcohol, la polimedicación y haber tenido múltiples hospitalizaciones33. En otro estudio, las variables asociadas a buen control fueron el consumo regular de vitamina K, el sexo masculino, duración del tratamiento anticoagulante > 2 meses, tener un apoyo familiar adecuado, presentar capacidades funcional y cognitiva adecuadas y no consumir alcohol habitualmente34. En el estudio PAULA, los predictores de mal control fueron presentar antecedentes de INR lábil, el sexo femenino, tener hábitos dietéticos que pudieran afectar al efecto de los AVK y la polimedicación. Conocer estos factores es importante para identificar a los pacientes para los que va a ser necesaria una vigilancia más estricta del control de la INR, incluso a los que, al menos a priori, pueden ser más susceptibles de beneficiarse potencialmente del empleo de los nuevos anticoagulantes de acción directa. En cuanto al peor control asociado al sexo femenino, varios estudios han encontrado esta misma tendencia, y probablemente se deba a que las características clínicas de una y otra población sean diferentes34,35.
LimitacionesLas limitaciones de este estudio son las propias de un estudio observacional. Además, muchas variables se recogieron de la historia clínica del paciente, con las limitaciones que esto conlleva. Sin embargo, el gran número de pacientes incluidos, así como la meticulosidad en el control de calidad de los datos registrados y el rigor en la monitorización, puede disminuir notablemente el efecto de estas posibles limitaciones. Por otra parte, se contó con la colaboración de los coordinadores regionales que se encargaron de velar por el buen funcionamiento del estudio, aclarando cualquier tipo de duda que pudiese surgir y asegurando que la introducción de los datos fuese correcta y en tiempo. Además, el propio sistema electrónico tenía un programa automático de validación, con unos valores límite adecuados que aseguraran la coherencia lógica de los datos, que generaba alertas cuando se detectaban discrepancias o incongruencias. Hay que tener en cuenta que este estudio es retrospectivo, pero este diseño, lejos de ser un inconveniente, es una notable ventaja, ya que permite conocer la realidad clínica del control de la anticoagulación en la práctica clínica diaria. En un estudio prospectivo, los controles de la INR podrían estar muy condicionados por la inclusión del paciente en el estudio. Por otra parte, el hecho de que el reclutamiento de los investigadores no se hiciera de manera aleatorizada, sino de conveniencia, pudo hacer que participaran investigadores más motivados, por lo que puede que se sobrestimara el grado de control de la INR. Sin embargo, el grado de control de la INR encontrado en este estudio no fue muy diferente del reportado en otros estudios, incluidos los grandes ensayos clínicos con los nuevos anticoagulantes orales de acción directa. Por otra parte, dado que el objetivo del estudio era conocer el grado de control de la INR de los pacientes tratados con AVK en el último año, hubo pacientes que llevaban años con este tratamiento, probablemente la mayoría, dado que el tiempo medio desde el diagnóstico de la FA fue de 6 años, y otros quizá solo el último año. Es posible que el grado de control de la INR difiera según esta situación, pero por desgracia este dato no se registró. Entre los criterios de inclusión se encontraba tener acceso al menos al 80% de las mediciones de la INR. Aunque lo óptimo habría sido el 100%, la realidad es que, aunque lo habitual es que el control de la INR se haga en el mismo sitio, esto no siempre es así (vacaciones, viajes, etc.). De hecho, incluso en los grandes ensayos clínicos no siempre se dispone de todos los datos. Por este motivo, el dato de al menos el 80% como criterio de inclusión permitía que, siendo realistas, se garantizara un mínimo de calidad. Con todo, el número total de registros de la INR en los 12 meses previos fue 21.982 y el número medio de determinaciones de INR registradas por paciente en el último año, 14,4. Asimismo, tampoco se registró a los pacientes que, cumpliendo los criterios de inclusión, declinaron participar en el estudio. Por último, los resultados de este estudio solo son extrapolables a países que tengan un perfil clínico de pacientes similar y con un sistema sanitario parecido al español.
CONCLUSIONESEl control de la INR en la práctica clínica en España es muy mejorable, ya que aproximadamente un 40% de los pacientes no están bien controlados. Los predictores de mal control de la INR fueron los antecedentes de INR lábil, el sexo femenino, tener hábitos dietéticos que pudieran afectar al efecto de los AVK y la polimedicación.
CONFLICTO DE INTERESESEl estudio fue patrocinado por Bayer Hispania S.L., sin que dicho patrocinio influyera en modo alguno en el desarrollo del estudio, la obtención de los resultados o su interpretación, a pesar de que dos de los autores pertenecieran al departamento médico de Bayer.
Los autores quieren agradecer a los investigadores y a los coordinadores el trabajo realizado, ya que sin su labor habría sido imposible la realización del presente estudio.
Los autores también quieren agradecer a la CRO Dynamic Solutions el trabajo realizado, que ha ayudado a garantizar la veracidad y la calidad de los datos recogidos.