Las fístulas coronarias son anomalías congénitas o adquiridas raras, con baja incidencia en la población general (0,3-0,8%), originadas primordialmente (50-60%) de la arteria coronaria derecha o la descendente anterior (30-40%); la menos afectada (10-20%) es la circunfleja (Cx)1. Las fístulas sintomáticas tienen indicación de cierre desde su diagnóstico, o cuando se relacionan con isquemia miocárdica, arritmias, dilatación o disfunción ventricular, sin que importe su tamaño. En pacientes asintomáticos, el tratamiento es controvertido, y algunos autores aconsejan el cierre debido al riesgo de complicaciones tardías1,2. Su detección en pacientes adultos implica mayor riesgo quirúrgico y comorbilidades. La cirugía fue el tratamiento habitual durante décadas, y el cierre percutáneo se restringía a pacientes sin opción quirúrgica y/o con una anatomía vascular favorable. No obstante, el tratamiento percutáneo es factible en centros experimentados. Presentamos el cierre percutáneo de 2 fístulas de Cx en 2 pacientes adultos con importantes comorbilidades y anatomía vascular compleja, que rechazaron cirugía.
El primero es un varón de 77 años, con hipertensión arterial, fibrilación auricular permanente, en anticoagulación oral, remitido por disnea de pequeños esfuerzos. La ecocardiografía transtorácica mostró marcada dilatación de cavidades derechas e insuficiencia tricuspídea grave. El cateterismo cardiaco mostró presión arterial pulmonar normal y cortocircuito izquierda-derecha con Qp/Qs de 1,7. La coronariografía reveló una Cx tortuosa, dilatada, con drenaje en la aurícula derecha, lo que se corroboró por tomografía computarizada (figuras 1A-D).
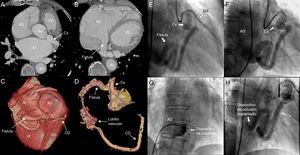
Tomografía computarizada (A y B) con reconstrucción tridimensional (C y D) que muestra la circunfleja ectásica drenando en la aurícula derecha muy dilatada, su disposición anatómica y su conexión distal con la arteria coronaria derecha mediante un lobillo vascular. Imágenes angiográficas que evidencian la fístula de la circunfleja a la aurícula derecha (E), el circuito arteriovenoso (F) y la liberación del dispositivo oclusor (G), que obtiene ausencia de flujo residual significativo (H). AD: aurícula derecha; AI: aurícula izquierda; Ao: aorta; CD: coronaria derecha; Cx: circunfleja; DA: descendente anterior; VD: ventrículo derecho; VI: ventrículo izquierdo.
Para el cierre percutáneo, el acceso vascular fue vía arteria femoral derecha y vena femoral izquierda, ambos de 6 Fr. Mediante un catéter Amplatz izquierdo, se canuló la fístula desde el tronco coronario izquierdo y se avanzó una guía coronaria extraflexible desde el lado arterial hasta su desembocadura en la aurícula derecha. Para establecer el circuito arteriovenoso, se usó un catéter lazo para capturar la guía coronaria en la aurícula derecha, que se exteriorizó por la vena femoral izquierda. Posteriormente, se canuló la fístula con un catéter multipropósito vía vena femoral izquierda, a través del cual se implantó con éxito un dispositivo Amplatzer® Vascular Plug (AVP) de 10mm (AGA; Minnesota, Estados Unidos) en el sitio más estrecho de la fístula. La coronariografía mostró mínimo cortocircuito residual, con adecuado posicionamiento y estabilidad del dispositivo (figuras 1E-H).
El segundo paciente es una mujer de 68 años, diabética, hipertensa, con obesidad de grado II, ingresada por dolor torácico y fibrilación auricular de novo, con anticoagulación oral. La coronariografía no mostró lesiones coronarias significativas, pero reveló el origen anómalo de la Cx desde la arteria pulmonar. La arteria descendente anterior tenía un origen normal. El cateterismo cardiaco derecho demostró Qp/Qs de 2,5 con presión arterial pulmonar normal. La tomografía computarizada confirmó una Cx tortuosa y ectásica que se originaba en la arteria pulmonar derecha proximal, se extendía por el surco auriculoventricular, daba una rama marginal obtusa y recibía colaterales desde las arterias bronquiales, para terminar en una rama posterolateral anastomosada directamente con la arteria descendente posterior procedente de la arteria coronaria derecha ectásica y tortuosa (figuras 2A-D).
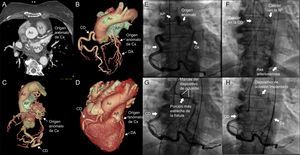
Tomografía computarizada (A) con reconstrucción tridimensional (B-D) que muestran la circunfleja dilatada, con origen anómalo desde la arteria pulmonar derecha, su recorrido y la anastomosis distal con la arteria coronaria derecha mediante ramos colaterales. Imágenes angiográficas que muestran el origen anómalo de la circunfleja desde la arteria pulmonar, su anastomosis distal con la descendente posterior (E), el circuito arteriovenoso (F), el posicionamiento del dispositivo (G) y la liberación exitosa que logra la oclusión completa de la fístula (H). Ao: aorta; AP: arteria pulmonar; CD: coronaria derecha; Cx: circunfleja; DA: descendente anterior; VI: ventrículo izquierdo.
Para el cierre percutáneo, el acceso vascular fue de 6 Fr vía arteria femoral derecha y vena femoral izquierda. Se canuló la arteria coronaria derecha con catéter Judkins derecho; con ayuda de un microcatéter, se avanzó una guía extraflexible vía anterógrada por una rama colateral epicárdica originada de la arteria coronaria derecha, llegando al origen de la Cx en la arteria pulmonar derecha. El circuito arteriovenoso se estableció capturando la guía con catéter lazo y exteriorizándola por la vena femoral izquierda. Inmediatamente se implantó, a través del acceso venoso hasta la arteria pulmonar, un dispositivo AVP II de 7mm en la parte más estrecha del defecto, con lo que se ocluyó con éxito la fístula (figuras 2E-H).
A ambos pacientes se les dio el alta con anticoagulación oral crónica. Al año del procedimiento permanecían asintomáticos y sin complicaciones.
Los pacientes con fístulas pequeñas pueden permanecer asintomáticos durante años. Cuando aparecen los síntomas, se deben principalmente a isquemia cardiaca por robo coronario, insuficiencia cardiaca por sobrecarga de volumen debido al cortocircuito izquierda-derecha, endocarditis infecciosa, arritmias, endarteritis o rotura o trombosis de la fístula. Las guías de tratamiento de cardiopatías congénitas en adultos recomiendan el cierre de todas las fístulas grandes o hemodinámicamente significativas independientemente de los síntomas, utilizando técnicas quirúrgicas o percutáneas3. Antes del advenimiento del intervencionismo percutáneo, la cirugía era la terapia habitual. Los principales criterios que influyen en la elección del tratamiento son las características anatómicas: fístulas cortas, anguladas, con drenaje cercano a la válvula tricúspide y que dan origen a ramas colaterales en proximidad al lugar que ocluir son contraindicaciones para el cierre percutáneo. Además, en fístulas múltiples, que afectan a grandes ramas, con conexión fistulosa estrecha y restrictiva que desembocan en una cámara cardiaca o con tortuosidad extrema que pueda impedir la entrega distal del dispositivo oclusor, generalmente se prefiere la cirugía. Sin embrago, con los dispositivos actuales de cierre percutáneo, la oclusión completa se logra en más del 80% de los casos, con escasas complicaciones periprocedimiento4,5, hospitalizaciones cortas, rápida recuperación y excelente aceptación del paciente.
El avance en estudios de imagen cardiaca, la creciente experiencia de los intervencionistas, el refinamiento en técnicas percutáneas y la mejora de los materiales hacen factible el cierre transcatéter de fístulas en poblaciones más amplias.