Palabras clave
INTRODUCCIÓN
La endocarditis sobre válvula protésica (EVP) es una complicación infrecuente aunque grave en los pacientes que han sido sometidos a una intervención de recambio valvular1,2. A pesar de los avances habidos en los últimos años en su diagnóstico y tratamiento, la EVP presenta una elevada morbimortalidad3-5. De hecho, la tasa de mortalidad de la EVP oscila entre el 25 y el 59%, aunque se han desarrollado indudables avances tanto en la profilaxis como en el diagnóstico y el tratamiento de esta enfermedad6-9.
El propósito de este trabajo es analizar la evolución en los factores epidemiológicos, la etiología y las características clínicas de los pacientes con EVP, así como estudiar el tratamiento realizado y el pronóstico de estos pacientes.
MÉTODOS
El estudio se llevó a cabo en el Hospital Universitario Marqués de Valdecilla de Santander (Cantabria), un centro hospitalario de nivel terciario, con una capacidad aproximada de 1.200 camas, que durante el periodo de estudio ha sido centro de referencia para la cirugía cardiovascular tanto de esa comunidad autónoma (unos 520.000 habitantes) como de otras próximas (Castilla y León, Galicia, Asturias, País Vasco y La Rioja), y se han realizado aproximadamente 1.000 intervenciones de cirugía cardiovascular al año, de las cuales 500 son operaciones de cirugía cardiaca.
Se realizó un estudio de cohortes retrospectivo en el que se incluyó a todos los pacientes mayores de 14 años diagnosticados de EVP en el Hospital Universitario Marqués de Valdecilla durante los años 1986 a 2005. La identificación de los casos se realizó retrospectivamente analizando los registros informatizados del Departamento de Cirugía Cardiovascular, el registro de la Unidad de Enfermedades Infecciosas y los registros informatizados del Servicio de Admisión y Documentación Clínica. Se estableció la definición de caso de endocarditis protésica de acuerdo con los criterios de Duke modificados10 más las modificaciones realizadas por nuestro grupo de trabajo, que son específicas para el diagnóstico de la EVP11. Sólo se incluyeron los casos con diagnóstico definitivo de EVP que habían sido intervenidos previamente en nuestro centro mediante recambio valvular. A los pacientes que padecieron más de un episodio de EVP se los consideró casos nuevos. Para diferenciar infección protésica precoz de la tardía, se utilizó el criterio clásico de 60 días desde la intervención hasta el inicio de los síntomas12. Se realizó el seguimiento de todos los pacientes incluidos en el estudio, desde el diagnóstico de EVP hasta el alta hospitalaria.
Con el objetivo de analizar las diferencias epidemiológicas y clínicas, se dividió el estudio en dos periodos: periodo 1 (P1) desde enero de 1986 a diciembre de 1995 y periodo 2 (P2) desde enero de 1996 a diciembre de 2005. Esta división tenía la ventaja de contar con dos periodos de igual duración y aprovechar el momento de la introducción generalizada de la ecocardiografía transesofágica en nuestro centro en el diagnóstico de EVP a partir de 1995. A efectos de análisis estadístico, se consideró como periodo de referencia el P1.
Definiciones
Se revisaron las historias clínicas de los pacientes de forma retrospectiva para analizar los factores siguientes:
- Datos epidemiológicos: edad, sexo, lugar de origen (Cantabria u otras comunidades); endocarditis previa, cirugía de la válvula previa (incluidos tipo de cirugía, duración y tipo de válvula); enfermedades subyacentes, entre las que se incluyeron EPOC, insuficiencia renal, diabetes mellitus, hepatopatía, accidente cerebrovascular previo y neoplasias; la comorbilidad se definió por la presencia de dos o más de los siguientes factores: diabetes mellitus, edad > 75 años, infección por el virus de la inmunodeficiencia humana (VIH), cáncer e inmunodeficiencia8. Se registraron asimismo las características de las prótesis (tamaño, posición y tipo).
- Hallazgos clínicos: se registró la presencia de fiebre, soplo nuevo o cambios en las características de soplo conocido, insuficiencia cardiaca y alteraciones neurológicas. La definición de EVP «complicada» se obtuvo de los criterios apuntados por Calderwood et al13 (soplo de reciente aparición, insuficiencia cardiaca, fiebre persistente más de 10 días o alteraciones en la conducción cardiaca). «Mala evolución» es un concepto que se aplicó en los siguientes casos: recaída, operación valvular debida a secuelas de la infección o muerte con elementos indicadores de infección no resuelta o disfunción de prótesis13. Se definió «infección incontrolada» por fiebre persistente, bacteriemia persistente o ambos después de 1 semana de tratamiento antimicrobiano apropiado14. Shock séptico se definió como hipotensión persistente (presión arterial sistólica ≤ 90 mmHg), no debida a shock cardiogénico, junto con al menos una de las siguientes anomalías de perfusión: oliguria, alteración aguda del estado mental o acidosis láctica15. Se definió mortalidad hospitalaria como la muerte ocurrida durante la hospitalización inicial por endocarditis infecciosa14.
- Datos microbiológicos: se obtuvieron datos de los hemocultivos, fecha de obtención, número de muestras extraídas y de muestras positivas y los resultados de las serologías y del cultivo de la válvula infectada, siempre que estuvieron disponibles.
- Ecocardiografía: se evaluaron resultados de ecocardiografía transtorácica y/o transesofágica: presencia de vegetaciones, disfunción protésica, dehiscencia protésica y absceso miocárdico16,17.
Análisis estadístico
Los datos recogidos se introdujeron en una base de datos creada con el programa estadístico SPSS 15.0. Para la comparación de las medias entre subgrupos, en el caso de variables cuantitativas se utilizó la prueba de la t de Student. Las comparaciones para las variables cualitativas se realizaron a partir de la prueba de la χ2 o la prueba exacta de Fisher (cuando las frecuencias esperadas eran < 5). Se calculó la magnitud del efecto mediante el cálculo del riesgo relativo (RR) con su intervalo de confianza (IC) del 95%, tomando como referencia el primer periodo de estudio. Se aceptaron como significativas diferencias correspondientes a errores α < 0,05.
RESULTADOS
Los 122 pacientes estudiados sufrieron 133 episodios de EVP: en 112 casos fueron episodios únicos, 9 sufrieron dos episodios y 1 paciente tuvo tres. Durante los 20 años del estudio se realizaron 6.079 intervenciones de recambio valvular, lo que originaría una incidencia acumulada aproximada de EVP en nuestro centro del 2,2%. De los 133 episodios estudiados, en 73 (54,9%) la EVP se diagnosticó en los primeros 10 años del estudio (1986-1995), mientras en 60 (45,1%) la EVP se diagnosticó después (1996-2005). El 65% de los pacientes tenían más de 65 años en el momento del diagnóstico.
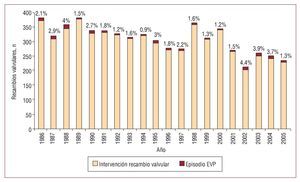
Durante el primer periodo se presentaron 73 episodios de EVP sobre 3.330 intervenciones de recambio valvular (incidencia, 2,19%). En el segundo periodo se presentaron 60 episodios de EVP sobre 2.749 intervenciones de recambio valvular (incidencia, 2,18%). La evolución temporal del número de casos de EVP con relación al número total de intervenciones de recambio valvular realizadas se muestra en la figura 1.
Fig. 1. Diagrama de barras en el que se representa sobre cada columna el porcentaje de episodios de endocarditis sobre válvula protésica en relación con las intervenciones de recambio valvular en el Hospital Universitario Marqués de Valdecilla durante los dos periodos de estudio. EVP: endocarditis sobre válvula protésica.
Al analizar la edad, se observó un envejecimiento de la población, con una media ± desviación estándar de edad de 52,6 ± 16,6 años en P1 y 66,2 ± 11,5 años en P2 (p = 0,0001). También se observó una disminución significativa de los varones (P1, 75 [3%]; P2, 35 [58,3%]; RR = 0,8; IC del 95%, 0,6-1; p = 0,04). Las características epidemiológicas de la población de estudio se muestran en la tabla 1.
Respecto al tipo de valvulopatía previa a la cirugía, se observó un descenso en la incidencia de valvulopatía reumática y un aumento de valvulopatía degenerativa (tabla 1). Asimismo se produjo un descenso en el porcentaje de bioprótesis implantadas: P2, 23 (39,7%), frente a P1, 44 (62%) (RR = 0,6; IC del 95%, 0,4-0,9; p = 0,012).
En cuanto a los factores de riesgo, sólo fue significativo el aumento de la incidencia de diabetes mellitus (P2 frente a P1, el 15 frente al 1%; RR = 10,9; IC del 95%, 1,4-84; p = 0,003), y no se observaron diferencias significativas entre los dos periodos en cuanto a otros factores analizados (tabla 1).
La infección de la prótesis fue tardía en 109 casos (82%) y precoz en 24 (18%). En las EVP tardías, 22 casos (20,2%) ocurrieron entre 3 y 12 meses tras el recambio valvular; 20 casos (18,3%), entre 12 y 36 meses y 67 (61,5%), después de 36 meses de la intervención. No se observaron diferencias significativas en la incidencia de EVP precoz y tardía en los dos periodos de estudio analizados (EVP precoz, P2 frente a P1, el 18,3 frente al 17,8%; RR = 1; IC del 95%, 0,5-2,1; p = 0,94).
Los datos clínicos más relevantes en el momento del diagnóstico fueron: fiebre, presente en el 80% de los casos y más frecuente en las EVP tardías (84%) que en las precoces (71%); insuficiencia cardiaca, presente en el 65% de los casos y, al contrario que la fiebre, más prevalente en las EVP precoces (75%) que en las tardías (64%); aparición de nuevos soplos o cambio en la cualidad de los ya presentes en el 64% de los casos, más frecuente en las EVP tardías (66%) que en las precoces (54%). Otros signos y síntomas clínicos no variaron significativamente durante el estudio.
En todos los episodios se realizaron hemocultivos. En 24 casos (18%) los hemocultivos fueron negativos, y no se apreciaron diferencias significativas en los dos periodos de estudio (P2 frente a P1, el 16,4 frente al 12%; RR = 1,2; IC del 95%, 0,5-2,7; p = 0,63). Los microorganismos aislados en los 109 casos restantes (82%) se muestran en la tabla 2. Los microorganismos más frecuentemente aislados fueron: estafilococo coagulasa negativo en 36 casos (33%; 31 eran S. epidermidis), estreptococos del grupo viridans en 25 casos (22,9%), Staphylococcus aureus en 17 casos (15,6%; 12 eran sensibles a meticilina [SASM] y 5, resistentes [SARM]) y Enterococcus en 9 casos (8,3%); otros aislamientos bacterianos tuvieron lugar en 17 casos (15,6%), y en 4 casos (3,6%) se aisló Candida sp. A la hora de analizar los hallazgos microbiológicos, no se encontraron diferencias significativas durante los dos periodos de estudio (1986-1995 y 1996-2005), a excepción del descenso de infecciones por estreptococos del grupo viridans (P2 frente a P1, el 12,5 frente al 31,1%; RR = 0,4; IC del 95%, 0,2-0,9; p = 0,02) (tabla 2).
El 49,2% de los ecocardiogramas fueron transtorácicos y el 50,8%, transesofágicos (con el 24% de transesofágicos en el P1 y el 84% en el P2; RR = 3,5; IC del 95%, 2,2-5,5; p < 0,0001). En 84 pacientes (63,1%) hubo vegetaciones; en 95 (71,4%), disfunción intrínseca de prótesis; en 13 (9,7%), dehiscencia valvular y en 39 casos (29,3%), invasión miocárdica. No hubo diferencias en los hallazgos ecocardiográficos entre P1 y P2.
Recibieron tratamiento quirúrgico 107 pacientes (80,5%), con una mayor tendencia a realizar tratamiento quirúrgico durante el primer periodo (en P1, el 90,4% [66/73] frente al 68,3% [41/60] de intervenciones en P2; RR = 0,8; IC del 95%, 0,6-0,9; p = 0,001).
Presentaron endocarditis bacteriana «complicada» 96 (72,2%) pacientes; infección incontrolada, 19 (14,3%), y mala evolución, 28 (21,1%).
La mortalidad intrahospitalaria fue de 39 casos (29,3%), el 41,7% de los casos de EVP precoz (10/24) y el 26,6% de los casos de EVP tardía (29/109); no se observaron diferencias entre ambos periodos (el 30% en P2 y el 28,8% en P1; RR = 1; IC del 95%, 0,6-1,8; p = 0,88).
DISCUSIÓN
Este trabajo se ha realizado durante un periodo largo, condicionado en parte por las características especiales de la EVP, que presenta una baja incidencia. No obstante, la aproximación realizada tiene la ventaja de permitir comparar dos periodos temporales para analizar los cambios en la epidemiología de la infección y el impacto de la práctica médica en la microbiología y en el pronóstico de la EVP. De hecho, la serie aquí presentada es, en nuestra revisión de la literatura, la más amplia presentada con criterios definitivos de EVP en un único centro hospitalario. Aunque existen trabajos multicéntricos con un número de pacientes reclutados mayor18,19, nuestra serie tiene la ventaja de que la recogida de información fue realizada por una misma persona, lo que garantiza la homogeneidad de la información suministrada; además, la permanencia durante el periodo de análisis de prácticamente los mismos equipos de trabajo médicos y quirúrgicos disminuye la variabilidad que pudiera atribuirse a la distinta práctica clínica. En este sentido, es interesante mencionar por su similitud el trabajo de Pablo Rivas et al20, que incluye sin embargo un periodo más largo de recogida de información (1970-2003). En nuestro trabajo, la media de edad en el momento del diagnóstico fue de 59 años para el conjunto de los casos. A la hora de analizar la edad en los dos periodos de estudio (1986-1995 y 1996-2005) se objetivó un envejecimiento de la población, con una media de edad en el primer periodo de 52,6 años, frente a 66,2 años en el segundo periodo (diferencia estadísticamente significativa), y además los pacientes con edad > 65 años eran significativamente más en el segundo periodo. Cuando procedimos a revisar series en la literatura sobre EVP, se constató un envejecimiento progresivo de la población (tabla 3), y llama la atención que en las EVP posteriores a 1990 la media de edad ha aumentado unos 9 años7-9,13,14,21-33.
Al estudiar los casos de EVP precoces (20%) y tardías (80%) durante los dos periodos de estudio (1986-1995 y 1996-2005), no se encontraron diferencias estadísticamente significativas, con una distribución similar en el porcentaje de EVP precoces y EVP tardías, dato que contrasta con las observaciones apuntadas por otros estudios20,34, que muestran un descenso progresivo de las EVP precoces y un leve ascenso en las EVP tardías, si bien ambos estudios tenían como punto de partida los años setenta, lo que puede justificar las diferencias.
Históricamente la EVP era predominantemente una enfermedad de pacientes con valvulopatía reumática de base35,36 y bacteriemia adquirida en la comunidad, y la etiología más frecuente era la estreptocócica, con un 60-80% de todos los casos. En cambio, en los últimos años la prevalencia de valvulopatías reumáticas ha decrecido37,38, mientras la prevalencia de pacientes crónicamente enfermos con procesos invasivos se ha incrementado39. En nuestro estudio, cuando procedimos a analizar los datos en los dos periodos, se vio una reducción progresiva de las valvulopatías reumáticas y un aumento de las valvulopatías degenerativas.
Durante los últimos 20 años, diversos autores han señalado la posibilidad de que los cambios en las características epidemiológicas de la población tengan un papel decisivo en las manifestaciones clínicas y el pronóstico de esta enfermedad37,40,41. Especialmente el progresivo incremento de la utilización de procedimientos invasivos (técnicas quirúrgicas, catéteres venosos centrales, hemodiálisis), con el consiguiente aumento de las infecciones nosocomiales, se ha implicado como un factor que puede aumentar la tasa de endocarditis42. Por otro lado, los avances habidos en la ecocardiografía y el uso de criterios validados para el diagnóstico han permitido a los clínicos la mejora en el diagnóstico de esta enfermedad10,43.
Aunque se han realizado estudios descriptivos centrados en la epidemiología de la endocarditis en los años ochenta y los noventa44-46, existen pocos trabajos destinados a comprender las relaciones entre el cambio de las características epidemiológicas y el pronóstico. Cabell et al41, de la Universidad de Duke, publicaron un estudio donde se intentaba identificar cambios en las características epidemiológicas y microbiológicas de los pacientes con endocarditis, para luego determinar su efecto en la supervivencia. Este trabajo, como todos los precedentes, tiene el inconveniente metodológico de analizar conjuntamente los episodios de endocarditis sobre válvula nativa y EVP. No obstante, constituye una serie extensa con 329 pacientes y un 30% de EVP. Se evidenció un mayor número de pacientes, según pasaban sus 7 años de duración, con inmunodeficiencia y hemodiálisis, lo que implicaba más infecciones por S. aureus, en contraste con un descenso de las endocarditis por estreptococos del grupo viridans. Asimismo, la endocarditis por S. aureus estaba ligada a una mayor mortalidad de los pacientes. En el presente estudio también encontramos un mayor número de pacientes con diabetes mellitus, inmunodeficiencia e insuficiencia renal en el segundo periodo de estudio.
En cuanto a la microbiología de las infecciones protésicas, queremos resaltar, por una parte, la concordancia con la experiencia de la mayor parte de los autores de que tanto S. epidermidis como S. aureus causan la mayoría de los episodios, tanto precoces47 como tardíos4, y que los estreptococos del grupo viridans causan un número importante de casos tardíos. Sin embargo, no hemos encontrado la preponderancia hallada en estudios más recientes de S. aureus14,41,48. En nuestra serie, fue llamativo el incremento de infecciones por enterococos en el segundo periodo de estudio, así como el descenso de las infecciones por estreptococos del grupo viridans. En particular, el número de infecciones por S. aureus permaneció similar durante los dos periodos analizados (el 14,7 frente al 12,3%), a diferencia del trabajo de Rivas et al20, donde se recogió un incremento de EVP por enterococos y S. aureus en los casos de EVP tardía.
La introducción de la ecocardiografía transesofágica en los años noventa ha revolucionado el diagnóstico ecocardiográfico de la EVP por su mayor sensibilidad diagnóstica (76-100%) y su especificidad (94%) para evaluar la extensión perivalvular de la infección49; por ello es una herramienta muy útil en el diagnóstico y la monitorización de la enfermedad, de gran ayuda para decidir a qué pacientes reintervenir16,49,50. En nuestro estudio aparece reflejado el cambio en el abordaje ecocardiográfico del EVP, con una utilización de la ecocardiografía transesofágica del 84% en el segundo periodo de estudio. Esta mejora en el diagnóstico de la EVP podría explicar el menor número de intervenciones quirúrgicas realizadas en el segundo periodo, ya que habría permitido una mejor selección de los pacientes que precisaron cirugía.
El 29% (38) de nuestros pacientes fallecieron durante su estancia hospitalaria secundariamente a las complicaciones de la EVP. La mortalidad intrahospitalaria fue del 41,7% de los casos de EVP precoz y el 26,6% de los casos de EVP tardía; no se registraron diferencias estadísticamente significativas entre los periodos 1986-1995 y 1996-2005. Son escasos los estudios acerca de la mortalidad de los pacientes con EVP. Además, parte de estos trabajos analizan conjuntamente la mortalidad de endocarditis sobre válvula nativa y por EVP o revisan específicamente la mortalidad relacionada en episodios de EVP por ciertos microorganismos, especialmente S. aureus48. Nuestras cifras son similares a las de otros estudios publicados, lo que refleja la gravedad de esta enfermedad y la posible influencia del cambio de las características epidemiológicas y microbiológicas de los pacientes. Es especialmente grave la mortalidad de la EVP precoz51,52, con cifras entre el 40 y el 75%, que se relaciona con microorganismos invasivos que causan abscesos y destrucciones del anillo valvular y, en consecuencia, un mayor número de complicaciones cardiacas53.
El presente trabajo tiene ciertas limitaciones que se debe mencionar: en primer lugar la realización del estudio fue retrospectiva y en un único centro hospitalario, lo que limita en cierto sentido la validez de los resultados, aunque debe señalarse que los casos de EVP se habían ido registrando de forma prospectiva en los registros informatizados de los servicios de Cirugía Cardiovascular y Enfermedades Infecciosas. Además, la incidencia de EVP no se calculó en un sentido estricto, ya que, si bien en el numerador sí se han incluido todos los casos nuevos de EVP que se diagnosticaron durante el periodo de estudio, no hubo un seguimiento de los 6.079 pacientes intervenidos, y podría darse que alguno de ellos contrajera EVP y no lo remitieran de nuevo a nuestro centro, aunque ésta no era la práctica clínica habitual. Por el contrario, se trata de un estudio realizado únicamente sobre casos con diagnóstico definitivo de EVP y aporta las ventajas de analizar de forma longitudinal la evolución de esta enfermedad durante un lapso importante y se reflejan los cambios en sus características.
CONCLUSIONES
Este trabajo, realizado durante 20 años de asistencia a pacientes con EVP, refleja un envejecimiento progresivo de la población con EVP, un cambio en la valvulopatía de base y un descenso progresivo de la etiología estreptocócica, pero no ha observado una reducción de la mortalidad.
ABREVIATURAS
EVP: endocarditis sobre válvula protésica.
IC: intervalo de confianza.
RR: riesgo relativo.
Full English text available from: www.revespcardiol.org
Correspondencia: Dr. M.C. Fariñas.
Unidad de Enfermedades Infecciosas. Servicio de Medicina Interna. Hospital Universitario Marqués de Valdecilla.
Avda. Valdecilla, s/n. 39008 Santander. Cantabria. España.
Correo electrónico: farinasc@unican.es; mirfac@humv.es
Recibido el 20 de marzo de 2009.
Aceptado para su publicación el 7 de octubre de 2009.