En pacientes con insuficiencia cardiaca y fracción de eyección reducida (IC-FEr), se ha demostrado en ensayos clínicos que diferentes terapias reducen la mortalidad, pero hay pocos datos de la práctica real acerca del efecto en los distintos tipos de muerte.
MétodosSe estudió a 2.351 pacientes ambulatorios con IC-FEr (FE <40%) procedentes de los registros prospectivos multicéntricos MUSIC (n=641, años 2003-2004) y REDINSCOR I (n=1.710, años 2007-2011). Las variables se registraron a la inclusión, y el seguimiento fue de 4 años. Un comité independiente adjudicó la mortalidad y sus causas.
ResultadosLos pacientes en el registro más contemporáneo recibieron con mayor frecuencia bloqueadores beta (el 85 frente al 71%; p <0,001), antialdosterónicos (el 64 frente al 44%; p <0,001), desfibrilador automático implantable (el 19 frente al 2%; p <0,001) y resincronización (el 7,2 frente al 4,8%; p=0,04). La población más contemporánea presentó menos muerte súbita (el 6,8 frente al 11,4%; p <0,001). Tras emparejar por puntuación de propensión, se obtuvieron 2 poblaciones comparables que solo diferían en los tratamientos (575 frente a 575 pacientes): la población más contemporánea presentó menor riesgo de muerte total (HR=0,70; IC95%, 0,57-0,87; p=0,001) y de muerte súbita (sHR=0,46; IC95%, 0,30-0,70; p <0,001), con una tendencia de muerte por IC (sHR=0,73; IC95%, 0,53-1,01; p=0,059) y sin diferencias por otras causas (sHR=1,17; IC95%, 0,78-1,75; p=0,445), independientemente de la clase funcional.
ConclusionesEn pacientes ambulatorios con IC-FEr, la mejora terapéutica se asoció con un menor riesgo de muerte, principalmente debido a la significativa reducción de las muertes súbitas.
Palabras clave
La actual atención terapéutica de los pacientes con insuficiencia cardiaca (IC) se basa en la fracción de eyección del ventrículo izquierdo (FEVI). En pacientes con FEVI reducida (< 40%), se encuentra bien establecido el beneficio en mortalidad del bloqueo neurohormonal mediante fármacos y el uso de dispositivos1,2. Además, se ha demostrado específicamente que los bloqueadores beta y los desfibriladores automáticos implantables (DAI) disminuyen las muertes súbitas, mientras que los inhibidores de la enzima de conversión de la angiotensina (IECA) (o los antagonistas del receptor de la angiotensina II), los antialdosterónicos y la terapia de resincronización reducen fundamentalmente la mortalidad por IC3–7. Recientemente se ha demostrado que la inhibición de la neprilisina y del receptor de la angiotensina disminuyen la mortalidad total, incluida la cardiovascular, las muertes por IC o las muertes súbitas8.
A pesar de que el uso de estas terapias se encuentra bien establecido en las guías de actuación clínica, su incorporación a la práctica médica ha sido lenta. Así, diversos registros europeos y nacionales han mostrado que su prescripción en la práctica clínica no es la adecuada9–11. Esta infrautilización de terapias con beneficio establecido es atribuible, al menos en parte, a que los pacientes de la práctica real son distintos de los de los ensayos clínicos y esto supone una barrera para incorporar a la práctica clínica el beneficio observado en los ensayos aleatorizados. En nuestro medio, los registros multicéntricos MUSIC y REDINSCOR I incluyeron a pacientes ambulatorios y la mortalidad se estudió y se clasificó de manera exhaustiva según su causa12–14. Recientemente, un análisis temporal de diferentes ensayos clínicos ha mostrado que la incidencia de muerte súbita en los grupos de control ha disminuido en los ensayos más contemporáneos, lo que se atribuye a la mejora terapéutica15. Sin embargo, se carece de datos de la práctica clínica sobre el efecto de la incorporación de tratamientos con beneficio pronóstico en los diferentes modos de muerte.
El objetivo de este estudio es evaluar el efecto en la mortalidad y los diferentes tipos de muerte de la incorporación de tratamientos con evidencia en poblaciones de la práctica clínica real.
MÉTODOSPoblación y diseño del estudioSe incluyó a 2.351 pacientes con FEVI <40% incluidos en 2 cohortes prospectivas procedentes de 2 registros longitudinales y multicéntricos de pacientes ambulatorios con IC crónica: el registro MUSIC se diseñó para evaluar los predictores de riesgo de mortalidad cardiaca y muerte súbita cardiaca. Este registro incluyó a 992 pacientes ambulatorios, que acudieron consecutivamente a consultas especializadas de IC de 8 hospitales universitarios españoles entre abril de 2003 y diciembre de 200412. Todos estos pacientes tenían IC crónica sintomática (clase funcional de la New York Heart Association [NYHA] II-IV) y se los trató según las recomendaciones contemporáneas; el registro REDINSCOR I se diseñó para evaluar los predictores de mortalidad y hospitalizaciones cardiacas. Se seleccionó en total a 2.507 pacientes ambulatorios consecutivos entre enero de 2007 y enero de 2011 en las unidades de IC de 18 hospitales, de los que 6 habían participado en el anterior registro13. Para el presente estudio se seleccionó solo a los pacientes con FEVI <40% (641 pacientes en el registro MUSIC y 1.710 pacientes en REDINSCOR I) determinada por ecocardiografía en el momento de la inclusión. Todos los pacientes estaban sintomáticos (NYHA II-IV), eran ambulatorios y recibían tratamientos optimizados a criterio del médico responsable acordes con las pautas clínicas contemporáneas. De ambos registros se excluyó a los pacientes que tuvieran alguna enfermedad valvular grave susceptible de reparación quirúrgica o cualquier otra enfermedad terminal concomitante. Ambas cohortes cumplieron con la Declaración de Helsinki, los protocolos se aprobaron por los comités de ética de cada centro participante y todos los pacientes dieron su consentimiento informado por escrito.
Variables de estudioLos datos se recogieron prospectivamente utilizando una base de datos online diseñada específicamente para ambos registros, y se realizaron controles de calidad mensualmente13,14. Para el objetivo de este estudio, las variables usadas fueron las recogidas en ambos registros con definiciones idénticas. El conjunto de variables basales se registró en el momento de la inclusión del paciente y se incluyeron los datos demográficos, los antecedentes clínicos, los síntomas y el examen físico, electrocardiograma, ecocardiografía, análisis de sangre de laboratorio y los tratamientos a la inclusión (tabla 1). Para definir cada variable, se usaron criterios estándar idénticos en cada registro12,13. Se consideraron tratamientos basados en la evidencia los inhibidores de la enzima de conversión de la angiotensina (o los antagonistas del receptor de la angiotensina II), los bloqueadores beta, los antialdosterónicos, los DAI y la terapia de resincronización.
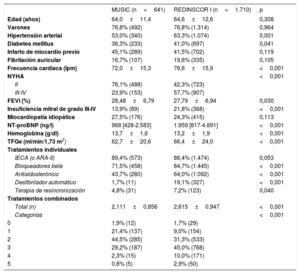
Características clínicas basales de las dos cohortes poblacionales comparadas
| MUSIC (n=641) | REDINSCOR I (n=1.710) | p | |
|---|---|---|---|
| Edad (años) | 64,0±11,4 | 64,6±12,6 | 0,308 |
| Varones | 76,8% (492) | 76,8% (1.314) | 0,964 |
| Hipertensión arterial | 53,0% (340) | 63,3% (1.074) | 0,001 |
| Diabetes mellitus | 36,3% (233) | 41,0% (697) | 0,041 |
| Infarto de miocardio previo | 45,1% (289) | 41,5% (702) | 0,119 |
| Fibrilación auricular | 16,7% (107) | 19,6% (335) | 0,105 |
| Frecuencia cardiaca (lpm) | 72,0±15,3 | 76,6±15,9 | <0,001 |
| NYHA | <0,001 | ||
| II | 76,1% (488) | 42,3% (723) | |
| III-IV | 23,9% (153) | 57,7% (907) | |
| FEVI (%) | 28,48±6,79 | 27,79±6,94 | 0,030 |
| Insuficiencia mitral de grado III-IV | 13,9% (89) | 21,8% (368) | <0,001 |
| Miocardiopatía idiopática | 27,5% (176) | 24,3% (415) | 0,113 |
| NT-proBNP (ng/l) | 968 [428-2.583] | 1.959 [817-4.891] | <0,001 |
| Hemoglobina (g/dl) | 13,7±1,6 | 13,2±1,9 | <0,001 |
| TFGe (ml/min/1,73 m2) | 62,7±20,6 | 66,4±24,0 | <0,001 |
| Tratamientos individuales | |||
| IECA (o ARA-II) | 89,4% (573) | 86,4% (1.474) | 0,053 |
| Bloqueadores beta | 71,5% (458) | 84,7% (1.445) | <0,001 |
| Antialdosterónico | 43,7% (280) | 64,0% (1.092) | <0,001 |
| Desfibrilador automático | 1,7% (11) | 19,1% (327) | <0,001 |
| Terapia de resincronización | 4,8% (31) | 7,2% (123) | 0,040 |
| Tratamientos combinados | |||
| Total (n) | 2,111±0,856 | 2,615±0,947 | <0,001 |
| Categorías | <0,001 | ||
| 0 | 1,9% (12) | 1,7% (29) | |
| 1 | 21,4% (137) | 9,0% (154) | |
| 2 | 44,5% (285) | 31,3% (533) | |
| 3 | 29,2% (187) | 45,0% (768) | |
| 4 | 2,3% (15) | 10,0% (171) | |
| 5 | 0,8% (5) | 2,9% (50) |
ARA-II: antagonistas del receptor de la angiotensina II; FEVI: fracción de eyección del ventrículo izquierdo; IECA: inhibidores de la enzima de conversión de la angiotensina; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; NYHA: New York Heart Association; TFGe: tasa de filtrado glomerular estimada.
Los valores expresan % (n), media±desviación estándar o mediana [intervalo intercuartílico].
Las visitas de seguimiento fueron ambulatorias cada 6-12 meses durante una mediana de 43 (29-46) meses en el registro MUSIC y durante una mediana de 40 (18-56) meses en el registro REDINSCOR I. Después de fusionar ambos registros, el horizonte de seguimiento común se truncó hasta los 48 meses (4 años). Durante el seguimiento se perdió a 6 pacientes en el registro MUSIC y 11 en el REDINSCOR I, y todos fueron censurados en el análisis de supervivencia. La información sobre los pacientes fallecidos se obtuvo de los registros médicos y administrativos. En cada caso se determinó de manera específica la naturaleza de la muerte, para lo cual la mortalidad total se dividió en no cardiovascular y cardiovascular, y esta última se clasificó como muerte por IC terminal (incluye IC refractaria o necesidad de trasplante cardiaco), muerte súbita cardiaca u otra muerte cardiovascular, utilizando definiciones previamente establecidas12–14. En todos los casos, los investigadores del estudio proporcionaron detalles sobre el evento de muerte y los datos se revisaron por un comité de adjudicación independiente para validar la causa de la muerte.
Análisis estadísticoLas variables cuantitativas se expresan como media±desviación estándar o mediana [intervalo intercuartílico] según corresponda, y las variables categóricas, como porcentaje (número). Se usaron la prueba de la χ2 o la exacta de Fisher para comparar variables cualitativas y ANOVA (análisis de la varianza), prueba de la t de Student o test de Wilcoxon para comparar variables cuantitativas. Debido a la naturaleza no aleatorizada del estudio, se realizó un análisis de emparejamiento por puntuación de propensión (paquete estadístico «MatchIt» del proyecto «R»), cuyo objetivo es hacer comparables poblaciones de series temporales o fuentes distintas y minimizar los posibles sesgos debidos a las diferencias en las características clínicas que podrían influir en el pronóstico16. Las características del modelo de emparejamiento por puntuación de propensión fueron: a) un protocolo 1:1 sin reemplazo; b) ancho del caliper ≤ 0,2 desviaciones estándares del logit de la puntuación de propensión; y c) método de coincidencia basado en el «emparejamiento del vecino más cercano». Para evaluar el equilibrio entre los grupos, se utilizó la «diferencia de medias estandarizada», que compara variables continuas y binarias. Este método no está influido por el tamaño de la muestra y permite la comparación entre variables de diferentes unidades17. En nuestro caso, se esperaban diferencias estandarizadas <0,2. Se utilizaron todas las variables excepto las de tratamientos, por ser objetivo del estudio: edad, sexo, hipertensión arterial, diabetes, infarto de miocardio previo, fibrilación auricular, frecuencia cardiaca, NYHA, FEVI, insuficiencia mitral de grado III-IV, etiología isquémica, fracción aminoterminal del propéptido natriurético cerebral (NT-proBNP), hemoglobina y tasa de filtrado glomerular. Mediante este análisis, 2 grupos de 575 pacientes se emparejaron para la pertenencia del registro MUSIC o REDINSCOR I, lo que mostró un adecuado grado de superposición, como se muestra en la figura 1 del material adicional. El análisis de supervivencia se realizó en toda la población con FEVI <40% y en los grupos emparejados derivados del emparejamiento por puntuación de propensión. El modelo de regresión de riesgos competitivos de Fine-Gray se utilizó para determinar el efecto de la variable explicativa (pertenencia a uno de los registros: MUSIC o REDINSCOR I) en el riesgo de cada causa específica de muerte. La calibración y discriminación del modelo fueron las adecuadas (figura 2 del material adicional). La prueba de residuos de Schoenfeld se usó para evaluar el supuesto de sub-hazard ratio (sHR) proporcional. Los datos faltantes se imputaron utilizando el paquete «mice» de imputación multivariada por ecuaciones encadenadas en el proyecto «R». Se realizó una imputación simple (m=1), debido a que el porcentaje de datos faltantes era <5% para todas las variables de análisis, excepto para el NT-proBNP, que se categorizó en 3 grupos según los terciles (< 750, 750-2.414 o ≥ 2.415 ng/l) y como «datos no disponibles» (28,9%), ya que no medir este parámetro también puede estar relacionado con el evento. El conjunto imputado fue toda la población disponible (n=2.351). Los análisis estadísticos se realizaron con los programas estadísticos SPSS v.25 y R v.3.2. Un valor de p <0,05 se usó para definir la significación estadística.
RESULTADOSPoblación de estudio y mortalidadEn este análisis se incluyó a 2.351 pacientes con FEVI <40% procedentes de los registros MUSIC (n=641, años 2003-2004) y REDINSCOR I (n=1.710, años 2007-2011). En la tabla 1 se muestran las diferencias entre ambos registros. En particular, los pacientes procedentes del REDINSCOR I presentaban un perfil de mayor riesgo, con mayor porcentaje de diabetes, peor clase funcional NYHA, mayor frecuencia cardiaca, menor FEVI, mayor prevalencia de insuficiencia mitral, mayor concentración de NT-proBNP y menor de hemoglobina. Solo la tasa de filtrado glomerular estimada fue inferior en la población procedente del MUSIC. No hubo diferencias en edad o sexo ni en prevalencia de infarto previo o fibrilación auricular. En cuanto al tratamiento, los pacientes procedentes del REDINSCOR I presentaron un tratamiento más optimizado, con diferencias importantes en la tasa de bloqueadores beta, antialdosterónicos y DAI y un mayor número de tratamientos combinados con evidencia.
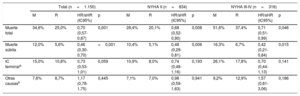
En la tabla 2 se muestra la mortalidad de cada cohorte y sus causas a los 48 meses. La mortalidad total fue similar en ambas poblaciones (el 33,0 frente al 32,3%); sin embargo, la distribución de las causas fue diferente y se observó un efecto debido a la mayor prevalencia de NYHA III-IV avanzada en la población procedente del REDINSCOR I (el 58 frente al 24%). La muerte súbita fue menos frecuente en la población más contemporánea (el 6,8 frente al 11,4%; p <0,001), y tanto en NYHA II (el 5,8 frente al 9,8%; p=0,009) como en NYHA III-IV (el 7,6 frente al 16,3%; p <0,001). La mayor presencia de clases avanzadas en la población más contemporánea del REDINSCOR I determinó una mayor frecuencia de mortalidad por IC terminal en esta población (el 16,4 frente al 13,7%; p=0,031); sin embargo, esta diferencia desapareció tras considerar por separado NYHA II (el 9,8 frente al 9,5%; p=0,866) y NYHA III-IV (el 23,2 frente al 26,1%; p=0,425) en ambas poblaciones. El mismo efecto se observó con otras causas cardiovasculares, que supusieron menos del 2% en cada población. La mortalidad por causas no cardiovasculares fue similar entre ambas poblaciones. En consecuencia, la contribución relativa de la muerte súbita al total de mortalidad fue diferente en cada población: de los pacientes en NYHA II, la muerte súbita supuso el 25,8% en el REDINSCOR I frente al 50,0% en el MUSIC, y de los pacientes en NYHA III-IV supuso el 18,5% de mortalidad en el REDINSCOR I frente al 31,5% en el MUSIC (p <0,001).
Mortalidad a los 48 meses por causas, clase funcional y cohorte poblacional
| Total (n=2.351) | Todos | NYHA II | NYHA III-IV | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Total(n=2.351) | MUSIC(n=641) | REDINSCOR I(n=1.710) | p | MUSIC(n=488) | REDINSCOR I(n=723) | p | MUSIC(n=153) | REDINSCOR I(n=987) | p | |
| Muerte total | 33,0% (776) | 32,3% (207) | 33,3% (569) | 0,652 | 26,2% (128) | 22,5% (163) | 0,141 | 51,6% (79) | 41,1% (406) | 0,015 |
| Muerte súbita | 8,1% (190) | 11,4% (73) | 6,8% (117) | <0,001 | 9,8% (48) | 5,8% (42) | 0,009 | 16,3% (25) | 7,6% (75) | <0,001 |
| Muerte por IC | 16,4% (386) | 13,7% (88) | 17,4% (298) | 0,031 | 9,8% (48) | 9,5% (69) | 0,866 | 26,1% (40) | 23,2% (229) | 0,425 |
| IC refractaria | 12,1% (284) | 10,8% (69) | 12,6% (215) | 0,231 | 7,6% (37) | 7,5% (54) | 0,942 | 20,9% (32) | 16,3% (161) | 0,158 |
| Trasplante | 4,3% (102) | 3,0% (19) | 4,9% (83) | 0,045 | 2,3% (11) | 2,1% (15) | 0,833 | 5,2% (8) | 6,9% (68) | 0,443 |
| Otras cardiacas | 1,9% (45) | 0,9% (6) | 2,3% (39) | 0,034 | 1,0% (5) | 1,8% (13) | 0,275 | 0,7% (1) | 2,6% (26) | 0,134 |
| Extracardiacas | 6,6% (155) | 6,2% (40) | 6,7% (115) | 0,673 | 5,5% (27) | 5,4% (39) | 0,917 | 8,5% (13) | 7,7% (76) | 0,733 |
IC: insuficiencia cardiaca; NYHA: New York Heart Association.
Los valores expresan % (n).
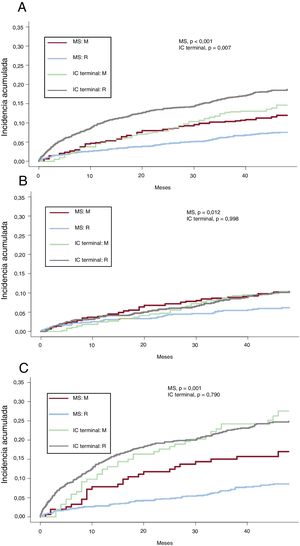
La figura 1 muestra la incidencia acumulada en el análisis de riesgos competitivos de muerte súbita y por IC refractaria, separada por clase funcional. La incidencia acumulada de muerte súbita fue menor en la población más contemporánea del REDINSCOR I, lo que supuso una reducción significativa del riesgo relativo en las poblaciones totales (sHR=0,61; intervalo de confianza del 95% [IC95%], 0,46-0,82; p <0,001), así como en pacientes en NYHA II (sHR=0,59; IC95%, 0,39-0,90; p=0,013) y NYHA III-IV (sHR=0,47; IC95%, 0,30-0,74; p=0,001). Por el contrario, la mortalidad por IC terminal fue similar en el total de población (p=0,081), en NYHA II (p=0,964) o en NYHA III-IV (p=0,374).
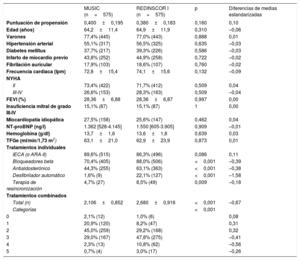
Emparejamiento por puntuación de propensiónSe realizó un emparejamiento por puntuación de propensión de riesgo, lo que permitió obtener 2 poblaciones comparables en factores de riesgo y clase funcional (575 pacientes del MUSIC frente a 575 pacientes del REDINSCOR I), que solo se diferenciaron por los tratamientos recibidos (tabla 3). La población más contemporánea recibió un tratamiento más optimizado basado en la evidencia, tanto terapias individuales como combinadas (p <0,001). Tras dicho emparejamiento, como muestra la figura 2, la población total contemporánea con tratamiento más optimizado presentó una menor incidencia acumulada de muerte (el 27,4 frente al 36,5%; p=0,001), y tanto en NYHA II (21,8 frente a 29,9%; p=0,008) como en NYHA III-IV (el 42,4 frente al 53,9%; p=0,047), principalmente por la significativa reducción de la muerte súbita. La distribución de causas de muerte por categorías se muestra en la tabla 1 del material adicional. En la tabla 4 se muestra la reducción del riesgo relativo de las diferentes causas de muerte y según clases funcionales. La menor mortalidad en la población contemporánea se debió a un menor riesgo de muerte súbita (sHR=0,46; IC95%, 0,30-0,70; p <0,001), mientras que la muerte por IC terminal presentó una tendencia (sHR=0,73; IC95%, 0,53-1,01; p=0,059) y no hubo diferencias en la muerte por otras causas (sHR=1,17; IC95%, 0,78-1,75; p=0,445). El impacto de la reducción de las muertes súbitas fue mayor entre los pacientes en NYHA II, por la mayor contribución relativa de la muerte súbita al total de fallecimientos de estos pacientes: supuso el 36,7% de mortalidad en NYHA II en el MUSIC frente al 25,3% en el REDINSCOR I; mientras que en NYHA III-IV supuso el 31,6% en el MUSIC y el 18,0% en el REDINSCOR I. Para confirmar el impacto de los diferentes tratamientos, se excluyó de forma secuencial a la población con terapia de resincronización cardiaca y DAI. Tras la exclusión de los dispositivos, persistía la reducción de la mortalidad total y la muerte súbita asociada con la mejora del tratamiento farmacológico en la población más contemporánea (tabla 2 del material adicional y tabla 3 del material adicional). En el análisis de predictores de muerte súbita basado en riesgos competitivos, la presencia de infarto previo, menos de 2 tratamientos basados en la evidencia, valores aumentados de NT-proBNP y una menor tasa de filtrado glomerular estimada fueron predictores independientes en la población total (índice C=0,640) (tabla 4 del material adicional). De ningún tratamiento se demostró que fuera predictor independiente por sí solo, y tampoco se encontraron interacciones entre tratamientos. La presencia de 2 o más tratamientos es la variable terapéutica con mejor sensibilidad y significación en el análisis realizado a posteriori (tabla 5 del material adicional). En un análisis de los tratamientos individuales en la población emparejada, mediante interacciones con «MUSIC frente a REDINSCOR I», no se observaron relaciones estadísticamente significativas (omnibus test, p=0,320).
Características clínicas basales comparadas de la población del MUSIC y el REDINSCOR I en las poblaciones emparejadas por puntuación de riesgo
| MUSIC (n=575) | REDINSCOR I (n=575) | p | Diferencias de medias estandarizadas | |
|---|---|---|---|---|
| Puntuación de propensión | 0,400±0,195 | 0,380±0,183 | 0,160 | 0,10 |
| Edad (años) | 64,2±11,4 | 64,9±11,9 | 0,310 | –0,06 |
| Varones | 77,4% (445) | 77,0% (443) | 0,888 | 0,01 |
| Hipertensión arterial | 55,1% (317) | 56,5% (325) | 0,635 | –0,03 |
| Diabetes mellitus | 37,7% (217) | 39,3% (226) | 0,586 | –0,03 |
| Infarto de miocardio previo | 43,8% (252) | 44,9% (258) | 0,722 | –0,02 |
| Fibrilación auricular | 17,9% (103) | 18,6% (107) | 0,760 | –0,02 |
| Frecuencia cardiaca (lpm) | 72,8±15,4 | 74,1±15,6 | 0,132 | –0,09 |
| NYHA | ||||
| II | 73,4% (422) | 71,7% (412) | 0,509 | 0,04 |
| III-IV | 26,6% (153) | 28,3% (163) | 0,509 | –0,04 |
| FEVI (%) | 28,36±6,88 | 28,36±6,87 | 0,997 | 0,00 |
| Insuficiencia mitral de grado III-IV | 15,1% (87) | 15,1% (87) | 1 | 0,00 |
| Miocardiopatía idiopática | 27,5% (158) | 25,6% (147) | 0,462 | 0,04 |
| NT-proBNP (ng/l) | 1.362 [528-4.145] | 1.550 [605-3.905] | 0,909 | –0,01 |
| Hemoglobina (g/dl) | 13,7±1,6 | 13,6±1,8 | 0,639 | 0,03 |
| TFGe (ml/min/1,73 m2) | 63,1±21,0 | 62,9±23,9 | 0,873 | 0,01 |
| Tratamientos individuales | ||||
| IECA (o ARA-II) | 89,6% (515) | 86,3% (496) | 0,086 | 0,11 |
| Bloqueadores beta | 70,4% (405) | 88,0% (506) | <0,001 | –0,39 |
| Antialdosterónico | 44,3% (255) | 63,1% (363) | <0,001 | –0,38 |
| Desfibrilador automático | 1,6% (9) | 22,1% (127) | <0,001 | –1,58 |
| Terapia de resincronización | 4,7% (27) | 8,5% (49) | 0,009 | –0,18 |
| Tratamientos combinados | ||||
| Total (n) | 2,106±0,852 | 2,680±0,916 | <0,001 | –0,67 |
| Categorías | <0,001 | |||
| 0 | 2,1% (12) | 1,0% (6) | 0,08 | |
| 1 | 20,9% (120) | 8,2% (47) | 0,31 | |
| 2 | 45,0% (259) | 29,2% (168) | 0,32 | |
| 3 | 29,0% (167) | 47,8% (275) | –0,41 | |
| 4 | 2,3% (13) | 10,8% (62) | –0,56 | |
| 5 | 0,7% (4) | 3,0% (17) | –0,26 | |
ARA-II: antagonistas del receptor de la angiotensina II; FEVI: fracción de eyección del ventrículo izquierdo; IECA: inhibidores de la enzima de conversión de la angiotensina; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; NYHA: New York Heart Association; TFGe: tasa de filtrado glomerular estimada.
Los valores expresan % (n), media±desviación estándar o mediana [intervalo intercuartílico].
Poblaciones emparejadas en el análisis de propensión. Función de incidencia acumulada de mortalidad y sus tipos en las poblaciones de los registros MUSIC (M) y REDINSCOR I (R), considerando la población total y según clase funcional de la NYHA. A: mortalidad total en población total; B: mortalidad total en NYHA II; C: mortalidad total en NYHA III-IV; D: tipos de muerte en población total; E: tipos de muerte en NYHA II; F: tipos de muerte en NYHA III-IV. IC: insuficiencia cardiaca; MS: muerte súbita; NYHA: New York Heart Association.
Análisis de regresión y riesgos competitivos de muerte a 48 meses en poblaciones emparejadas por análisis de propensión: REDINSCOR I frente a MUSIC
| Total (n=1.150) | NYHA II (n=834) | NYHA III-IV (n=316) | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| M | R | HR/sHR (IC95%) | p | M | R | HR/sHR (IC95%) | p | M | R | HR/sHR (IC95%) | p | |
| Muerte total | 34,6% | 25,0% | 0,70 (0,57-0,87) | 0,001 | 28,4% | 20,1% | 0,68 (0,52-0,90) | 0,008 | 51,6% | 37,4% | 0,71 (0,51-0,99) | 0,046 |
| Muerte súbita | 12,0% | 5,6% | 0,46 (0,30-0,70) | <0,001 | 10,4% | 5,1% | 0,48 (0,29-0,81) | 0,006 | 16,3% | 6,7% | 0,42 (0,21-0,84) | 0,015 |
| IC terminala | 15,0% | 10,8% | 0,73 (0,53-1,01) | 0,059 | 10,9% | 8,0% | 0,74 (0,48-1,16) | 0,193 | 26,1% | 17,8% | 0,70 (0,44-1,13) | 0,141 |
| Otras causasb | 7,6% | 8,7% | 1,17 (0,78-1,75) | 0,445 | 7,1% | 7,0% | 0,98 (0,59-1,63) | 0,941 | 9,2% | 12,9% | 1,57 (0,81-3,06) | 0,186 |
HR: hazard ratio; IC: insuficiencia cardiaca; IC95%: intervalo de confianza del 95%; M: MUSIC; NYHA: New York Heart Association; R: REDINSCOR I; sHR: sub-hazard ratio.
El presente estudio, basado en registros de la práctica clínica con cohortes bien caracterizadas, muestra que la incorporación de un tratamiento basado en terapias con beneficio demostrado y recomendadas en las guías de práctica clínica conlleva una reducción de la mortalidad y en particular del riesgo de muerte súbita, de manera independiente de la clase funcional.
Mejora de la mortalidad según causasEl análisis incluyó a 2.351 pacientes ambulatorios y con FEVI <40%, y ambas poblaciones tuvieron un seguimiento de 4 años. Sin embargo, las 2 poblaciones no eran comparables en características de riesgo ni en tratamientos recibidos, de modo que la más contemporánea tenía a pacientes en clases funcionales más avanzadas y con un perfil clínico de mayor riesgo, pero que a la vez recibían un mejor tratamiento médico tanto farmacológico como de dispositivos. Estos hallazgos podrían indicar un empeoramiento del perfil del paciente atendido en las unidades participantes, a la vez que la incorporación progresiva de los tratamientos basados en la evidencia. Si bien considerando las poblaciones totales la mortalidad fue similar en ambas cohortes, tras considerar las clases funcionales, la mortalidad y en particular la muerte súbita, fue significativamente menor en la población más contemporánea a pesar del perfil de mayor riesgo de sus pacientes. En este contexto, el ajuste de propensión permitió obtener 2 poblaciones comparables en variables de riesgo, pero que mantenían sus diferencias en tratamientos basados en la evidencia. Este análisis confirmó un menor riesgo de muerte en la población más contemporánea, principalmente debido a la reducción aproximada del 50% en el riesgo de muerte súbita. Esta reducción fue significativa tanto en NYHA II como en las clases avanzadas III-IV. La magnitud de la reducción fue similar en ambas clases funcionales, pero la repercusión fue mayor en NYHA II por la mayor contribución relativa de la muerte súbita al total de fallecimientos en estadios menos avanzados de la enfermedad. La mortalidad por IC terminal fue también inferior, con una clara tendencia, aunque sin alcanzar significación estadística tras el ajuste por riesgos competitivos, lo que muestra que, si bien hubo un impacto en la progresión de la IC, este fue menor o al menos no tan precoz como en la muerte súbita. Por último, como era de esperar, las demás formas de muerte fueron similares en ambas poblaciones a pesar de las diferencias de tratamiento.
Reducción de la muerte súbitaEl efecto del tratamiento en la mortalidad de pacientes con IC y fracción de eyección reducida se basa en los ensayos clínicos aleatorizados individuales de cada fármaco. Recientemente, Shen et al. compararon la incidencia acumulada de muerte súbita en los distintos ensayos clínicos pivotales, y observaron una reducción de su incidencia en los grupos de control a la vez que estos incorporaban los tratamientos basados en la evidencia previa con el paso de los años15. La disminución del riesgo de muerte súbita fue del 44% entre los distintos estudios, un porcentaje similar al observado en nuestro análisis. Sin embargo, nuestro estudio tiene el valor añadido de reflejar el impacto en la práctica clínica real, un aspecto poco estudiado hasta ahora. Thorvaldsen et al. estudiaron una cohorte de 5.908 pacientes con IC, FEVI <30% y NYHA II-IV durante el periodo 2003 a 2012, pero no encontraron relación entre tratamientos basados en la evidencia y una mejora de la supervivencia total18. Sin embargo, este análisis no consideró las distintas formas de muerte ni la interacción con las clases funcionales, lo que pudo afectar a los resultados observados. De hecho, en nuestro estudio la supervivencia total no muestra diferencias, que solo se hacen evidentes tras considerar causas de muerte y clases funcionales por separado, dado que la población más contemporánea incluye a pacientes con estadios más avanzados de la enfermedad. Por lo tanto, nuestros resultados expanden los hallazgos del análisis de Shen et al.15 a poblaciones de la práctica clínica, en las que la mejora del tratamiento conllevó una reducción del riesgo de muerte, en particular de muerte súbita, independientemente del estadio funcional.
Influencia del cambio en la forma de muerteEl mayor efecto en la muerte súbita que en la muerte por IC terminal hace que disminuya la contribución relativa de la primera al total de la mortalidad. Por tanto, también se produce un cambio en el modo de muerte, de manera que los pacientes aumentan su tiempo de supervivencia y terminan falleciendo por IC terminal. Este hecho puede tener repercusión en la indicación de DAI, en particular para pacientes con menor riesgo de muerte súbita, como aquellos sin infarto previo. Así, en un ensayo clínico reciente, la indicación de DAI basada solo en la FEVI no se asoció con una reducción de la mortalidad total de los pacientes sin infarto previo, que tenían tasas elevadas de tratamientos farmacológicos recomendados por las guías de práctica clínica19. El papel del tratamiento farmacológico se observa también en nuestro análisis, dado que la reducción de muerte súbita persistía tras eliminar a la población con dispositivos. Recientemente, la inhibición dual de la neprilisina y el receptor de la angiotensina ha mostrado reducciones aún mayores del riesgo de muerte y, en particular, muerte súbita en pacientes poco sintomáticos8. Este fármaco, actualmente incorporado a la práctica clínica, previsiblemente tendrá un impacto adicional en la mortalidad y el modo de muerte durante los próximos años.
Adherencia terapéutica en vida realEn nuestro análisis, tras el ajuste por puntuación de propensión, la única diferencia fueron los tratamientos recibidos. En particular, las tasas fueron superiores en los fármacos cuyos manejo e introducción son más difíciles, como los bloqueadores beta y los antialdosterónicos, y entre los dispositivos destacó la mayor tasa de implantes de DAI. Estas tasas en el registro más contemporáneo (2007-2010) fueron superiores a las del registro europeo de inicio de los 2000 (EuroHeart Failure Survey)9 y similares a las indicadas en otros registros europeos inmediatamente posteriores, como el ESC Heart Failure Long-Term (2011-2013)20,21 y el QUALIFY (2013-2014)22. Esta lenta incorporación de terapias con evidencia se ha descrito en numerosos registros, y sus causas son multifactoriales, como la falta de adherencia de los profesionales a las guías debida a la inercia asistencial, la falta de formación y las dificultades añadidas, como la mayor comorbilidad del paciente de la práctica clínica23. Más allá de los tratamientos individuales, la combinación de tratamientos con evidencia también fue superior en la población más contemporánea. Este hecho es relevante, tal y como muestra el análisis de predictores en el que solo tener 2 o más tratamientos basados en la evidencia se asoció con menor riesgo independiente de muerte súbita. Este hallazgo concuerda con los de estudios recientes que muestran que una mayor combinación de tratamientos, y al menos el 50% de las dosis recomendadas, se asocia con menos mortalidad y hospitalizaciones22,24.
LimitacionesEntre las limitaciones se encuentran precisamente la falta de datos sobre dosis utilizadas y la persistencia de los tratamientos, así como ser un estudio observacional de cohortes con diferencias entre poblaciones. El análisis de propensión se utilizó para obtener 2 grupos de pacientes con características clínicas similares y, por lo tanto, comparables aun encontrándose en periodos temporales distintos, solo diferenciados en las variables de tratamiento. Esto último pudo conllevar diferencias residuales en las muestras emparejadas, diferentes de la variable en estudio. Además, otras variables no medibles pudieron influir, entre ellas la adherencia del paciente, el tiempo desde el diagnóstico y las mejoras organizativas o en otros tratamientos como la revascularización coronaria. Por otro lado, la participación de diferentes centros en ambos registros pudo ocasionar un sesgo de selección derivado del perfil de pacientes que atiende cada centro. Los centros que componen los 2 periodos de estudio no son los mismos al completo; de los 18 centros, se repiten solo 6, y eso impidió tener en cuenta el efecto cluster de los centros para la estimación de la puntuación de propensión. La causa de muerte es en muchos casos de difícil adjudicación, aunque la existencia de un comité independiente predefinido y la adjudicación a ciegas minimizan esta limitación. A pesar de estas limitaciones, los análisis realizados respaldan los hallazgos obtenidos, que a su vez permiten expandir a la práctica clínica los resultados de poblaciones de ensayos aleatorizados16, considerando la variabilidad de la práctica real.
CONCLUSIONESEn pacientes con IC y fracción de eyección reducida, la mejora del tratamiento médico basado en la evidencia se asocia con una reducción de la mortalidad en registros de práctica clínica, principalmente debido a un riesgo de muerte súbita significativamente menor, independientemente de la clase funcional. Estos resultados confirman la necesidad de estrategias que faciliten la incorporación de los tratamientos basados en la evidencia a la práctica clínica.
FINANCIACIÓNEste trabajo se financió parcialmente por el Instituto de Salud Carlos III, Madrid, España (RD12/0042/0049) (PI14/01637; INT16/00172) y Fondos FEDER (CIBER Cardiovascular; CB16/11/00385).
CONFLICTO DE INTERESESNinguno relacionado con este trabajo.
- –
Para los pacientes con IC y FEVI reducida, se dispone de tratamientos recomendados con base en la reducción de la mortalidad demostrada en ensayos clínicos.
- –
Hay pocos datos sobre su traslación a la práctica clínica y el efecto en los distintos tipos de muerte.
- –
En la práctica clínica real, la incorporación de las terapias basadas en la evidencia para pacientes con IC y FEVI reducida se asocia con un menor riesgo de muerte.
- –
La mejora de la supervivencia se debió principalmente a la significativa reducción del riesgo de muerte súbita independientemente de la clase funcional.
- –
Por lo tanto, su beneficio conlleva tanto una mayor supervivencia como un cambio en el modo de muerte de los pacientes.