Palabras clave
INTRODUCCIÓN
La regurgitación mitral isquémica (RMI) es una enfermedad compleja con una historia natural de mal pronóstico. La restricción de la movilidad de los velos mitrales durante la fase telesistólica (disfunción IIIb de Carpentier, tabla 1), más acentuada en el velo posterior, se ha descrito como la causa principal de la insuficiencia mitral de origen isquémico1. Tras un daño miocárdico severo, el ventrículo izquierdo sufre un cambio en su morfología elíptica para adquirir una conformación esferoidal2. El aumento en el índice de esfericidad ventricular causa un desplazamiento apical y lateral de los músculos papilares (particularmente en el músculo papilar posteromedial), con lo que se crea un desequilibrio entre las fuerzas de tracción y coaptación en el aparato subvalvular mitral. El desplazamiento de los músculos papilares conlleva la angulación apical de los velos valvulares. Este fenómeno impide que los bordes libres de los velos alcancen el plano anular fisiológico (fig. 1), con lo que se produce la regurgitación mitral. La afección isquémica de los músculos papilares se suma a la creación de una tensión excesiva en las cuerdas tendinosas, e impide la correcta coaptación de los velos mitrales y empeora todavía más el grado de regurgitación mitral. En la RMI, el remodelado ventricular postisquémico es el principal factor inductor de la disfunción mitral; no obstante, la dilatación y la posterior deformación anular, consecuencia de la falta de coaptación valvular, se encuentran asociadas con frecuencia a la disfunción de tipo IIIb.
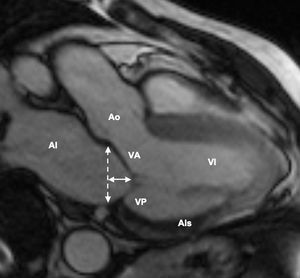
Fig. 1. Resonancia magnética cardiaca (eje largo vertical, vista bicameral, máxima presión sistólica). Se objetiva el área de isquemia (AIs) que involucra al músculo papilar posteromedial (cortesía del Dr. Javier Sanz). AI: aurícula izquierda; Ao: arteria aorta; línea continua: altura de la angulación; línea discontinua: plano fisiológico de coaptación y diámetro anular; VA: velo mitral anterior; VI: ventrículo izquierdo; VP: velo mitral posterior.
La ecocardiografía tridimensional ha refinado el análisis de los velos valvulares y permite un mayor grado de detección y cuantificación de la RMI. Kwan et al3 corroboraron algo previamente postulado por nuestro grupo y demostraron que la deformación de la válvula mitral seguía un patrón asimétrico a lo largo de su diámetro intercomisural. También ratificaron que en pacientes con RMI se comprueba una marcada angulación de ambos velos en su límite posteromedial (segmentos A3 y P3), mientras que no se objetiva una angulación tan pronunciada en los segmentos del límite anterolateral (segmentos A1 y P1). Además, en un modelo ovino de insuficiencia mitral isquémica crónica, Gorman et al4 evidenciaron que todos los segmentos del anillo mitral, incluso los segmentos anteriores, se encuentran dilatados asimétricamente, especialmente en la porción posteromedial del anillo.
Hasta la fecha, el tratamiento quirúrgico de elección para los pacientes que presentan RMI es la anuloplastia mitral, mediante gran variedad de técnicas quirúrgicas en combinación con la revascularización miocárdica5. Hallazgos recientes, algunos de ellos mencionados anteriormente, indican que la mayoría de las técnicas quirúrgicas utilizadas durante la última década pueden no ser el tratamiento óptimo para prevenir a largo plazo la aparición de regurgitación residual o la recurrencia de regurgitación mitral (RM), observada en un 10-15% de los pacientes durante el período de seguimiento clínico6-8.
Una mejor comprensión del mecanismo pfisiopatológico de la RMI de tipo IIIb condujo al desarrollo de un anillo específico para esta entidad clínica: el anillo de Carpentier-McCarthy-Adams IMR Etlogix® (CMA-E)9. Este nuevo anillo protésico no solamente tiene en consideración la dilatación general del anillo nativo, sino que también tiene por objetivo la corrección de la dilatación asimétrica y de la angulación de los segmentos P2 y P3. El incremento resultante de la superficie de coaptación de los velos significaría una funcionalidad más durable a largo plazo. En este estudio describimos nuestra experiencia clínica inicial con el nuevo anillo mitral protésico en pacientes con RMI de tipo IIIb.
MÉTODOS
Se estudió a 40 pacientes intervenidos consecutivamente por insuficiencia mitral isquémica de tipo IIIb mediante el nuevo anillo mitral protésico CMA-E (Edwards LifeSciences, Irving, California, Estados Unidos) entre diciembre de 2003 y junio de 2005. A los pacientes que ya se habían sometido a cirugía y/o requerían cirugía valvular tricuspídea adicional, se los incluyó igualmente en el grupo de estudio. Se utilizó un registro informático para identificar a todos los pacientes de manera retrospectiva. La historia clínica de cada paciente fue revisada para obtener información adicional. El estudio fue aprobado por el comité ético de investigación de nuestra institución (IRB) y el período de investigación se rigió por las recomendaciones internacionales de investigación clínica (HIPPA) establecidas en la declaración de Helsinki de la Asociación Médica Mundial (1975).
Todos los pacientes fueron sometidos preoperatoriamente a un estudio ecocardiográfico transtorácico, y se confirmó la restricción de movilidad de los velos valvulares durante la fase telesistólica en todos los casos (RMI de tipo IIIb, Clasificación Funcional de Carpentier). La severidad de la RM se valoró prospectivamente en todos los pacientes a partir del área del jet regurgitante (Doppler color) y el volumen regurgitante, cuantificados por Doppler semicuantitativo y ecocardiografía bidimensional. El grado de RM se cuantificó de 0 a 4+ (0, inexistente; 0,5+, ligero; 1+, leve; 2+, moderado; 3+, moderado a severo, y 4+, severo)10. Además, la geometría del aparato mitral se evaluó midiendo el diámetro anular, la altura de la angulación mitral (distancia entre el punto de coaptación de los velos mitrales y su plano fisiológico de coaptación) y el área de angulación mitral.
Anillo de Carpentier-McCarthy-Adams IMR Etlogix
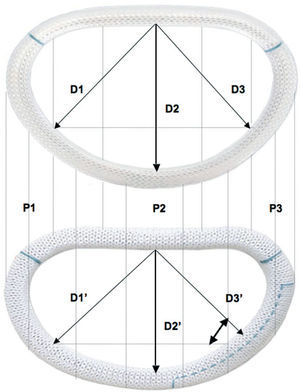
En la creación del nuevo anillo confluyeron dos conceptos básicos: la reducción del diámetro anular mediante un anillo sobrecorrector y la corrección de la deformación anular asimétrica del anillo mitral nativo para devolverle, por consiguiente, su característica forma en silla de montar. Este nuevo diseño da lugar a un incremento de la superficie de coaptación de los velos valvulares debido a la reducción de los ejes anteroposterior (D2 contra D2', invariable a lo largo de todo el ciclo cardiaco gracias a su estructura rígida de titanio) y septolateral (D3 contra D3'). Con ello se alcanza una reducción anular de 1 talla para el eje anteroposterior (D2') y de 2 tallas para el eje septolateral (D3') en comparación con el anillo Carpentier-Edwards Physio® (fig. 2). Este hecho hace posible una selección del tamaño del anillo protésico basada en las dimensiones del velo mitral anterior (calibrado mediante un medidor estándar Carpentier-Edwards), lo que permite una remodelación valvular con una línea de coaptación óptima en los segmentos P2 y P3.
Fig. 2. Comparación entre el anillo clásico Physio (superior) y el nuevo anillo CMA-E (inferior). Se objetivan las diferencias entre los ejes delineados en ambos anillos: eje septomedial (D1 y D1'), eje anteroposterior (D2 y D2') y eje septolateral (D3 y D3'). D2' equivale a una talla inferior a D2 y D3' equivale a 2 tallas inferiores a D3.
Análisis estadístico
Todos los valores se expresan como media ± desviación estándar (DE) o mediana y rango intercuartílico (RIC) para las variables cuantitativas. Se utilizó la prueba de la t de Student para datos emparejados y comparar las dimensiones ecocardiográficas antes y después del procedimiento quirúrgico. Las variables discretas se presentan como porcentajes y se las comparó mediante la prueba de la χ2. Se consideró significativos los valores de p < 0,05. Se empleó el paquete informático SPSS (versión 15.0, SPSS Inc., Chicago, Ilinois, Estados Unidos) para el análisis estadístico.
RESULTADOS
Las características clínicas de los pacientes están descritas en la tabla 2. La población de estudio incluyó a 30 pacientes varones (75%) y 10 mujeres (25%). La media de edad fue de 68 ± 10 años. La fracción de eyección (FE) media fue del 39% ± 14% (intervalo, 14%-64%). La distribución de pacientes respecto al grado de enfermedad coronaria fue la siguiente: 9 (22%) pacientes presentaban enfermedad coronaria de 1 vaso; 14 (35%), enfermedad coronaria de 2 vasos, y 17 (43%), enfermedad coronaria de 3 vasos.
La distribución de los pacientes en cuanto al grado ecocardiográfico preoperatorio de RM fue la siguiente: 28 (70%) pacientes presentaron RM de grado 4+ y 12 (30%), RM de grado 3+.
Procedimientos quirúrgicos
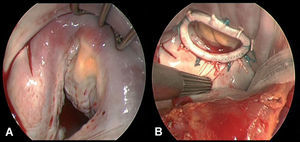
Se realizó revascularización miocárdica en 27 (68%) pacientes. La media de injertos coronarios fue de 2,7 ± 1,3. Antes de la reparación mitral se llevó a cabo la técnica modificada de Maze en 9 (22%) pacientes con historia de fibrilación auricular, y se consiguió la ablación tisular por criotermia (Cryocath Technology®, Pointe-Claire, Canadá)11. La exploración intraoperatoria confirmó los hallazgos ecocardiográficos previos en todos los casos. En la totalidad de los pacientes se implantó con éxito el anillo protésico CMA-E; para fijarlo se empleó suturas interrumpidas «de colchonero» (en 12-15 puntos) alrededor del anillo nativo. A nivel de P2, P3, y de la comisura posteromedial, se solaparon las suturas con el objetivo de liberar el exceso de tensión y evitar así el riesgo potencial de dehiscencia anular. El tamaño del anillo se decidió tras medir la distancia intercomisural y el área de superficie del velo anterior, empleando en ambos casos un medidor estándar Carpentier-Edwards. Tras su implantación y fijación al anillo nativo, se inspeccionó la válvula y se descartó cualquier posibilidad de fuga residual mediante la inyección de suero salino a presión en la cavidad ventricular, con lo que se confirmó que hubiera una superficie de coaptación idónea (é 8 mm). La línea de coaptación fue típicamente asimétrica debido a la gran angulación previa en los segmentos P2, P3 y en el área comisural posteromedial (fig. 3). La distribución de tamaños del anillo protésico y los procedimientos asociados a la cirugía de remodelación mitral se detallan en la tabla 3. Los tiempos medios de circulación extracorpórea y pinzamiento aórtico fueron de 162 ± 70 min y 115 ± 50 min, respectivamente.
Fig. 3. A: vista intraoperatoria previa a la anuloplastia mitral. B: vista intraoperatoria del anillo CMA-E implantado.
Morbimortalidad
La tasa de mortalidad durante la estancia hospitalaria o durante los 30 días siguientes al procedimiento quirúrgico fue del 2,5% (n = 1). La causa de la muerte fue un fallo multiorgánico secundario a un síndrome prolongado de bajo gasto cardiaco. Postoperatoriamente, se produjo 1 caso (2,5%) de accidente cerebrovascular, 1 (2,5%) de insuficiencia renal (creatinina > 2,5 mg/dl durante más de 7 días o necesidad de diálisis), 4 (10%) de insuficiencia respiratoria (necesidad de ventilación mecánica durante más de 72 h) y 1 (2%) de infección esternal. Requirieron la inserción de marcapasos permanente 3 (7%) pacientes. No se dieron casos de dehiscencia anular o endocarditis precoz. El tiempo de hospitalización (mediana) fue de 11 (RIC, 7-15) días. Los eventos posteriores a la cirugía se detallan en la tabla 4.
Resultados ecocardiográficos
Los hallazgos ecocardiográficos encontrados en el período de estudio se representan en la figura 4. El grado de insuficiencia mitral se redujo de forma significativa en todos los pacientes (3,8 ± 0,4 y 0,3 ± 0,3; p = 0,001). Los parámetros geométricos mitrales también se vieron significativamente reducidos tras la cirugía: diámetro anular (3,2 ± 0,8 cm y 2,3 ± 0,05 cm; p = 0,001), altura de la angulación (0,6 ± 0,2 cm y 0,4 ± 0,1 cm; p = 0,001), área de angulación (1,2 ± 0,4 cm y 0,6 ± 0,3 cm; p = 0,001) (fig. 5). No se observaron cambios significativos en cuanto a la FE media (39% ± 14% y 40% ± 11%; p = 0,631) y no se produjo ningún caso de movimiento sistólico anterior «SAM». En el momento del alta hospitalaria, 36 (90%) pacientes no presentaron RM residual postoperatoria y únicamente 3 (10%) presentaron RM residual de grado leve.
Fig. 4. Cambios ecocardiográficos en el grado de regurgitación mitral durante el período de estudio. RMI: regurgitación mitral isquémica.
Fig. 5. Comparación entre los valores preoperatorios y postoperatorios relativos a las variables geométricas mitrales (diámetro anular, altura de la angulación y área de la angulación) y la fracción de eyección
Seguimiento clínico y ecocardiográfico
Se obtuvo el seguimiento clínico y ecocardigráfico del 97% (38/39) de los pacientes que superaron la intervención quirúrgica y recibieron el alta hospitalaria; se produjeron 2 (8%) muertes tardías a los 7 y los 12 meses respectivamente. Por consiguiente, 36 (92%) pacientes tuvieron un seguimiento ecocardiográfico é 15 (intervalo, 15-34) meses. El estudio ecocardiográfico reveló la ausencia de RM en 22 (61%) pacientes, RM de grado leve en 13 (36%) y RM de grado moderado en 1 (3%); la tasa de RM recurrente fue del 3%.
DISCUSIÓN
En este estudio observacional describimos nuestra primera experiencia clínica con el nuevo anillo mitral protésico CMA-E, diseñado para el tratamiento quirúrgico de pacientes con RMI de tipo IIIb. El nuevo anillo corrige de manera efectiva la RMI de tipo IIIb y proporciona resultados clínicos iniciales prometedores. El seguimiento clínico y ecocardiográfico del 97% de los pacientes muestra la fiabilidad y durabilidad del nuevo anillo y ha rendido una tasa de RM recurrente del 3% (n = 1). Durante el período de estudio no se objetivaron complicaciones relacionadas con el anillo protésico como dehiscencia anular, endocarditis precoz o eventos tromboembólicos.
Un anillo específico para una disfunción específica
Son numerosos los estudios que se han llevado a cabo para lograr entender mejor los mecanismos fisiopatológicos causales de la RMI, y de esa manera potenciar el desarrollo de nuevas técnicas quirúrgicas y dispositivos dirigidos al tratamiento de esta compleja lesión valvular12-14. Las primeras publicaciones que abordaron este tema descubrieron múltiples técnicas de reparación valvular, como la anuloplastia de sutura (tipo De Vega mitral), la utilización de anillos pericárdicos o la implantación de anillos incompletos de flexibilidad variable, todas ellas de escasa durabilidad, que conllevan tanto RM residual como reaparición de ésta a corto plazo15-17. Hausmann et al16,18 publicaron una serie de 140 pacientes operados de RMI mediante anuloplastia de sutura con una incidencia de RM residual (é 2+) del 28%. En una publicación perteneciente al grupo de la Cleveland Clinic Foundation, Bhudia et al19 demostraron que la anuloplastia posterior con la implantación de un anillo incompleto flexible en combinación con una reparación borde a borde (edge-to-edge) tenía relación con una tasa de reincidencia de la RM del 30% a los 18 meses de seguimiento clínico.
En un estudio clinicoanatómico del corazón humano, Hueb et al20 aportaron datos interesantes sobre la geometría valvular mitral en pacientes con RMI, demostrando que tanto en aquellos pacientes con cardiomiopatía isquémica como en aquellos con miocardiopatía dilatada, la deformación anular abarcaba todos los segmentos del anillo, incluidos los segmentos anteriores. Estos hallazgos los constataron posteriormente Gorman et al21 en un modelo ovino de RMI crónica. En ese estudio se comprobó que la dilatación de los segmentos anteriores y posteriores del anillo mitral, junto con la dilatación ventricular asimétrica, era la causa de la angulación y por consiguiente de la regurgitación mitral. La experiencia de los diversos grupos de investigación señala que la anuloplastia mediante anillos incompletos flexibles podría no ser la técnica óptima de tratamiento para pacientes con RMI de tipo IIIb. Pensamos que estos anillos protésicos no remodelan de manera completa el anillo nativo y descuidan particularmente la zona de inserción del velo mitral anterior.
Se han sido descritos hallazgos similares con la anuloplastia mediante anillos flexibles completos en pacientes con RMI. Tahta et al22 analizaron los resultados a largo plazo en 100 pacientes sometidos a cirugía combinada (anuloplastia mitral y bypass coronario) mediante la implantación de un anillo flexible de Duran. Durante un seguimiento clínico medio de casi 36 meses, un 29% de los pacientes presentaron regurgitación mitral recidivante de grado moderado (2+). En nuestra opinión, los anillos flexibles no conseguirían estabilizar el anillo orgánico durante la fase sistólica; reducen la distancia intercomisural del anillo nativo, pero tienen escaso impacto sobre su diámetro anteroposterior, parámetro crítico en este tipo de pacientes. En cambio, la remodelación anular mediante el uso de un anillo rígido o semirrígido, concepto respaldado por el equipo de investigación de Craig Miller23, restablecería el tamaño y la conformación del anillo mitral, con lo que además aporta una significativa reducción del diámetro anteroposterior. De esta manera, en 2004 Bax et al24 describieron la eficacia de la anuloplastia remodeladora sobrecorrectora con anillo de Carpentier-Edwards Physio® (anillo rígido de Carpentier) para el tratamiento de la regurgitación mitral de tipo IIIb. En una serie compuesta por 51 pacientes con RM de grado 3+/4+, los autores publicaron la ausencia de RM tras un seguimiento clínico medio de 2 años.
La restricción de movilidad de los velos valvulares en la RMI de tipo IIIb ocasiona una disminución del tejido velar disponible para lograr una óptima coaptación, por lo que creemos que una reducción agresiva del diámetro anteroposterior proporcionaría una adecuada superficie de coaptación. A mediados de los años noventa, Bolling et al25 introdujeron el concepto de la plastia mitral mediante un anillo protésico sobrecorrector para reducir la incidencia de RM residual y/o recurrente. Actualmente, este concepto se encuentra ampliamente aceptado por la mayoría de los cirujanos y se aplica habitualmente para la anuloplastia mitral en pacientes con RMI de tipo IIIb. Además, los excelentes resultados descritos por Bax et al24 sustentan y respaldan la utilización de anillos sobrecorrectores.
CONCLUSIONES
El nuevo anillo CMA-E representa un avance más en la aplicación de la anuloplastia mitral remodeladora. Este anillo protésico combina el principio de la sobrecorrección con la reparación de la deformación anular asimétrica existente en la disfunción de tipo IIIb. Su morfología proporciona un incremento en la superficie de coaptación de los velos valvulares gracias a la reducción del diámetro anteroposterior. Su diseño tridimensional asimétrico, con una reducción en la curvatura correspondiente a los segmentos P2 y P3, permite una mayor corrección de la angulación. Nuestro estudio muestra que el anillo corrige de forma efectiva la RMI de tipo IIIb. Tras un período de seguimiento clínico de entre 15 y 34 meses, los resultados ecocardiográficos respaldan la eficacia de la reparación. Sin embargo, son necesarias series clínicas con mayor número de pacientes y seguimientos clínicos más prolongados, si cabe, para confirmar la durabilidad de esta técnica reconstructiva.
Full English text available from: www.revespcardiol.org
Véase editorial en págs. 1022-6
ABREVIATURAS
CMA-E: Carpentier-McCarthy-Adams IMR Etlogix.
FE: fracción de eyección.
RIC: rango intercuartílico.
RM: regurgitación mitral.
RMI: regurgitación mitral isquémica.
Proyecto financiado por el Departamento de Cirugía Cardiotorácica.
Correspondencia: Dr. J. Castillo / Dr. F. Filsoufi.
Research Fellow. Department of Cardiothoracic Surgery.
Mount Sinai Medical Center.
1190 Fifth Avenue. New York, NY 10029-1028 USA.
Correo electrónico: javier.castillo@mountsinai.org
Recibido el 18 de marzo de 2007.
Aceptado para su publicación el 29 de junio de 2007.