La fibrilación auricular es una enfermedad de abordaje complejo que tiene como punto estratégico el control de los pacientes tratados con antagonistas de la vitamina K. El objetivo de este estudio fue evaluar el impacto, en resultados de salud, de una herramienta para la toma de decisiones en fibrilación auricular no valvular, que mostrara el tiempo en rango terapéutico en la historia clínica informatizada de atención primaria.
MétodosEnsayo clínico aleatorizado llevado a cabo durante 2018 en 325 centros de atención primaria de Cataluña con 1 año de seguimiento. En los centros de intervención se instaló la herramienta para controlar el tiempo en rango terapéutico de los pacientes tratados con antagonistas de la vitamina K, y no se visualizó en el grupo control.
ResultadosSe evaluó a 44.556 pacientes. La intervención resultó protectora del ingreso por ictus (odds ratio [OR] ajustada: 0,70; intervalo de confianza del 95% [IC95%], 0,55-0,88). El número necesario a tratar fue de 3.502 (IC95%, 3.305-3.725) y el número de ingresos por ictus evitados fue 12,63 (IC95%, 11,88-13,38). La intervención redujo la mortalidad (OR ajustada: 0,78; IC95%, 0,67-0,90), el número necesario a tratar fue de 13.687 (95%CI, 10.789-18.714) y el número de muertes evitadas de 3,23 (IC95%, 2,36-4,10).
ConclusionesLa herramienta para visualizar el tiempo en rango terapéutico se asoció a una discreta reducción de los ingresos por ictus isquémico y de la mortalidad. Aunque el tiempo de seguimiento fue corto y el efecto de la intervención pequeño, los resultados son importantes y podrían mejorar con la implementación de la herramienta.
El ensayo se registró en ClinicalTrials.gov (NCT03367325).
Palabras clave
La prevalencia de la fibrilación auricular en adultos en España se estima actualmente en el 2-4%, que se eleva al 4,4% en los individuos de más de 40 años1,2. La morbilidad que muestra una mayor asociación con la fibrilación auricular es el ictus isquémico3 y en 2019 hubo alrededor de 12,2 millones de casos nuevos de ictus y 6,5 millones de muertes por ictus en todo el mundo4. El ictus asociado a fibrilación auricular supone, aproximadamente, el 25% del total de ictus y es el que causa una mayor discapacidad3.
Los anticoagulantes orales son los fármacos de elección para prevenir el ictus en la fibrilación auricular5. En el caso de la fibrilación auricular no valvular (FANV), se pueden administrar 2 tipos de anticoagulantes orales para prevenir los eventos tromboembólicos: antagonistas de la vitamina K y anticoagulantes orales de acción directa6.
La guía europea para el tratamiento de la FANV recomienda el empleo de anticoagulantes de acción directa y, en el caso de que estén contraindicados, el de antagonistas de la vitamina K6. Los antagonistas de la vitamina K fueron los anticoagulantes más ampliamente utilizados en España en 2018, pues constituyeron el 57,7% del total7,8. En la actualidad, los anticoagulantes de acción directa se utilizan en el 58,1% de los pacientes de España, en el 59,0% de los de Cataluña y en alrededor del 80,0% de los de Europa9.
Hay algunas cuestiones estratégicas del tratamiento de la FANV con anticoagulantes que deben mejorarse. Uno de los problemas es que los pacientes tratados con antagonistas de la vitamina K no puedan controlar adecuadamente el tiempo en rango terapéutico (TRT)10. Esto puede mejorarse no solo con el conocimiento del índice normalizado internacional (INR), que determina el grado de control de la anticoagulación en un momento determinado sino también permitiendo que los profesionales de atención primaria tengan acceso al TRT calculado automáticamente con el método de Rosendaal11 como parte integrante de la historia clínica electrónica de sus pacientes. Este parámetro mide el tiempo durante el cual los pacientes han tenido un buen control en los últimos 6 meses y es necesario para tomar decisiones sobre el cambio de tratamiento anticoagulante. Además, puede facilitar la optimización del control cuando se emplean antagonistas de la vitamina K en pacientes que no tienen buena adherencia al tratamiento.
Los sistemas de apoyo para la toma de decisiones clínicas son cada vez más frecuentes en los registros electrónicos de historias clínicas. Aunque se ha observado que estos sistemas mejoran los procesos de asistencia en diferentes enfermedades, la evidencia de una mejora de los resultados clínicos o económicos es escasa12. En la práctica clínica, estas herramientas no reducen la mortalidad cuando se integran en las historias clínicas electrónicas, si bien pueden reducir moderadamente las tasas de morbilidad13. En los últimos años, varios estudios han elaborado herramientas para la toma de decisiones en el control de la fibrilación auricular. La mayor parte de estas soluciones se centran en el inicio de la anticoagulación después de un diagnóstico de fibrilación auricular14,15. Algunas de estas herramientas mejoran la adherencia a las guías de práctica clínica13 y conducen a una ligera mejora en la reducción de las hemorragias14.
Dado que los pacientes tratados con antagonistas de la vitamina K tienen un mal control de la anticoagulación, sería útil disponer de un conocimiento del TRT en atención primaria, donde se lleva a cabo el tratamiento de la mayor parte de los pacientes. En este contexto, una herramienta para la toma de decisiones que visualice el TRT en atención primaria podría mejorar los resultados de salud. Así pues, el objetivo de este estudio fue evaluar la repercusión que tenía en los resultados de salud la herramienta de apoyo para la toma de decisiones clínicas en la fibrilación auricular no valvular (CDS-NVAF) incorporada a las historias clínicas electrónicas de atención primaria, basándose en la visualización del TRT.
MÉTODOSDiseño y población del estudioEl diseño del estudio se ha publicado ya con anterioridad16. Se describen a continuación el diseño general del estudio y las desviaciones respecto al protocolo del estudio. Este ensayo clínico se registró en ClinicalTrials.gov (NCT03367325).
Se llevó a cabo un ensayo clínico aleatorizado de grupos paralelos, con una aleatorización según el sector del centro de atención primaria16. Un sector es un grupo de centros de atención primaria que comparten el mismo servidor. El Institut Català de la Salut tiene 15 sectores, con un total de 325 centros de atención primaria. Los sectores se aleatorizaron mediante extractores de datos, utilizando el método de aleatorización simple en una relación 1:1, y con una generación aleatoria de los números 0 y 1. Los pacientes con un valor<0,5 se asignaron al grupo de control y los que tenían un valor ≥ 0,5 se asignaron al grupo de intervención. El estudio mantuvo un enmascaramiento para los pacientes del ensayo, los investigadores y los gestores de datos, pero no para los profesionales de atención primaria (figura 1).
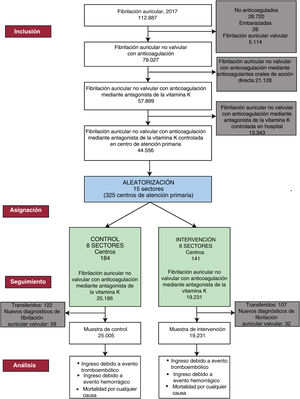
Las variables del estudio se obtuvieron de la base de datos poblacional del Sistema de Información para el Desarrollo de la Investigación en Atención Primaria16. En enero de 2017 se detectó un total de 112.887 personas con un diagnóstico activo de fibrilación auricular (figura 2). Se incluyó en el estudio a los pacientes con unos antecedentes de al menos 1 año de FANV en enero de 2018, a los cuales se les había administrado un tratamiento anticoagulante con antagonistas de la vitamina K (acenocumarol o warfarina) durante un mínimo de 6 meses en el momento de inicio del estudio y disponían de determinaciones del INR de al menos 6 meses en los últimos 6 meses de 2017. Se consideró que estaban recibiendo tratamiento anticoagulante con antagonistas de la vitamina K si tenían una prescripción activa en el momento de inicio de estudio y 2 meses antes. Se consideró que se había modificado su anticoagulante si habían recibido más de 2 meses de tratamiento con anticoagulantes de acción directa (dabigatrán, rivaroxabán, apixabán o edoxabán) en 2018.
Se excluyó del estudio a los pacientes con fibrilación auricular valvular que presentaban estenosis mitral o eran portadores de una válvula cardiaca protésica (texto 1 del material adicional). También se excluyó a los pacientes que no estaban anticoagulados, a las mujeres embarazadas, a los pacientes en tratamiento con anticoagulantes de acción directa en el momento de inicio del estudio y a los pacientes en quienes el seguimiento se realizaba en el hospital de referencia. Las pérdidas del seguimiento por traslados de los pacientes a otro sistema de asistencia sanitaria y los nuevos diagnósticos de fibrilación auricular valvular en los pacientes incluidos se descontaron del análisis (figura 2). Se llevó a cabo un análisis por intención de tratar 1 año después del inicio de la intervención y según las características de los pacientes.
Todos los centros de atención primaria del Institut Català de la Salut se consideraron aptos para la participación en el estudio. El momento de aplicación de la herramienta CDS-NVAF para iniciar el ensayo clínico lo determinó la Dirección de Atención Primaria del Institut Català de la Salut, que informó a los directores territoriales del inicio del estudio. Las desviaciones respecto al protocolo y la descripción de la versión final de la herramienta CDS-NVAF se incluyen en el textos 2 y 3 del material adicional.
Tamaño muestralLa muestra la formaron 44.556 personas con FANV anticoaguladas con antagonistas de la vitamina K, en tratamiento dentro del sistema de atención primaria. De ellas, 25.186 (de 184 centros de salud) y 19.370 (de 141 centros de salud) formaron parte de los grupos de control y de intervención, respectivamente. Partiendo del supuesto de un potencia estadística del 90% y de un error alfa del 5%, con corrección para el diseño de estudio de ensayo de conglomerados, este estudio permitía detectar una diferencia del 0,5% para una tasa de ictus de 1,32×100 ingresos por ictus por paciente y año17.
Análisis estadísticoLas diferencias estadísticamente significativas entre los grupos de control y de intervención se identificaron mediante pruebas de Z para las variables cualitativas y mediante pruebas de U de Mann-Whitney no paramétricas para las variables continuas. Se calcularon los valores de la incidencia de ingresos (con los intervalos del 95% [IC95%]) a causa de eventos tromboembólicos y hemorrágicos, así como la mortalidad. Las diferencias significativas entre las proporciones de los grupos de control y de intervención se detectaron con la prueba de Z. El efecto de la intervención (y el IC95%) se estimó con el empleo de la h de Cohen para las proporciones (efecto pequeño, h<0,2; efecto grande, h>0,8).
La asociación entre la probabilidad de muerte, ingreso por ictus y las variables relacionadas con esos eventos se cuantificó mediante una regresión logística multivariable para estimar los valores de odds ratio (OR). Se calculó la diferencia de riesgo media, el número que era necesario tratar y el número de eventos evitados18.
El umbral para la significación estadística se estableció en el 5%. Los análisis estadísticos se llevaron a cabo con el programa informático R versión 4.0.2 (R Foundation for Statistical Computing, Austria).
RESULTADOSNo hubo diferencias entre el grupo de control y el grupo de intervención en cuanto a las pérdidas del seguimiento debidas a traslados de los pacientes (122 de 25.186 pacientes frente a 107 de 19.370 pacientes; p=0,320) ni en los nuevos diagnósticos de fibrilación auricular valvular (59 de 25.186 pacientes frente a 32 de 19.370 pacientes; p=0,109) (figura 2). Así pues, al final del periodo de seguimiento se pudo analizar a 25.005 y 19.321 pacientes de los grupos de control e intervención, respectivamente.
En la situación inicial, en el grupo de intervención había una proporción superior de mujeres y de pacientes con antecedentes de arteriopatía periférica y de insuficiencia cardiaca, puntuaciones más altas (≥ 4) de las escalas CHA2DS2-VASc y HAS-BLED, y una mediana de edad superior que en el grupo de control. En cambio, en el grupo de control hubo una mayor proporción de pacientes con antecedentes de ictus isquémico y una mediana de TRT superior. En los pacientes del grupo de intervención era más probable la atención en un centro de atención primaria en las zonas de los quintiles de privación 1, 2 y 5, mientras que en los del grupo de control era más probable la atención en centros de los quintiles 3 y 4. Los pacientes del grupo de control tenían una mayor probabilidad de residir en áreas rurales que los del grupo de intervención (tabla 1). Con la excepción de la mediana de edad, las diferencias en todas las variables persistieron tras eliminar a los pacientes que se perdieron en el seguimiento (tabla 1 del material adicional).
Características de la población inicial
| Control | Intervención | ||
|---|---|---|---|
| Número (%) | Número (%) | p | |
| Total | 25.186 | 19.370 | |
| Sexo | |||
| Femenino | 12.379 (49,15) | 9.868 (50,94) | <0,001 |
| Masculino | 12.807 (50,85) | 9.502 (49,06) | <0,001 |
| Edad (años) | 81,5 (11,33) | 81,67 [11,42] | 0,049 |
| <60 | 583 (2,31) | 460 (2,37) | 0,678 |
| 60-69 | 2.388 (9,48) | 1.867 (9,64) | 0,576 |
| 70-79 | 7.771 (30,85) | 5.743 (29,65) | 0,006 |
| ≥80 | 14.444 (57,35) | 11.300 (58,34) | 0,036 |
| Tiempo desde el diagnóstico de fibrilación auricular | 6,04 (6,79) | 5,9 [7,00] | 0,363 |
| Tiempo en rango terapéutico | 68,75 [29,56] | 68,15 [29,39] | 0,010 |
| Antecedentes cardiovasculares | |||
| Arteriopatía periférica | 1.693 (6,72) | 1.424 (7,35) | 0,010 |
| Cardiopatía isquémica | 4.642 (18,43) | 3.670 (18,95) | 0,166 |
| Ateromatosis aórtica | 251 (1,00) | 180 (0,93) | 0,472 |
| Evento cerebrovascular previo | |||
| Ictus isquémico | 4.244 (16,85) | 3.119 (16,10) | 0,035 |
| Ictus de etiología indeterminada | 428 (1,70) | 294 (1,52) | 0,132 |
| Hemorragia intracraneal | 221 (0,88) | 188 (0,97) | 0,307 |
| Morbilidad | |||
| Diabetes mellitus | 8.381 (33,28) | 6.304 (32,55) | 0,104 |
| Hipertensión | 20.147 (79,99) | 15.625 (80,67) | 0,077 |
| Insuficiencia cardiaca | 3.389 (13,46) | 3.162 (16,32) | <0,001 |
| Insuficiencia renal | 7.678 (30,49) | 6.062 (31,30) | 0,066 |
| Antecedentes de riesgo hemorrágico | |||
| Alcohol | 525 (2,08) | 363 (1,87) | 0,115 |
| Hipertensión portal | 43 (0,17) | 29 (0,15) | 0,584 |
| Insuficiencia hepática | 130 (0,52) | 117 (0,60) | 0,216 |
| Hemorragias no digestivas ni intracraneales | 6.328 (25,13) | 4.779 (24,67) | 0,273 |
| Hemorragia digestiva | 2.098 (8,33) | 1.531 (7,90) | 0,103 |
| Índice CHA2DS2-VASc | |||
| 0 | 225 (0,89) | 188 (0,97) | 0,399 |
| 1 | 1.153 (4,58) | 859 (4,43) | 0,470 |
| 2 | 4.107 (16,31) | 3.055 (15,77) | 0,128 |
| 3 | 8.801 (34,94) | 6.667 (34,42) | 0,249 |
| ≥ 4 | 10.900 (43,28) | 8.601 (44,40) | 0,018 |
| Índice HAS-BLED | |||
| 0 | 250 (0,99) | 198 (1,02) | 0,756 |
| 1 | 3.800 (15,09) | 2.886 (14,90) | 0,581 |
| 2 | 8.417 (33,42) | 6.357 (32,82) | 0,182 |
| 3 | 7.705 (30,59) | 5.916 (30,54) | 0,909 |
| ≥ 4 | 5.014 (19,91) | 4.013 (20,72) | 0,035 |
| Pacientes atendidos fuera del centro de atención primaria | |||
| Asistencia domiciliaria | 2.873 (11,41) | 2.105 (10,87) | 0,073 |
| Institucionalizados | 1.389 (5,51) | 1.065 (5,50) | 0,939 |
| Ubicación de los centros de atención primaria según las categorías urbanas de MEDEA y de ruralidad | |||
| MEDEA 1a | 2.749 (10,91) | 2.846 (14,69) | <0,001 |
| MEDEA 2a | 3.274 (13,00) | 3.029 (15,64) | <0,001 |
| MEDEA 3a | 3.845 (15,27) | 2.819 (14,55) | 0,036 |
| MEDEA 4a | 4.072 (16,17) | 2.729 (14,09) | <0,001 |
| MEDEA 5a | 3.229 (12,82) | 2.777 (14,34) | <0,001 |
| Ruralb | 6.279 (24,93) | 3.945 (20,37) | <0,001 |
| Pérdida del seguimiento | 1.738 (6,90) | 1.225 (6,32) | 0,015 |
CHA2DS2-VASc: puntuación de riesgo tromboembólico; HAS-BLED: escala de riesgo hemorrágico; p: significación de la prueba Z de proporciones; RIC: rango intercuartílico.
Los valores expresan n (%) o mediana [RIC].
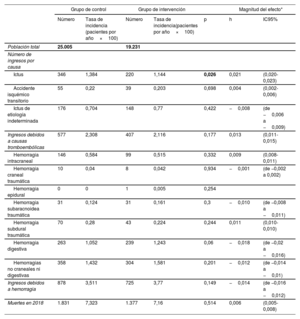
La incidencia de ingresos por ictus fue menor en el grupo de intervención que en el grupo de control (1,14 frente a 1,38 ingresos por ictus por paciente y año×100; p=0,026). No se detectaron diferencias entre los 2 grupos en la incidencia de ningún otro evento tromboembólico o hemorrágico. La magnitud del efecto de la intervención medida con la h de Cohen para el ingreso por ictus fue de 0,021 (IC95%, 0,020-0,023) (tabla 2).
Resultados principales de los ingresos debidos a eventos tromboembólicos, hemorrágicos y muertes
| Grupo de control | Grupo de intervención | Magnitud del efecto* | |||||
|---|---|---|---|---|---|---|---|
| Número | Tasa de incidencia (pacientes por año×100) | Número | Tasa de incidencia(pacientes por año×100) | p | h | IC95% | |
| Población total | 25.005 | 19.231 | |||||
| Número de ingresos por causa | |||||||
| Ictus | 346 | 1,384 | 220 | 1,144 | 0,026 | 0,021 | (0,020-0,023) |
| Accidente isquémico transitorio | 55 | 0,22 | 39 | 0,203 | 0,698 | 0,004 | (0,002-0,006) |
| Ictus de etiología indeterminada | 176 | 0,704 | 148 | 0,77 | 0,422 | −0,008 | (de −0,006 a −0,009) |
| Ingresos debidos a causas tromboembólicas | 577 | 2,308 | 407 | 2,116 | 0,177 | 0,013 | (0,011-0,015) |
| Hemorragia intracraneal | 146 | 0,584 | 99 | 0,515 | 0,332 | 0,009 | (0,008-0,011) |
| Hemorragia craneal traumática | 10 | 0,04 | 8 | 0,042 | 0,934 | −0,001 | (de −0,002 a 0,002) |
| Hemorragia epidural | 0 | 0 | 1 | 0,005 | 0,254 | ||
| Hemorragia subaracnoidea traumática | 31 | 0,124 | 31 | 0,161 | 0,3 | −0,010 | (de −0,008 a −0,011) |
| Hemorragia subdural traumática | 70 | 0,28 | 43 | 0,224 | 0,244 | 0,011 | (0,010-0,010) |
| Hemorragia digestiva | 263 | 1,052 | 239 | 1,243 | 0,06 | −0,018 | (de −0,02 a −0,016) |
| Hemorragias no craneales ni digestivas | 358 | 1,432 | 304 | 1,581 | 0,201 | −0,012 | (de −0,014 a −0,01) |
| Ingresos debidos a hemorragia | 878 | 3,511 | 725 | 3,77 | 0,149 | −0,014 | (de −0,016 a −0,012) |
| Muertes en 2018 | 1.831 | 7,323 | 1.377 | 7,16 | 0,514 | 0,006 | (0,005-0,008) |
p: significación de la prueba Z de proporciones.
Los ingresos por ictus se asociaron al aumento de la edad (OR ajustada, 1,02; IC95%, 1,01-1,04), al cambio del tratamiento de un antagonista de la vitamina K a un anticoagulante de acción directa (OR ajustada, 13,41; IC95%, 10,63-16,91) y al antecedente cerebrovascular (OR ajustada, 2,39; IC95%, 1,87-3,06), que incluía el antecedente de ictus, el antecedente de ictus indeterminado y el antecedente de hemorragia intracraneal antes del inicio de la intervención. En los pacientes del grupo de intervención se observó una protección frente al ingreso por ictus (OR ajustada, 0,70; IC95%, 0,55-0,88) (figura 3) y fue necesario el uso de la herramienta CDS-NVAF en un total de 3.502 (IC95%, 3.305-3.725) pacientes para prevenir el ingreso de 1 paciente por ictus. En total, se evitaron 12,63 (IC95%, 11,88-13,38) ingresos por ictus (tabla 3).
Factores asociados a los ingresos por ictus y a la mortalidad por cualquier causa.
ACOD: anticoagulante oral de acción directa; IC 95%: intervalo de confianza de 95%.
a Los eventos cerebrovasculares previos incluyen el ictus, el ictus de etiología indeterminada y la hemorragia intracraneal.
b MEDEA es un índice de la privación material y social (1: privación baja; 5: privación alta) para la ubicación de los centros de atención primaria urbanos en los cuales se atiende a los pacientes.
c Rural indica los centros de atención primaria que atienden a poblaciones rurales.
Medidas de impacto de la herramienta de apoyo a la toma de decisiones en la fibrilación auricular no valvular
| Criterio de valoración principal | OR (IC95%)* | DRM (IC95%) | NNT (IC95%) | Número de eventos evitados (IC95%) |
|---|---|---|---|---|
| Pacientes ingresados por ictus | 0,70 (0,55-0,88) | 2,86×10−4 (2,66×10−4-3,05×10−4) | 3.502 (3.305-3.725) | 12,63 (11,88-13,38) |
| Mortalidad | 0,78 (0,67-0,90) | 7,30×10−5 (5,34×10−5-9,26×10−5) | 13.687 (10.789-18.714) | 3,23 (2,36-4,10) |
DRM: diferencia de riesgo media; IC: intervalo de confianza; NNT: número que es necesario tratar; OR: odds ratio.
La probabilidad de muerte más alta se asoció a mayor edad (OR ajustada, 1,12; IC95%, 1,11-1,14), el sexo masculino (OR ajustada, 1,25; IC95%, 1,08-1,44), el antecedente previo cerebrovascular (OR ajustada, 1,39; IC95%, 1,18-1,63) y la atención en un centro sanitario rural (OR ajustada, 1,48; IC95%, 1,25-1,74). El hecho de pertenecer al grupo de intervención supuso una protección frente a la muerte (OR ajustada, 0,78; IC95%, 0,67-0,90) (figura 3) y fue necesario el empleo de la herramienta CDS-NVAF en 13.687 (IC95%, 10.789-18.714) pacientes para prevenir 1 muerte. En total, se evitaron 3,23 (IC95%, 2,36-4,10) muertes (tabla 3).
El TRT (≥ 65%) y el TRT (> 70%) no mejoraron el control en 1 año de seguimiento en el grupo de intervención en comparación con el grupo de control. El cambio de tratamiento a anticoagulantes orales de acción directa fue más probable en el grupo de intervención (tabla 2 del material adicional).
DISCUSIÓNEn el presente estudio se analizó una herramienta de apoyo a la toma de decisiones integrada en la historia clínica electrónica. La herramienta CDS-NVAF permite a los profesionales de atención primaria evaluar el grado de control de la anticoagulación en los pacientes con FANV anticoagulados con antagonistas de la vitamina K. Esta herramienta dio lugar a una leve reducción del número de ingresos por ictus y es posible que se asocie también a una disminución de la mortalidad. La intervención tuvo una repercusión favorable por lo que respecta a la evitación de ingresos por ictus y a la tasa de mortalidad, y es posible que la mejora de su implementación aporte futuros beneficios.
Los pacientes en los que la herramienta CDS-NVAF aporta beneficio son los tratados con anticoagulación con antagonistas de la vitamina K. Estos fármacos tienen un margen terapéutico estrecho y la respuesta al tratamiento muestra grandes diferencias en distintas personas. Esto hace necesaria una supervisión de la anticoagulación y ajustes de la dosis en función del INR, que es un cálculo estandarizado del tiempo de protrombina. Existe un consenso en cuanto a que los pacientes con FANV tratados con antagonistas de la vitamina K deben mantener un INR de entre 2 y 3 durante el mayor tiempo posible para alcanzar un TRT elevado6. Estas recomendaciones se basan en la capacidad de estos anticoagulantes de prevenir los eventos tromboembólicos en estos rangos de valores y en el aumento de los efectos adversos hemorrágicos a partir de un valor de INR de 419. La guía europea actual sobre la fibrilación auricular considera que un TRT >70% a los 6 meses constituye un buen control6. Sin embargo, dado que en la guía española considera que un TRT ≥ 65% representa un buen control20, hemos utilizado este valor en este estudio. El TRT mal controlado es un parámetro que se emplea para decidir un cambio de tratamiento de un antagonista de la vitamina K a un anticoagulante de acción directa, siempre que se haya verificado la buena adherencia al tratamiento.
Por lo que respecta a los resultados de salud, los ingresos por ictus fueron menos frecuentes en el grupo de intervención que en el grupo de control, si bien el efecto fue pequeño, con una incidencia de 1,14 y 1,38 ingresos por ictus por 100 pacientes y año, respectivamente. En estudios con un periodo de seguimiento más prolongado se observó una incidencia similar de ictus en un grupo tratado con warfarina (1,32-1,66 ictus por 100 pacientes y año) a la observada en este grupo de control. En estos estudios se observó una reducción del riesgo de ictus con el empleo de anticoagulantes de acción directa de 0,97 a 1,33 ictus por 100 pacientes y año, una cifra que está más próxima a la tasa observada en este grupo de intervención17,21.
El CDS-NVAF tuvo poco efecto en cuanto a la reducción de los ingresos por ictus. Esto podría deberse al hecho de que la herramienta se introdujo en un formato de ensayo clínico aleatorizado, según la práctica clínica estándar. La herramienta se instaló y se anunció en las historias clínicas electrónicas según como se hace para innovaciones similares, pero la información aportada podría no haber sido suficiente para garantizar un conocimiento y un uso adecuados de la herramienta. Sin embargo, la efectividad observada se basa en la práctica clínica real y no en la eficacia en ensayos clínicos aleatorizados llevados a cabo en unas condiciones ideales. Además, no hubo mejoría alguna del TRT en el grupo de intervención, lo cual implica que parte del efecto beneficioso de la herramienta podría atribuirse al cambio de tratamiento al cambiar a un anticoagulante oral de acción directa.
En un estudio de la mortalidad en pacientes anticoagulados de una mediana de edad entre 70 y 73 años se identificó una media de mortalidad de 4,63 muertes por 100 pacientes y año22. En este estudio con una muestra de pacientes con una mediana de edad de 81 años, la tasa de mortalidad fue menor en el grupo de intervención que en el grupo de control (7,16 y 7,32 muertes por 100 pacientes y año, respectivamente). En un estudio reciente de mortalidad en una población española de pacientes tratados con antagonistas de la vitamina K se observó que la mortalidad por cualquier causa fue del 6,14% con un buen control de la anticoagulación y del 11,62% con un control desfavorable23.
La herramienta CDS-NVAF se asoció a una reducción de los ingresos por ictus. Los pacientes del grupo de intervención con el CDS-NVAF mostraron cierta protección frente a los ingresos por ictus, con una OR ajustada de 0,70 (IC95%, 0,55-0,88). En cambio, los factores asociados a un aumento de la probabilidad de ingreso por ictus fueron la edad, el cambio a un tratamiento con un anticoagulante de acción directa durante el periodo del estudio y los antecedentes de enfermedad cerebrovascular. La edad y los antecedentes de enfermedad cerebrovascular son factores bien establecidos que aumentan el riesgo de ictus en las personas con fibrilación auricular. La edad es el factor que tiene mayor influencia en las personas de edad igual o superior a 75 años. La evidencia existente sugiere que los antecedentes de ictus pueden ser el factor más importante para determinar la aparición de un nuevo ictus24. Según estos resultados, la existencia de antecedentes de enfermedad cerebrovascular aumentó la probabilidad ajustada de ingreso por ictus en una OR 2,39 (IC95%, 1,87-3,06). Este resultado se tuvo en cuenta para introducir un ajuste respecto a las diferencias iniciales de ictus isquémico entre los 2 grupos. La tasa de recidiva es menor para los ictus isquémicos de vasos pequeños y ha disminuido en la última década. En cambio, los ictus cardioembólicos, la mayor parte de los cuales son causados por la fibrilación auricular, muestran un riesgo de recidiva del 54% y su incidencia se ha estabilizado a lo largo de la última década. Estos hechos resaltan el valor de aplicar estrategias preventivas eficaces en los pacientes con fibrilación auricular, a fin de prevenir el ictus tromboembólico25.
Asimismo, en este estudio, el factor que mostró una asociación más intensa con el ingreso por ictus fue el cambio de anticoagulante durante el periodo de intervención (OR ajustada, 13,43; IC95%, 10,63-16,91). El tipo de análisis realizado en este caso no permite determinar la causa de un ictus como relacionada con los cambios del tratamiento anticoagulante. Por tanto, el ictus podría haberse debido a un cambio previo del tipo de anticoagulante asociado a un mayor riesgo de ictus durante los meses iniciales o a que el ingreso por ictus se produjera antes del cambio del anticoagulante. Los pacientes con FANV que presentan un ictus isquémico agudo tienen un riesgo de transformación hemorrágica y también de recidiva de ictus isquémico en el periodo posterior al ictus. No se sabe cuál es el momento óptimo para anticoagular a los pacientes con un ictus isquémico26.
Se observó que la intervención protegía frente al ingreso por ictus. Hasta donde se sabe, este es el primer ensayo clínico en la práctica clínica real de una herramienta de apoyo a la toma de decisiones integrada en las historias clínicas electrónicas con el fin de respaldar el tratamiento de la fibrilación auricular en el que se han reducido los ingresos por ictus13,14. Debe señalarse que esta herramienta permite una mejor detección de los pacientes que son candidatos a un cambio de tratamiento para pasar a anticoagulantes de acción directa. Esto puede explicar en parte la reducción observada en las tasas de ingresos por ictus y, tal vez, en la mortalidad.
La visualización del TRT por parte de los profesionales de atención primaria redujo el riesgo de mortalidad tras ajustar por otras variables (OR ajustada, 0,78; IC95%, 0,67-0,90). En dos revisiones sistemáticas de metanálisis diseñadas para estudiar la efectividad de herramientas de apoyo a la toma de decisiones clínicas no se obtuvo una evidencia indicativa de reducción de la mortalidad12,27. En este estudio, la mayor probabilidad de mortalidad se asoció también a la edad avanzada, el sexo masculino, los antecedentes de enfermedad cerebrovascular y la atención en un centro de atención primaria de ámbito rural. En estudios previos se ha confirmado que la mortalidad por cualquier causa es más alta en las áreas rurales que en las urbanas y esto está relacionado con las desigualdades de salud y sus determinantes28,29. El principal elemento que subyace en las desigualdades entre áreas urbanas y rurales es la menor esperanza de vida en la población rural29. Un factor importante en esta brecha entre áreas urbanas y áreas rurales es la enfermedad cardiovascular, y en particular el ictus, con una tasa de mortalidad por ictus el 30% superior en las áreas rurales en comparación con las urbanas30.
Es probable que los resultados de este estudio tengan validez externa en los sistemas de salud pública de otras regiones de España y probablemente también en sistemas de atención de salud pública de Europa. La evidencia actual indica que la visualización del cálculo del TRT es una herramienta esencial para el control de la anticoagulación en un contexto hospitalario y en la atención primaria31,32. En estudios futuros deberá determinarse si la herramienta CDS-NVAF fue visualizada y comprendida por los profesionales de la asistencia sanitaria. Deberá fortalecerse su extensión asegurando que los profesionales de atención primaria reciban formación para su uso.
LimitacionesUna de las limitaciones del estudio radica en las diferencias existentes entre el grupo de intervención y el grupo de control en la situación inicial. Dado que el trabajo comportó un estudio de población a gran escala, las diferencias de proporciones entre los 2 grupos fueron estadísticamente significativas, a pesar de ser pequeñas y de tener poca relevancia sustantiva. En segundo lugar, no fue posible obtener datos sociodemográficos sobre los profesionales de la asistencia sanitaria, a causa de las limitaciones impuestas por la protección de datos; esto impidió llevar a cabo un análisis de múltiples niveles para identificar las características de los profesionales de la asistencia sanitaria que se asocian a un mejor resultado de salud. En tercer lugar, aunque se incluyó a menos pacientes de los estimados en 2015, esto no afectó al poder estadístico del estudio, dado el tamaño de la muestra final. Aunque el efecto de la intervención fue pequeño y el periodo de seguimiento fue corto, los resultados son de nivel poblacional y coherentes. Además, la reducción futura del uso de los antagonistas de la vitamina K podría reducir el efecto de la herramienta. En cuarto lugar, los resultados no se han desglosado por sexo, pero se presentan con las proporciones de hombres y mujeres, y el resultado principal incluye el sexo como factor predictor. Por último, el diseño del CDS-NVAF no permite la confirmación de que el profesional de atención primaria viera el TRT y siguiera la recomendación, basada en el porcentaje de TRT, para confirmar el cumplimiento o cambiar el anticoagulante. En consecuencia, es esencial conocer las opiniones de los profesionales que tratan a los pacientes del grupo de intervención por lo que respecta a los obstáculos para conocer la herramienta.
CONCLUSIONESEl impacto de la intervención fue favorable por lo que respecta a evitar el ingreso por ictus y la reducción de la mortalidad. La CDS-NVAF se asoció a reducciones discretas de la tasa de ingresos por ictus isquémico y de la mortalidad. No se observaron diferencias en las tasas de hemorragia. La CDS-NVAF es el primera herramienta de toma de decisiones que ha reducido los ingresos por ictus y la mortalidad. Aunque el periodo de seguimiento fue breve y el efecto de la intervención fue modesto, los resultados deben tenerse en cuenta. Deberá estudiarse la efectividad de la herramienta a más largo plazo y tras mejorar su implementación.
- -
La fibrilación auricular es una enfermedad compleja, en la cual es preciso mejorar el abordaje terapéutico en algunos aspectos estratégicos, como el control de los pacientes tratados con antagonistas de la vitamina K.
- -
La fibrilación auricular es una patología que podría beneficiarse del empleo de herramientas destinadas a facilitar la toma de decisiones que se integren en la historia clínica electrónica.
- -
Se ha observado que varias herramientas para la toma de decisiones clínicas en el tratamiento de la fibrilación auricular han mejorado el cumplimiento de las guías de práctica clínica y han reducido las hemorragias.
- -
Evaluamos CDS-NVAF, una herramienta para la toma de decisiones clínicas en el tratamiento de la FANV que permite visualizar el TRT en la historia clínica electrónica de atención primaria.
- -
CDS-NVAF podría ser la primera herramienta con la cual se reducen los ingresos por ictus isquémico y la mortalidad.
- -
Los resultados de salud podrían ser importantes a nivel poblacional y podrían extrapolarse a otras regiones de España y de Europa.
Este trabajo contó con el apoyo del Departament de Sanitat de la Generalitat de Catalunya, Pla Estratègic de Recerca i Innovació en Salut (PERIS) (subvenciones números SLT002/16/00146 y SLT008/18/00021) y del Instituto Carlos III (subvención número PI21/01435).
CONSIDERACIONES ÉTICASEl estudio se llevó a cabo según las normas nacionales e internacionales (Declaración de Helsinki) relativas a las cuestiones éticas. El protocolo de este estudio fue aprobado por el comité de ética de investigación clínica del Institut Universitari d’Investigació en Atenció Primària (IDIAP) Jordi Gol, el 15 de marzo de 2017 (código P17/091). Además, el estudio fue autorizado por la Direcció d’Atenció Primària del Institut Català de la Salut. Los datos incluidos en la base de datos del Sistema de Información para el Desarrollo de la Investigación en Atención Primaria se anonimizaron y se identificaron mediante un código interno, lo cual imposibilitaba la identificación de los individuos, incluso para el equipo de investigación. Esto garantizaba la confidencialidad de los datos de los participantes en el estudio que fueron incluidos en el ensayo atendiendo a lo establecido en la Ley Orgánica de Protección de Datos y Garantía de los Derechos Digitales33. Dado que el estudio se basa en el análisis de una base de datos anonimizada, no se recabó el consentimiento informado de los pacientes. El comité de ética estableció que no era necesario el consentimiento informado.
DECLARACIÓN SOBRE EL USO DE INTELIGENCIA ARTIFICIALNo se ha utilizado inteligencia artificial en la elaboración de este trabajo.
CONTRIBUCIÓN DE LOS AUTORESConcepción y diseño del estudio: M. R. Dalmau Llorca, C. Aguilar Martín y A. Queiroga Gonçalves. Obtención de financiación: M. R. Dalmau Llorca, C. Aguilar Martín, N. Carrasco-Querol, Z. Hernández Rojas, D. Rodríguez Cumplido, E. Castro Blanco, A. Queiroga Gonçalves, J. Fernández-Sáez y J. Pérez-Villacastín. Metodología: M. R. Dalmau Llorca, C. Aguilar Martín, D. Rodríguez Cumplido, A. Queiroga Gonçalves y J. Fernández-Sáez. Análisis de los datos: M. R. Dalmau Llorca, C. Aguilar Martín, Z. Hernández Rojas, E. Castro Blanco y J. Fernández-Sáez. Interpretación de los datos: M. R. Dalmau Llorca, C. Aguilar Martín, D. Rodríguez Cumplido, E. Castro Blanco, J. Fernández-Sáez y J. Pérez-Villacastín. Análisis estadístico: M. R. Dalmau Llorca, C. Aguilar Martín, Z. Hernández Rojas, E. Castro Blanco y J. Fernández-Sáez. Preparación de la propuesta inicial del original: M. R. Dalmau Llorca, C. Aguilar Martín, N. Carrasco-Querol, Z. Hernández Rojas, D. Rodríguez Cumplido, E. Castro Blanco, A. Queiroga Gonçalves, J. Fernández-Sáez y J. Pérez-Villacastín. Revisión y corrección del original: M. R. Dalmau Llorca, C. Aguilar Martín, N. Carrasco-Querol, Z. Hernández Rojas, D. Rodríguez Cumplido, E. Castro Blanco, A. Queiroga Gonçalves, J. Fernández-Sáez y J. Pérez-Villacastín. Revisión final: M. R. Dalmau Llorca, C. Aguilar Martín, N. Carrasco-Querol, Z. Hernández Rojas, D. Rodríguez Cumplido, E. Castro Blanco, A. Queiroga Gonçalves, J. Fernández-Sáez y J. Pérez-Villacastín.
CONFLICTO DE INTERESESM. R. Dalmau Llorca, C. Aguilar Martín, Z. Hernández Rojas, Dolores Rodríguez Cumplido, A. Queiroga Gonçalves y J. Fernández-Sáez declaran haber recibido financiación parcial para el estudio de Bayer Hispania SL. El promotor no participó en el diseño y la realización del estudio; la obtención, gestión, análisis e interpretación de los datos, ni la redacción, revisión y aprobación del manuscrito o la decisión de enviarlo a publicación. Bayer Hispania SL aportó apoyo técnico al Institut Català de la Salut para realizar el cálculo del TRT en las historias clínicas electrónicas, pero no influyó en el diseño del estudio ni en la visualización de la herramienta.
Los autores desean expresar su agradecimiento a los siguientes departamentos por su contribución: Gestió d’Atenció Primària del Institut Català de la Salut, Sistemes d’Informació dels Serveis d’Atenció Primària, Gestió Regional i Gestió d’Atenció Primària de les Terres de l’Ebre, Unitat de Sistemes d’Informació de la Gestió Regional de les Terres de l’Ebre, Centre de Competències Funcionals de l’eCAP del Àrea de Sistemes d’Informació y SIDIAP.