Palabras clave
INTRODUCCIÓN
La reserva fraccional de flujo (RFF) ha demostrado utilidad para determinar la repercusión funcional de lesiones angiográficamente moderadas o dudosas1-5 y para decidir la conveniencia de su revascularización6-10. La obtención de una RFF > 0,75 o 0,8 en una determinada lesión permite aplazar de forma segura su revascularización sin que se produzcan más eventos adversos a largo plazo y con similar control de los síntomas que en los pacientes tratados6,8. Los principales estudios que demuestran esta utilidad de la RFF se han realizado en pacientes con cardiopatía isquémica estable. Actualmente, la mayoría de los cateterismos realizados en la práctica diaria tienen como indicación un síndrome coronario agudo (SCA). Un porcentaje variable de las coronariografías realizadas en estos pacientes no presentan lesiones significativas o muestran estenosis angiográficamente moderadas o de difícil cuantificación. En estos casos, el valor pronóstico de la RFF obtenida mediante guía de presión ha sido poco estudiado o es controvertido3,11. El carácter dinámico de las lesiones en el SCA, con presencia de un tono vaso-motor alterado, trombo, zonas de miocardio aturdido o embolizaciones distales pueden hacer cuestionable la toma de decisiones basada en la RFF3,11.
En el presente estudio analizamos el pronóstico a 1 año de una serie de pacientes con SCA y lesiones moderadas en la angiografía no revascularizados de acuerdo con la cifra de RFF obtenida mediante el estudio con guía intracoronaria de presión.
MÉTODOS
Estudio observacional descriptivo de una cohorte consecutiva de pacientes. Se analizaron todos los procedimientos de nuestro centro en los que, entre el 1 de enero de 2006 y el 30 de junio de 2008, se realizó un estudio con guía de presión en una lesión angiográficamente moderada (estenosis visual entre el 50 y el 70%). De estos procedimientos, se seleccionaron los realizados durante un ingreso por SCA. Sólo se incluyeron los casos en cuya historia clínica figuraba el juicio de SCA emitido por un cardiólogo (de acuerdo con la vigente definición de éste)12 y siempre que la coronariografía se hubiera solicitado por tal indicación. Se realizó seguimiento de los pacientes en los que se decidió no revascularizar ninguna lesión por la cifra de RFF obtenida.
Se excluyeron los estudios solicitados por dolor torácico de dudosa filiación o los casos en que una valvulopatía o miocardiopatía podía ser la causa de la clínica del paciente. Se excluyeron también los casos en que se realizó intervencionismo sobre una lesión causal y la guía de presión se empleó para estudiar otras lesiones distintas de las tratadas. La realización de estudio funcional de la lesión con guía de presión dependió del criterio del intervencionista. La práctica habitual en el centro donde se realizó este trabajo es no realizar estudio con guía de presión cuando, a pesar de tratarse de una lesión angiográficamente moderada, es evidente la presencia de trombo, la lesión causa un flujo distal menor que TIMI 3 o se aprecia una imagen compatible con disección espontánea o placa ulcerada.
Coronariografía, estudio invasivo y tratamiento
Dentro del protocolo habitual del centro donde se realizó el estudio, todos los pacientes incluidos recibieron, antes del procedimiento, aspirina (100 mg/día o una dosis de carga de 300 mg si no la tomaban previamente) y clopidogrel (75 mg/día o una carga de 600 mg si no lo había tomado con anterioridad). Salvo contraindicaciones, en los pacientes ingresados por SCA, la doble antiagregación oral se mantiene durante 1 año tras el alta hospitalaria. Al decidirse el estudio con guía de presión, se administraron 5.000 U de heparina sódica intravenosa si no había sido suministrada previamente. Tras decidirse la realización del estudio funcional de la lesión angiográficamente moderada, el catéter diagnóstico fue sustituido por un catéter guía de 6 Fr. Se repitieron con este catéter las proyecciones con que se obtuvo la mejor visualización de la lesión, con mayor estenosis visual y sin la superposición de ramas o pérdida de longitud por curvatura. La valoración funcional se realizó con una guía intracoronaria de presión de 0,014" (Pressure Wire, Radi Medical Systems, Uppsala, Suecia). La guía fue calibrada externamente y posteriormente se avanzó hasta el extremo distal del catéter guía y se verificó la igualdad entre las curvas de presión en el catéter y la guía de presión. Tras suministrar una dosis intracoronaria de 200-300 μg de nitroglicerina, la guía fue avanzada hasta ubicar su sensor al menos 10 mm distal a la lesión en estudio. La RFF se obtuvo administrando 300-500 μg de adenosina intracoronaria, prestando especial atención a que no hubiera enclavamiento del catéter en el ostium coronario tras la inyección del bolo de fármaco. La RFF se determinó mediante el cociente, latido a latido, entre las medias de la presión aórtica (Pa) (en el extremo del catéter guía) y la presión distal (Pd) a la lesión (recogida por la guía de presión), en situación de hiperemia máxima. Se realizaron al menos tres determinaciones de la RFF. Se utilizó para la decisión el menor valor de RFF obtenido. Se intentó una dosis intracoronaria máxima de 500 μg de adenosina siempre que una dosis inferior no produjera un periodo de asistolia ≥ 6 s. Los pacientes con lesiones con una RFF ≥ 0,75 no recibieron revascularización coronaria.
El tratamiento médico recibido por el paciente antes y después del procedimiento fue decidido por el médico responsable de aquél en cada caso.
Variables
Las características basales de los pacientes y los resultados del procedimiento se recogieron de la historia clínica hospitalaria, el registro de procedimientos existente en la unidad de hemodinámica del hospital donde se realizó el estudio o la visualización de la grabación angiográfica del procedimiento. Se consideró que había elevación enzimática compatible con necrosis miocárdica cuando antes de la realización de la coronariografía las cifras de troponina I o T o de fracción MB de la creatincinasa (MB-CK) eran superiores a los valores normales del laboratorio donde se hubiera realizado la extracción.
Análisis cuantitativo
Lo realizó offline, sin conocimiento del resultado del estudio funcional, un intervencionista experimentado. Para las mediciones se utilizó el software MEDIS QAngio XA v 7.1 (Medis Medical Imaging Systems, Leiden, Países Bajos).
Seguimiento
Se llevó a cabo 1 año después del estudio funcional, mediante llamada telefónica y consulta de la historia clínica en caso de que se hubieran producido nuevos ingresos hospitalarios del paciente. En los pacientes a los que se realizó una nueva coronariografía, se revisó la grabación para determinar el estado de la lesión estudiada previamente. Se consideraron variables objetivo principal del estudio en el seguimiento: la muerte de causa cardiaca o desconocida, el infarto agudo de miocardio no fatal, la necesidad de revascularización de la lesión estudiada y el evento combinado de las tres. Se recogió también la mortalidad no cardiaca, la necesidad de reingreso por cardiopatía isquémica y la necesidad de revascularización en una lesión distinta de la estudiada.
Se consideró infarto de miocardio en el seguimiento el ingreso hospitalario con un informe clínico de alta con tal diagnóstico.
Análisis estadístico
Las variables continuas se muestran como media ± desviación estándar y las cualitativas, como valor absoluto y porcentaje. Para las comparaciones se utilizó la prueba de la t de Student para las variables cuantitativas, siempre que se comprobara una distribución normal mediante el test de Kolmogorov-Smirnov. En caso de distribución no normal, se utilizó la prueba no paramétrica de la U de Mann-Whitney. Se realizó un estudio de regresión lineal entre los valores del porcentaje de estenosis por diámetro resultantes de la cuantificación digital offline en cada una de las lesiones estudiadas y el valor de RFF obtenido con la guía intracoronaria de presión. Se realizó el correspondiente análisis de supervivencia (curvas de Kaplan-Meier) para cada uno de los eventos analizados en el año de seguimiento. Se empleó en los análisis el paquete estadístico SPSS (versión 15.0) para Windows.
RESULTADOS
Entre el 1 de enero de 2006 y el 30 de junio de 2008, 111 pacientes cumplieron criterios de inclusión en el estudio. De ellos, se excluyó a priori a 5 pacientes por tratarse de extranjeros transeúntes en nuestro país, sin posibilidad de seguimiento al año. La muestra final consistió en 106 pacientes. En el mismo periodo, fueron tratadas por presentar una RFF < 0,75 otras 37 lesiones moderadas sospechosas de ser la causa del episodio en 33 pacientes con SCA. El total de 144 pacientes estudiados con guía de presión en lesiones moderadas posibles causas del cuadro clínico era el 7,8% de los 1.843 pacientes cateterizados en nuestro centro con el diagnóstico de SCA en ese periodo.
Las características basales de los pacientes incluidos se muestran en la tabla 1. El 21 y el 28% de los pacientes, respectivamente, habían presentado elevación de marcadores de necrosis miocárdica o cambios dinámicos en el segmento ST durante los episodios de dolor (el 13% elevación del segmento ST; el 15% descenso del segmento ST) cuando éstos habían sido presenciados. Un 12% de los pacientes con SCA sin elevación del segmento ST (SCASEST) fueron dados de alta con el diagnóstico de infarto agudo de miocardio sin elevación del segmento ST (IAMSEST), el 80,4% con el diagnóstico de angina inestable y el resto como dolor torácico sin lesiones significativas. Más de un 95% de los pacientes recibieron fármacos antiagregantes antes de la coronariografía y un 73%, doble antiagregación oral con aspirina y clopidogrel. El resto del tratamiento se muestra en la tabla 2.
Se estudiaron 127 lesiones en los 106 pacientes incluidos. En 14 pacientes se estudiaron 2 lesiones (13%); en 2 pacientes, 3 lesiones (1,9%), y en 1 paciente, 4 lesiones (0,9%). En la mayoría de los casos, 89 (86%), se estudió una sola lesión. De las 127 lesiones estudiadas, 8 fueron reestenosis en el stent (6%) y el resto, lesiones de novo.
No se observaron complicaciones durante los procedimientos, salvo frecuentes episodios de bloqueo auriculoventricular y un caso de fibrilación auricular paroxística tras la pausa producida por la adenosina, que se revirtió espontáneamente a las 3 h. Todos los episodios de bradicardia cedieron espontáneamente.
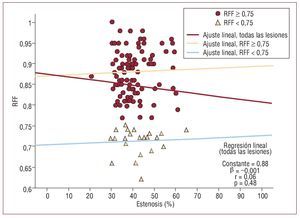
Los resultados de la cuantificación computarizada de las lesiones se muestran en la tabla 3. Se observaron diferencias estadísticamente significativas en el diámetro de referencia y el diámetro luminal mínimo de las lesiones con RFF superior e inferior a 0,75, aunque estas diferencias no fueron relevantes en su magnitud. Se observó una evidente superposición del porcentaje de estenosis entre las lesiones que eran funcionalmente significativas y las que no (fig. 1). Diez lesiones (7,9%) tuvieron una RFF entre 0,75 y 0,8. En el análisis de regresión lineal realizado, no se observó correlación (r = 0,06) entre los valores de RFF obtenida y la cuantificación computarizada de las lesiones (fig. 1).
Fig. 1. Correlación entre la estenosis angiográfica (por diámetro) obtenida mediante cuantificación digital off-line y la reserva fraccional de flujo obtenida. RFF: reserva fraccional de flujo.
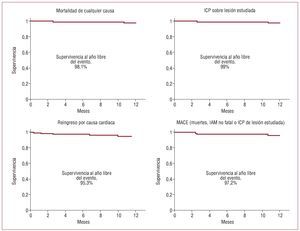
En el seguimiento no se observaron complicaciones hospitalarias. Se logró el seguimiento completo al año de 103 pacientes (97,2%); 2 varones de 78 y 73 años fallecieron durante el seguimiento (RFF 0,85 y 0,96), ambos con disfunción ventricular grave en el momento del estudio funcional; el primero murió en un ingreso por insuficiencia cardiaca a los 78 días de la coronariografía (sin haber presentado nueva clínica anginosa ni elevación de marcadores cardiacos) y el segundo, mientras dormía en su domicilio a los 325 días de la coronariografía. Un paciente (RFF = 0,92) reingresó a los 70 días de la coronariografía por un nuevo episodio de angina de reposo y se le practicó una intervención coronaria percutánea (ICP) sobre la lesión previamente estudiada al comprobarse una clara progresión angiográfica de la estenosis. No se registró ningún episodio de infarto agudo de miocardio durante el seguimiento al año. Un 97,2% de los pacientes permaneció libre del evento combinado mayor durante el año de seguimiento. Las curvas de supervivencia se muestran en la figura 2.
Fig. 2. Curvas de supervivencia para los distintos eventos analizados (método de Kaplan-Meier). ICP: intervencionismo coronario percutáneo.
Doce pacientes (11,3%) reingresaron en el primer año de seguimiento. Únicamente 5 de ellos reingresaron por causa cardiaca (4,7%). En 2 casos se repitió la coronariografía con la ICP anteriormente descrita en uno de ellos y mejoría angiográfica de la lesión estudiada en otro, sin presencia de lesiones significativas.
DISCUSIÓN
El presente trabajo muestra el buen pronóstico de una serie consecutiva de más de 100 pacientes ingresados por SCA en los que, por tener lesiones angiográficamente moderadas como única posible causa del cuadro clínico, no se realizó revascularización con base en la cifra de RFF obtenida mediante el estudio con guía de presión. El estudio es la serie consecutiva de pacientes más larga publicada hasta la actualidad en la que la RFF se ha empleado para decidir la revascularización de las únicas lesiones que podrían ser causa de un SCA. En un estudio previo13 en el que se incluyó a 124 pacientes con SCA, se utilizó la RFF para decidir también la revascularización de lesiones angiográficamente moderadas. A diferencia de nuestro estudio, en un 28% de los casos se trataron en el mismo procedimiento otras lesiones significativas que probablemente eran la causa de la clínica del paciente.
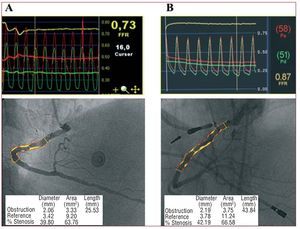
La RFF obtenida mediante guía intracoronaria de presión ha demostrado utilidad tanto en la valoración de lesiones angiográficamente moderadas1-10 como, recientemente, para decidir la revascularización en lesiones angiográficamente significativas14. La mayoría de estos estudios se han realizado en pacientes con cardiopatía isquémica estable, pero se ha cuestionado el valor de la guía de presión en la valoración de lesiones en el SCA3,11,15,16. En la práctica diaria, el SCA es la más frecuente indicación de coronariografía. El manejo invasivo precoz de esta afección y la disponibilidad de la coronariografía hacen que una gran parte de estas exploraciones se realicen sin un test de isquemia previo. En hasta un 6-10% de las coronariografías realizadas por SCA pueden observarse lesiones moderadas o ausencia de lesiones significativas17. A esta cifra se añade un número de casos no determinado en los que el hallazgo puede consistir en lesiones crónicas o enfermedad difusa no relacionada con el SCA y lesiones de dudosa significación funcional en otras localizaciones del árbol coronario. En nuestra experiencia, la angiografía no fue suficiente para discriminar la repercusión funcional de las lesiones analizadas (fig. 3).
Fig. 3. Ejemplo de 2 pacientes con síndrome coronario agudo y sendas lesiones en coronaria derecha. A: estenosis larga en coronaria derecha cuantificada en el 39,8% y RFF significativa (0,73). B: estenosis en coronaria derecha cuantificada en el 42,2% y RFF no significativa (0,87).
La decisión de revascularizar lesiones de significación moderada puede realizarse en la propia sala de hemodinámica teniendo en cuenta las variables clínicas y angiográficas disponibles o apoyarla con una prueba funcional invasiva durante el propio procedimiento o con pruebas no invasivas, y aplazar la toma de decisiones y una posible revascularización para una segunda intervención. En este contexto, en un pequeño estudio18 la RFF obtenida con guía de presión en el momento de la coronariografía mostró beneficios en la reducción de costes con igualdad de eventos clínicos a largo plazo respecto a la gammagrafía isotópica en pacientes con lesiones dudosas y SCA.
Aunque no hay suficiente evidencia científica para avalar su empleo, la guía intracoronaria de presión se usa cotidianamente para determinar la significación funcional de lesiones en el SCA7,10,13,14,19. Las dudas sobre la validez de la guía de presión en el SCA se justifican, por una parte, por los cambios transitorios en la microcirculación en las primeras horas del SCA (presencia de trombo, disfunción microvascular isquémica, contusión miocárdica)20 que pueden limitar de forma temporal la respuesta vasodilatadora al fármaco suministrado, lo que ocasiona una sobrestimación de la RFF por no lograrse la hiperemia máxima. Por otra parte, el carácter dinámico de las lesiones impide que la guía de presión sea capaz de predecir la progresión de la estenosis estudiada.
En nuestra serie no se observaron eventos adversos directamente atribuibles a las lesiones estudiadas y no revascularizadas, excepto un caso de necesidad de revascularización en el seguimiento. De acuerdo con las recomendaciones vigentes en el SCA, la práctica habitual de anticoagular y antiagregar en el momento del ingreso y mantener tras el alta la doble antiagregación, junto con el tratamiento con estatinas12, sin duda favorece la estabilización de unas lesiones en las que, por los propios criterios de selección, la estenosis no es importante, el flujo es normal y no hay datos angiográficos de inestabilidad.
En nuestro estudio, de las 127 lesiones estudiadas, 1 (0,8%) precisó revascularización durante el seguimiento porque el grado de estenosis había progresado respecto al momento en que se realizó la valoración funcional. Ya se había publicado un caso similar11. El caso cursó como un nuevo reingreso por angina de reposo sin infarto ni otro evento mayor. En el 99,2% de las lesiones restantes, aunque no se realizó coronariografía en el seguimiento, la favorable evolución clínica de los pacientes induce a asumir la estabilidad de las lesiones estudiadas.
El diagnóstico de SCA es fundamentalmente clínico. En nuestra serie, de acuerdo con los criterios de inclusión, todos los pacientes habían sido diagnosticados de SCA por un cardiólogo y la coronariografía se solicitó por esta indicación. A la vista de los hallazgos de la coronariografía, no es descartable que la clínica de alguno de los pacientes incluidos tuviera un origen no coronario. Este hecho, lejos de disminuir el valor de la guía de presión en estos casos, creemos que lo aumenta, pues evita revascularizaciones que deberían considerarse aún más innecesarias.
A partir de los resultados de este trabajo, no es posible ni es el propósito de los autores considerar la RFF medida con guía intracoronaria de presión como el parámetro que, de forma aislada, permite decidir la revascularización de lesiones angiográficamente moderadas en el SCA. En nuestro estudio se excluyeron las lesiones que presentaban signos angiográficos de inestabilidad evidentes. El valor de la guía intracoronaria de presión en presencia de trombo visible, ulceraciones, disecciones o deterioro del flujo coronario no ha sido estudiado, y no se debe utilizar como herramienta de decisión en estas situaciones clínicas. Por los resultados de este trabajo, creemos que la RFF obtenida con la guía intracoronaria de presión es una herramienta útil que, sumada a la angiografía y a la clínica, permite con seguridad no revascularizar a pacientes ingresados con el diagnóstico de SCA y lesiones coronarias moderadas, incluso en caso de duda sobre su posible relación con el cuadro clínico que motivó el ingreso del paciente.
Limitaciones
Más del 80% de los pacientes tenían una troponina normal, lo cual indica que se trata de una población de SCA con bajo riesgo y/o dolor torácico de origen incierto. No obstante, esto no resta validez al estudio, que intenta valorar la RFF como método de respuesta a una duda clínica en un ambiente real, suscitada por el paciente que ingresa en el hospital por dolor torácico, llega a la sala de hemodinámica y presenta una lesión que ofrece dudas al cardiólogo intervencionista.
Como ya se ha comentado, las conclusiones de este estudio sólo son aplicables a lesiones que cumplan las características de las incluidas. No es posible asegurar la validez de la RFF para tomar decisiones en caso de trombo visible, disección o ulceración o un flujo inferior a TIMI 3.
En todas las determinaciones de la RFF se utilizó adenosina intracoronaria. Diversos estudios han mostrado que el grado de hiperemia alcanzado es inferior con esta vía que cuando se utiliza adenosina intravenosa21-24. En todos los estudios publicados hasta la fecha, la dosis de adenosina intracoronaria utilizada ha sido < 250 μg21-25. De hecho, uno de los estudios comparativos publicados encontró que con dosis de 150 μg no se observaban diferencias significativas entre la administración intravenosa y la intracoronaria26. Incluso un estudio reciente ha encontrado que la administración intracoronaria de altas dosis de adenosina en perfusión pueden ser superiores a la administración intravenosa para asegurar la obtención de hiperemia máxima27. Nuestro grupo utiliza habitualmente dosis > 300 μg de adenosina intracoronaria, sin evidencia de efectos adversos y con una cuidadosa técnica en su administración y cálculo de la RFF. Creemos improbable una sobrestimación significativa de las cifras de RFF obtenidas. Por otra parte, dado el objetivo del estudio (comprobar la seguridad de no revascularizar determinadas lesiones con base en la RFF obtenida), pequeñas sobrestimaciones de la RFF no modificarían las conclusiones.
Es imposible descartar que en alguno de los casos incluidos la lesión causal fuera otra distinta de la estudiada que no ocasionara siquiera una estenosis moderada. Tampoco puede descartarse, como se comenta en la discusión, una causa distinta de la cardiaca en el cuadro clínico de alguno de los pacientes incluidos. Creemos que estos aspectos no restan validez al estudio. Incluso en esa minoría de pacientes el trabajo respondería a la pregunta de si es válido utilizar la RFF en lesiones moderadas consideradas como potencial causa (acertadamente o no) en pacientes diagnosticados (acertadamente o no) de SCA para evitar innecesarias revascularizaciones.
CONCLUSIONES
Como en la cardiopatía isquémica estable, en el SCA la reserva fraccional de flujo obtenida mediante guía intracoronaria de presión puede ser una herramienta útil para evitar revascularizaciones innecesarias de lesiones coronarias angiográficamente moderadas, siempre que hayan sido cuidadosamente seleccionadas para excluir los casos con signos angiográficos de inestabilidad.
ABREVIATURAS
RFF: reserva fraccional de flujo.
SCA: síndrome coronario agudo.
Full English text available from: www.revespcardiol.org
Correspondencia: Dr. R. López Palop.
Vía Láctea, 38. Urbanización la Glorieta. 30110 Churra. Murcia. España.
Correo electrónico: mlopezs@meditex.es
Recibido el 25 de agosto de 2009.
Aceptado para su publicación el 20 de enero de 2010.