Sacubitrilo-valsartán tiene demostrada eficacia en disminuir las hospitalizaciones y las muertes por insuficiencia cardiaca en los ensayos clínicos, y los datos de práctica clínica real corroboran su efectividad y su seguridad. Asimismo su uso temprano durante la hospitalización, incluso en pacientes con insuficiencia cardiaca de inicio y/o sin tratamiento previo, también parece ser seguro y recomendable para simplificar el tratamiento del paciente y facilitar la transición de cuidados. También tiene un efecto favorable sobre el remodelado cardiaco, como demuestran los resultados del estudio PROVE-HF, que es mayor con un inicio temprano y a dosis más altas en estudios observacionales.
Información sobre el suplemento: este artículo forma parte del suplemento titulado «Controversias para una nueva era en el tratamiento de la insuficiencia cardiaca», que ha sido patrocinado por Novartis.
Palabras clave
El tratamiento durante la hospitalización es muy relevante para el pronóstico a corto y largo plazo de los pacientes con insuficiencia cardiaca (IC) con fracción de eyección del ventrículo izquierdo (FEVI) reducida. El ingreso hospitalario es el momento idóneo para decidir iniciar, cambiar o titular la medicación del paciente con insuficiencia cardiaca, bien sea de inicio o que haya sufrido una descompensación.
La decisión de iniciar o suspender, cambiar o titular la medicación recae en el médico que atiende al paciente, y se suelen incluir factores clínicos como el grado de congestión, hemodinámicos como la presión arterial y la frecuencia cardiaca y analíticos como la función renal e iones.
No se dispone de datos sólidos, del tipo de ensayos clínicos específicos, sobre el inicio del tratamiento con bloqueadores beta, inhibidores de la enzima de conversión de la angiotensina (IECA)/antagonistas del receptor de la angiotensina II (ARA‑II) o antagonistas de la aldosterona durante el ingreso hospitalario, aunque los datos derivados de los ensayos clínicos arrojan un beneficio precoz del uso del tratamiento1. Esto también se deduce de los datos del estudio PARADIGM con sacubitrilo-valsartán (SV), en el que se aprecia una disminución de los eventos clínicos en los pacientes que habían tenido ingresos recientes2. Este beneficio precoz de los fármacos es fundamental porque actúan en el periodo más vulnerable del paciente tras el alta, en el que la mortalidad es mayor3, hasta 6 veces mayor durante el primer mes.
El inicio del tratamiento durante el ingreso se asocia con una mayor adherencia al tratamiento tras el alta. Esto es particularmente evidente con los antagonistas de la aldosterona, en los que el inicio después del alta es significativamente menor si los pacientes no lo hubieran iniciado durante el ingreso o en el momento del alta. Por lo tanto, se trataría de un mecanismo más para evitar la inercia terapéutica.
Con base en los datos del registro PINNACLE de 11.064 pacientes con IC y FEVI reducida, 1.851 (17%) sufrieron un empeoramiento de la IC en un tiempo promedio de 1,5 años desde el diagnóstico. Estos pacientes tuvieron más riesgo de mortalidad y reingreso por IC a los 2 años, y se apreció un menor uso de los fármacos recomendados por las guías de práctica clínica en IC, tanto antes como después del ingreso por descompensación4.
La mayoría de los ingresos por IC corresponden a descompensaciones, lo que significa que muchos pacientes ya deberían tener el tratamiento médico instaurado. Sin embargo, dependiendo de la situación del paciente, puede ser necesario interrumpir, titular, añadir o cambiar el tratamiento. El estudio TRANSITION5 se diseñó para probar la seguridad del tratamiento con SV durante el ingreso hospitalario por IC. Se incluyó a 993 pacientes aleatorizados a tratamiento con SV antes del alta (n = 497) o inmediatamente después (n = 496); el 28,8% de los pacientes tenían IC de inicio6. Tras 10 semanas de tratamiento, no hubo diferencias significativas en cuanto a la dosis alcanzada en ambos grupos ni en la incidencia de eventos adversos6. De hecho, los predictores para alcanzar la dosis recomendada de 97/103 mg/12 h al seguimiento fueron: tener IC de inicio, presión arterial sistólica (PAS) ≥ 120 mmHg, edad < 65 años, FG > 60 ml/min/1,73 m2, no tener fibrilación auricular y haber iniciado el tratamiento con la dosis de 49+51 mg/12 h7.
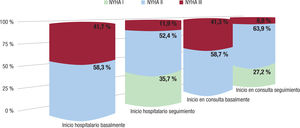
Los pacientes de la práctica clínica habitual, a diferencia de los ensayos clínicos, no están seleccionados; sin embargo, datos similares se han observado en estudios observacionales de la práctica clínica8 en pacientes tratados con SV desde el ingreso hospitalario. En el estudio observacional SAVE-RLife de pacientes con IC con FEVI reducida tratados con SV, de una muestra de 231 pacientes incluidos, el 20,8% iniciaron el tratamiento durante el ingreso. El cambio en la clase funcional observado en los pacientes que iniciaron el tratamiento durante la hospitalización o después fue similar, como se puede ver en la figura 1. La incidencia de eventos adversos, considerando empeoramiento de la función renal, hiperpotasemia o hipotensión sintomática o no, fue similar en ambos grupos.
Beneficios de la (re)evaluación terapéutica durante el ingreso por insuficiencia cardiaca
| • Disminución del riesgo de reingreso a corto y medio plazo |
| • Disminución de la mortalidad a largo plazo |
| • Adecuación del tratamiento a las guías de práctica clínica |
| • Aumento de la adherencia al tratamiento por parte del paciente |
| • Evita la inercia terapéutica, si el tratamiento se inicia durante el ingreso |
Clase funcional de la New York Heart Association (NYHA) al inicio y al último seguimiento de pacientes con inicio del tratamiento durante la hospitalización o en consulta. La media de seguimiento de los pacientes (n = 48) con inicio durante la hospitalización fue de 218 (128-455) días, mientras que la media de seguimiento de los pacientes con inicio del tratamiento en la consulta (n = 183) fue 338 (215-563) días.
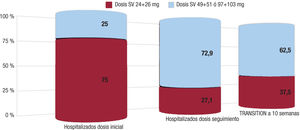
En cuanto a la dosis de SV alcanzada en los pacientes hospitalizados, objetivo principal en el estudio TRANSITION, también fue parecida en ambos grupos. Se alcanzó las dosis media o alta en el 62,5% de los pacientes a las 10 semanas, frente al 72,9% en el estudio SAVERLife, aunque el seguimiento es mayor en este último estudio, como se puede apreciar en la figura 2.
En el total de la población del estudio los predictores para alcanzar la dosis media o alta, frente a los que se mantuvieron en la dosis baja fueron: menor edad (63,5 frente a 69,4 años; p = 0,004), la etiología no isquémica (el 43,6 frente al 65,3%; p = 0,002), no tener fibrilación auricular (el 31 frente al 46,7%; p = 0,02), tener una PAS ≥ 110 mmHg (el 17 frente al 39,7%; p = 0,001) y no tener un FG < 60 ml/min (el 30,1 frente al 44%; p = 0,038).
Primer ingreso por insuficiencia cardiaca y pacientes sin tratamiento previoEl primer ingreso por IC de un paciente es muy importante, ya que se determina si el paciente tiene FEVI reducida o conservada, y establecer precozmente el tratamiento es crucial.
En los estudios conocidos recientemente, TRANSITION5 y PIONEERHF9, se utiliza por primera vez SV en pacientes con IC de inicio durante el ingreso hospitalario. En el estudio PARADIGM10 se incluyó por seguridad un periodo de prueba con IECA/ARA‑II antes de iniciar el tratamiento con SV, plasmándose en las guías su uso tal cual. La mayoría de los pacientes con IC de inicio son también sin tratamiento previo, es decir, que recibieron tratamiento con SV sin haber recibido previamente un IECA/ARA‑II. No todos los pacientes con IC de inicio son sin tratamiento previo porque pueden haber tomado previamente IECA/ARA‑II por alguna otra indicación, como la hipertensión arterial.
El PIONEER-HF9 es el estudio en que se demostró que el SV disminuye la concentración de NT-proBNP en mayor medida que el enalapril en pacientes con IC aguda descompensada (un –46,7 frente al –25,3%; hazard ratio [HR] = 0,71; intervalo de confianza del 95% [IC95%], 0,63-0,81; p < 0,001). Se incluyó a 881 pacientes (440 tratados con SV y 441 con enalapril). Lo más relevante es que el 34% de los pacientes tuvieron su primer ingreso por IC y se les inició el tratamiento directamente con SV. Además, el 36% eran afroamericanos, lo que avala su seguridad en este grupo étnico más susceptible se sufrir angioedema. El tratamiento se instauró en pacientes con PAS ≥ 100 mmHg y se tituló conforme al protocolo, a diferencia del TRANSITION5, en el que se hizo a criterio del clínico responsable y con PAS ≥ 110 mmHg. Por último, cabe resaltar la disminución de la mortalidad cardiovascular u hospitalización por IC (el 15,2 frente al 9,2%; HR = 0,58; IC95%, 0,39-0,87; p = 0,007), así como de las rehospitalizaciones (el 8,5 frente al 13,6%; HR = 0,61; IC95%, 0,40-0,63; p = 0,021), como objetivos secundarios del PIONEER-HF11. Esto refuerza la importancia del inicio precoz del tratamiento, en este caso del SV, al igual que sucedió en el paciente estable en el estudio PARADIGM10. Asimismo, el subanálsis predefinido del subgrupo de pacientes con IC de debut del estudio PIONEER-HF mostró una reducción significativa de los niveles de NT-proBNP con respecto a enalapril, así como un descenso mayor con respecto al grupo de pacientes que ingresaron por descompensación.
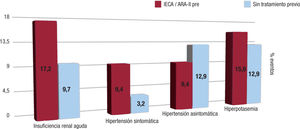
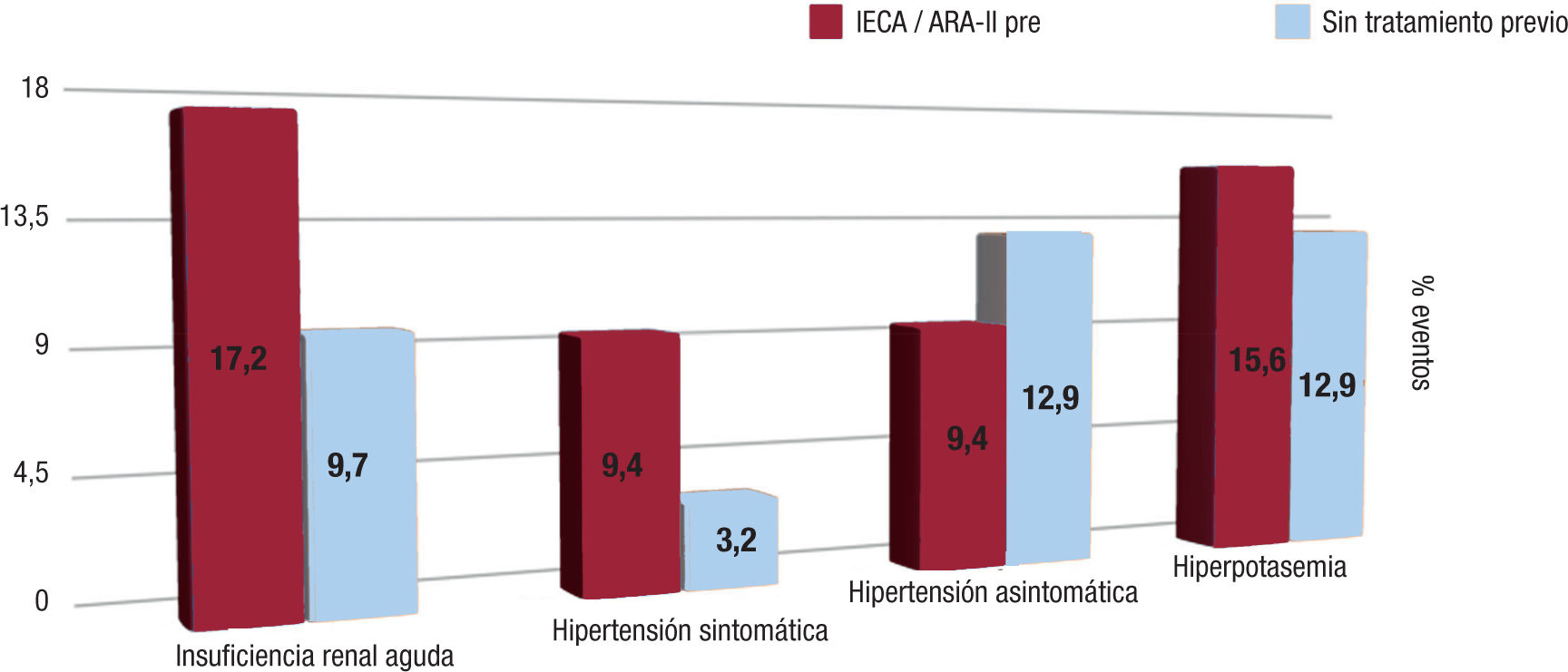
En el estudio SAVE-RLife también se incluyó a pacientes sin tratamiento previo, donde se objetivó que no presentaron más eventos adversos (empeoramiento de la función renal, hipotensión o hiperpotasemia) que los pacientes que tomaban previamente IECA/ARA-II.
El remodelado y el impacto del tratamiento precozLa función ventricular puede fluctuar según determinantes como la enfermedad de base y elementos modificadores de la progresión de la enfermedad, entre los que puede estar el tratamiento. Parece claro que los pacientes con un diagnóstico de IC inferior a los 12 meses y los de etiología no isquémica tienen más probabilidad de mejoría de la función ventricular a corto plazo12. Sin embargo, en un subanálisis del estudio PARADIGM, la respuesta clínica de los pacientes tratados con SV es independiente de la etiología13.
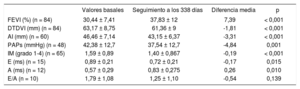
Parámetros ecocardiográficos basales y al seguimiento de los pacientes tratados con SV (n = 84)
| Valores basales | Seguimiento a los 338 días | Diferencia media | p | |
|---|---|---|---|---|
| FEVI (%) (n = 84) | 30,44 ± 7,41 | 37,83 ± 12 | 7,39 | < 0,001 |
| DTDVI (mm) (n = 84) | 63,17 ± 8,75 | 61,36 ± 9 | -1,81 | < 0,001 |
| AI (mm) (n = 60) | 46,46 ± 7,14 | 43,15 ± 6,37 | -3,31 | < 0,001 |
| PAPs (mmHg) (n = 48) | 42,38 ± 12,7 | 37,54 ± 12,7 | -4,84 | 0,001 |
| IM (grado 1-4) (n = 65) | 1,59 ± 0,89 | 1,40 ± 0,867 | -0,19 | < 0,001 |
| E (ms) (n = 15) | 0,89 ± 0,21 | 0,72 ± 0,21 | -0,17 | 0,015 |
| A (ms) (n = 12) | 0,57 ± 0,29 | 0,83 ± 0,275 | 0,26 | 0,010 |
| E/A (n = 10) | 1,79 ± 1,08 | 1,25 ± 1,10 | -0,54 | 0,139 |
AI: aurícula izquierda; DTDVI: diámetro telediastólico del ventrículo izquierdo; FEVI: fracción de eyección del ventrículo izquierdo; IM: infarto de miocardio; PAPs: presión arterial pulmonar sistólica.
En el estudio SAVE-RLife, de los 84 pacientes en los que se realizó ecocardiografía después de iniciar el tratamiento con SV, siempre transcurridos al menos 6 meses, se apreció una mejoría de la función ventricular, disminución del tamaño de la aurícula izquierda y disminución de la insuficiencia mitral, entre otros parámetros ecocardiográficos, que se muestran en la tabla 2. El impacto del tratamiento con SV en la insuficiencia mitral secundaria ya se ha descrito en el estudio PRIME, en el que se aleatorizó a 118 pacientes a recibir SV o valsartán y se observó una reducción significativa en la gravedad de la IM, tanto por el orificio regurgitante efectivo (–0,058 ± 0,095 frente a –0,018 ± 0,105 cm2; p = 0,032) como por el volumen regurgitante (diferenciamedia, –7,3 ml; IC95%, –12,6 a –1,9; p = 0,009) en los pacientes tratados con SV14.
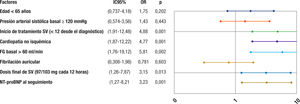
Cuando se analizan los factores asociados con un remodelado inverso favorable (estimando como tal un aumento del 5% de la FEVI), se aprecia que los pacientes que alcanzaron una mayor dosis de SV y los que iniciaron el tratamiento precozmente en los primeros 12 meses desde el diagnóstico de la IC tenían mayor probabilidad de mejora de la FEVI (figura 4), así como los pacientes con etiología no isquémica, aquellos con mejor función renal (FG > 60 ml/min/1,73 m2) o en los que el NT-proBNP desciende más.
En el estudio PROVE-HF15 se evaluó el remodelado ventricular en pacientes tratados con sacubitrilo-valsartán mediante ecocardiografía, basal, a los seis meses y al año. Los pacientes presentaron mejoría significativa de todos los parámetros, con un incremento medio de la FEVI de 9,4% (8,8-9,9%; IC95%), asociada también a la disminución de los niveles de NT-proBNP15. Asimismo la FEVI mejoró también en los pacientes de novo/sin tratamiento previo un 12,8% (11,05-14,5%; IC95%), los pacientes que no alcanzaban niveles de NT-proBNP para entrar en el PARADIGMHF un 9,4% (8,6-10,3%; IC95%), así como en los pacientes que no llegaron a la dosis objetivo de sacubitrilo-valsartán un 9,4% (8,4-10,3%; IC95%).
ConclusionesSi bien estos estudios no tienen como objetivo principal la muerte o el reingreso por IC, las guías de práctica clínica incorporarán probablemente las evidencias aportadas por los estudios PIONEER y TRANSITION. De hecho, un consenso de expertos ha actualizado las recomendaciones de la guía clínica de la ESC de 2016. Este consenso establece que, con base en la evidencia aportada por los estudios PIONEER y TRANSITION, el inicio del SV en lugar de un IECA o un ARA‑II puede considerarse para pacientes hospitalizados con IC de novo o IC descompensada para reducir el riesgo a corto plazo de eventos adversos y simplificar el tratamiento (al evitar la necesidad de titular el IECA primero y luego cambiar a SV). Asimismo, tampoco es necesaria la determinación previa de péptidos natriuréticos antes de iniciar el tratamiento en este subgrupo de pacientes, que ya tiene un alto riesgo de eventos16.
En cuanto al remodelado, tanto los datos obtenidos del estudio PROVE-HF15 como los obtenidos en estudios observacionales, muestran un mejor resultado cuando el tratamiento se inicia precozmente desde el diagnóstico de la enfermedad, por lo que puede ser particularmente relevante empezar el tratamiento con sacubitrilo-valsartán desde el ingreso hospitalario y tenerlo en cuenta durante la transición alta y el seguimiento en los meses posteriores.
Conflicto de interesesNo se declara ninguno.
Información sobre el suplementoEste artículo forma parte del suplemento titulado «Controversias para una nueva era en el tratamiento de la insuficiencia cardiaca», que ha sido patrocinado por Novartis.