Los datos del ensayo clínico PARADIGM-HF y otros estudios relevantes en insuficiencia cardiaca con fracción de eyección reducida (IC-FEr) demuestran que los pacientes que etiquetamos de «estables» (la mayoría en clase funcional II de la NYHA y sin ingresos recientes por insuficiencia cardiaca [IC]) en realidad presentan un pronóstico clínico muy desfavorable, ya que tienen una gran incidencia de ingresos por IC y/o mortalidad cardiovascular (un 25% en los siguientes 3 años). Además, la mayoría de los pacientes con IC-FEr que sufren muerte súbita no presentan un gran deterioro de su capacidad funcional. Por lo tanto, la «falsa sensación de estabilidad clínica» no implica buen pronóstico ni ausencia de progresión de la enfermedad. En el estudio PARADIGM-HF, que incluyó a pacientes en su mayoría estables en clase funcional II de la NYHA, el tratamiento con sacubitrilo-valsartán redujo de manera significativa el riesgo de muerte e ingreso por IC frente a enalapril. De manera muy llamativa, este redujo también muy significativamente el riesgo de muerte súbita. Tradicionalmente, el desfibrilador automático implantable (DAI) es el método más eficaz disponible para reducir las muertes súbitas en estos pacientes. Sin embargo, no protege del 100% de las muertes súbitas en esta población. Hasta un 50% de los pacientes portadores de DAI pueden sufrir un evento de muerte súbita por diversos mecanismos. Este es un ejemplo de por qué se debería intensificar el tratamiento médico durante la fase de estabilidad clínica, que constituye el contexto del que proviene la inmensa mayoría de la evidencia científica contrastada. Por esto se debe actuar con todo el peso de la evidencia una vez se diagnostique IC-FEr al paciente, sin esperar a la aparición de un problema agudo. La inercia terapéutica y el retraso en la actuación a solo cuando el deterioro clínico sea evidente solamente lleva al «empirismo desesperado». Sin embargo, en la práctica clínica real la penetración de fármacos como el sacubitrilo-valsartán sigue siendo relativamente baja pese a que se cumplan los criterios de indicación que marcan las guías de consenso, hecho que sin duda debe ser motivo de reflexión.
Información sobre el suplemento: este artículo forma parte del suplemento titulado «Controversias para una nueva era en el tratamiento de la insuficiencia cardiaca», que ha sido patrocinado por Novartis.
Palabras clave
La práctica clínica moderna se apoya cada vez más en actos clínicos respaldados por resultados provenientes de estudios controlados que afortunadamente nos proporcionan mayor certeza sobre la seguridad y la eficacia de nuestro proceder clínico. De este tipo de estudios, surgen las recomendaciones tipo A o B en las guías de práctica clínica. Desafortunadamente, gran parte de nuestros actos clínicos en el área cardiovascular siguen siendo fruto de recomendaciones de expertos o incluso fruto de nuestra propia experiencia1,2.
La actitud clínica frente a un problema se basa en un delicado equilibrio entre riesgo y beneficio. En las enfermedades cardiovasculares, la respuesta clínica frente a un problema «agudo» ha demostrado resultados beneficiosos en situaciones como síndromes coronarios agudos y arritmias. Esta actitud reactiva, muy ligada a una medicina hospitalaria, es un comportamiento muy extendido en nuestra profesión médica, en la que en muchas ocasiones, ante la ausencia de un problema agudo o emergente, se opta por decisiones conservadoras. Desgraciadamente, este enfoque conservador no parece el más adecuado para el manejo de situaciones crónicas, donde un enfoque preventivo es crucial para evitar la progresión de la enfermedad y la aparición de complicaciones. Este enfoque es el requerido para situaciones clínicas paucisintomáticas como la hipertensión arterial o la diabetes mellitus, en las que es frecuente la inercia terapéutica3-6.
El espejismo de la insuficiencia cardiaca estable. la necesidad de un cambio de actitudEn el campo de la IC-FEr, los avances en cuanto a diagnóstico, estratificación de riesgo y tratamiento han sido muy importantes en las últimas 3 décadas. La llegada de los inhibidores de la enzima de conversión de la angiotensina (IECA), los antagonistas del receptor de la angiotensina II, los bloqueadores beta y los antialdosterónicos ha supuesto una reducción de la morbimortalidad asociada con este síndrome7. Aun así, la morbimortalidad asociada con la IC sigue siendo muy alta y supera a la mayoría de las neoplasias8. Así pues, la mortalidad a 5 años supera en la mayoría de los casos el 50% y los ingresos hospitalarios por IC aguda ya suponen la causa más importante de ingresos de mayores de 65 años9.
En IC, y emulando lo que sucede en otro tipo de situaciones, los clínicos seguimos manteniendo un enfoque dirigido a paliar o solucionar problemas agudos o emergentes. A pesar de que la evidencia en la que se basan las recomendaciones de práctica clínica procede de pacientes en situación de estabilidad clínica, la mayoría de nosotros seguimos actuando solo ante situaciones «emergentes», para las que no hay evidencia clínica sólida.
Sacubitrilo-valsartán en insuficiencia cardiaca estable: una oportunidadLos estudios en la práctica clínica demuestran que todavía hay un margen de mejora significativo en cuanto a la adherencia a las guías internacionales sobre el uso de los fármacos para la IC-FEr. Por ejemplo, la tasa de uso de sacubitrilo-valsartán es de tan solo el 12,8% de los pacientes que cumplen los criterios de las guías internacionales10. Existen diversos motivos a los que se podría atribuir este bajo uso de fármacos que reducen mortalidad e ingresos en estos pacientes, entre los que se podría incluir: inercia terapéutica, sobrecarga asistencial o argumentar que el «paciente está estable».
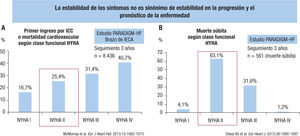
Los pacientes con disfunción sistólica del ventrículo izquierdo que son etiquetados como «estables» serían habitualmente aquellos en clase funcional de la New York Heart Association (NYHA) I-II y sin ingresos recientes por IC. El ensayo clínico PARADIGM-HF mostró que estos pacientes en NYHA II no deberían ser considerados estables, ya que en el brazo de enalapril hasta un 25% de los pacientes tuvieron un ingreso por IC o muerte de causa cardiovascular en un seguimiento de 3 años11(figura 1A). Además, los pacientes en NYHA II son especialmente susceptibles a la muerte súbita12. Asimismo, el estudio PARA- DIGM-HF mostró que la mayoría de las pacientes que padecen una muerte súbita están en NYHA II (figura 1B). Este estudio demostró que el sacubitrilo-valsartán frente al enalapril reduce un 20% la muerte súbita y un 21% la muerte por empeoramiento de la IC11.
La falsa sensación de estabilidad del paciente en NYHA II. A: el riesgo de ingresos por insuficiencia cardiaca o mortalidad cardiovascular de los pacientes en NYHA II con función sistólica reducida según el ensayo PARADIGM-HF (en el brazo de enalapril). B: los pacientes en NYHA II con función sistólica reducida son los más susceptibles a sufrir muerte súbita según el ensayo PARADIGM-HF. ICC: insuficiencia cardiaca congestiva; IECA: inhibidores de la enzima de conversión de la angiotensina; NYHA: clase funcional de la New York Heart Association.
La doble inhibición del receptor de la angiotensina y de la neprili- sina permite el bloqueo del eje renina-angiotensina, que promueve a su vez el aumento de péptidos natriuréticos que poseen efectos bene ficiosos, como favorecer la diuresis y la vasodilatación, entre otros13. La muerte súbita disminuyó un 20% adicional en los pacientes asignados a sacubitrilo-valsartán en comparación con el brazo de enalapril en el ensayo PARADIGM-HF11. Si consideramos muerte súbita la que sucede en las primeras 24 h desde el inicio de los síntomas, múltiples causas podrían estar implicadas, como las arritmias ventriculares, pero también asistolia, disociación electromecánica, shock cardiogénico u otros.
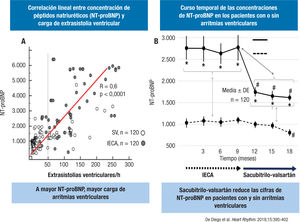
Dos estudios prospectivos (con seguimiento antes y después de sacubitrilo-valsartán idéntico) han explorado el efecto del sacubi- trilo-valsartán en las arritmias ventriculares de pacientes portadores de DAI. En estos estudios se empleó la monitorización del DAI a distancia, que evita la pérdida de eventos arrítmicos14,15. En ambos casos, los pacientes estaban en una fase de tratamiento con IECA y se documentaba la carga de extrasistolia ventricular y las incidencias de taquicardia ventricular sostenida o no sostenida y de descargas apropiadas. Posteriormente, se procedía a cambiar el IECA por sacubitrilo- valsartán y se realizaba un seguimiento temporal idéntico. Los 2 estudios observaron una reducción de arritmias ventriculares y de descargas apropiadas en la fase de tratamiento con sacubitrilo-valsar- tán. Los valores de péptidos natriuréticos (NT-proBNP) se correlacionaron con la incidencia de arritmias ventriculares14, de manera que los pacientes con arritmias ventriculares presentaron cifras de péptidos natriuréticos más altas (figura 2). El sacubitrilo-valsartán redujo las concentraciones de péptidos natriuréticos y esto se relacionó con una reducción en las arritmias ventriculares.
Los péptidos natriuréticos y las arritmias ventriculares. A: la correlación lineal entre la concentración de péptidos natriuréticos y la carga ventricular por extrasistolia ventricular. B: los pacientes con arritmias ventriculares presentaban cifras de NT-proBNP más altas; el sacubitrilo-valsartán redujo los valores de NT-ProBNP en pacientes con y sin arritmias ventriculares. IECA: inhibidores de la enzima de conversión de la angiotensina; SV: sacubitrilo-valsartán.
Tanto los estudios en modelos experimentales con animales como los estudios clínicos han mostrado que la doble inhibición del receptor de la angiotensina y de la neprilisina reduce más el remodelado ventricular que la simple inhibición del eje renina-angiotensina con IECA14-17.
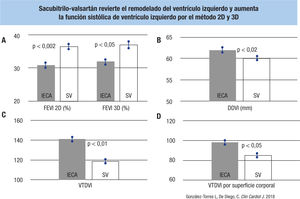
En la figura 3 se ilustra una mejoría de la función sistólica del ventrículo izquierdo del ~5% después de iniciar el sacubitrilo-valsartán, documentada tanto por el método 2D (cuantificado por el método de Simpson biplano) como por ecocardiograma 3D con cálculo automático de la función sistólica, que minimiza la variabilidad interobservadores. Además, se observó una disminución del tamaño diastólico del ventrículo izquierdo y de los volúmenes diastólicos del ventrículo izquierdo con sacubitrilo-valsartán.
Sacubitrilo-valsartán y el remodelado del ventrículo izquierdo en 250 pacientes con función sistólica reducida (seguimiento, 9 meses). A: la mejoría de la FEVI tanto con el método 2D como con el método 3D (con cálculo automático de la FEVI) con sacubitrilo-valsartán. B: la disminución del diámetro diastólico del ventrículo izquierdo (DDVI) con sacubitrilo-valsartán. C y D: la disminución del volumen telediastólico del ventrículo izquierdo (VTDVI) y el volumen telediastólico ajustado a la superficie corporal del paciente con sacubitrilo-valsartán. FEVI: fracción de eyección del ventrículo izquierdo; IECA: inhibidores de la enzima de conversión de la angiotensina; SV: sacubitrilo-valsartán.
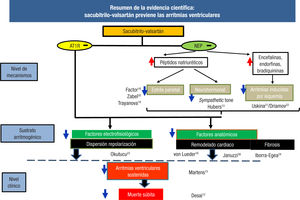
En la figura 4 se resume toda la evidencia científica disponible sobre el efecto protector del sacubitrilo-valsartán contra las arritmias ventriculares y la muerte súbita. Esta evidencia se describe en 3 niveles: de mecanismos, de sustrato arritmogénico y clínico.
La inhibición de la neprilisina promueve el aumento de los péptidos natriuréticos, lo que disminuye el estrés parietal18-20 y el tono simpático13, ambos mecanismos implicados en la génesis de arritmias. Por otro lado, la inhibición de la neprilisina aumenta las ence- falinas y las bradiquininas, lo que protege de las arritmias inducidas por la isquemia21,22. En el sustrato arritmogénico hay 2 factores principales implicados en el origen de las arritmias: los factores electro- fisiológicos (como la dispersión de la repolarización) y los factores anatómicos (como el remodelado cardiaco o la fibrosis). Se ha observado que el sacubitrilo-valsartán disminuye la dispersión de la repolarización23, revierte el remodelado cardiaco16 y reduce la fibrosis24 en comparación con el uso de IECA. Todo ello conlleva una disminución de las arritmias ventriculares14,15 y, por ende, de las muertes súbitas12.
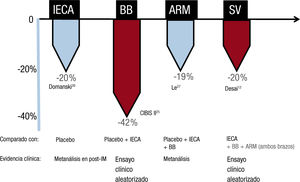
Fármacos para la insuficiencia cardiaca con función sistólica reducida y su efecto en la prevención de la muerte súbita. optimización del tratamiento antes y después de implantar un desfibriladorLos bloqueadores beta y el sacubitrilo-valsartán son los 2 fármacos con la evidencia científica más sólida respecto a la reducción adicional de las muertes súbitas. En el caso de los bloqueadores beta25 y el sacubitrilo-valsartán11, la evidencia proviene de ensayos clínicos alea- torizados, los de mayor robustez científica. Esto subraya la importancia de optimizar apropiadamente a nuestros pacientes. Por el contrario, los 1ECA y los antagonistas del receptor de mineralocorticoides han demostrado una disminución de la muerte súbita en metanálisis, pero no en ensayos clínicos aleatorizados fuera del ámbito del posinfarto de miocardio26,27(figura 5).
La reducción adicional de las muertes súbitas con los tratamientos farmacológicos para la insuficiencia cardiaca. Se adjunta la evidencia clínica: metanálisis o ensayo clínico. Se expone frente a los comparadores del estudio. Nótese que los BB y el SV exhiben el mayor nivel de evidencia, con ensayos clínicos aleatorizados que demuestran una disminución de las muertes súbitas en los pacientes con FEVI reducida. Por el contrario, los IECA y los ARM poseen cierta evidencia en este sentido basada en metanálisis, pero no hay ensayos clínicos que demuestren disminución de las muertes súbitas con IECA o ARM fuera del contexto del posinfarto agudo de miocardio. ARM: antagonistas del receptor de mineralocorticoides; BB: bloqueadores beta; FEVI: fracción de eyección del ventrículo izquierdo; IECA: inhibidores de la enzima de conversión de la angiotensina; SV: sacubitrilo-valsartán.
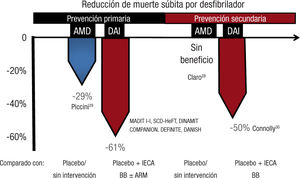
El DA1 es el método disponible más eficaz para reducir la muerte súbita28-31 cuando está indicado según la guía vigente para pacientes con función sistólica < 35% después de al menos 3 meses de tratamiento farmacológico optimizado31. Sin embargo, aun siendo el desfi- brilador el método más efectivo, no previene el 100% de las muertes súbitas en estos pacientes. El DA1 puede prevenir una muerte súbita por taquicardia ventricular sostenida, una fibrilación ventricular o una asistolia gracias a su función de marcapasos asociada. Por el contrario, no podría prevenir una muerte súbita por una tormenta arrítmica que agote la batería del desfibrilador o tras múltiples descargas que desemboquen en un shock cardiogénico o una disociación electromecánica. De hecho, los principales ensayos clínicos más conocidos que han sentado las indicaciones de un desfibrilador en las guías internacionales han obtenido una reducción de la muerte súbita con el desfibrilador de entre el 50 y el 61% (figura 6). Es decir, hasta un 39-50% de los pacientes portadores de un desfibrilador continúan falleciendo por muerte súbita según los principales ensayos clínicos31.
La reducción de las muertes súbitas con el desfibrilador frente a fármacos antiarrítmicos. El DAI, aun siendo el método más efectivo y que supera claramente a los fármacos antiarrítmicos como la AMD, no protege del 100% de las muertes súbitas, como ilustra la figura basada en datos de los principales ensayos clínicos de DAI. Hasta un 39-50% de los pacientes sufren una muerte súbita siendo portadores de un DAI. AMD: amiodarona; ARM: antagonistas del receptor de mineralocorticoides; BB: bloqueadores beta; DAI: desfibrilador automático implantable; IECA: inhibidores de la enzima de conversión de la angiotensina.
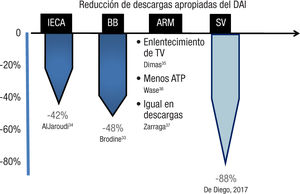
Una vez se ha implantado un DAI a un paciente, la tarea de prevención de muerte súbita no ha terminado. Una adecuada optimización de los fármacos para la 1C sigue siendo crucial en estos pacientes. Como se sabe, múltiples descargas del desfibrilador presentan un efecto deletéreo en los pacientes y, por lo tanto, hay que evitar las descargas del dispositivo salvo que sean estrictamente necesarias. La figura 7 muestra cómo los fármacos para 1C reducen las descargas apropiadas del desfibrilador. En particular, una vez más, los bloqueadores beta y el sacubitrilo-valsartán son los que más reducen las descargas apropiadas del desfibrilador por la disminución de las arritmias ventriculares que presentan estos pacientes14,32-37.
La disminución de descargas apropiadas del desfibrilador con la optimización adecuada de los fármacos para la insuficiencia cardiaca con FEVI reducida. Nótese que los BB y el SV reducen de manera significativa las descargas de DAI. ARM: antagonistas del receptor de mineralocorticoides; BB: bloqueadores beta; FEVI: fracción de eyección del ventrículo izquierdo; IECA: inhibidores de la enzima de conversión de la angiotensina; SV: sacubitrilo-valsartán; TV: taquicardias ventriculares.
J. Núñez declara que ha recibido honorarios por consultoria de Novartis, Boehringer Ingelheim y Pfizer, y honorarios por ponencias de Novartis, Boehringer Ingelheim y Rovi. C. de Diego no declara ninguno.
Información sobre el suplementoEste articulo forma parte del suplemento titulado «Controversias para una nueva era en el tratamiento de la insuficiencia cardiaca», que ha sido patrocinado por Novartis.