Palabras clave
INTRODUCCION
La insuficiencia cardiaca se ha convertido, en los últimos años, en uno de los problemas más importantes de salud pública en los países desarrollados, tanto por el aumento progresivo de su incidencia como por las grandes repercusiones de tipo personal, social y económico que supondrá en un futuro cercano1,2. En la actualidad afecta a más de 22 millones de personas en todo el mundo3 y constituye la tercera causa de muerte por enfermedad cardiovascular, además de ser una importante causa de morbilidad y carga hospitalaria4.
En este contexto, la estimulación biventricular se presenta como un tratamiento alternativo para los pacientes con insuficiencia cardiaca y sus beneficios se han demostrado en ensayos prospectivos aleatorizados5-11. Los estudios realizados ponen de manifiesto beneficios en términos de clase funcional, calidad de vida y distancia recorrida en el test de los 6 min5-7 y, más recientemente, se ha demostrado la disminución de la mortalidad global11 y la morbilidad y la mortalidad por insuficiencia cardiaca12.
Los beneficios de la resincronización cardiaca dependen, sin embargo, no sólo de una cuidadosa selección de los pacientes, sino también de la posición final de los electrodos, particularmente del causante de la estimulación del ventrículo izquierdo (VI). Diversos estudios experimentales13 y en humanos14-16 demuestran una estrecha relación entre el lugar de estimulación y la magnitud de la respuesta de la función ventricular a la terapia de resincronización cardiaca. De este modo, los datos disponibles hasta el momento indican que la localización ideal es la región lateral o posterolateral, ya que es ésta la que presenta el mayor retraso contráctil en presencia de bloqueo de rama izquierda17.
Hoy en día, el implante de un sistema de resincronización cardiaca se puede realizar por vía intravenosa sin dificultades mayores en el 90% de los casos gracias a los avances tecnológicos de los últimos tiempos y a la mayor experiencia de los operadores en la colocación del electrodo ventricular izquierdo3,18-22. Con todo, puede suceder que el implantador se encuentre con dificultades durante el procedimiento en el 10-20% de los casos. Las consecuencias de ello pueden ser serias, puesto que la colocación del electrodo del ventrículo izquierdo en una posición inadecuada es la causa de fracasos de la terapia de resincronización cardiaca. La única alternativa disponible al implante intravenoso es el implante mediante toracotomía, si bien actualmente ésta es una opción no deseable.
Hay diferentes obstáculos que pueden dificultar el proceso de implante del electrodo coronario epicárdico. Las causas principales de fracaso en el implante del electrodo venoso coronario incluyen la imposibilidad de avanzar el catéter guía en el seno coronario (SC), una anatomía venosa desfavorable, la presencia de estimulación frénica y/o inestabilidad del electrodo en la posición seleccionada y, excepcionalmente, la incapacidad de canular el ostium del seno coronario23-25.
En este trabajo analizamos nuestra experiencia con el uso de la técnica de la doble guía durante el implante de electrodos coaxiales en pacientes con anatomía desfavorable tras haber verificado la imposibilidad de implante con la técnica convencional.
MÉTODOS
En el período comprendido entre mayo de 2002 y octubre de 2006 se han tratado, en nuestro centro, 170 pacientes (edad 66,7 ± 9,1 años, 72% varones, clase funcional de la New York Heart Association [NYHA] 2,98 ± 0,56, fracción de eyección 29,2 ± 11,3%, complejo QRS 156,3 ± 26,8 ms) con dispositivos de resincronización cardiaca. En 20 de esos pacientes (11,8%) se recurrió al uso de una segunda guía hidrofílica en paralelo para el implante del electrodo en la vena diana, dada la imposibilidad de implante del electrodo con la técnica convencional. En la tabla 1 se resumen las características clínicas de los pacientes.
Técnica de implante
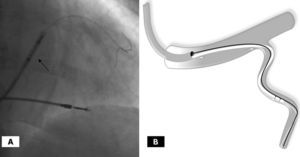
En todos los casos se accedió al SC con un catéter guía de curva amplia (CS-Wide, Guidant Corp., St. Paul, MN, Estados Unidos), un catéter telescópico y una guía hidrofílica (Whisper o PT-Graphic). El uso de una válvula hemostática permitía la manipulación de las guías y la inyección de contraste. En primer lugar, se avanzó el catéter guía en el seno coronario y, tras ser retirado el catéter telescópico, se progresó un catéter balón sobre una guía coronaria y se practicó una senovenografía oclusiva utilizando 4 ml de contraste a 3 ml/s de flujo en proyecciones anteroposterior y oblicua anterior izquierda 20º. Después de la retirada del catéter balón, se accedió con la guía coronaria a la vena diana y se intentó progresar un electrodo coaxial (Easy Track 2, Guidant Corp., St. Paul, MN, Estados Unidos) sobre una guía coronaria. Se consideró que había fracaso de la técnica de implante convencional en los casos en que, una vez posicionada la guía en la vena seleccionada, no fue posible avanzar el electrodo a ella, documentándose el retroceso del catéter guía de forma repetida. Una vez comprobada la imposibilidad de avance del electrodo, se indagó mediante angiografía selectiva la naturaleza del obstáculo y, posteriormente, se recurrió a la inserción en la vena diana de una segunda guía hidrofílica, recubierta con polímero (Whisper o PT-Graphic), reintentando el avance del electrodo (fig. 1). Durante esta maniobra, un segundo operador controlaba la segunda guía con el objeto de evitar su progresión indeseada, mientras que el primer operador realizaba el implante de la forma habitual. Tras implantar el electrodo, la segunda guía fue retirada sin dificultad y se procedió a la retirada del catéter guía, tras sustituir la guía que ocupaba la luz del electrodo por una guía de finalización.
Fig. 1. A: muestra el catéter guía próximo a la desembocadura de la vena y 2 guías hidrofílicas, una en el interior de la luz del electrodo (flecha) y otra en paralelo. B: diagrama ilustrando el catéter guía con 2 guías exteriorizadas y el electrodo en la vena diana.
RESULTADOS
El electrodo se implantó en una vena lateral del ventrículo izquierdo en 18 casos (90%), en un ramo secundario ascendente, con trayecto en la pared libre del ventrículo izquierdo, de una vena con desembocadura próxima al ostium del SC en uno (5%) y en una vena anterolateral (tributaria de la interventricular anterior) en uno (5%). El diámetro medio de la vena diana fue de 4,4 ± 1,3 mm.
La presencia de una válvula de Tebesio restrictiva y fenestrada fue, en 2 pacientes, la causa de la falta de soporte del catéter guía durante el implante. En uno de los casos no se pudo avanzar el catéter guía más allá del ostium del SC por la presencia de una válvula de Tebesio de gran tamaño y restrictiva, que cubría el 95% del orificio. En el otro caso, la guía pasó a través de una fenestración de la válvula de Tebesio que, debido a su pequeño diámetro, no permitía el acceso del catéter guía. En ambos casos, con la ayuda de una segunda guía hidrofílica en paralelo, se pudo implantar el electrodo sin un soporte adecuado del catéter guía.
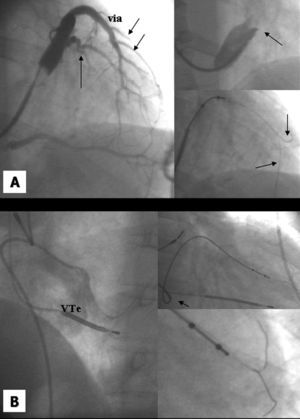
Otro factor anatómico que limitó el avance del catéter guía en el interior del sistema venoso coronario fue la presencia de una válvula de Vieussens prominente (2 pacientes). En estos casos, aunque la guía coronaria superó con cierta dificultad la válvula de Vieussens, ésta no permitió la progresión del catéter guía y/o electrodo. La introducción de una segunda guía en paralelo posibilitó la apertura de dicha válvula y proporcionó el soporte adecuado para el implante del electrodo en la vena diana. La figura 2 ilustra dos ejemplos de falta de soporte del catéter guía en relación con la presencia de una válvula de Vieussens restrictiva y una válvula de Tebesio fenestrada, en los que la segunda guía fue decisiva para implantar con éxito el electrodo.
Fig. 2. A. Senovenografía oclusiva que muestra una vena diana lateral (flecha) y la vena interventricular anterior con múltiples venas anterolaterales (flechas). El recuadro superior derecho muestra una imagen amplificada de la válvula de Vieussens muy restrictiva que impedía el avance del catéter guía. En el recuadro inferior se muestran las 2 guías (flechas) que posibilitaron el avance del electrodo. B. Angiografía no selectiva que muestra una válvula de Tebesio muy prominente que impidió el avance de la punta del catéter guía. Con una segunda guía, el electrodo pudo ser implantado en la vena diana, previamente identificada mediante senovenografía de retorno. via: vena interventricular anterior; VTe: válvula de Tebesio.
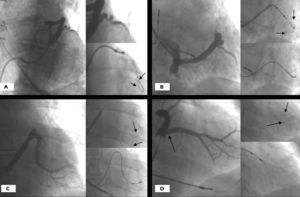
En todos los casos, la vena diana presentó características diversas que dificultaban el implante del electrodo. En 5 pacientes se observó una tortuosidad importante en la desembocadura que se rectificó con el uso de la técnica de la doble guía. En 7 casos, la presencia de un ángulo superior a 90º en la desembocadura de la vena hizo necesaria la utilización de la segunda guía hidrofílica para rectificar la agudeza de éste. Por último, ante la imposibilidad de avanzar un electrodo en una vena diana aparentemente idónea, se intuyó la existencia de una estructura valvular en la desembocadura de la vena (8 pacientes). Esta suposición fue confirmada por la ausencia de muesca al inflar un balón en dicha zona. El avance de la segunda guía, manteniendo la previa, nos permitió desplazar la válvula y facilitar el implante del electrodo. En la figura 3 se exponen ejemplos de obstáculos relacionados con la vena diana en los que se empleó la técnica de la doble guía (tortuosidad extrema de la vena diana en la región próxima a su desembocadura, ángulo pronunciado de la vena diana próximo a la desembocadura y presencia de una válvula venosa restrictiva en la desembocadura de una vena diana de gran tamaño).
Fig. 3. A. Senovenografía oclusiva que muestra una vena diana con tortuosidad múltiple en la que el uso de doble guía (flechas) posibilitó el avance del electrodo. B. Tortuosidad pronunciada de la vena diana donde el implante del electrodo fue posible con doble guía (flechas). C. Ángulo muy pronunciado en la desembocadura que pudo ser solucionado con la doble guía. D. Se intuye la existencia de una válvula venosa (flecha) en la desembocadura de una vena de gran calibre que, tras ser desplazada por una segunda guía (flechas), permitió el avance del electrodo.
En la tabla 2 se resumen las causas que hicieron necesaria la utilización de una guía hidrofílica en paralelo para facilitar el implante del electrodo.
El implante del electrodo en la vena diana fue posible tras avanzar una segunda guía hidrofílica en los 20 pacientes, obteniéndose una amplitud del electrograma local de 15,4 ± 7,9 mV, un umbral de estimulación de 1,8 ± 1,2 V y una impedancia de 1.089 ± 215,9 Ohms. En 3 casos se documentó estimulación frénica con energías superiores a 8 V, sin que fuera preciso recolocar el electrodo, ya que el umbral de estimulación de éste fue < 2 V. En 2 pacientes se produjo un pequeño tatuaje tras la inyección de contraste que se resolvió espontáneamente en pocos minutos y sin impedir el implante. No hubo otras complicaciones durante el procedimiento y, tras un seguimiento de 21 meses (rango, 6-37 meses), el electrodo ha permanecido estable en todos los casos.
DISCUSION
De acuerdo con la evidencia actual, la estimulación en la región lateral del ventrículo izquierdo es la que produce mayor beneficio en la terapia de resincronización cardiaca13-16. Sin embargo, hay diferentes obstáculos en esta región que dificultan la progresión de un electrodo a una vena diana de diámetro y trayecto adecuados. La identificación de estos obstáculos, en ocasiones múltiples, se realiza por medio de la angiografía y, a veces, especialmente en el caso de la válvula de Vieussens, se intuyen por la imposibilidad de progresar el sistema. En estas situaciones, la segunda guía puede ser utilizada tras constatar la imposibilidad de avanzar el electrodo con la técnica convencional26.
La válvula de Tebesio y su tamaño en relación con el diámetro del ostium del SC es la primera dificultad de acceso al sistema venoso coronario, así como la presencia de fenestraciones en ella25. La presencia de dilatación auricular derecha en conjunción con la dilatación del ventrículo izquierdo añade un cierto grado de dificultad, al desplazar el ostium del seno coronario. La válvula de Vieussens, con frecuencia asociada a la presencia de la vena oblicua de Marshall en dicha localización, representa otro impedimento para el avance del sistema, al tener que ser superada «contracorriente»24. La tortuosidad extrema de la vena, una angulación marcada próxima a la desembocadura y/o una válvula venosa prominente en la desembocadura de la vena diana en ocasiones imposibles de visualizar por angiografía son otros obstáculos anatómicos que limitan la progresión del catéter guía y, por tanto, el soporte necesario para la progresión del electrodo26.
La técnica de la doble guía es una maniobra que ha sido utilizada en el árbol arterial coronario con otras finalidades, tales como l a estabilización del balón en el tratamiento de reestenosis intra-stent27, así como para el avance de un stent coronario premontado en caso de anatomía desfavorable y la protección de ramos secundarios en el tratamiento de bifurcaciones. Asimismo, también ha sido utilizada para facilitar la navegación en otros territorios vasculares, como es el caso del sistema nervioso central28. No obstante, en el sistema venoso coronario, su uso ha sido únicamente descrito en un paciente con un ángulo marcado en la desembocadura de la vena diana29.
Gracias a diversos avances en la tecnología utilizada durante el implante del electrodo venoso (mejoría en el diseño de los electrodos, guías y catéteres guía) y a la mayor experiencia del médico implantador, es posible alcanzar una tasa de éxito en el implante superior al 90% en la actualidad3,18-22, aunque en al menos un 20% de los casos el implante es laborioso y requiere el uso de técnicas adicionales.
En 169 de 170 pacientes de nuestra serie (99,4%) ha sido posible el implante del electrodo del ventrículo izquierdo con éxito y en ocasiones ha sido necesario aplicar técnicas especiales (técnica de la doble guía, progresión extrema de la guía, uso del catéter balón, etc.)30. En un paciente (0,6%), debido a hipoplasia extrema del ostium del seno coronario, no fue posible el acceso al sistema venoso coronario.
La pretensión de este artículo es describir una técnica simple, reproducible y segura que permite superar diversos aspectos anatómicos desfavorables durante el implante del electrodo venoso ventricular izquierdo. En nuestra experiencia hemos utilizado exclusivamente guías hidrofílicas, recubiertas de polímero, ya que constituyen una plataforma deslizante que facilita el avance del electrodo. En ningún caso hemos observado deterioro del electrodo en relación con la fricción con la segunda guía. Técnicamente, los catéteres guía de 8 Fr permiten el paso de un electrodo y la guía, dejando suficiente luz residual para controlar el procedimiento con inyecciones selectivas de contraste, en caso de precisarlo. Asimismo, durante el implante, la segunda guía debe ser controlada por otro operador para evitar una migración excesiva durante el avance del electrodo.
Es posible que, en el futuro, la aparición de nuevas guías en el mercado permita el avance del electrodo hasta la posición deseada, sin recurrir a maniobras especiales, en un mayor número de casos. Sin embargo, la técnica de la doble guía representa una herramienta más a disposición del médico en el implante de dispositivos de resincronización cardiaca, ya que facilita el acceso a la vena diana en caso de anatomías desfavorables.
CONCLUSIONES
El uso de una segunda guía hidrofílica en paralelo (técnica de la doble guía) es un procedimiento seguro, reproducible y eficaz para el implante del electrodo venoso ventricular izquierdo en pacientes con algún rasgo anatómico desfavorable en la vena diana y/o seno coronario que dificulta el implante.
Véase editorial en págs. 97-100
Correspondencia: Dra. E. Arbelo Lainez.
Crta. General del Centro, 239.
35017 Las Palmas de Gran Canaria. España.
Correo electrónico: elenaarbelo@secardiologia.es
Recibido el 28 de agosto de 2006.
Aceptado para su publicación el 2 de noviembre de 2006.