Los pacientes con un episodio sincopal inexplicable único (ESU) y bloqueo completo de rama del haz de His (BcR) con frecuencia se tratan de manera más conservadora que aquellos con episodios recurrentes (ESR). El objetivo fue analizar si existen diferencias entre pacientes con ESU o ESR y BcR en cuanto al riesgo arrítmico, el rendimiento diagnóstico de las pruebas y los resultados clínicos.
MétodosEstudio de cohorte de pacientes consecutivos con seguimiento medio de 3 años. Fueron estudiados mediante un protocolo escalonado basado en un estudio electrofisiológico y seguimiento con un monitor cardiaco implantable (MCI).
ResultadosDe los 503 pacientes incluidos en el estudio, 238 (47,3%) referían un ESU. El riesgo de síncope arrítmico fue similar en ambos grupos (58,8% ESU frente a 57,0% ESR; p=0,68), también tras ajustar por variables de confusión (HR=1,06; IC95%, 0,81-1,38; p=0,674). No se encontraron diferencias significativas en cuanto a los resultados del estudio electrofisiológico y la rentabilidad diagnóstica del monitor cardiaco implantable. Un total de 141 (59,2%) pacientes con ESU y 154 (58,1%) con ESR requirieron el implante de un dispositivo cardiaco (p=0,797). Tras el tratamiento adecuado, 35 (7%) pacientes presentaron recurrencia del síncope. La tasa de recurrencia y la mortalidad también fueron similares.
ConclusionesLos pacientes con BcR y síncope tienen un alto riesgo de tener una etiología arrítmica, aunque solo hayan presentado un episodio aislado. Los pacientes con ESU y ESR tienen un riesgo arrítmico similar y presentan un pronóstico similar, por lo que no existe una justificación clínica para no tratarlos de la misma manera.
Palabras clave
La arritmia, y específicamente el bloqueo auriculoventricular avanzado (BAVa), es la causa más frecuente de síncope inexplicado en los pacientes con un bloqueo completo de rama del haz de His (BcR)1,2. Sin embargo, en hasta casi un 40% de los casos puede deberse a una causa no arrítmica1,3,4. Las guías de práctica clínica recomiendan o bien un estudio sistemático de la posible causa (con el empleo de un estudio electrofisiológico [EEF] y el implante de un monitor cardiaco [MCI]) o bien el implante empírico de un marcapasos en los pacientes con síncope y BcR1,5. El antecedente de haber sufrido un síncope previos o la presencia de episodios de síncope recurrentes, son características que no se tienen en cuenta de manera específica en estas recomendaciones ni se incluyen en las puntuaciones de riesgo de síncope más comúnmente utilizadas1,6,7. No obstante, en la práctica clínica habitual, los pacientes con un primer episodio de síncope son tratados con frecuencia de forma conservadora y son dados de alta sin que se les haya realizado una evaluación completa o aplicado un tratamiento específico8,9. Es posible que esto se deba a que algunos clínicos partan del supuesto de que el riesgo de eventos adversos mayores es inferior en los pacientes con un primer síncope que en los que tienen síncopes recurrentes. Por ejemplo, en una reciente encuesta de la EHRA, el 79% de los médicos respondieron que optaban por el implante de un MCI en los pacientes de riesgo alto que presentaban síncopes recurrentes, pero no se hizo referencia alguna a los pacientes que presentaban su primer episodio de síncope8. Además, solo un 67% de ellos contemplaban la posibilidad de realizar un EEF a los pacientes con síncope y resultados no concluyentes de otras exploraciones en presencia de un bloqueo bifascicular. Por otro lado, en un estudio reciente que tuvo como objetivo analizar las estrategias diagnósticas y terapéuticas utilizadas en los pacientes con síncope y un BcR, solamente se consideró aptos para la inclusión en el estudio a los pacientes con síncopes recurrentes10.
Son pocos los estudios en los que se ha investigado el riesgo arrítmico y la evolución clínica de los episodios de síncope recurrente, y algunos de los resultados obtenidos han sido contradictorios. Además, hasta donde nosotros sabemos, no ha habido estudios previos en los que se haya evaluado específicamente el posible aumento del riesgo arrítmico en pacientes con un síncope inexplicado y un BcR en función de si se trata de un episodio aislado o recurrente. Nuestra hipótesis es que los pacientes que presentan un primer episodio de síncope podrían tener un riesgo arrítmico similar al de los pacientes con episodios recurrentes y, por consiguiente, no debiera haber diferencias en su forma de tratamiento.
El objetivo de este estudio fue analizar las posibles diferencias de riesgo arrítmico, rendimiento diagnóstico de las exploraciones y resultados clínicos en los pacientes con síncopes inexplicados y BcR en un único episodio en comparación con los pacientes con episodios recurrentes.
MÉTODOSPoblación del estudioSe llevó a cabo un estudio prospectivo observacional de una cohorte de pacientes consecutivos de un hospital de referencia terciario (Hospital Universitari Vall D’Hebron, Barcelona, España). Entre enero de 2010 y octubre de 2021, incluimos a pacientes que fueron hospitalizados por un síncope con BcR y en los que no se alcanzó un diagnóstico definitivo del síncope en la evaluación inicial llevada a cabo en el servicio de urgencias. Excluimos a los pacientes de menos de 18 años, los pacientes que eran portadores de marcapasos o desfibriladores automáticos implantables, los pacientes con una fracción de eyección ventricular izquierda<35% u otra indicación directa para el uso de un desfibrilador automático implantable, los pacientes con comorbilidades graves que hacían impracticable la aplicación del protocolo del estudio (como los que tenían una esperanza de vida inferior a 1 año o mostraban una dependencia completa para las actividades de la vida diaria) y los pacientes que no dieron su consentimiento informado para la realización de algunas de las exploraciones incluidas en el estudio diagnóstico. En mayo de 2022, obtuvimos los datos finales de seguimiento de los pacientes. En el momento de ingreso en el hospital se registraron los datos clínicos de los pacientes, las características del síncope, el manejo terapéutico y el seguimiento. Algunos de los pacientes incluidos en este artículo (n=443) han sido incluidos anteriormente en un estudio destinado a evaluar las diferencias asociadas al sexo en esa población4.
El estudio se atuvo a lo establecido en la Declaración de Helsinki y fue aprobado por el comité de ética de investigación local.
Protocolo del estudioEl manejo de los pacientes se realizó de manera sistemática según el protocolo clínico local4, que se basó en las recomendaciones establecidas en la guía sobre el síncope de la Sociedad Europea de Cardiología (ESC)1,2. De forma resumida, el protocolo de diagnóstico clínico aplicado en el estudio se basa en 3 fases o pasos. El paso 1, previo a la inclusión de los pacientes en el estudio, consiste en la evaluación inicial llevada a cabo en el servicio de urgencias. Los casos en los que no hay un diagnóstico de certeza o de alta probabilidad se consideran episodios de síncope inexplicado, y esos pacientes son ingresados en el hospital bajo monitorización electrocardiográfica (ECG) continua. El paso 2 comporta el ingreso hospitalario bajo monitorización continua del ECG y la aplicación de un EEF invasivo. En el paso 3 se implanta un MCI con posterior monitorización clínica (figura 1). El síncope se trató según las guías de práctica clínica, dependiendo de la etiología confirmada1. Después del alta del hospital, los pacientes fueron objeto de un seguimiento en una consulta ambulatoria de cardiología, y aquellos a los que se había implantado un dispositivo cardiaco fueron seguidos también con la función de seguimiento a distancia correspondiente.
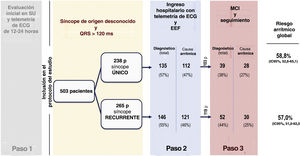
Figura central. Esquema del protocolo diagnóstico y diagrama de flujo de la inclusión de pacientes en el estudio. IC, intervalo de confianza; ECG, electrocardiograma; SU, servicio de urgencias; EEF, estudio electrofisiológico; MCI, monitor cardiaco implantable; p, pacientes; ms, milisegundos.
En el material adicional se presenta una información más detallada sobre el protocolo diagnóstico, el EEF, la monitorización del MCI y el tratamiento.
Definiciones y criterios de valoraciónSe estableció el mecanismo etiológico principal del síncope con certeza o con alta probabilidad según las definiciones incluidas en la guía sobre el síncope de la ESC1 (tabla 1 del material adicional). Los casos de síncope debido a un BAVa o a trastornos de la conducción graves (TCg), disfunción del nódulo sinusal, taquicardia ventricular (TV) o taquicardia supraventricular rápida se consideraron sincopes arrítmicos. Las características de los pacientes fueron analizadas por 2 cardiólogos especializados en síncope para establecer el diagnóstico definitivo según las definiciones. La etiología de los episodios de síncope recurrentes se definió del mismo modo.
Los criterios de valoración del estudio fueron el riesgo de sufrir un síncope arrítmico, el rendimiento de las pruebas diagnósticas, la necesidad de estimulación cardiaca en relación con el síncope, los episodios de sincope recurrentes después del tratamiento y la mortalidad.
Análisis estadísticoLas variables cualitativas se presentan en forma de número absoluto (n) y porcentaje. Las variables cuantitativas continuas se presentan en forma de mediana y rango intercuartílico [RIC]. Las comparaciones de variables numéricas se llevaron a cabo con la prueba de t de Student o la prueba de suma de orden de Wilcoxon, según cuál fuera la distribución de las variables. Se utilizó la prueba de χ2 o la prueba exacta de Fisher para comparar las variables cualitativas según procediera. Se empleó el método de Wald para calcular el intervalo de confianza de las proporciones y las tasas poblacionales. Se estimaron las funciones de supervivencia con el empleo del método de Kaplan-Meier y la comparación de estas funciones se llevó a cabo con la prueba de orden logarítmico (log-rank). Se utilizó la prueba de Manten-Hazel para evaluar la relación lineal entre el número de episodios de síncope previos y el riesgo arrítmico. Se elaboró un modelo riesgos proporcionales de Cox multivariante para evaluar la asociación entre los episodios de síncope previos y el síncope arrítmico y para introducir un ajuste respecto a posibles factores de confusión. Al estimar el modelo de riesgos proporcionales de Cox, verificamos las diferentes interacciones posibles entre pares de variables explicativas y no observamos ningún resultado significativo. Se elaboró un modelo saturado que incluía todas las covariables clínicamente relevantes1,2,4,11–19 y se evaluaron modelos simplificados. Se consideró que el efecto de un factor de confusión era relevante cuando los valores de hazard ratio (HR) con y sin el ajuste respecto al posible factor de confusión diferían en más de un 10%. Finalmente se eligió el modelo más preciso con todas las covariables clínicas relevantes. En todas las pruebas se consideró estadísticamente significativo un valor de p<0,05 Todos los análisis estadísticos se llevaron a cabo con el empleo del programa Stata, versión 15.1.0 (StataCorp LLC College Station, Estados Unidos).
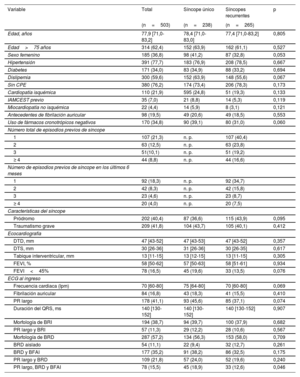
RESULTADOSPoblación del estudioSe incluyó en el estudio a un total de 503 pacientes, de los cuales 265 (52,7%) presentaban un síncope recurrente (grupo de síncope recurrente [GSR]) y 238 (47,3%) no habían tenido episodios previos de síncope (grupo de síncope único [GSU]) antes del episodio de cualificación para el estudio (episodio índice). Las características basales de los pacientes se muestran en la tabla 1. La mediana de edad fue de 77,9 años [RIC: 71,0-83,2] y el 36,8% eran mujeres. No se observaron diferencias clínicas de interés entre los grupos. En el GSR, el 40,4% de los pacientes había tenido 1 episodio previo de síncope, mientras que el 16,6% indicó haber sufrido 4 episodios previos o más de síncope.
Características basales de los pacientes incluidos en el estudio
| Variable | Total | Síncope único | Síncopes recurrentes | p |
|---|---|---|---|---|
| (n=503) | (n=238) | (n=265) | ||
| Edad, años | 77,9 [71,0-83,2] | 78,4 [71,0-83,0] | 77,4 [71,0-83,2] | 0,805 |
| Edad>75 años | 314 (62,4) | 152 (63,9) | 162 (61,1) | 0,527 |
| Sexo femenino | 185 (36,8) | 98 (41,2) | 87 (32,8) | 0,053 |
| Hipertensión | 391 (77,7) | 183 (76,9) | 208 (78,5) | 0,667 |
| Diabetes | 171 (34,0) | 83 (34,9) | 88 (33,2) | 0,694 |
| Dislipemia | 300 (59,6) | 152 (63,9) | 148 (55,6) | 0,067 |
| Sin CPE | 380 (76,2) | 174 (73,4) | 206 (78,3) | 0,173 |
| Cardiopatía isquémica | 110 (21,9) | 595 (24,8) | 51 (19,3) | 0,133 |
| IAMCEST previo | 35 (7,0) | 21 (8,8) | 14 (5,3) | 0,119 |
| Miocardiopatía no isquémica | 22 (4,4) | 14 (5,9) | 8 (3,1) | 0,121 |
| Antecedentes de fibrilación auricular | 98 (19,5) | 49 (20,6) | 49 (18,5) | 0,553 |
| Uso de fármacos cronotrópicos negativos | 170 (34,8) | 90 (39,1) | 80 (31,0) | 0,060 |
| Número total de episodios previos de síncope | ||||
| 1 | 107 (21,3) | n. p. | 107 (40,4) | |
| 2 | 63 (12,5) | n. p. | 63 (23,8) | |
| 3 | 51(10,1) | n. p. | 51 (19,2) | |
| ≥ 4 | 44 (8,8) | n. p. | 44 (16,6) | |
| Número de episodios previos de síncope en los últimos 6 meses | ||||
| 1 | 92 (18,3) | n. p. | 92 (34,7) | |
| 2 | 42 (8,3) | n. p. | 42 (15,8) | |
| 3 | 23 (4,6) | n. p. | 23 (8,7) | |
| ≥ 4 | 20 (4,0) | n. p. | 20 (7,5) | |
| Características del síncope | ||||
| Pródromo | 202 (40,4) | 87 (36,6) | 115 (43,9) | 0,095 |
| Traumatismo grave | 209 (41,8) | 104 (43,7) | 105 (40,1) | 0,412 |
| Ecocardiografía | ||||
| DTD, mm | 47 [43-52] | 47 [43-53] | 47 [43-52] | 0,357 |
| DTS, mm | 30 [26-36] | 31 [26-36] | 30 [26-35] | 0,617 |
| Tabique interventricular, mm | 13 [11-15] | 13 [12-15] | 13 [11-15] | 0,305 |
| FEVI, % | 58 [50-62] | 57 [50-63] | 58 [51-61] | 0,934 |
| FEVI<45% | 78 (16,5) | 45 (19,6) | 33 (13,5) | 0,076 |
| ECG al ingreso | ||||
| Frecuencia cardiaca (lpm) | 70 [60-80] | 75 [64-80] | 70 [60-80] | 0,069 |
| Fibrilación auricular | 84 (16,8) | 43 (18,3) | 41 (15,5) | 0,410 |
| PR largo | 178 (41,1) | 93 (45,6) | 85 (37,1) | 0,074 |
| Duración del QRS, ms | 140 [130-152] | 140 [130-152] | 140 [130-152] | 0,907 |
| Morfología de BRI | 194 (38,7) | 94 (39,7) | 100 (37,9) | 0,682 |
| PR largo y BRI | 57 (11,3) | 29 (12,2) | 28 (10,6) | 0,567 |
| Morfología de BRD | 287 (57,2) | 134 (56,3) | 153 (58,0) | 0,709 |
| BRD aislado | 54 (11,1) | 22 (9,4) | 32 (12,7) | 0,261 |
| BRD y BFAI | 177 (35,2) | 91 (38,2) | 86 (32,5) | 0,175 |
| PR largo y BRD | 109 (21,8) | 57 (24,0) | 52 (19,6) | 0,240 |
| PR largo, BRD y BFAI | 78 (15,5) | 45 (18,9) | 33 (12,6) | 0,046 |
lpm, latidos por minuto; DTD, diámetro telediastólico; DTS, diámetro telesistólico; BFAI, bloqueo fascicular anterior izquierdo; BRI, bloqueo de rama izquierda del haz; FEVI, fracción de eyección ventricular izquierda; mm, milímetros; ms, milisegundos; n. p., no procede; BRD, bloqueo de rama derecha del haz; CPE, cardiopatía estructural; IAMCEST, infarto de miocardio con elevación del segmento ST.
Los valores se expresan en forma de número (%). Las variables cuantitativas se expresan en forma de mediana [rango intercuartílico].
En la figura 1 se resume el diagrama de flujo del estudio. Se estableció un diagnóstico definitivo o muy probable de la causa principal del síncope en 372 pacientes (74%) (73,1% en el GSU y 74,3% en el GSR, p=0,754). En 281 (55,9%) pacientes, el diagnóstico se estableció en el paso 2 (en 252 pacientes después de un EEF positivo y en otros 29 después de que presentaran síntomas correspondientes a los criterios diagnósticos durante su estancia en el hospital). En el paso 3 se estableció un diagnóstico definitivo en otros 91 pacientes más (18,1%) (en 80 gracias a los resultados del MCI y en 11 según los criterios clínicos). En la figura 2A se muestra el diagnóstico de las principales causas de síncope. No se observaron diferencias significativas entre los 2 grupos. En la tabla 2 del material adicional se presenta una información detallada sobre el diagnóstico obtenido en cada uno de los pasos.
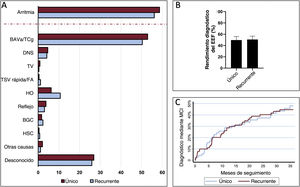
Diagnóstico etiológico y rendimiento de las pruebas diagnósticas. A: diagnóstico etiológico alcanzado en el grupo. La línea roja a trazos separa el diagnóstico general de arritmia de las etiologías específicas. B: rendimiento del estudio electrofisiológico en los distintos grupos. C: Rendimiento diagnóstico acumulativo del MCI a lo largo del tiempo de seguimiento (curva de estimaciones del fallo de Kaplan-Meier). BAVa/TCg, bloqueo auriculoventricular avanzado o trastornos de la conducción graves; FA, fibrilación auricular; HSC, hipersensibilidad del seno carotídeo; EEF, estudio electrofisiológico; MCI, monitor cardiaco implantable; BGC, bajo gasto cardiaco; HO, hipotensión ortostática; DNS, disfunción del nódulo sinusal; TSV, taquicardia supraventricular; TV, taquicardia ventricular.
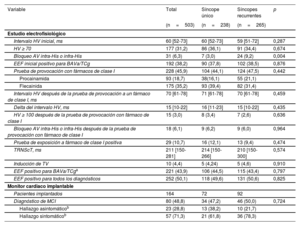
En la tabla 2 se presentan los resultados principales del EEF y del MCI. El EEF tuvo un rendimiento diagnóstico similar en los dos grupos (49,6% en el GSU frente a 50,6% en el GSR, p=0,825) (figura 2B) y un valor predictivo negativo para el síncope arrítmico también similar (74,2% [IC95%, 65,7-81,2] en el GSU frente a 77,1% [IC95%, 69,2-83,5] en el GSR). El rendimiento diagnóstico del MCI fue también similar en los dos grupos (47,2% en el GSU frente a 50,0% en el GSR, p=0,724) (figura 2C).
Estudio electrofisiológico y monitor cardiaco implantable
| Variable | Total | Síncope único | Síncopes recurrentes | p |
|---|---|---|---|---|
| (n=503) | (n=238) | (n=265) | ||
| Estudio electrofisiológico | ||||
| Intervalo HV inicial, ms | 60 [52-73] | 60 [52-73] | 59 [51-72] | 0,287 |
| HV ≥ 70 | 177 (31,2) | 86 (36,1) | 91 (34,4) | 0,674 |
| Bloqueo AV intra-His o infra-His | 31 (6,3) | 7 (3,0) | 24 (9,2) | 0,004 |
| EEF inicial positivo para BAVa/TCg | 192 (38,2) | 90 (37,8) | 102 (38,5) | 0,876 |
| Prueba de provocación con fármacos de clase I | 228 (45,9) | 104 (44,1) | 124 (47,5) | 0,442 |
| Procainamida | 93 (18,7) | 38(16,1) | 55 (21,1) | |
| Flecainida | 175 (35,2) | 93 (39,4) | 82 (31,4) | |
| Intervalo HV después de la prueba de provocación a un fármaco de clase I, ms | 70 [61-78] | 71 [61-78] | 70 [61-78] | 0,459 |
| Delta del intervalo HV, ms | 15 [10-22] | 16 [11-23] | 15 [10-22] | 0,435 |
| HV ≥ 100 después de la prueba de provocación con fármaco de clase I | 15 (3,0) | 8 (3,4) | 7 (2,6) | 0,636 |
| Bloqueo AV intra-His o infra-His después de la prueba de provocación con fármaco de clase I | 18 (6,1) | 9 (6,2) | 9 (6,0) | 0,964 |
| Prueba de exposición a fármaco de clase I positiva | 29 (10,7) | 16 (12,1) | 13 (9,4) | 0,474 |
| TRNScT, ms | 211 [150-281] | 214 [150-266] | 210 [150-300] | 0,574 |
| Inducción de TV | 10 (4,4) | 5 (4,24) | 5 (4,6) | 0,910 |
| EEF positivo para BAVa/TCga | 221 (43,9) | 106 (44,5) | 115 (43,4) | 0,797 |
| EEF positivo para todos los diagnósticos | 252 (50,1) | 118 (49,6) | 131 (50,6) | 0,825 |
| Monitor cardiaco implantable | ||||
| Pacientes implantados | 164 | 72 | 92 | |
| Diagnóstico de MCI | 80 (48,8) | 34 (47,2) | 46 (50,0) | 0,724 |
| Hallazgo asintomáticob | 23 (28,8) | 13 (38,2) | 10 (21,7) | |
| Hallazgo sintomáticob | 57 (71,3) | 21 (61,8) | 36 (78,3) |
BAVa/TCg, bloqueo auriculoventricular avanzado o trastornos de la conducción graves; TRNScT, tiempo de recuperación del nódulo sinusal corregido; EEF, estudio electrofisiológico; MCI, monitor cardiaco implantable; HV, intervalo de His a ventrículo; ms, milisegundos; TV, taquicardia ventricular.
Los valores se expresan en forma de número absoluto (%) o mediana [rango intercuartílico].
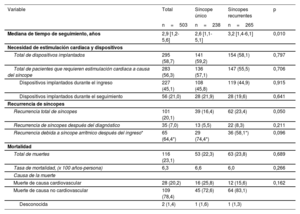
En un total de 295 (58,7%) pacientes había sido necesario el implante de un dispositivo al final del seguimiento (tabla 3), (en la tabla 3 del material adicional se muestra el tipo de dispositivo implantado). En la mayor parte de los pacientes (283 [56,3%] pacientes), la indicación para ello fue una bradicardia relacionada con el síncope. Se implantaron 2 desfibriladores cardiacos implantables y 2 desfibriladores de resincronización cardiaca a causa de una TV. Se trató a 3 pacientes con TV solo con fármacos antiarrítmicos debido a sus comorbilidades. Se implantaron, además, 5 marcapasos a causa de un bloqueo AV postquirúrgico y otros 3 marcapasos debido a una insuficiencia cronotrópica.
Resultados durante el seguimiento
| Variable | Total | Síncope único | Síncopes recurrentes | p |
|---|---|---|---|---|
| n=503 | n=238 | n=265 | ||
| Mediana de tiempo de seguimiento, años | 2,9 [1,2-5,6] | 2,6 [1,1-5,1] | 3,2 [1,4-6,1] | 0,010 |
| Necesidad de estimulación cardiaca y dispositivos | ||||
| Total de dispositivos implantados | 295 (58,7) | 141 (59,2) | 154 (58,1) | 0,797 |
| Total de pacientes que requieren estimulación cardiaca a causa del síncope | 283 (56,3) | 136 (57,1) | 147 (55,5) | 0,706 |
| Dispositivos implantados durante el ingreso | 227 (45,1) | 108 (45,8) | 119 (44,9) | 0,915 |
| Dispositivos implantados durante el seguimiento | 56 (21,0) | 28 (21,9) | 28 (19,6) | 0,641 |
| Recurrencia de síncopes | ||||
| Recurrencia total de síncopes | 101 (20,1) | 39 (16,4) | 62 (23,4) | 0,050 |
| Recurrencia de síncopes después del diagnóstico | 35 (7,0) | 13 (5,5) | 22 (8,3) | 0,211 |
| Recurrencia debida a síncope arrítmico después del ingreso* | 65 (64,4*) | 29 (74,4*) | 36 (58,1*) | 0,096 |
| Mortalidad | ||||
| Total de muertes | 116 (23,1) | 53 (22,3) | 63 (23,8) | 0,689 |
| Tasa de mortalidad, (x 100 años-persona) | 6,3 | 6,6 | 6,0 | 0,266 |
| Causa de la muerte | ||||
| Muerte de causa cardiovascular | 28 (20,2) | 16 (25,8) | 12 (15,6) | 0,162 |
| Muerte de causa no cardiovascular | 109 (78,4) | 45 (72,6) | 64 (83,1) | |
| Desconocida | 2 (1,4) | 1 (1,6) | 1 (1,3) |
Los valores se expresan en forma de número (%) o mediana [rango intercuartílico].
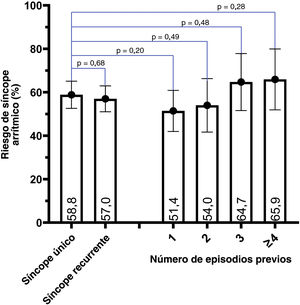
Se identificó un síncope arrítmico en 291 (57,9%) pacientes; en la mayor parte de los casos fue secundario a una bradicardia, sobre todo por un BAVa/TCg (figura 3; tabla 2 del material adicional). En la tabla 4 del material adicional se resumen las diferencias existentes en las características basales entre los pacientes con y sin síncope arrítmico. En la figura 1 del material adicional se muestra el riesgo arrítmico en función del tipo de BcR.
El riesgo arrítmico fue similar en los pacientes con y sin un ESU (58,8% [IC95%, 52,6%-65,1%]) frente a 57,0% [IC95%, 51,0%-62,9%]), lo cual corresponde a una razón de riesgos de 0,97 (IC95% 0,83-1,12) (figura 3). Además, en el modelo de Cox multivariante, tras aplicar un ajuste para los posibles factores de confusión (incluido el tipo de BcR), la presencia de episodios de síncope recurrentes no se asoció a un mayor riesgo de síncope arrítmico (HR, 1,06; IC95%, 0,81-1,38; p=0,674) (tabla 5 del material adicional y figura 1 del material adicional).
Aunque se observó una tendencia lineal entre el número de episodios previos de síncope y el riesgo de síncope arrítmico en el GSR (prueba de MH para la tendencia lineal: 3,9; p=0,0487), no se apreciaron diferencias significativas según el número de síncopes previos en comparación con un ESU (figura 3).
Seguimiento: recurrencias y pronóstico (criterios de valoración secundarios)Se realizó un seguimiento de los pacientes durante una mediana de 2,9 [RIC, 1,2-5,6] años. Después del ingreso hospitalario, un total de 101 (20,1%) pacientes presentaron una recurrencia del síncope (tabla 3). En la mayor parte de ellos (66 pacientes), la recurrencia se produjo antes de que se estableciera la causa del síncope, y de hecho se utilizó para establecer el diagnóstico en el paso 3. La recurrencia se debió a una causa arrítmica en el 74,4% de los pacientes del GSU y en el 58,1% de los pacientes del GSR (p=0,096). Es importante señalar que, una vez determinado el diagnóstico etiológico y establecido el tratamiento apropiado, solo 35 pacientes (7,0%) presentaron otra recurrencia de síncope (13 [5,5%] pacientes del GSU y 22 [8,3%] del GSR, p=0,211), en la mayor parte de los casos a causa de mecanismos ortostáticos o reflejos (tabla 6 del material adicional). La tasa de incidencia de recurrencias en el GSU fue de 1,7 por 100 años-persona y en el GSR fue de 2,2 por 100 años-persona (RTI, 0,76; IC95%, 0,35-1,58).
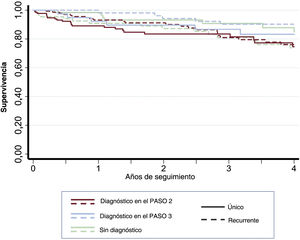
Durante el seguimiento fallecieron en total 116 (23,1%) pacientes, un 78,4% de ellos debido a causas no cardiovasculares (tabla 3). La tasa de mortalidad en el GSU y en el GSR fue de 6,6 por 100 años-persona y 6,0 por 100 años-persona, respectivamente (RTI, 1,12; IC95% 0,76-1,64). En la figura 4 se muestran las curvas de supervivencia de Kaplan-Meier según el momento del diagnóstico para los dos grupos.
Análisis de la supervivencia. Curvas de supervivencia de Kaplan-Meier según el momento del diagnóstico etiológico y según el grupo. No se observan diferencias significativas entre el GSU y el GSR (prueba de orden logarítmico o log-rank p=0,438) en función de que se diagnostiquen en el PASO 2 o en otro momento (log-rank) p=0,081).
En este amplio estudio observacional de cohorte en una población de pacientes con un síncope inexplicado y un BcR, comparamos el riesgo de síncope arrítmico asociado a los antecedentes de episodios sincopales previos. Los principales resultados del estudio son los siguientes: a) la mitad de los pacientes que acudieron por un síncope tenía antecedentes de al menos 1 episodio previo; b) el riesgo de síncope de origen arrítmico es elevado y no difiere en función de los antecedentes de episodios previos; c) El EEF y el MCI aportan un rendimiento diagnóstico similar en los dos grupos; d) no hay diferencias clínicamente trascendentes entre los dos grupos por lo que respecta al pronóstico después de una mediana de seguimiento de 3 años.
Observamos que la mitad de los pacientes referían 1 o varios episodios previos de síncope, y hasta una tercera parte de ellos habían presentado como mínimo 1 episodio en los 6 meses previos. El riesgo de recurrencias de síncope en la población general se ha estimado en entre un 2% y un 30% a lo largo de toda la vida20–23. Sin embargo, es probable que el riesgo sea muy superior en los pacientes con trastornos de la conducción y con una edad media más elevada, como ocurre en nuestro grupo de estudio. De forma análoga, en el estudio B43 y en el ensayo Spritelly recientemente publicado24, en el que se evaluó a pacientes con síncope y bloqueo bifascicular, los pacientes incluidos presentaban una mediana de 2 episodios de síncope previos, y en el estudio ISSUE25, la media del número de episodios de síncope durante los 2 últimos años fue de 3.
El principal resultado de nuestro estudio es que un primer episodio de síncope y BcR se asocia a un riesgo elevado de que exista un origen arrítmico, pero este riesgo es similar al de los pacientes con episodios recurrentes, incluso tras ajustar por a posibles factores de confusión, incluido el tipo de BcR.
Hasta donde nosotros sabemos, no ha habido estudios previos en los que se haya investigado explícitamente esta relación. Disponemos de algunos datos sobre las recurrencias en trabajos previos que se centraron en otros objetivos y que incluyeron un número de pacientes más limitado. En un estudio previo realizado por nuestro grupo, observamos que el tipo de patrón de trastorno de la conducción y el intervalo PR mostraban una asociación con los resultados del EEF. Sin embargo, el número de episodios previos de síncope no mostró correlación con la probabilidad de que el EEF diera un resultado positivo11. A este respecto, Azocar et al.26investigaron el rendimiento diagnóstico de un uso escalonado del EEF y el MCI en una cohorte de 85 pacientes. Estos autores observaron que el riesgo de BAVa era más alto en los pacientes con un PR prolongado o una desviación de eje, pero no observaron diferencias significativas al comparar a los pacientes con episodios únicos o recurrentes. Es de destacar que estos estudios previos no se diseñaron para investigar esta relación, y que no se usaron técnicas estadísticas para evaluar posibles factores de confusión o interacciones. También conviene mencionar que el rendimiento diagnóstico del EEF y del MCI fue similar en los dos grupos. El uso de un MCI permitió establecer el diagnóstico durante el seguimiento en la mitad de los pacientes en los que el resultado del EEF fue negativo. Esta observación respalda los resultados de otros estudios previos sobre la utilidad de una monitorización temprana en los pacientes con un BcR y un EEF negativo, incluso después de un primer episodio de síncope27.
El pronóstico observado fue también similar en los dos grupos. Tal como se preveía, en consonancia con lo indicado por estudios previos, los pacientes sin un diagnóstico en el paso 2 presentaron un riesgo de recurrencia del síncope superior al de los pacientes que fueron diagnosticados en el paso 2 y en los que la primera recurrencia del síncope condujo al diagnóstico final en el paso 3. Después de un diagnóstico etiológico, fueron pocos los pacientes que presentaron nuevas recurrencias (7,0%) y la mayoría de estos episodios fueron secundarios a un mecanismo no arrítmico. Dado que se sabe que la tasa de recurrencias se reduce con el tratamiento1,5,28, esta observación sugiere que los diagnósticos fueron específicos y permitieron orientar de manera efectiva el tratamiento en los dos grupos. El tratamiento apropiado puede explicar también el hecho de que no se observaran diferencias en la mortalidad, a diferencia de lo ocurrido en estudios previos20,22,23.
En definitiva, según los resultados de este estudio, no hay una justificación clínica para no llevar a cabo un estudio diagnóstico completo del síncope, o como alternativa implantar un marcapasos permanente, en los pacientes con un episodio aislado de síncope y BcR. En las futuras directrices y recomendaciones clínicas deberán tenerse en cuenta los resultados de este estudio para mejorar la asistencia de los pacientes y la adherencia a las recomendaciones y para evitar retrasos innecesarios en la aplicación del tratamiento apropiado.
LimitacionesEste estudio tiene ciertas limitaciones. Se trata de un estudio observacional llevado a cabo en un único centro de alto volumen y con una consulta específica para el síncope. Con objeto de reducir al mínimo los posibles sesgos inherentes al diseño del estudio, se incluyó a los pacientes de forma consecutiva. Además, se analizaron los posibles factores de confusión, incluidos los relacionados con un posible sesgo temporal debido al período de inclusión relativamente largo. No se analizaron las razones por las que los pacientes no habían consultado por episodios previos. Los pacientes fueron incluidos en el estudio después del paso 1, por lo que esta serie no corresponde a la etiología global del síncope en esta población, sino más bien a los pacientes en los que no hubo un diagnóstico inicial evidente. No se excluyó a los pacientes con un episodio aislado/único de BcR derecho. A pesar de que el riesgo arrítmico en este subgrupo de pacientes es significativamente inferior al observado en otros tipos de BcR11, el riesgo arrítmico continúa siendo significativo (de aproximadamente 1 de cada 4) y similar en los 2 grupos (figura 1 del material adicional), por lo que la conclusión general de este estudio no debería verse afectada por ello. Además, el tipo de BcR se incluyó como variable en el análisis multivariante. Por otra parte, no se utilizó la prueba de basculación en el protocolo de estudio diagnóstico, debido a su baja especificidad en esta población1. Sin embargo, en pacientes seleccionados, la prueba de basculación podría haber revelado la presencia de una indicación para la estimulación cardiaca1. Además, el estudio no se diseñó para evaluar los factores predictivos del implante de un marcapasos en los 2 grupos.
CONCLUSIONESLos pacientes con un BcR y un síncope inexplicado presentan un riesgo alto de tener una etiología arrítmica, incluso después del primer episodio de síncope. En comparación con los pacientes con episodios de síncope recurrentes, los que presentan un episodio aislado tienen un riesgo arrítmico similar, una tasa de incidencia de recurrencias después del tratamiento similar, un pronóstico similar y un rendimiento de las pruebas diagnósticas similar. Con objeto de garantizar que todos los pacientes reciben el tratamiento correcto en el momento apropiado, las futuras directrices clínicas deberían resaltar la necesidad de usar un manejo similar en los pacientes con un BcR y un síncope inexplicado, con independencia de los posibles antecedentes de síncopes previos.
FINANCIACIÓNEste proyecto fue financiado por ISCIII, CIBER y la Fundació Marató TV3 y cofinanciado por el Fondo Europeo de Desarrollo Regional (ERDF-FEDER).
CONTRIBUCIÓN DE LOS AUTORESJ. Francisco-Pascual preparó el concepto y dirigió el diseño del estudio, llevó a cabo los análisis estadísticos, y diseñó, redactó la propuesta inicial y corrigió el manuscrito; M. Maymi-Ballesteros, C. Badia-Molins y M. Bach-Oller participaron en la obtención y revisión de los datos. N. Rivas-Gándara y B. Benito participaron en la preparación del concepto y revisaron los datos y los resultados. Todos los demás autores participaron en la inclusión de pacientes en el estudio, la obtención de los datos y la revisión del manuscrito. Todos los autores han expresado su acuerdo con el contenido de la versión final del manuscrito.
- -
La arritmia, y específicamente el bloqueo auriculoventricular avanzado paroxístico, es la causa más frecuente del síncope inexplicado en los pacientes con bloqueo de rama del haz. Sin embargo, hasta cerca de un 40% de los casos pueden deberse a una causa no arrítmica.
- -
Las guías de práctica clínica recomiendan o bien un estudio sistemático de la posible causa o el implante de un marcapasos empírico. Sin embargo, muchos pacientes son tratados de una forma más conservadora, en especial si el episodio de síncope es el primero que presenta el paciente.
- -
La mitad de los pacientes que consultan por un síncope y BcR refieren haber tenido como mínimo 1 episodio previo.
- -
En comparación con los pacientes con episodios de síncope recurrentes, los que han tenido un episodio aislado/único tienen un riesgo arrítmico similar, una tasa de incidencia de recurrencias después del tratamiento similar y un pronóstico similar.
- -
Según los resultados de este estudio, no hay una justificación clínica para no llevar a cabo un estudio diagnóstico completo del síncope, o como alternativa implantar un marcapasos permanente, en los pacientes con un episodio aislado/único de síncope y un BcR.
La Unidad de Arritmia de Vall d’Hebron recibe subvenciones para formación posterior a la residencia de Boston Scientific y subvenciones de investigación de Abbott. J. Francisco-Pascual recibe honorarios por asesoramiento y conferencias de Abbott y Microport. N. Rivas-Gándara recibe honorarios por asesoramiento y conferencias de Abbott. B. Benito, J. Pérez-Rodón y A. Santos-Ortega reciben honorarios por conferencias de Abbott. Los demás autores no declaran ningún conflicto de intereses.
Los autores quisieran dar las gracias al personal del departamento de cardiología y de la unidad de arritmias por su apoyo en el manejo, la monitorización y el seguimiento de los pacientes.