Palabras clave
INTRODUCCIÓN
El flujo coronario está subordinado a un complejo mecanismo de regulación multifactorial que actúa sobre los pequeños vasos que componen la microcirculacion1. El estado de la microcirculación es especialmente importante en el contexto de la angioplastia en el infarto agudo de miocardio (IAM) ya que, una vez revascularizada la lesión causante del infarto, determina la calidad de la reperfusión miocárdica2.
El empleo en cardiología intervencionista de las guías intracoronarias con sensores de presión y Doppler ha permitido aplicar el estudio de la fisiología coronaria a la resolución de problemas clínicos. En concreto, estos dispositivos se han aplicado en el diagnóstico de la viabilidad miocárdica en el seno del IAM: una adecuada presión de oclusión en el vaso causante del IAM3 o la recuperación progresiva de la reserva de flujo coronario inicialmente deteriorada tras el infarto4 se han asociado con el mantenimiento de la viabilidad miocárdica. Igualmente, el análisis de las características fásicas del flujo coronario con guía Doppler se ha relacionado con el grado de perfusión miocárdica en el IAM5, con la recuperación de la función contráctil postinfarto6 y, por ende, con el pronóstico de los pacientes7.
Hasta la actualidad, los estudios que relacionan las características del flujo coronario con la viabilidad miocárdica se han realizado en la fase aguda del infarto. Nuestro objetivo es estudiar si, una vez pasada la fase aguda del infarto, el estudio del flujo coronario sigue teniendo valor para analizar la viabilidad miocárdica.
PACIENTES Y MÉTODO
Población del estudio
Los pacientes fueron incluidos de forma consecutiva entre los remitidos al departamento de Cardiología Intervencionista del Hospital do Meixoeiro, bien desde el propio hospital o procedentes de otros centros sin disponibilidad de hemodinámica, con los siguientes criterios: firma de un consentimiento informado donde figuran las características del estudio; primer infarto con elevación del segmento ST, con menos de 1 mes de evolución; enfermedad de 1 vaso, con lesión de novo (> 50% estenosis) sobre la que se practica una intervención coronaria percutánea (ICP) con éxito angiográfico (< 20% de estenosis residual con flujo TIMI 3); alteraciones importantes de la contractilidad segmentaria (acinesia) en la ventriculografía de contraste y, por último, ausencia de reestenosis binaria (estenosis < 50%) en la revisión angiográfica a los 4-6 meses de la ICP.
De los 21 pacientes inicialmente incluidos, finalmente fueron 19 los que constituyeron la población (2 pacientes no pudieron ser revaluados, 1 porque se negó serlo y 1 por haber fallecido de causa no cardíaca).
Antes de realizar la ICP se evaluó la severidad de la lesión mediante el cálculo de la reserva fraccional de flujo coronario (RFF) con guía de presión y de la reserva de flujo coronario (RFC) con guía Doppler. Terminada la ICP, se calculó nuevamente la RFF para valorar el éxito funcional de la revascularización; asimismo, con la guía Doppler se determinaron la RFC y el patrón de flujo coronario. Por último, en el control de seguimiento (4-6 meses post-ICP) se volvieron a estudiar la RFC y el patrón de flujo en la arteria coronaria diana, así como la extensión de la acinesia mediante ventriculografía de contraste.
Intervención coronaria percutánea
La revascularización se realizó con el implante electivo y directo de prótesis intravascular o stent siguiendo las normas habituales en nuestro departamento. El operador eligió el tipo, el diámetro y la longitud del stent implantado. Se empleó la guía Doppler como soporte para la introducción de los dispositivos de angioplastia.
Angiografía cuantitativa
Se realizó un análisis angiográfico cuantitativo (DLX, GE Medical System, Milwakee, Estados Unidos) de la lesión causante del infarto antes y después de la revascularización, así como en el control de seguimiento. Antes de la angiografía se administraron 200 mg de nitroglicerina intracoronaria. Se determinaron los siguientes parámetros: diámetro de referencia del vaso, diámetro mínimo luminal, porcentaje de estenosis y longitud de la lesión.
Por otro lado, la función contráctil ventricular se analizó mediante ventriculografía de contraste en proyección OAD 30°, realizada antes de la ICP y en el control de seguimiento, y se cuantificaron la fracción de eyección (método de Dodge) y la contractilidad segmentaria en el territorio del vaso causante del infarto.
Se analizó la contractilidad segmentaria mediante el método de la línea central. Este método consiste en la división de la silueta cardíaca en 100 segmentos, generados por radios que parten desde el centro de la cavidad hacia su periferia. El movimiento telesistólico de cada segmento se expresa en acortamiento fraccional según su posición en telediástole. Este valor es posteriormente convertido en unidades de desviación estándar (DE) de una media obtenida en una población de referencia normal. El miocadio acinético es el que tiene una contractilidad < -2 DE de la media de referencia. En ventriculografía OAD 30°, la silueta miocárdica que queda delimitada entre el segmento 10 y el 65 corresponde al territorio vascular de la arteria descendente anterior; entre los segmentos 50 y 81 se encuentra definido el territorio vascular de las arterias coronaria derecha y circunfleja. El estado de la contractilidad regional se expresó como porcentaje de superficie miocárdica acinética con respecto al total del territorio dependiente de la arteria causante del infarto.
Nos servimos del estado de la contractilidad regional en el seguimiento para valorar el grado de viabilidad del territorio vascular afectado. Clasificamos a la población en dos grupos según la extensión de acinesia:
- Contractilidad regional preservada (CR+), cuando la superficie acinética era < 30% del área miocárdica dependiente de la arteria causante del infarto.
- Contractilidad regional deteriorada (CR), cuando el porcentaje de acinesia era ≥ 30% del área vascular afectada.
Fisiología del flujo coronario
La fisiología del flujo coronario fue analizada con el empleo de una guía de presión (WaveWire, Cardiometrics, Rancho Cordova, Estados Unidos) y guía Doppler (FloWire, Cardiometrics, Rancho Cordova, Estados Unidos). Estos dispositivos consisten en guías de 0,014 pulgadas dotadas con un sensor que recoge la presión intracoronaria (guía de presión), y con un sensor Doppler de 12 MHz que registra el espectro sistólico y diastólico de la velocidad del flujo sanguíneo (guía Doppler)8. El estado de hiperemia se obtuvo mediante la administración intracoronaria de un bolo de adenosina (Adenocor, Sanofi Winthrop, Barcelona) en dosis de hasta 50 mg.
Evaluación con guía de presión
Mediante la guía de presión se calculó la RFF el cociente entre la presión media distal a la lesión y aórtica en condición de máxima hiperemia, y que representa el flujo coronario que irriga el territorio vascular expresado como porcentaje del que lo haría en ausencia de la lesión.
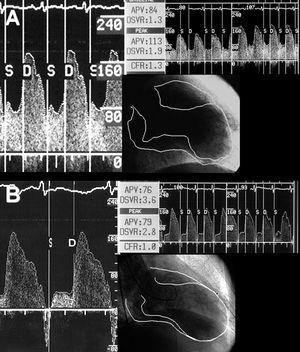
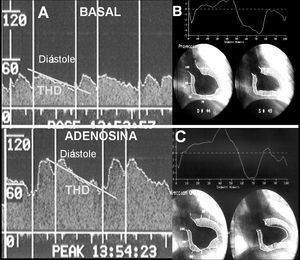
Evaluación con guía Doppler (figs. 1 y 2)
Fig. 1. Patrón de flujo coronario tras revascularización (A) y en el control de seguimiento (B) en un paciente con función contráctil regional que persiste deteriorada en el territorio de la arteria descendente anterior. El componente diastólico del flujo muestra una abrupta disminución de su velocidad pico promediada.
Fig. 2. Evaluación del patrón de flujo coronario de la arteria coronaria derecha en un paciente con recuperación de la función contráctil en la cara inferior en el control de seguimiento (B y C). A diferencia del caso anterior, el tiempo de hemidesaceleración diastólico es más prolongado (A).
Mediante esta guía se estudió la RFC, cociente entre velocidad pico promediada del flujo coronario en hiperemia y en situación basal. Por otro lado, también se cuantificaron las siguientes características fásicas del flujo coronario: velocidad pico promediada del componente diastólico del flujo coronario (cm/s); velocidad pico promediada del componente sistólico del flujo coronario (cm/s) y, por último, el tiempo de hemidesaceleración de la velocidad diastólica del flujo coronario (ms), que consiste en el tiempo en que el máximo de la velocidad pico promediada se reduce a la mitad.
Análisis estadístico
Se trata de un estudio observacional compuesto por dos cortes transversales, en el que a cada paciente se le realizan determinaciones en dos tiempos (inicial y seguimiento) que se comparan en función de un criterio obtenido en el seguimiento. Los resultados se han expresado como media ± DE. Dado el escaso número de efectivos incluidos, no se ha asumido la distribución normal de los datos, por lo que las comparaciones entre grupos se han realizado mediante tests no paramétricos (prueba de Mann-Whitney para las variables numéricas y test exacto de Fisher para las categóricas). Para analizar la evolución de las variables en el seguimiento dentro de cada grupo se realizó la prueba de los rangos con signo de Wilcoxon. Para cada test se consideró significativo un valor de p < 0,05.
RESULTADOS
Clasificación de los pacientes según la contractilidad regional en el control de seguimiento. Características clínicas y angiográficas
Los 19 pacientes que finalmente completaron el estudio fueron divididos en dos grupos, según la extensión regional de miocardio acinético en el control de seguimiento (149 ± 40 días): el grupo CR+, formado por 11 pacientes con una extensión de acinesia del 8 ± 11%; y el grupo CR-, compuesto por los 8 pacientes restantes, con una superficie acinética del 72 ± 16%.
Los dos grupos estudiados no se diferenciaron en las características clínicas y la situación hemodinámica durante la revascularización (presión arterial y frecuencia cardíaca). La única diferencia entre los grupos fue la localización del infarto, con una tendencia más frecuente a la localización anterior en el grupo con CR- (el 75 frente al 27%; p = 0,05) (tabla 1).
En cuanto al análisis angiográfico antes y después de la revascularización, destaca un mayor porcentaje de lesiones localizadas en la arteria descendente anterior en el grupo con CR- (el 88 frente al 27%; p = 0,01). No hubo diferencias en cuanto a la severidad angiográfica y funcional de las lesiones (tabla 2). En el control de seguimiento, el análisis angiográfico no mostró diferencias entre grupos para el grado de estenosis residual.
Análisis funcional de la arteria causante del infarto durante el procedimiento de revascularización
Antes de la revascularización, la evaluación funcional del flujo coronario no mostró diferencias entre los grupos CR+ y CR- para la RFF (0,51 ± 0,24 frente a 0,56 ± 0,27) y la RFC (1,3 ± 0,4 frente a 1,5 ± 0,4).
Tras la revascularización, la RFF fue ≥ 0,90 en 17 de los 19 pacientes finalmente analizados (en los dos casos restantes, un caso por grupo, no se pudo determinar este parámetro por problemas técnicos). Los valores medios de RFF fueron idénticos para los pacientes con CR+ y CR- (0,95 ± 0,04).
El valor de la RFC tras el implante del stent tampoco mostró diferencias significativas entre grupos (1,8 ± 0,5 frente a 2,3 ± 0,5 respectivamente; p = 0,09) (tabla 2).
En cuanto a las características fásicas del flujo coronario, el tiempo de hemidesaceleración diastólico fue significativamente superior en los pacientes con CR+ (628 ± 188 frente a 376 ± 131 ms; p = 0,004 en situación basal, y 639 ± 111 frente a 426 ± 176 ms; p = 0,01 en hiperemia) (fig. 3).
Fig. 3. Comparación del tiempo de hemidesaceleración diastólico entre los pacientes de los grupos CR+ y CR. En el análisis realizado inmediatamente post-ICP, los pacientes del grupo CR+ presentaron un significativo mayor tiempo de hemidesaceleración, tanto en condición basal como en hiperemia. Estas diferencias desaparecen en el control de seguimiento. CR: contractilidad regional; THV: tiempo de hemidesaceleración diastólico.
Análisis funcional del flujo coronario en el control de seguimiento
En el control de seguimiento no se registraron diferencias entre grupos en cuanto al análisis funcional del flujo coronario, ni para la RFC (2,3 ± 0,5 frente a 2,3 ± 0,7, para los grupos CR+ y CR-, respectivamente), ni para las características fásicas del flujo coronario, tanto en condición basal como en hiperemia (fig. 3).
Evolución de los parámetros funcionales del flujo durante el seguimiento (tabla 3)
Las características del flujo coronario de los pacie ntes con contractilidad regional preservada evolucionaron en el seguimiento de forma diferente de las de los que tenían una contractilidad persistentemente deteriorada. En los pacientes con CR+ se produjo un aumento significativo de la RFC entre el valor obtenido tras el implante del stent y el control de seguimiento (1,8 ± 0,5 frente a 2,3 ± 0,5, respectivamente; p = 0,01), cambios que no se produjeron en los pacientes con CR- (2,3 ± 0,5 frente a 2,3 ± 0,7) (fig. 4). La mejoría en el control de seguimiento de la reserva de flujo coronario del grupo con CR+ se debió al aumento de los valores de velocidad pico promediada en hiperemia con respecto al estudio post-ICP, significativo únicamente para el componente diastólico (86,6 ± 42,1 frente a 64,1 ± 23,5 cm/s; p = 0,03).
Fig. 4. Evolución de la reserva de flujo coronario entre la evaluación inicial post-ICP y el control de seguimiento en los pacientes con (A) y sin viabilidad (B).
En ambos grupos de pacientes se registraron diferencias evolutivas en los valores del tiempo de hemidesaceleración diastólica, aunque en sentido contrario, lo que explica la homogeneidad de los registros de ambos grupos en el control de seguimiento. Así, en situación basal, el tiempo de hemidesaceleración diastólico aumentó significativamente en el grupo CR- (376 ± 131 frente a 509 ± 198 ms; p = 0,03) y disminuyó en los pacientes CR+ (628 ± 188 frente a 480 ± 143 ms; p = 0,01).
DISCUSIÓN
El principal hallazgo de este trabajo ha sido que, en el primer mes tras un IAM, el flujo coronario en la arteria causante analizado con guía Doppler posee características diferenciales entre los pacientes con y sin viabilidad en el territorio vascular afectado. Posteriormente, estas diferencias del flujo coronario desaparecen.
Patrón del flujo coronario en la arteria causante del infarto tras la revascularización
En diferentes trabajos se han analizado las características fásicas de la velocidad del flujo coronario en la arteria causante del infarto tras su revascularización en el marco de la angioplastia primaria6,7. Se han descrito dos patrones diferenciados de flujo coronario indicativos de la calidad de la perfusión miocárdica, así como del grado de recuperación de la función contráctil en el seguimiento. El patrón de flujo característico de una escasa perfusión tisular muestra una rápida desaceleración del componente diastólico, junto con un escaso e incluso negativo componente sistólico. Este patrón patológico de la velocidad del flujo se debe al aumento de las resistencias microvasculares y a la disminución del volumen sanguíneo intramiocárdico por el daño isquémico severo9. El deterioro microvascular impide un normal vaciamiento sanguíneo sistólico hacia el sistema venoso, y en el grado máximo de afección, el flujo vuelve de modo retrógrado hacia el vaso epicárdico (componente protosistólico negativo). Por otro lado, el escaso volumen sanguíneo en el miocardio gravemente isquémico tiene como consecuencia un llenado rápido en la fase diastólica, lo que explica el aumento de la pendiente de desaceleración diastólica.
En nuestro estudio, la revascularización no se realizó en la fase aguda del infarto sino en el primer mes. Sin embargo, nuestros resultados continúan confirmando la presencia de un patrón de flujo diferente entre los pacientes con viabilidad en el territorio afectado (mostrado por una menor extensión de acinesia junto con una mayor recuperación de la contractilidad regional en el seguimiento) y los que tienen la alteración de contractilidad más severa y persistente en el seguimiento. El tiempo de hemidesaceleración diastólico fue el único parámetro fásico del flujo coronario diferente en ambos grupos, tanto en condición basal como durante hiperemia: los pacientes con viabilidad presentaban en la arteria causante un tiempo de hemidesaceleración diastólico significativamente mayor, lo que indicaría un mejor relleno sanguíneo miocárdico durante la fase diastólica.
Reserva de flujo coronario en la arteria causante del infarto
La RFC puede encontrarse inicialmente deteriorada tras la revascularización percutánea, a pesar de que el resultado angiográfico sea adecuado10. Este fenómeno es especialmente evidente en el IAM11. Varios son los mecanismos que pueden justificar en este contexto una reserva coronaria patológica tras eliminar la obstrucción epicárdica: el flujo hiperémico en situación basal, el aumento reversible de la resistencia en la microcirculación o microvascular stunning, o el incremento pasivo de las resistencias microvasculares por destrucción tisular y embolización distal de componentes del trombo oclusor.
En nuestro trabajo no hubo diferencias significativas en la RFC entre los pacientes con y sin viabilidad en el estudio realizado post-ICP. Sin embargo, un hallazgo interesante es el incremento de la RFC que se produce en el seguimiento únicamente en el grupo de pacientes con viabilidad, debido básicamente al aumento de la velocidad de flujo en hiperemia. Esta evolución indicaría la presencia de un aturdimiento microvascular inicial y reversible en los pacientes con mayor extensión de miocardio viable.
Aunque de forma global en el grupo no viable la RFC no presentó cambios entre el control inicial y el de seguimiento, analizados de forma individualizada, en la mitad de los casos (4 pacientes) hubo un incremento de la reserva coronaria. La pequeña población estudiada limita la obtención de mayores conclusiones y es posible que en la recuperación de la RFC estén implicados otros factores aparte de la viabilidad. En cualquier caso, parece que hay una diferente evolución de la RFC de la arteria casusante del infarto en función de la viabilidad en su territorio miocárdico, hallazgo que no había sido anteriormente descrito.
Equiparación en el control de seguimiento de las características del flujo coronario en la arteria causante del infarto, independientemente de la preservación de la contractilidad miocárdica
Transcurridos 4-6 meses tras la revascularización, el flujo coronario de la arteria causante se uniformiza, sin que aparezcan diferencias entre los pacientes con función contráctil regional prácticamente conservada y los que presentan una gran superficie de miocardio discinético. Esta equiparación se produce tanto para la RFC como para las características fásicas del flujo, y en concreto para el tiempo de hemidesaceleración diastólico.
Limitaciones
La principal limitación de este estudio es el pequeño número de pacientes, aunque similar al de otros estudios con parecido planteamiento. Dado que el estudio de los patrones de flujo coronario se realizó una vez practicada la ICP, las conclusiones que se obtienen de este trabajo no pueden aplicarse para decidir sobre la revascularización de una lesión en función de la viabilidad de su territorio. Por otro lado, la realización de la ICP dentro del primer mes del infarto puede ser una limitación, ya que se trata de un período lo suficientemente amplio como para que se pudieran producir variaciones espontáneas en las características del flujo coronario. Otra limitación es la diferente localización del infarto en los grupos con y sin viabilidad y, por tanto, la presencia de diferentes arterias implicadas; teniendo en cuenta que el patrón de flujo puede presentar diferencias según la arteria coronaria, no se puede descartar que en las diferencias entre patrones de flujo viable y no viable pudieran influir las características particulares de cada arteria analizada. Además, como consecuencia del pequeño tamaño muestral no es posible calcular un valor de corte para el tiempo de hemidesaceleración que fuera predictor de viabilidad. Por último, las conclusiones obtenidas no se aplican necesariamente a ciertos grupos de pacientes (diabéticos, con enfermedad multivaso, disfunción ventricular severa, etc.) que han sido escasamente incluidos o bien excluidos del estudio.
CONCLUSIONES
En pacientes con infarto de miocardio reciente, el flujo coronario de la arteria causante muestra un patrón diferente en función de la extensión de miocardio viable. En el análisis precoz posrevascularización, el tiempo de hemidesaceleración diastólico fue la única característica fásica del flujo coronario que diferenció entre territorios vasculares viables y no viables. Transcurridos 4-6 meses de la revascularización, desaparecen las diferencias en las características de flujo coronario entre pacientes con y sin viabilidad. El incremento de la reserva coronaria en el seguimiento de los pacientes con mayor extensión de miocardio viable podría indicar la presencia inicial de un fenómeno reversible de aturdimiento microvascular.
Este trabajo ha sido financiado, en parte, gracias a una Beca de Investigación de la Fundación MAPFRE Medicina.
Correspondencia: Dr. R.J. Ruiz-Salmerón.
Departamento de Hemodinámica y Cardiología Intervencionista. Hospital Clínic i Provincial.
Villarroel, 170. 08036 Barcelona. España.
Correo electrónico: rjruiz@clinic.ub.es