El propósito de este artículo es presentar los resultados del trasplante cardiaco desde que se inició esta modalidad terapéutica en España en mayo de 1984.
MétodosSe ha realizado un análisis descriptivo de todos los trasplantes cardiacos realizados hasta el 31 de diciembre de 2011.
ResultadosEl número total de trasplantes cardiacos es de 6.528. El perfil clínico medio del paciente que se trasplantó en España en 2011 fue el de un varón de 53 años, diagnosticado de cardiopatía isquémica no revascularizable con depresión grave de la función ventricular y situación funcional avanzada, al que se implantó un corazón de 38 años procedente de un donante fallecido por hemorragia cerebral y con un tiempo en lista de espera de 122 días. El tiempo medio de supervivencia se ha incrementado con los años. Así, mientras en la serie total la probabilidad de supervivencia tras 1, 5, 10 y 15 años es del 77, el 66, el 53 y el 39%, respectivamente, en los últimos 5 años la probabilidad de supervivencia tras 1 y 5 años es del 80 y el 73%, respectivamente. La causa más frecuente de fallecimiento es el fallo agudo del injerto (16%), seguido de infección (15,6%), combinado de enfermedad vascular del injerto y muerte súbita (14%), tumores (12,3%) y rechazo agudo (7,7%).
ConclusionesLa supervivencia obtenida en España con el trasplante cardiaco, sobre todo en los últimos años, lo sitúa como el tratamiento de elección para cardiopatías irreversibles en situación funcional avanzada y sin otras opciones médicas o quirúrgicas establecidas.
Palabras clave
Como es norma de nuestra sección desde 1991, se presenta el análisis descriptivo de los resultados de la actividad trasplantadora realizada en España desde que se inició esta modalidad terapéutica, en mayo de 1984, hasta el 31 de diciembre del año previo a su publicación1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22.
Este registro comprende todos los trasplantes cardiacos (TC) realizados por todos los grupos y en todos los centros (anexo). Por ello, representa de forma fiel la realidad de esta técnica en nuestro país. Apoya su fiabilidad que todos los grupos de trasplante utilicen una base de datos idéntica y consensuada previamente. Este hecho homogeneiza las variables y unifica las posibilidades de respuesta.
MétodosPacientes y centrosEl número de centros que aportan sus datos al registro es 19 (Tabla 1), aunque son 18 los centros que actualmente hacen trasplantes.
Tabla 1. Registro Español de Trasplante Cardiaco 1984-2011. Centros participantes
| 1. Hospital de la Santa Creu i Sant Pau, Barcelona |
| 2. Clínica Universitaria de Navarra, Pamplona |
| 3. Clínica Puerta de Hierro, Majadahonda, Madrid |
| 4. Hospital Marqués de Valdecilla, Santander |
| 5. Hospital Reina Sofía, Córdoba |
| 6. Hospital Universitario y Politécnico La Fe, Valencia |
| 7. Hospital Gregorio Marañón, Madrid |
| 8. Fundación Jiménez Díaz, Madrid |
| 9. Hospital Virgen del Rocío, Sevilla |
| 10. Hospital 12 de Octubre, Madrid |
| 11. Hospital Universitario A Coruña, A Coruña |
| 12. Hospital de Bellvitge, L’Hospitalet de Llobregat, Barcelona |
| 13. Hospital La Paz, Madrid |
| 14. Hospital Central de Asturias, Oviedo |
| 15. Hospital Clínic, Barcelona |
| 16. Hospital Virgen de la Arrixaca, El Palmar, Murcia |
| 17. Hospital Miguel Servet, Zaragoza |
| 18. Hospital Clínico, Valladolid |
| 19. Hospital Vall d’Hebron, Barcelona |
Orden según inicio del primer trasplante.
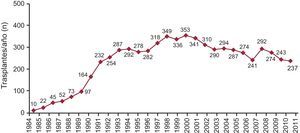
En los más de 25 años de actividad trasplantadora, se han realizado 6.528 TC en total. En la Figura 1 se puede apreciar la distribución del número de TC por año. El 94% de ellos son aislados ortotópicos. En la Tabla 2 se expone la distribución de los TC según el tipo de procedimiento.
Figura 1. Número de trasplantes por año.
Tabla 2. Registro Español de Trasplante Cardiaco 1984-2011. Tipo de procedimiento
| Trasplantes cardiacos de novo | 6.202 |
| Retrasplantes cardiacos | 191 |
| Trasplantes combinados | |
| Corazón-pulmón | 77 |
| Corazón-riñón | 50 |
| Corazón-hígado | 8 |
| Total | 6.528 |
La base de datos consta de 175 variables clínicas con datos del receptor, del donante, quirúrgicos, de inmunosupresión y de seguimiento. Cada año, los centros envían los datos al Director del Registro, que organiza la metodología estadística con la empresa contratada a tal efecto (actualmente ODDS, S.L.). También se organiza periódicamente la auditoría de los centros para control de los datos. La auditoría se realiza mediante una empresa externa independiente que aleatoriza los centros y los TC, extrae una muestra representativa y comprueba la fiabilidad de los datos remitidos.
En 2008 se remitió el Registro al Comité Ético de Investigación Biomédica del Hospital Universitario La Fe de Valencia, que lo aprobó. Por otro lado, se está en vías de registrarlo en el Ministerio de Sanidad, Servicios Sociales e Igualdad para garantizar el cumplimiento de la Ley Orgánica de Protección de Datos 15/1999. Además, se espera que la base de datos esté disponible online en 2013.
EstadísticaLas variables se presentan como media ± desviación estándar y porcentaje. Las curvas de supervivencia se han calculado mediante el test de Kaplan-Meier y la comparación entre ellas, con el método de log rank test. Se ha considerado diferencia significativa si p < 0,05. Los análisis de supervivencia se han realizado sin incluir los retrasplantes ni los trasplantes combinados.
ResultadosPerfil del paciente trasplantadoEl perfil clínico medio del paciente que se trasplanta en España es el de un varón de 53 años, diagnosticado de cardiopatía isquémica o miocardiopatía dilatada idiopática de grupo sanguíneo A o 0. En la Tabla 3 se expone el perfil clínico de los receptores de un TC aislado distribuidos por edad y analizando aparte los retrasplantes.
Tabla 3. Registro Español de Trasplante Cardiaco 1984-2011. Perfil clínico de los receptores según se trate de pediátricos, adultos o retrasplante
| < 16 años | ≥ 16 años | Retrasplantes | |
| Número | 288 | 5.694 | 155 |
| Varones (%) | 62,5 | 81,7 | 78,1 |
| Edad (años) | 6 ± 5,7 | 53,2 ± 11,9 | 50,1 ± 14 |
| IMC | 15,7 ± 4,9 | 25,3 ± 4 | 25 ± 4,1 |
| Etiología de base (%) | CI: 1,4 | CI: 34,4 | EVI: 34,6 |
| MCDi: 34 | MCDi: 29,8 | FAI: 16,3 | |
| Valv.: 0,7 | Valv.: 8,9 | REA: 11,1 | |
| CC: 39,7 | CC: 1,5 | Otras: 38 | |
| Otras: 24,1 | Otras: 25,4 | ||
| Grupo sanguíneo | |||
| A | 54 | 49 | 57 |
| B | 7 | 9 | 8 |
| AB | 4 | 5 | 5 |
| 0 | 35 | 38 | 30 |
| CF III-IV/IV | 68 | 62 | 69 |
| Creatinina > 2 (mg/dl) | 3 | 5 | 27 |
| PAPm (mmHg) | 30 ± 13 | 30 ± 11 | 27 ± 9 |
| RVP (UW) | 3 ± 2 | 2 ± 2 | 2 ± 1 |
| Bilirrubina > 2 (mg/dl) | 18 | 16 | 19 |
| GOT/GPT × 2 (mg/dl) | 22 | 26 | 28 |
| Diabetes mellitus ID | 1 | 14 | 18 |
| HTA | 2 | 28 | 42 |
| Hipercolesterolemia | 3 | 37 | 44 |
| EPOC moderada-severa | 2 | 11 | 7 |
| CCV previa | 28 | 25 | 100 |
| Tratamiento inotrópico | 68 | 34 | 53 |
| Ventilación mecánica | 31 | 10 | 31 |
CC: cardiopatía congénita; CCV: cirugía cardiaca; CF: clase funcional de la New York Heart Association; CI: cardiopatía isquémica; EPOC: enfermedad pulmonar obstructiva crónica; EVI: enfermedad vascular del injerto; FAI: fallo agudo del injerto; GOT (ASAT): aspartatoaminotransferasa; GPT (ALAT): alaninaminostransferasa; HTA: hipertensión arterial; ID: insulinodependiente; IMC: índice de masa corporal; MCDi: miocardiopatía dilatada idiopática; PAPm: presión media de arteria pulmonar; REA: rechazo agudo; RVP: resistencias vasculares pulmonares; UW: unidades Wood; Valv.: valvulopatía.
Los valores se expresan como media±desviación estándar y porcentajes.
Trasplantes combinados no incluidos.
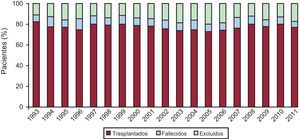
En el año 2011, la mortalidad en lista de espera fue del 5%. Los pacientes excluidos para TC, una vez incorporados a la lista, fueron el 20%. La Figura 2 representa el porcentaje anual de pacientes que, tras ser incluidos en lista de espera, recibieron un TC, fueron excluidos de la lista o fallecieron antes de recibirlo.
Figura 2. Destino de los pacientes una vez incluidos en lista de espera de trasplante cardiaco.
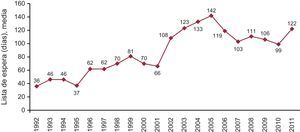
El tiempo medio que tuvieron que esperar los receptores para realizarse el TC en 2011 fue de 122 días. La evolución de los últimos 20 años se puede apreciar en la Figura 3.
Figura 3. Evolución anual de la media de días en lista de espera de los receptores para trasplante cardiaco.
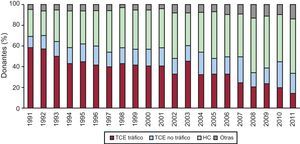
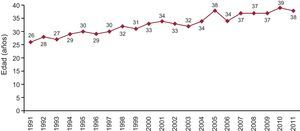
Causa de muerte y media de edad de los donantesLa mayoría de los corazones que se implantan actualmente proceden de donantes fallecidos por hemorragias cerebrales. La media de edad en 2011 fue de 38 años (Figura 4, Figura 5).
Figura 4. Evolución anual de las causas de muerte de los donantes cardiacos. HC: hemorragia cerebral; TCE: traumatismo craneoencefálico.
Figura 5. Evolución anual de la media de años de los donantes cardiacos.
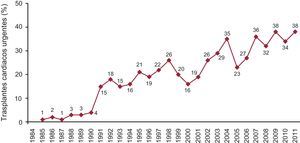
Trasplante urgenteEl porcentaje de indicación de TC urgente en el año 2011 fue del 38%. La Figura 6 ilustra como ha evolucionado esta opción de TC a lo largo de los años.
Figura 6. Evolución anual del porcentaje de trasplantes cardiacos urgentes.
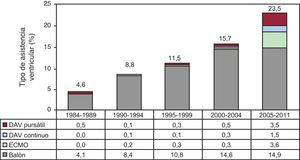
Asistencia ventricularLa proporción de pacientes trasplantados con asistencia se ha incrementado con el tiempo. En los últimos 7 años ha alcanzado el 24%. La distribución por periodos, así como el tipo de asistencia implantada, se puede apreciar en la Figura 7.
Figura 7. Distribución del tipo de asistencia ventricular previa al trasplante, por periodos. DAV: dispositivo de asistencia ventricular; ECMO: oxigenador de membrana extracorpóreo.
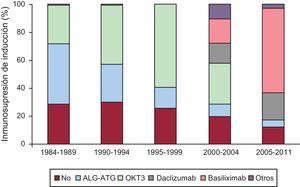
InmunosupresiónA la mayoría de los pacientes que reciben un TC en España se les administra tratamiento inmunosupresor de inducción. Los diversos fármacos utilizados y la distribución por periodos se observan en la Figura 8.
Figura 8. Inmunosupresión de inducción. Fármacos utilizados.
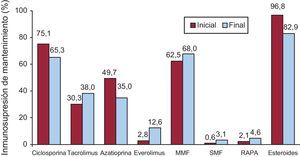
El tratamiento inmunosupresor de mantenimiento de novo y los cambios realizados durante la evolución del paciente trasplantado se reflejan en la Figura 9.
Figura 9. Inmunosupresión de mantenimiento. Variaciones evolutivas según el tipo de fármaco. Inmunosupresión al inicio del trasplante y al final del seguimiento. MMF: micofenolato mofetilo; RAPA: rapamicina; SMF: micofenolato sódico.
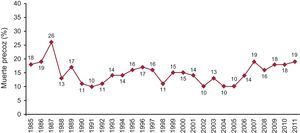
SupervivenciaLa mortalidad precoz (primeros 30 días tras el TC) el pasado año fue del 19%, como se puede apreciar en la Figura 10. Esta mortalidad es ligeramente superior a la media de los 5 años previos (17%).
Figura 10. Evolución anual del porcentaje de trasplantados fallecidos precozmente (primeros 30 días).
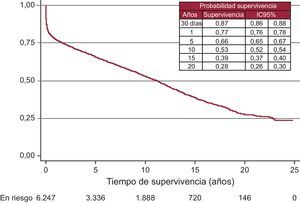
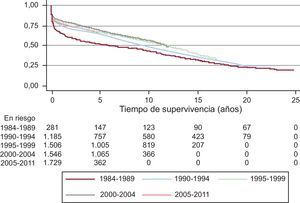
Al incorporar los datos de supervivencia del 2011 a los años anteriores, se obtuvo una probabilidad de supervivencia actuarial al mes del 87%, y a 1, 5, 10, 15 y 20 años, del 77, el 66, el 53, el 39 y el 28% respectivamente (Figura 11). La supervivencia por periodos mostró mejores resultados en las últimas etapas, con una probabilidad de supervivencia a 1 y 5 años del 80 y el 73% respectivamente (Figura 12).
Figura 11. Curva de supervivencia general de toda la serie. IC95%: intervalo de confianza del 95%.
Figura 12. Curvas de supervivencia por periodos de tiempo.
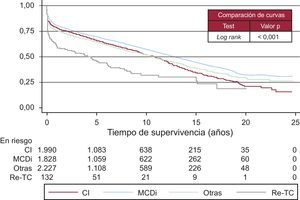
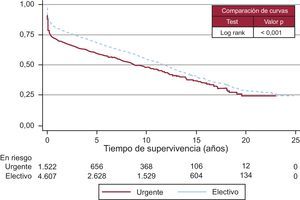
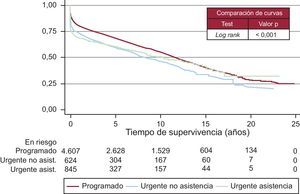
Las curvas de supervivencia fueron distintas según la etiología que motivó el TC (Figura 13). También el grado de urgencia influyó en la probabilidad de supervivencia (Figura 14). Sin embargo, no hubo diferencias entre los pacientes trasplantados urgentes con asistencia, bien fuera con balón intraaórtico, con oxigenador de membrana o con asistencia ventricular o sin ella (Figura 15).
Figura 13. Curvas de supervivencia por etiología que motiva el trasplante. CI: cardiopatía isquémica; MCDi: miocardiopatía dilatada idiopática; Re-TC: retrasplante cardiaco.
Figura 14. Curvas de supervivencia por grado de urgencia.
Figura 15. Curvas de supervivencia por grado y tipo de urgencia. Significación estadística entre grado urgente y no urgente. No se han encontrado diferencias entre tipos de urgencias (con y sin asistencia). La asistencia comprende: balón de contrapulsación intraaórtico, oxigenador de membrana extracorpóreo y asistencia ventricular pulsátil o continua. asist.: asistencia.
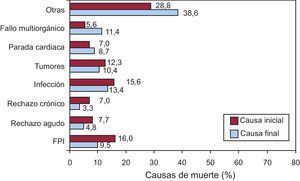
Causas de fallecimientoLa causa más frecuente de fallecimiento fue el fallo precoz del injerto (16%), seguido de infección (15,6%), el combinado de enfermedad vascular del injerto y muerte súbita (14%), los tumores (12,3%) y el rechazo agudo (7,7%) (Figura 16).
Figura 16. Causas de muerte. Causa inicial que desencadena el fallecimiento y causa final de la muerte. FPI: fallo precoz del injerto.
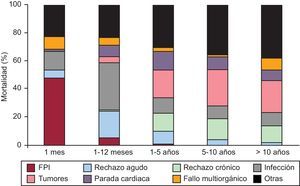
Al distribuir las causas de mortalidad en varios periodos, podemos apreciar que difieren: en el primer mes predomina el fallo precoz del injerto; del primer mes al primer año, las infecciones y el rechazo, y después del primer año, los tumores y la combinación de muerte súbita con rechazo crónico. En la Figura 17 podemos ver cómo se distribuyen las causas de mortalidad por periodos.
Figura 17. Causas de mortalidad por tiempo desde el trasplante. FPI: fallo precoz del injerto.
DiscusiónTras cerca de 30 años de desarrollo del TC en España, y con más de 6.500 TC realizados, se puede decir que esta modalidad terapéutica se puede ofrecer a toda la población asegurando unos niveles de conocimiento, control, estándares de calidad y supervivencia similares o superiores a los de otros países desarrollados de nuestro entorno y el resto del mundo. Este hecho, se puede observar si comparamos nuestros resultados con la publicación anual del Registro de la Sociedad Internacional de Trasplante Cardiaco y Pulmonar23, 24, 25, 26.
Se debe hacer constar que una de las grandes ventajas que posee el Registro Español de Trasplante Cardiaco es haber elaborado, entre todos los grupos españoles de trasplante, una base de datos homogénea, consensuando las posibilidades de respuesta. Cada año, todos los grupos actualizan sus datos y los envían al director del registro que, tras fusionarlos, los remite a una empresa estadística independiente para su análisis. Se considera que este método confiere gran fiabilidad a los resultados y evita resultados erróneos, tan habituales en las bases de datos no homogeneizadas. En 2007 se incrementó el número de variables a analizar por paciente hasta 175. También, en aras de una mayor calidad y fiabilidad de los datos, se pretende continuar con la auditoría de los centros mediante empresas externas independientes que garanticen al máximo la validez de los datos.
El número de centros con actividad trasplantadora en la actualidad es de 18. El hecho de que se autoricen en España centros para TC sin un estudio adecuado de necesidades preocupa mucho a los grupos de trasplante. Ello se debe a que, dado que hay una clara tendencia a que el número de donantes óptimos disminuya en España, la relación número de TC/número de centros disminuye. La realización de un reducido número de TC redunda, por un lado, en la infrautilización de recursos en los hospitales preparados para un gran número de actos y, por otro, en un incremento del periodo de aprendizaje necesario para conseguir unos resultados adecuados. El único beneficio para el paciente es la comodidad que supone no tener que desplazarse a otra área geográfica; lo que tampoco sería una ventaja en el caso de que ya exista un centro autorizado en su ciudad. Las autoridades sanitarias, que en su día decidieron abrir más centros, deberán valorar si se está realizando una auténtica optimización de los recursos en «tiempo de crisis».
El pasado año volvió a descender el número de TC realizados (237 en 2011 frente a 243 en 2010), a causa de la tendencia progresiva a que el número de donantes se reduzca. No hay una única explicación para esta disminución, pero parece evidente una menor mortalidad por traumatismo craneoencefálico relacionado con tráfico junto con un mejor control y manejo de los pacientes en las unidades de politraumatizados. Al descender el número de donantes, las posibilidades de TC disminuyen y el número de pacientes en lista se incrementa. De este modo, la proporción de pacientes con insuficiencia cardiaca avanzada a los que, una vez en lista, no se puede trasplantar y se los excluye de ella (por fallecimiento o deterioro) alcanza el 20%. Los grupos de trasplante, conscientes de este problema, intentan abrir el abanico de posibles donantes mediante la donación con criterios expandidos. Aun así, la edad de los donantes sufre pocas variaciones (38 años en 2011 frente a 39 años en 2010).
La espera de los pacientes hasta obtener un órgano compatible aumentó significativamente en 2011, pasando de 99 días en 2010 a 122 días en 2011. En años anteriores la espera había disminuido al incrementarse el porcentaje de trasplantes urgentes. No obstante, debido a que el tiempo transcurrido hasta la aparición del órgano de los trasplantes urgentes es cada vez mayor, es probable que este parámetro vaya aumentando progresivamente en los próximos años.
El perfil clínico de los pacientes no ha variado en los últimos años. Se han dividido los TC en tres grupos (pediátricos, adultos y retrasplantes), ya que poseen características clínicas distintas. Así, se trasplanta a los pacientes pediátricos por cardiopatías congénitas o miocardiopatía dilatada idiopática, que tienen resistencias pulmonares más elevadas y ausencia de factores de riesgo cardiovascular, mientras que los retrasplantes suelen hacerse por enfermedad vascular del injerto, con mayor deterioro orgánico y más factores de riesgo. Quizá, esto podría contribuir a un peor pronóstico de estos pacientes más que el hecho de ser un segundo TC.
Los TC urgentes están sujetos a cierta controversia, ya que son intervenciones que, por sus características (receptor en peores condiciones clínicas, donantes no idóneos y tiempos de isquemia más largos), conllevan peor pronóstico que cuando pueden realizarse de manera programada. En los últimos años se ha incrementado ostensiblemente el número de trasplantes urgentes (el 38% en 2011 frente al 34% en 2010). El porcentaje de pacientes a los que se incluye en código urgente varía de unas zonas a otras y se modifica notablemente de unos años a otros. No están completamente aclarados los motivos por los que se producen estas oscilaciones ni la distinta distribución geográfica. Aunque parece evidente que el número bajo de donantes y el mejor mantenimiento del paciente crítico (asistencia ventricular) hacen que se potencie esta posibilidad. Se ha cuestionado la indicación del trasplante urgente, ya que ofrece resultados claramente peores. No obstante, los grupos de trasplante consideran que debe seguir existiendo, aunque de forma «controlada». Para asegurar el máximo posible la supervivencia del paciente al que se trasplanta en situación crítica, debemos tener presente, tal y como recomiendan las recientes guías europeas de insuficiencia cardiaca, que conviene más estabilizar la insuficiencia cardiaca antes de indicar el TC urgente y que no se debe considerar el TC como un tratamiento de la insuficiencia cardiaca aguda inestable27 (entre otras cosas, por el tiempo que se tarda en conseguir un donante incluso con este grado de urgencia).
La proporción de pacientes que llegan al TC con algún tipo de asistencia ventricular ha ido en aumento, sobre todo en los últimos 5 años. El balón de contrapulsación intraaórtico sigue siendo el más utilizado, aunque no se ha incrementado su uso en los últimos 5 años; en cambio, el oxigenador de membrana extracorpóreo y los dispositivos pulsátiles sí han visto significativamente incrementada su utilización. En los últimos 5 años, más de la mitad de los pacientes trasplantados urgentes llevaban implantado algún tipo de asistencia ventricular. Estos dispositivos son cruciales para el mantenimiento y la estabilización previa al trasplante de los pacientes con insuficiencia cardiaca aguda. Por ello, es aconsejable que todos los grupos de trasplante puedan disponer de ellos para los pacientes más críticos. Además, resultan de mucha utilidad ante un fallo grave del injerto inmediatamente tras el implante. Esta complicación es cada vez es más frecuente por la peor situación del receptor, los donantes subóptimos y los tiempos de isquemia del órgano más prolongados inherentes al grado de urgencia del receptor y la mayor distancia hasta el órgano.
En la mayoría de los TC se ha utilizado inmunosupresión de inducción. El tratamiento más empleado desde los inicios ha sido los anticuerpos antilinfocitarios OKT3. No obstante, los más utilizados en los últimos 5 años son los antagonistas de la interleucina 2, que representan el 85% de los trasplantes realizados. El tratamiento inmunosupresor de mantenimiento que se utiliza es la denominada triple asociación: de ciclosporina frente a tacrolimus, azatioprina frente a micofenolato mofetilo y los esteroides. No obstante, en la evolución del paciente es habitual la introducción de otros fármacos inmunosupresores como rapamicina, everolimus, ácido micofenólico y, más recientemente, tacrolimus de liberación sostenida. De estos fármacos, se está incrementando más la administración de everolimus, que se administra al 2,8% de los pacientes al inicio del trasplante pero que se introduce hasta en el 12,6% de los trasplantes cuando concurren disfunción renal, tumores o enfermedad vascular del injerto.
La mortalidad precoz ascendió de un 18% en 2010 a un 19% en 2011. Esta tendencia viene incrementándose en los últimos 4 años y se cree que puede estar relacionada con un mayor número de urgencias y la utilización de asistencias ventriculares, con lo que el paciente llega al TC en condiciones más críticas. El periodo precoz es probablemente el más importante para mejorar la supervivencia, ya que la curva de supervivencia se estabiliza a partir de los primeros meses del TC.
La supervivencia general revela una clara tendencia a mejorar progresivamente con los años. No obstante, y como es lógico, el número de pacientes incorporados al registro supone cada año una proporción menor del total, y por eso la probabilidad de grandes cambios en un año es muy remota y resulta más ilustrativo analizar la supervivencia por periodos de tiempo. En los últimos años la supervivencia ha mejorado de manera significativa con respecto a las etapas más antiguas. Sin embargo, hay un «estancamiento» en la curva de supervivencia que se ha atribuido a la peor situación clínica de los receptores y a que los órganos son menos óptimos y con mayor tiempo de isquemia. No obstante, la supervivencia, incluso en grupos de alto riesgo, es mucho mayor que la que conlleva la insuficiencia cardiaca avanzada sin trasplante.
La causa que motiva el trasplante tiene relación evidente con la supervivencia. De tal forma que los pacientes con diagnóstico de miocardiopatía dilatada idiopática tienen una supervivencia más alta que los trasplantados por otras causas. Ello se debe a la edad más joven y a la menor presencia de factores de riesgo cardiovascular.
La causa más frecuente de fallecimiento son el fallo precoz del injerto (16%), seguido de la infección (15,6%), la combinación de enfermedad vascular del injerto y muerte súbita (14%), los tumores (12,3%) y el rechazo agudo (7,7%). No obstante, el motivo de fallecimiento suele estar en relación con el tiempo desde el TC, de tal forma que durante el primer mes la causa más frecuente es el fallo del injerto, y desde el primer mes hasta el primer año, la infección y el rechazo. En periodos posteriores, la causa de fallecimiento más usual es el combinado de muerte súbita junto con rechazo crónico y tumores. La distribución que se observa de las causas de fallecimiento no se han modificado en los últimos años, y deben hacernos reflexionar sobre la necesidad de alcanzar un «equilibrio» en la inmunosupresión, ya que la muerte por fallo en la prevención del rechazo es del 7,7%, mientras que el fallecimiento relacionado directamente con una inmunosupresión excesiva (infección y tumores) es del 28,2%.
ConclusionesLos grupos de trasplante deberán considerar a los donantes con criterios expandidos para poder ofrecer este tratamiento a la mayoría de los pacientes con insuficiencia cardiaca avanzada y evitar su pésimo pronóstico.
Las tasas de supervivencia del Registro Español de Trasplante Cardiaco son similares a las de otros registros. No obstante, se debe incrementar los esfuerzos para mejorar la probabilidad de supervivencia del periodo precoz, que redundará en una mejoría general importante.
La asistencia ventricular ha experimentado un gran auge. Estos dispositivos permiten mantener a los receptores en unas condiciones adecuadas hasta la aparición de un órgano compatible. No obstante, debido a que en ocasiones el tiempo de espera del órgano puede ser de semanas, se hace necesario disponer de dispositivos de asistencia ventricular de media y larga duración para evitar el deterioro del paciente y que se mantenga en buenas condiciones hasta el TC.
Sigue habiendo un gran desequilibrio entre las complicaciones que la inmunosupresión evita (rechazo) y las que favorece (tumores, infección). En los próximos años se deberá abordar estos problemas y personalizar la inmunosupresión según determinadas características de los pacientes.
FinanciaciónEl análisis estadístico ha sido realizado por ODDS, S.L. gracias a una ayuda no condicionada de Novartis Trasplante.
Conflicto de interesesNinguno.
Agradecimientos
Este año se celebran elecciones a Director del Registro Español de Trasplante Cardiaco, cargo que ocupo desde 1997. A lo largo de estos años he intentado llevar el cargo con orgullo y honor. Debo dar las gracias por todo lo que se me ha permitido aprender; pero sobre todo, por la enorme satisfacción que significa que todos los Grupos Españoles de Trasplante Cardiaco hayan confiado en mí enviándome, año tras año, los datos de sus trasplantes. ¡Muchísimas gracias a todos! (palabras del primer autor, Luis Almenar).
Anexo. Colaboradores del Registro Español de Trasplante Cardiaco 1984-2011| Clínica Puerta de Hierro Majadahonda, Madrid | Manuel Gómez-Bueno, María D. García-Cosío, Pablo García-Pavía, Luis Alonso-Pulpón |
| Hospital Universitario y Politécnico La Fe, Valencia | Luis Martínez-Dolz, Ignacio Sánchez-Lázaro, Mónica Cebrián |
| Hospital Universitario A Coruña, A Coruña | María J. Paniagua-Martín, Eduardo Barge-Caballero, Raquel Marzoa-Rivas, Zulaika Grille-Cancela |
| Hospital Gregorio Marañón (adultos), Madrid | Juan Fernández-Yáñez, Adolfo Villa, Yago Sousa, Iria González, Manuel Martínez-Sellés |
| Hospital Reina Sofía, Córdoba | Amador López-Granados, Juan Carlos Castillo |
| Hospital Marqués de Valdecilla, Santander | José Antonio Vázquez de Prada, Manuel Cobo |
| Hospital 12 de Octubre, Madrid | María J. Ruiz, Pilar Escribano, Miguel A. Gómez, Marta Paradina |
| Hospital de la Santa Creu i Sant Pau, Barcelona | Vicenç Brossa, Sonia Mirabet, Laura López, Josep Padró |
| Hospital Virgen del Rocío, Sevilla | José Manuel Sobrino, Alejandro Adsuar |
| Hospital de Bellvitge, L’Hospitalet de Llobregat, Barcelona | Josep Roca, José González-Costello |
| Clínica Universitaria de Navarra, Pamplona | Beltrán Levy, Rafael Hernández |
| Hospital Clínic, Barcelona | Montserrat Cardona, Marta Farrero, M. Ángeles Castel |
| Hospital Central de Asturias, Oviedo | Beatriz Díaz |
| Hospital Gregorio Marañón (niños), Madrid | Enrique Maroto, Constancio Medrano |
| Hospital Virgen de la Arrixaca, El Palmar, Murcia | Iris Garrido |
| Hospital Miguel Servet, Zaragoza | María L. Sanz, Ana Portolés |
| Hospital Clínico, Valladolid | Javier López-Díaz, Amada Recio |
| Hospital La Paz, Madrid | Daniel Borches, Luz Polo, Carlos Labrandero, Lucía Deiros |
| Hospital Vall d’Hebron, Barcelona | Ferran Gran, Raúl Abella |
Autor para correspondencia: Hospital Universitario y Politécnico La Fe, Avda. Bulevar Sur s/n, 46026 Valencia, España. lualmenar@gmail.com