Desde el primer implante percutáneo de válvula aórtica (TAVI) realizado por Cribier et al. en 20021 hasta la actualidad, la técnica y los dispositivos empleados se han desarrollado tanto que una intervención diseñada para pacientes inoperables2 ha cambiado el paradigma de la estenosis aórtica3, y se presenta como opción segura y eficaz para pacientes con bajo riesgo, según los resultados del estudio PARTNER 34.
La elección del dispositivo para TAVI se realiza en función de la experiencia de los operadores, la gestión del centro y la mejor opción para el paciente. En nuestro entorno la gama de prótesis autoexpandibles está en aumento: Evolut R/Pro (Medtronic, Estados Unidos), ACURATE neo (Boston Scientific, Suiza), Portico (Abbott, Estados Unidos) y Allegra (NVT, Alemania). Sin embargo, hasta ahora la única opción de prótesis balón expandible era SAPIEN 3 (Edwards Lifesciences, Estados Unidos), del que se han demostrado resultados clínicos superiores a los de las prótesis quirúrgicas en muchos contextos y mejores que los de las prótesis autoexpandibles en pacientes no seleccionados5.
La innovación en este campo ha permitido el desarrollo de la prótesis balón expandible Myval (Meril Life Sciences Pvt. Ltd., India), que obtuvo la marca Comunidad Europea (CE) tras el estudio Myval-16, desarrollado en 30 pacientes con riesgo intermedio-alto, al demostrar su eficacia y su seguridad, sin que se registrasen fuga paravalvular, insuficiencia aórtica significativa o necesidad de marcapasos definitivo tras el implante, con una supervivencia a 12 meses del 86,67%. Son datos competitivos con el brazo percutáneo del estudio PARTNER-3, aunque aún escasos. Su estructura es similar a la del SAPIEN 3 (figura 1A), y presenta ciertas ventajas. Una de las principales novedades es que sus medidas, según el diámetro de la válvula, incluyen 20, 23, 26 y 29 mm, como el sistema SAPIEN 3, pero además 21,5, 24,5 y 27,5mm, lo que limita el grado de sobreexpansión del anillo aórtico y reduce el riesgo de rotura, una de las principales preocupaciones al implantar prótesis balón expandible, y añade los tamaños 30,5 y 32 mm, con lo que se cubre una mayor gama de tamaños. Además, el sistema se inserta a través de un introductor de 14 Fr expandible, lo que supone una reducción del perfil de entrada respecto a otros dispositivos.
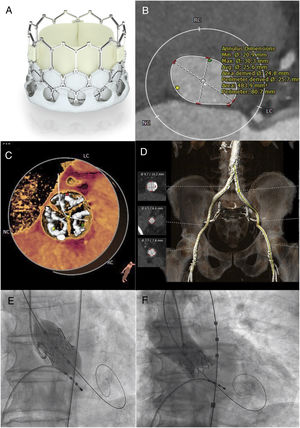
A: prótesis Myval. B: medición del anillo aórtico mediante tomografía computarizada (paciente 1). C: distribución del calcio en los velos (paciente 1). D: eje aortoiliaco femoral (paciente 1). E: imagen angiográfica del momento del implante de la prótesis aórtica Myval. F: angiografía con contraste final tras el implante de Myval. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
Antes del implante, se recomienda efectuar una predilatación con balón Mammoth (Meril Life Sciences Pvt. Ltd., India), compatible con guías convencionales de 0,035 pulgadas. La válvula se prensa sobre el sistema de liberación con balón coaxial (Navigator, Meril Life Sciences Pvt. Ltd., India), con capacidad flexora, que disminuye el traumatismo en el cayado aórtico, minimiza el riesgo de ictus periprocedimiento y optimiza la alineación con la aorta. El balón inicia su inflado semejante a un hueso de perro y estabiliza, junto con la estimulación ventricular rápida por marcapasos, la posición durante el inflado. La prótesis se introduce ya montada en el balón, al contrario que en el sistema SAPIEN 3, en el que se monta en el balón en la aorta descendente.
Se describen a continuación los primeros 2 implantes de Myval en España. El primero fue un varón de 83 años en clase funcional de la New York Heart Association (NYHA) III por estenosis aórtica grave con gradiente medio de 78 mmHg y área valvular aórtica de 0,60 cm2, con fracción de eyección conservada. Su riesgo quirúrgico calculado por Euroscore II era del 2,99%; se lo descartó para cirugía por su edad avanzada y su bajo peso (57 kg). Se obtuvieron accesos arteriales femoral y radial derechos y se colocó un marcapasos temporal a través de la vena femoral izquierda. Se realizó precierre con 2 Proglide (Abbott Vascular, Estados Unidos) y se colocó el introductor de 14 Fr. En estimulación ventricular rápida, se realizó una predilatación con balón Mammoth de 18 mm y, de acuerdo con las medidas y el análisis anatómico y de calcio obtenidos en el análisis de la tomografía computarizada (figura 1B-D), se implantó una Myval de 24,5 mm (figura 1E), con fuga paravalvular trivial (figura 1F).
El segundo fue un varón de 79 años en NYHA II secundaria a estenosis aórtica grave (gradiente medio, 50 mmHg; área valvular aórtica, 0,60 cm2; fracción de eyección, 67%) y Euroscore II del 1,55%, rechazado para cirugía por enfermedad pulmonar grave. Se le implantó una válvula de 23 mm siguiendo el proceso descrito, sin incidencias y con mínima insuficiencia periprotésica final (vídeo 1 del material adicional). Ambos pacientes ingresaron las primeras 24 h en la unidad coronaria para monitorización hemodinámica y fueron trasladados posteriormente a la planta de cardiología, donde se confirmó con ecocardiograma que las prótesis estaban correctamente posicionadas, con leve insuficiencia paravalvular en el primer caso, sin datos de insuficiencia en el segundo y gradientes medios de 9 y 10 mmHg respectivamente. Se les dio el alta a los 4 y los 5 días respectivamente, sin complicaciones.
El desarrollo de la prótesis aórtica percutánea Myval evidencia la importancia de la innovación técnica para responder a la creciente demanda de esta intervención y a la exigencia de los profesionales de una eficacia máxima al menor coste. Su valor añadido reside en el menor tamaño del introductor, que hace que sea una buena alternativa para pacientes con mal acceso vascular, y su mayor versatilidad de tamaños, que permite evitar la sobreexpansión y minimizar el riesgo de rotura anular, además de cubrir tamaños mayores.
Esta eficiencia deberá demostrarse a través del estudio LANDMARK, que se encuentra en sus primeras fases.