Palabras clave
INTRODUCCIÓN
El cor triatriatum es una malformación cardíaca producida por un defecto en la incorporación de la vena pulmonar común a la aurícula izquierda (AI). Ésta queda dividida en 2 cámaras: una posterosuperior que recibe las venas pulmonares, denominada cámara accesoria, y otra anteroinferior que incluye la orejuela y la válvula mitral, conocida como AI verdadera. Se asocia con frecuencia a otras malformaciones, sobre todo comunicación interauricular (CIA)1. Presentamos en este trabajo el cuadro clínico, el diagnóstico y el tratamiento de 4 casos de cor triatriatum.
CASOS CLÍNICOS
Caso 1
Niña de 21 meses de edad que fue remitida a nuestro servicio por soplo, retraso ponderal e infecciones respiratorias de repetición.
En la exploración se apreciaba un soplo sistólico II-III/VI en el foco pulmonar, con desdoblamiento fijo del segundo tono y soplo diastólico II/VI en el foco tricuspídeo. En la radiografía de tórax se observaban cardiomegalia y plétora pulmonar. El ECG puso de manifiesto un eje derecho y signos de crecimiento auricular y ventricular derechos.
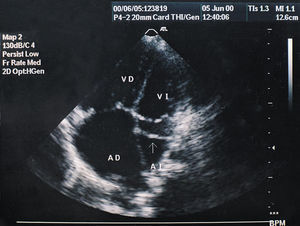
En el ecocardiograma se observó (fig. 1) una imagen de membrana diafragmática en la AI con una única fenestración de 1 cm de tamaño, con flujo ligeramente turbulento a su través y un gradiente pico de 9 mmHg. Existía asociada una dilatación de las cavidades derechas y una CIA de 13 mm que comunicaba la aurícula derecha (AD) y la cámara accesoria.
Fig. 1. Ecocardiograma en plano apical de 4 cámaras del caso 1. Se observa un eco lineal en la parte media de la aurícula izquierda (flecha) que corresponde a la membrana fibromuscular.
Dado que el gradiente a través de la membrana fibromuscular no era muy grande, y debido al tamaño de la CIA, se decidió realizar un estudio hemodinámico para cuantificar la repercusión de la malformación. La membrana fibromuscular se objetivó en las proyecciones oblicua anterior derecha y posteroanterior. El gradiente medio obtenido fue de 1,9 mmHg. La relación Qp/Qs fue de 2,9/1. No existía hipertensión pulmonar.
Se indicó cirugía a los 4 años de edad. Se realizó abordaje vía AD, con resección de la membrana y cierre de la CIA con parche de pericardio.
Un mes después de la intervención la paciente se encuentra asintomática. Se observan por ecocardiografía imágenes de restos de membrana sin gradiente.
Caso 2
Niño de 5 meses remitido por disnea con las tomas, crisis de cianosis, infecciones pulmonares de repetición y retraso ponderal.
En la exploración física existía un soplo II/VI en el mesocardio y desdoblamiento fijo del segundo tono. La radiografía de tórax ponía de manifiesto cardiomegalia y plétora pulmonar. En el ECG existía eje derecho y signos de crecimiento de las cavidades derechas.
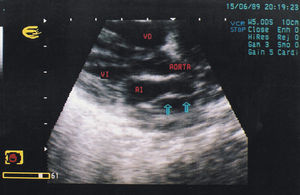
Mediante ecocardiografía (fig. 2A) se objetivó una imagen sugestiva de membrana de tipo diafragmático en la AI, con una única fenestración. Existía una clara dilatación de las cavidades derechas y una CIA de 8 mm que comunicaba la AD con la AI verdadera. A través de la fenestración existía un gradiente pico de 5 mmHg, que aumentó a 17 mmHg 2 meses después.
Fig. 2. A: ecocardiograma en plano paraesternal eje largo del caso 2 en el que se observa la membrana que divide a la aurícula izquierda (flechas verticales). B: imagen postoperatoria del mismo paciente que pone de manifiesto restos de membrana en las paredes de la aurícula izquierda. AI: aurícula izquierda; VD: ventrículo derecho; VI: ventrículo izquierdo.
Ante el diagnóstico ecocardiográfico y el cuadro clínico, sin estudio hemodinámico previo, se indicó cirugía a los 8 meses de edad. Se realizó abordaje quirúrgico vía AD con resección de la membrana y cierre de la CIA con parche de pericardio.
Cuatro años después el paciente se encuentra asintomático. En el ECG van disminuyendo los signos de crecimiento derecho. Por ecocardiograma se observan restos de la membrana resecada sin que exista gradiente (fig. 2B). Las cavidades derechas persisten algo dilatadas.
Caso 3
Niño de 4 meses de edad que ingresó en insuficiencia cardíaca. No presentaba soplos a la auscultación. La radiografía de tórax ponía de manifiesto signos de congestión venocapilar sin cardiomegalia. El ECG tenía eje derecho y signos de crecimiento de cavidades derechas.
Por ecocardiograma se objetivó en la AI una imagen sugestiva de membrana de tipo diafragmático, con una única fenestración entre la cámara accesoria y la AI verdadera con flujo turbulento a su través y un gradiente pico de 35 mmHg. Se asociaba un pequeño foramen oval permeable con flujo izquierda-derecha entre la cámara accesoria y la AD, y existía un gradiente entre ambas cámaras de 20 mmHg. Se apreciaba una insuficiencia tricuspídea moderada que permitía estimar una presión pulmonar sistólica de 95 mmHg.
En los siguientes días se indicó cirugía con abordaje por vía AD, con resección de la membrana.
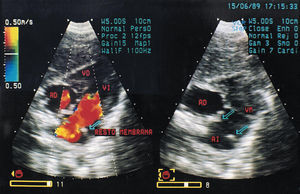
Tres años después el paciente se encuentra asintomático, salvo por dos crisis aisladas de taquicardia auricular que ocurrieron en el postoperatorio precoz y que no se volvieron a presentar. En el ECG basal se aprecia un ritmo del seno coronario. El ecocardiograma evidencia restos de membrana sin generar gradiente (fig. 3).
Fig. 3. Ecocardiograma en el plano subxifoideo de 4 cámaras correspondiente al caso 3 tras la intervención quirúrgica. Se observan restos de membrana que no producen obstrucción, observándose un flujo laminar con Doppler color. AD: aurícula derecha; AI: aurícula izquierda; VD: ventrículo derecho; VI: ventrículo izquierdo; VM: válvula mitral.
Caso 4
Niña de 5 años de edad clínicamente asintomática que fue remitida a nuestro servicio para el estudio preoperatorio de un soplo. En la exploración se apreciaba un soplo sistólico I/VI. La radiografía de tórax y el ECG eran normales.
En el ecocardiograma se observó una imagen en la AI sugestiva de membrana tipo diafragmática con fenestración amplia sin turbulencia ni gradiente a su través. No existían lesiones asociadas.
Tres años después la paciente permanece asintomática y los hallazgos ecocardiográficos son similares.
DISCUSIÓN
El cor triatriatum es una cardiopatía congénita poco frecuente que representa el 0,4% de las cardiopatías congénitas2. La cámara accesoria comunica con la AI verdadera a través de uno o varios orificios. Existen tres tipos anatómicos de cor triatriatum: diafragmático, «en reloj de arena» y tubular. El tipo diafragmático se caracteriza por la presencia de una membrana fibromuscular que divide a la AI en cámara accesoria y AI verdadera. El tipo diafragmático es el más frecuente y los 4 casos presentados pertenecen a esta forma anatómica. En el tipo «en reloj de arena» se aprecia una constricción externa en la unión de la cámara accesoria y la AI verdadera. En el tipo tubular, la confluencia de las venas pulmonares conecta con la AI a través de un canal3. Su asociación más frecuente (50-60% de los casos) es la CIA, que se sitúa en la mayoría de los casos entre la cámara accesoria y la AD1.
Su presentación clínica es muy variada. Existen pacientes, como el caso 4, asintomáticos, diagnosticados de forma casual ante el hallazgo de un soplo, en los que la membrana no genera una obstrucción significativa4. En los casos en los que la membrana genera obstrucción significativa y no existe CIA (caso 3), o existe CIA que comunica la AI verdadera y la AD (caso 2), los síntomas se producen por hipertensión venosa pulmonar; en algunos de estos casos el aumento de presión en la cámara accesoria favorece la persistencia de la vena cava superior izquierda como forma de retorno venoso anómalo. Si la membrana genera obstrucción y existe asociada una CIA amplia que comunica la cámara accesoria y la AD (caso 1), los síntomas dependerán del hiperaflujo pulmonar, que puede ir asociado a bajo gasto sistémico5,6.
En el ECG se suele observar un eje derecho y signos de crecimiento derechos, como ocurre en los 3 casos que presentaban síntomas7. En pacientes asintomáticos y sin obstrucción, como el caso 4, el ECG y la radiografía de tórax son normales.
El ecocardiograma permite establecer un diagnóstico preciso del cor triatriatum y de su repercusión hemodinámica8,9. En los casos presentados existe muy buena correlación entre los hallazgos quirúrgicos y el diagnóstico ecocardiográfico, que permite valorar la existencia de membrana fibromuscular, el número de fenestraciones y su tamaño, y el gradiente transmembrana. También facilita el diagnóstico de lesiones asociadas, fundamentalmente la CIA.
La ecocardiografía transesofágica es de utilidad en pacientes adultos o con mala ventana ecoica10,11. Así mismo, cuando existen prolapso e insuficiencia mitral asociados, la ecocardiografía transesofágica intraoperatoria permite valorar de manera adecuada la morfología de la válvula mitral y la severidad de la insuficiencia mitral tras la resección de la membrana, ya que el grado de severidad puede ser infraestimado preoperatoriamente debido a la presencia de la membrana12.
La resonancia magnética es otra técnica de imagen que se ha utilizado para el diagnóstico de cor triatriatum, y puede ser de gran utilidad cuando la ecocardiografía o el estudio hemodinámico no son diagnósticos13,14.
No es necesario realizar estudio hemodinámico en la mayoría de los casos, pero sí estará indicado en casos con lesiones asociadas que lo precisen. En el caso 1 existía, por ecocardiografía, un gradiente pico de 9 mmHg y una CIA asociada de 13 mm entre la cámara accesoria y la AD. Se indicó estudio hemodinámico para cuantificar el cortocircuito, ya que el gradiente a través de la membrana no era muy alto.
El abordaje quirúrgico de elección es la vía auricular derecha, que facilita un buen acceso para resecar la membrana y corregir las lesiones asociadas, fundamentalmente la CIA15.
Tras la intervención los pacientes quedan asintomáticos, siendo el pronóstico a largo plazo muy bueno7. Es frecuente encontrar imágenes sugestivas de restos de membrana por ecocardiografía, sin gradiente. La presión pulmonar se normaliza y regresan la cardiomegalia y los signos ECG de crecimiento derecho.
Uno de los casos presentados corresponde a una paciente asintomática con cor triatriatum no obstructivo. Se creía que estos casos tenían una evolución benigna16, pero últimamente se ha descrito que con el tiempo pueden desarrollar degeneración mixomatosa de la válvula mitral con insuficiencia mitral4. También se ha asociado a taquiarritmias supraventriculares del tipo aleteo y fibrilación auricular y a accidente cerebrovascular en pacientes relativamente jóvenes sin factores de riesgo17. Aún son pocos casos los descritos, y sólo el seguimiento de estos pacientes asintomáticos indicará con qué frecuencia se desarrollan estas complicaciones y qué actitud tomar.