La embolia de líquido amniótico (ELA) es una complicación obstétrica rara. Su presentación clínica varía desde disfunción orgánica moderada a shock cardiogénico, insuficiencia respiratoria, coagulación intravascular diseminada y muerte en el 60% de los pacientes. El tratamiento de la ELA se basa en medidas de asistencia cardiopulmonar y corrección de la coagulopatía1.
El oxigenador extracorpóreo de membrana venoarterial (ECMO-VA) se ha utilizado en pacientes con ELA con evolución a shock cardiogénico e insuficiencia respiratoria2, aunque este tratamiento podría ser insuficiente. Se presenta el primer caso publicado de una paciente con clínica compatible con ELA que precisó asistencia cardiorrespiratoria con ECMO-VA y asistencia del ventrículo izquierdo con Impella CP.
Mujer de 34 años, en segunda gestación y con cesárea previa, que ingresó en la semana 38 de embarazo por rotura prematura de membranas. Analítica: hemoglobina, 12,1 g/dl; plaquetas, 180.000 /μl; tiempo de protrombina, 96%; razón internacional normalizada, 1,02; tiempo de tromboplastina parcial activado, 24,8 s y fibrinógeno, 334 mg/dl. A las 4 h del ingreso, se realizó cesárea urgente por bradicardia fetal. Finalizando la cirugía, sufrió hemorragia en sábana y atonía uterina con inestabilidad hemodinámica y respiratoria, y se indicó reanimación con fluidoterapia, vasopresores, uterotónicos, ventilación mecánica y transfusión de hemoderivados. La paciente presentaba actividad sin pulso, que recuperó tras 7min de reanimación cardiopulmonar avanzada.
Posteriormente se la trasladó a la unidad de reanimación en ventilación mecánica, hemodinámicamente inestable, con noradrenalina a 0,8 μg/kg/min y analítica compatible con coagulación intravascular diseminada (26.000 plaquetas/μl; razón internacional normalizada, 1,67; tiempo de tromboplastina parcial activado, 75,2 s; fibrinógeno, 81 mg/dl y dímero D, 88.332 ng/ml). Se corrigió la coagulopatía dirigida por tromboelastografía, se pudo reducir la dosis de noradrenalina, y se realizó una arteriografía en la que se observó hemorragia activa a expensas de ambas arterias uterinas, que se embolizaron. A las 12 h del ingreso, se decidió cirugía urgente por persistencia de la hemorragia abdominal con inestabilidad hemodinámica y respiratoria importante, entrando en edema agudo de pulmón. En la ecocardiografía transesofágica se observó disfunción biventricular grave con fracción de eyección del ventrículo izquierdo por Simpson del 8%.
Se decidió implantar ECMO-VA femorofemoral (Cardiohel Maquet Cardiopulmonary; Hirlinge, Alemania) y balón de contrapulsación intraaórtico. Se mantuvo un buen intercambio gaseoso con ECMO-VA a 4,0–4,5 lpm, pero en la ecocardiografía transesofágica se observó un ventrículo izquierdo acinético, gravemente dilatado e incapaz de abrir la válvula aórtica, a pesar de las dosis altas de dobutamina y del descenso del flujo del ECMO-VA. Se decidió implantar un Impella CP percutáneo a través de la arteria femoral izquierda, previa retirada del balón de contrapulsación intraaórtico, para lograr descargar el ventrículo izquierdo. Se necesitó hemostasia quirúrgica para evitar una hemorragia en el punto de inserción.
La paciente volvió a la unidad de reanimación con ECMO-VA a 4,0-4,5 lpm e Impella CP a 2,0-2,4 lpm, lo que permitió la paulatina reducción de catecolaminas. Presentaba oligoanuria y se inició terapia de sustitución renal con anticoagulación regional con citrato cálcico.
El segundo día de ingreso se iniciaron dosis bajas de heparina intravenosa para evitar complicaciones asociadas con el ECMO-VA y el Impella CP, pero ante la persistencia de la hemorragia y la coagulopatía con riesgo vital, se decidió una estrategia libre de heparina.
Al tercer día de ingreso, la paciente se encontraba hemodinámicamente más estable, y se observó en la ecocardiografía transesofágica una mejoría de la función ventricular con apertura de la válvula aórtica, por lo que se retiró el Impella CP (48 h de uso) y se mantuvo el ECMO-VA por la importante insuficiencia respiratoria. La paciente presentaba alta demanda transfusional y coagulopatía con hemorragia activa, por lo que se la intervino en otras 2 ocasiones por hemoperitoneo (días 3 y 4 de ingreso). En el día 4 de ingreso, se logró controlar la hemorragia, tras transfusión total de 104 concentrados de hematíes, 66 unidades de plasma fresco congelado, 30 pools de plaquetas, 28g de fibrinógeno, 20g de cloruro cálcico, 20 μg desmopresina y 2 dosis de 70g de inmunoglobulinas.
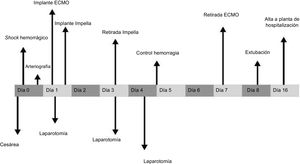
Se mantuvo ECMO-VA a 4 lpm, para la asistencia respiratoria, sin anticoagulación por el alto riesgo de hemorragia y terapia de sustitución renal para balance hídrico negativo, que permitió la mejoría de la función respiratoria y la recuperación de la diuresis. El ECMO-VA se retiró el día 7 de ingreso (144 h de uso). La paciente despertó sin focalidad neurológica; se la extubó con buena tolerancia el día 8 y se le dio el alta de la unidad de reanimación tras 16 días de ingreso. El curso clínico se resume en la figura 1.
La ELA es una complicación obstétrica que produce insuficiencia cardiorrespiratoria y coagulopatía. Aunque el ECMO-VA se ha utilizado con éxito en casos de ELA, en nuestra paciente esta medida no bastó para descargar el ventrículo izquierdo, por lo que se agregó un Impella CP3. Pappalardo et al.4 recientemente han observado que la terapia combinada con ECMO-VA e Impella puede disminuir la mortalidad y mejorar la evolución de pacientes con shock cardiogénico comparado con ECMO-VA como terapia única. Normalmente, la anticoagulación es imperativa para los pacientes con ECMO-VA e Impella CP para evitar las trombosis del circuito3. Dados los trastornos de coagulación que presentaba nuestra paciente y la hemorragia activa, se decidió una terapia libre de heparina4,5 con flujos altos en la ECMO-VA (> 4 l/min) y mantener el Impella CP a 2,0-2,4 l/min para minimizar la hemolisis secundaria, manteniendo como solución de cebado del sistema la dextrosa al 20%.
El caso presentado describe por primera vez el uso combinado de ECMO-VA e Impella CP en shock cardiogénico y trabajo respiratorio secundario a ELA en una paciente con coagulopatía asociada a shock hemorrágico.