Tras el desarrollo del implante percutáneo de válvula aórtica (TAVI) y su primer uso en el ser humano por parte de Alain Cribier en 2002, este tratamiento ha pasado a ser el patrón de referencia para la estenosis aórtica (EA) grave sintomática en pacientes considerados inoperables o con alto riesgo de muerte perioperatoria1. Recientemente se ha demostrado que el TAVI proporciona unos resultados similares a los de la sustitución de la válvula aórtica tanto clínicos como en la calidad de vida (CdV).
Desde 2002, la tecnología para el TAVI se ha perfeccionado y el número de implantes ha aumentado en los últimos años, con más de 500.000 intervenciones realizadas en más de 70 países de todo el mundo. El TAVI es actualmente una intervención habitual y sus indicaciones se han ampliado, y han pasado de ser tan solo los pacientes inoperables y de alto riesgo en el momento inicial a los pacientes con riesgo intermedio e incluso los considerados en alto riesgo2. En un reciente artículo de opinión sobre el futuro del TAVI, Kim y Hamm plantearon la hipótesis de que esta intervención pudiera pasar a ser el tratamiento de primera línea para la estenosis valvular aórtica (o la insuficiencia aórtica) de moderada a grave con independencia de los síntomas o del riesgo operatorio dentro de 10 a 15 años3.
Aunque en la actualidad el TAVI es una intervención habitual, continúa habiendo pacientes con una EA grave sintomática en los que no se obtiene un beneficio con esta intervención costosa y que además tiene riesgos inherentes, como ictus, hemorragia y muerte. El consenso actual en los equipos multidisciplinarios es que los pacientes para los que se programa un TAVI deben tener una CdV razonable y una esperanza de vida mínima de 1 año. Se considera que el TAVI no aporta un beneficio en pacientes con demencia grave o fragilidad grave, pacientes encamados y pacientes con enfermedades concomitantes en fase terminal (p. ej., enfermedad renal o hepática terminal o enfermedad pulmonar obstructiva crónica) o con cánceres metastásicos. El diagnóstico y la detección de estos pacientes es crucial para evitar intervenciones innecesarias que causan costes evitables y, sobre todo, para evitar causar un daño en cuanto a complicaciones y hospitalización, con la consiguiente reducción de la CdV.
EVALUACIÜN DEL RIESGO EN EL TAVILa evaluación del riesgo se considera crucial en la selección de los pacientes para el TAVI. Se utilizan sistemas de puntuación, como el de la Society of Thoracic Surgeons (STS) y el EuroSCORE logístico, pero estos parámetros muestran tan solo una correlación débil con el verdadero riesgo periintervención4. Además, la fragilidad (debilidad, emaciación muscular, desnutrición y marcha lenta) y la función neurológica son factores importantes que influyen en los resultados tras el TAVI5. Sin embargo, el cálculo de los sistemas de puntuación existentes es complejo y la fragilidad podría resultar difícil de evaluar. Por otra parte, hay diversos métodos para cuantificar la fragilidad. Esta suele medirse mediante una evaluación clínica que combina la exploración física con información sobre las capacidades del paciente en la vida cotidiana. Hay varias puntuaciones, pero la Clinical Frailty Scale ha dado resultados satisfactorios al compararla con otras herramientas de valoración y es relativamente fácil de utilizar6. Recientemente, Gilbert et al.7 han propuesto y validado otro enfoque para cuantificar la fragilidad mediante la inclusión de los datos clínicos basados en los códigos de la CIE-10. Este enfoque podría ser útil para objetivar la fragilidad y facilitar la predicción del riesgo en los pacientes tratados con TAVI.
Aunque los parámetros objetivos para la evaluación del riesgo, que pueden determinarse con facilidad y a un coste bajo, son útiles para los procesos de toma de decisión del equipo multidisciplinario, los biomarcadores podrían ser también candidatos ideales para ello. Ya se han evaluado varios biomarcadores en cohortes de pacientes tratados con TAVI y se han demostrado su importancia pronóstica y sus ventajas.
GALECTINA-3 Y CA125 EN ONCOLOGýA Y EN INSUFICIENCIA CARDIACAEn un artículo publicado recientemente en Revista Española de Cardiología, Rheude et al.8 evaluaron la galectina-3 y el antígeno carbohidrato 125 (CA125) para la determinación del riesgo de los pacientes tratados con TAVI. La galectina-3, que forma parte de la familia de la lectina, desempeña un papel importante en la inflamación, la reparación tisular y la fibrosis cardiaca. Especialmente en la insuficiencia cardiaca (IC), se ha observado que la galectina-3 es un biomarcador útil para el pronóstico y la estratificación del riesgo. En modelos experimentales se ha determinado que la galectina-3 participa en la fibrosis cardiaca y el remodelado patológico del corazón9. El uso de la galectina-3 se menciona también en la guía del American College of Cardiology Foundation y la American Heart Association para el tratamiento de la IC como biomarcador pronóstico en pacientes con IC (indicación de clase IIb)10.
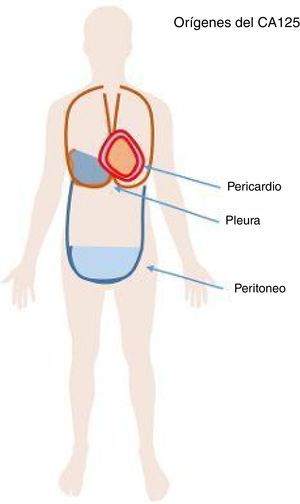
El CA125 es una glucoproteína de la familia de la mucina. Se sabe que esta glucoproteína es liberada en la superficie celular tras una fragmentación proteolítica y puede detectarse en la sangre, el derrame pleural y pericárdico y la ascitis (figura 1). El CA125 se detectó inicialmente en líneas celulares de cáncer de ovario y se ha utilizado como marcador para el seguimiento del tratamiento de pacientes con este cáncer durante muchas décadas en las clínicas especializadas. En otros cánceres, como el de pulmón, el teratoma y el linfoma no hodgkiniano, se han descrito también valores elevados de CA125 en la cirrosis hepática. El CA125 se produce también por el tejido pericárdico y pleural, y varios estudios han descrito un aumento de las concentraciones de CA125 en pacientes con una descompensación de la IC, en especial los que presentan un derrame pleural. En los pacientes con IC y fracción de eyección conservada (IC-FEc), se ha descrito una elevación del CA125. Se planteó la hipótesis de que el CA125 se libera a causa del estrés sufrido por las células mesoteliales como respuesta a estímulos hemodinámicos e inflamatorios11.
Orígenes de la liberación del antígeno carbohidrato 125 (CA125). El CA125 es liberado por las células mesoteliales (p. ej., del pericardio, la pleura o el peritoneo) como consecuencia de estímulos inflamatorios o de estrés general. Su presencia puede detectarse en el líquido de derrame pericárdico o pleural, así como en el líquido ascítico.
La estratificación del riesgo y la selección adecuada de los pacientes son de capital importancia para los pacientes programados para TAVI. Los sistemas de puntuación y los biomarcadores cardiacos ya establecidos, como la fracción aminoterminal del propéptido natriurético cerebral (NT-proBNP), podrían ser útiles para la toma de decisiones por el equipo multidisciplinario, pero no bastan para estratificar el riesgo de cada paciente individual.
Un enfoque que combine el uso de distintas herramientas para la estratificación del riesgo resulta interesante. El grupo de Hengstenberg12,13 se centró en este aspecto en estudios anteriores e intentó analizar la aplicabilidad pronóstica de sistemas de puntuación junto con el CA125 en el contexto de la EA y el TAVI (p. ej., NT-proBNP y EuroSCORE logístico).
Se han investigado también otros biomarcadores cardiovasculares novedosos, como el factor 2 de supresión de la tumorogenicidad (ST2) o el factor 15 de diferenciación del crecimiento (GDF-15), que se han investigado en ensayos clínicos en este contexto14,15. El ST2 tiene especial interés, puesto que se ha observado que es superior o, como mínimo, comparable al NT-proBNP por lo que respecta a la predicción de resultados adversos no solo tras el TAVI, sino también en la IC con fracción de eyección tanto conservada como reducida16.
Otro biomarcador interesante podría ser la proteína de unión del factor de crecimiento de tipo insulina 2 (IGFBP2), que se ha observado que da mejores resultados que los de puntuaciones complejas como las de EuroSCORE y STS17. Se ha observado que otros factores de crecimiento de tipo insulínico (IGFBP7) predicen la disfunción diastólica; por consiguiente, la IGFBP podría aportar una perspectiva adicional en comparación con la de los biomarcadores cardiovasculares tradicionales18.
CONSECUENCIAS DE LA ELEVACIÜN DEL CA125 EN PACIENTES NO ONCOLÜGICOSEl CA125 es liberado, como respuesta a estímulos de estrés, por las células mesoteliales del peritoneo, el pericardio y la pleura. El CA125 es un marcador de la inflamación tisular inespecífico, y no es específico de las enfermedades malignas. En consecuencia, no se recomienda su empleo para la detección sistemática de los pacientes con un valor de CA125 aumentado sin otros síntomas de enfermedad maligna. El CA125 no es diagnóstico de ningún cáncer y su uso se ha establecido tan solo para el seguimiento de la enfermedad maligna, y en especial del cáncer de ovario. Los valores de CA125 aumentados a causa de la IC podrían llevar a confusión, al promover la sospecha de un cáncer, tal como han descrito Hopman et al.19. Conocer el fundamento fisiopatológico exacto de la elevación del CA125 es, pues, esencial para evitar interpretaciones erróneas de un solo resultado de análisis de laboratorio. Esta cuestión podría adquirir gran importancia si, en función de los resultados recientes, llega a establecerse el uso del CA125 como proteína marcadora para el seguimiento de la enfermedad cardiovascular en el futuro.
CONSECUENCIAS ECONÜMICASEn paralelo con el aumento del número de TAVI realizados, se han investigado nuevos biomarcadores para la evaluación del riesgo y para el seguimiento en múltiples estudios en los que se han utilizado estrategias complejas. Sin embargo, los métodos analíticos de nuevos biomarcadores proteicos mediante ensayos de inmunoadsorción enzimática (ELISA) en sándwich, realizados manualmente o mediante análisis de inmunofluorescencia automáticos para la determinación cuantitativa, tal como se hace en la mayoría de los ensayos clínicos en que se estudian biomarcadores cardiacos en pacientes con TAVI, requieren recursos técnicos y económicos considerables. Esto podría hacer que fueran poco prácticos y laboriosos, especialmente cuando se trata de analizar un gran número de muestras. Estos factores podrían dificultar un uso generalizado de los nuevos biomarcadores.
Estos problemas pueden evitarse al utilizar el CA125, ya que este marcador está introducido desde hace tiempo en los laboratorios clínicos y su determinación se realiza con métodos de análisis ordinarios. Además, la determinación de la concentración de CA125 en muestras de sangre de pacientes es considerablemente más barata que la de los biomarcadores cardiacos como el NT-proBNP. Ordu et al.20 señalaron que la realización de un análisis del CA125 es 10 veces más barata que la de un análisis del NT-proBNP (aproximadamente, 1 frente a 11 dólares, datos de mediados de enero de 2012).
CUESTIONES TðCNICASEl CA125 es un marcador proteico que se ha utilizado en el ámbito clínico durante muchos años con métodos de análisis estandarizados. Sin embargo, la aplicación a gran escala de análisis de laboratorio de los marcadores galectina-3, ST2 o IGFBP2 no es frecuente. En la mayor parte de los estudios en los que se investigan nuevos biomarcadores se utilizan kits de ELISA comerciales, y su precisión podría no satisfacer los requisitos de alta precisión de los parámetros analíticos ordinarios determinados en centros de análisis de laboratorio grandes.
INVESTIGACIÜN FUTURATal como mencionan Rheude et al.8, los modelos de predicción del riesgo en los pacientes tratados con TAVI continúan siendo inadecuados. Los biomarcadores podrían facilitar la toma de decisiones del equipo multidisciplinario y aportar una información adicional necesaria en el contexto clínico cotidiano.
El conocimiento de diferentes vías fisiopatológicas involucradas en la progresión de la enfermedad en la EA podría esclarecerse mejor con el empleo de biomarcadores, que facilitarían un diagnóstico más temprano y una mejor valoración del riesgo. Aunque resulta difícil, el desarrollo de nuevos conceptos de biomarcadores, por ejemplo mediante proteómica/espectrometría de masas o secuenciación de nueva generación (como el análisis de microARN), podría proporcionar nuevos datos de interés desde un punto de vista de ciencias básicas. No obstante, estos análisis son complejos, laboriosos y costosos, y ello puede dificultar su empleo en ensayos clínicos grandes. El empleo de biomarcadores ya conocidos, como el CA125, aplicados en otros entornos o contextos de enfermedad, podría obviar esta dificultad de manera coste-efectiva y elegante.
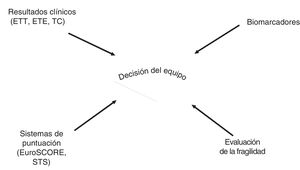
Los biomarcadores podrían facilitar los procesos de toma de decisión, en especial en los pacientes con riesgo muy alto. Creemos que se podría identificar a los pacientes con un riesgo «extremo» combinando una información clínica sencilla, como la de la fracción de eyección del ventrículo izquierdo, la hipertensión pulmonar y también la fragilidad, junto con los biomarcadores: la combinación e integración de la información clínica, la capacidad funcional general de los pacientes (fragilidad) y los marcadores de predicción del riesgo (biomarcadores) podría ser útil para predecir el riesgo. Los posibles biomarcadores de interés son los siguientes: CA125, galectina-3, ST2 e IGFBP2. Un enfoque integrado podría ser especialmente útil para optar entre estrategias de tratamiento conservadora o intervencionista (figura 2). También podría facilitar la identificación de áreas de vulnerabilidad: ante un paciente con una buena fracción de eyección, una presión pulmonar baja y una constelación de biomarcadores favorable, pero con fragilidad, los clínicos y los geriatras deben colaborar en el intento de reducir la fragilidad y revaluar al paciente tras un periodo determinado. Sin embargo, serán necesarios nuevos estudios prospectivos para respaldar este concepto.
La evaluación del riesgo para la toma de decisiones en el Heart Team interdisciplinario debe basarse en los resultados clínicos, las puntuaciones y la evaluación de la fragilidad. El uso de nuevos biomarcadores podría ser útil en este proceso. ETE: ecocardiografía transesofágica; ETT: ecocardiografía transtorácica; STS: puntuación de la Society of Thoracic Surgeons; TC: tomografía computarizada.
El CA125, antes considerado tan solo un marcador del cáncer de ovario, es un parámetro que atrae una atención creciente en la investigación de la IC, puesto que es barato y está ya disponible en muchos laboratorios. La combinación del CA125 con otros nuevos biomarcadores, junto con una información clínica sencilla y una evaluación de la fragilidad, podría mejorar la estratificación del riesgo de los pacientes evaluados para el TAVI.
CONCLUSIONESVarios biomarcadores han mostrado que agregan valor predictivo a las puntuaciones de riesgo establecidas. Los marcadores CA125, galectina-3, ST2 e IGFBP2 son algunos de los más prometedores para predecir el riesgo de los pacientes tratados con TAVI. El CA125 podría tener especial interés, puesto que es barato y está disponible en la mayor parte de los laboratorios. Un abordaje integrado que combine biomarcadores potentes con la información clínica y la evaluación de la fragilidad sería fácil de aplicar y optimizaría la estratificación del riesgo de los pacientes tratados con TAVI.
CONFLICTO DE INTERESESNo se declara ninguno.