Palabras clave
INTRODUCCIÓN
Después de 15 años de trayectoria1, el acceso radial para la realización del cateterismo cardíaco está siendo adoptado por cada vez más cardiólogos intervencionistas2,3. En comparación con el acceso femoral, la vía radial ofrece mayor seguridad y comodidad para el paciente4, especialmente en ciertos subgrupos (ancianos, obesos, intervencionismo en el infarto, etc.)5,6. La arteria radial es un vaso con un gran espesor de pared compuesto fundamentalmente por células musculares lisas dispuestas en capas concéntricas. Esta importante composición muscular de la arteria, así como la alta densidad de receptores alfa-1, hace que sea un vaso especialmente proclive al espasmo7. La aparición del espasmo radial limita las ventajas de este acceso, ocasiona un mayor grado de incomodidad al paciente y reduce las posibilidades de éxito del procedimiento. Incluso en centros con gran experiencia en la vía radial, el espasmo radial ocurre en un 15-30% de los procedimientos8.
El espasmo de la arteria radial empleada como injerto coronario, así como las medidas para prevenirlo, han sido ampliamente estudiados9-10. Sin embargo, pocos han sido los trabajos dirigidos a analizar los factores implicados en el espasmo de la arteria radial cuando se emplea como vía de acceso en el cateterismo cardíaco8,11.
El motivo de nuestro trabajo ha sido el estudio del espasmo radial en el cateterismo cardíaco transradial y, en concreto, la identificación de los factores asociados con su aparición, así como el análisis de sus consecuencias en los días siguientes al procedimiento.
PACIENTES Y MÉTODO
Pacientes
Entre noviembre de 2003 y abril de 2004, de los 659 pacientes en los que se intentó realizar el cateterismo por vía radial se incluyó de forma consecutiva a los 637 casos en los que se consiguió canular la arteria radial con éxito y de forma atraumática.
Procedimiento
El abordaje por vía radial ha sido extensamente descrito. En nuestro centro, la arteria radial es el acceso de elección; el operador seleccionó el acceso radial y el lado de punción (izquierdo o derecho) según la calidad del pulso y un correcto resultado del test de Allen modificado. Los pacientes fueron sistemáticamente sedados con 10 mg de diacepam oral 1 h antes del procedimiento. Algunos pacientes, de forma indiscriminada, fueron preparados mediante la aplicación tópica de una pomada anestésica (lidocaína, AstraZeneca®) en la zona de punción radial. Una vez en el laboratorio, todos los pacientes recibieron anestesia local con 1 ml de mepivacaína, tras lo cual la arteria radial fue canulada con una aguja de 20 G (Vigon®). A través del introductor (Maximun, St Jude Medical®) se administraron 5.000 U de heparina y un agente espasmolítico (2,5 mg de verapamilo o fentolamina) disueltos en 20 ml de suero fisiológico.
El diámetro del introductor, así como el diámetro y la curva de los catéteres, fueron elegidos libremente por el operador. En un principio todos los procedimientos fueron planteados como diagnósticos y tras su conclusión se decidió sobre la necesidad de realizar una intervención coronaria percutánea, realizada siempre ad hoc.
Evaluación del espasmo radial
El espasmo radial fue valorado por el operador mediante un cuestionario sobre la presencia de cada una de estas 5 manifestaciones: dolor persistente en el antebrazo, dolor con la manipulación del catéter, dolor al retirar el introductor, dificultad de manipulación del catéter al estar «atrapado» por la arteria radial, e importante resistencia en la retirada del introductor.
Se consideró que había espasmo radial en los casos que presentaban al menos 2 de las 5 manifestaciones anteriores, o bien una única manifestación cuando el operador consideró necesario administrar una segunda dosis de agente espasmolítico.
Además de la presencia del espasmo radial, se analizaron las siguientes variables relacionadas con el procedimiento:
- Preparación previa con pomada anestésica tópica.
- Intensidad de dolor percibido por el paciente durante la canulación de la arteria radial (punción radial e inserción del introductor). El dolor fue clasificado en 4 grados: grado 0 (ausencia de dolor), grado 1 (dolor ligero), grado 2 (dolor moderado) y grado 3 (dolor intenso). En cada caso se pidió al paciente que diferenciara entre este dolor sufrido en la canulación radial y el que pudiera acontecer durante el cateterismo propiamente dicho (espasmo radial).
- Arteria radial canulada, derecha o izquierda.
- Tipo de procedimiento: diagnóstico o combinado (diagnóstico continuado con intervención ad hoc).
- Tiempo de procedimiento. Fue el transcurrido entre la inserción del introductor y su retirada.
- Tortuosidad de arteria subclavia. Se consideró que la arteria subclavia era tortuosa cuando la superación del tramo tortuoso precisó ciertas maniobras: inspiración forzada mantenida, giro de la cabeza a la zona contralateral y sustitución de la guía de teflón estándar por una guía de terumo. La arteria subclavia retroesofágica fue incluida como tortuosa.
- Número total de catéteres empleados (hasta 3 catéteres, y más de 3).
- Diámetro (en unidades French) inicial y máximo de los catéteres empleados.
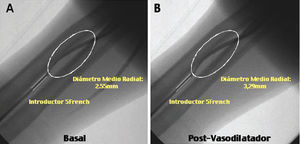
Análisis angiográfico de la arteria radial (fig. 1)
Fig. 1. Análisis angiográfico de la arteria radial, en estado basal (A) y a los 2 min de la administración intrarradial del agente vasodilatador (B).
Con la finalidad de valorar el diámetro de la arteria radial se realizó una angiografía mediante la inyección de contraste a través del introductor, en situación basal y tras 2 min de la administración del vasodilatador.
El diámetro medio de la arteria fue medido con un método automático de cuantificación (QUANTCOR, Siemens®), para lo que seleccionó un segmento de unos 30-40 mm de longitud. La parte distal del introductor fue empleada como referencia. Con la ayuda de marcadores anatómicos precisos, se midió el mismo segmento de la arteria en situación basal y tras la administración del vasodilatador. Además de los diámetros medios, calculamos la capacidad de vasodilatación radial mediante la siguiente ecuación: diámetro posvasodilatador - diámetro basal/diámetro basal.
Todas las mediciones fueron realizadas por un mismo operador.
La angiografía radial nos sirvió, además, para detectar las anomalías anatómicas de este vaso, que fueron recogidas sistemáticamente.
Seguimiento
Los pacientes incluidos fueron citados para una revisión del acceso radial en el primer mes tras el procedimiento. En esta consulta, realizada por operadores que desconocían lo acontecido durante el procedimiento, se valoró la presencia en algún momento del seguimiento de:
- Dolor. Se preguntó por la presencia de dolor en la zona de punción radial en los días posteriores al procedimiento. El grado de dolor nuevamente fue valorado mediante una escala de 4 puntos: grado 0 (ausencia de dolor), grado 1 (dolor ligero), grado 2 (dolor moderado) y grado 3 (dolor intenso).
- Hematoma. Se registró como hematoma cuando éste fue > 3 cm, incluso aunque su distribución fuera superficial.
- Permeabilidad de la arteria radial. La permeabilidad de la arteria radial fue evaluada mediante pulsioximetría y pletismografía en el dedo pulgar durante la maniobra de Allen invertida. Este método se ha empleado para el análisis de la permeabilidad de las estructuras vasculares que integran el arco palmar12 y tiene la ventaja de su mayor disponibilidad y menor variabilidad que el estudio por ultrasonografía. Se registraron 3 grados de permeabilidad radial: arteria radial permeable (onda de pulso y saturación normales), semiocluida (durante la compresión cubital se pierde la onda de pulso, manteniéndose la saturación) y ocluida (pérdida de la onda de pulso y saturación). Los casos con oclusión radial fueron citados para una nueva evaluación.
Los pacientes que no pudieron acudir a la revisión fueron entrevistados telefónicamente y se valoraron la intensidad del dolor durante el seguimiento y la presencia de hematoma.
Análisis estadístico
El análisis estadístico fue realizado mediante el programa SPSS versión 10.0 para Windows. Se ha escogido un diseño híbrido (corte transversal y descripción de cohorte) con el fin de analizar las variables asociadas con la aparición del espasmo durante el procedimiento y evaluar sus consecuencias durante el seguimiento. Las variables continuas fueron expresadas como media ± desviación estándar y las categóricas en porcentajes. Tras dividir a la población en 2 grupos según la presencia o no de espasmo radial, se comparó el valor de cada variable mediante el test de la t de Student para las continuas y la prueba de la χ² para las categóricas. Las variables que en el análisis univariable fueron diferentes entre los 2 grupos (edad, sexo, número de catéteres empleados [≤ 3 frente a > 3], intensidad del dolor en la canulación radial [ausente o ligero frente a moderado o severo], tiempo de procedimiento, cocktail vasodilatador [fentolamina frente a verapamilo], variante anatómica radial, y diámetro de la arteria radial posvasodilatador) se analizaron con un análisis de regresión logística por introducción por pasos hacia delante, para determinar su poder de asociación (odds ratio [OR]) con el espasmo radial. La variable «tipo de procedimiento» no fue incluida en este modelo al comprobar su potente asociación con la variable «número de catéteres empleados». Se analizó la adecuación del ajuste del modelo logístico mediante la prueba de Hosmer-Lemeshow.
RESULTADOS
La población estudiada estaba compuesta por 637 pacientes y en 127 (20,2%) de ellos se produjo un espasmo radial durante el procedimiento. En 25 pacientes (3,9%) se realizó un cambio de la vía de acceso (en 13 casos debido al espasmo radial, 2% del total).
Las características clínicas de la población incluida, distribuidas según la aparición o no de espasmo radial, se exponen en la tabla 1.
Los pacientes que presentaron vasospasmo tenían una edad media significativamente menor (61,0 ± 14,0 frente a 63,5 ± 11,3 años; p = 0,03) y una tendencia hacia un mayor porcentaje relativo de mujeres.
Características diferenciales del procedimiento entre los pacientes con y sin espasmo radial (tabla 2)
La mayor parte de los procedimientos se realizó por vía radial derecha (88,5%) y se eligió el diámetro 5 Fr (66,4%) para comenzar el cateterismo. Ni el lado de acceso (radial derecha o izquierda) ni el diámetro inicial o máximo de los catéteres (4-6 Fr) se asociaron con la aparición de vasospamo radial durante el procedimiento.
El agente vasodilatador administrado al inicio del procedimiento tuvo influencia en la aparición del espasmo radial. Los pacientes que recibieron fentolamina (el 48% de los casos) tuvieron una significativa mayor tasa de vasospasmo que los que recibieron verapamilo (el 23,2 frente al 16,9%, respectivamente; p = 0,04).
La percepción del paciente de la intensidad de dolor en la canulación de la arteria radial se relacionó significativamente con la aparición del espasmo radial. De forma global, la mayor parte de los pacientes refirieron que la canulación radial les ocasionó dolor de grado ligero; sin embargo, en el grupo de pacientes con vasospasmo, el dolor durante la canulación radial fue percibido como moderado o severo en el 23,8% de los casos, frente al 8,5% en los pacientes que no experimentaron vasospasmo (p < 0,001). Por otro lado, el procedimiento combinado con intervención ad hoc (comparado con el diagnóstico) y el empleo de más de 3 catéteres en el cateterismo también se relacionaron significativamente con el espasmo radial (p < 0,001 en ambos).
Características angiográficas de la arteria radial y aparición del vasospasmo
De forma global, el diámetro medio de la arteria radial en nuestra población fue basalmente de 2,20 ± 0,55 mm (0,65-4,30 mm), y se incrementó hasta 2,46 ± 0,54 mm (0,65-4,43 mm) tras el uso del vasodilatador. Los pacientes con vasospasmo durante el cateterismo tuvieron un diámetro radial significativamente menor, tanto basal (2,03 ± 0,48 frente a 2,24 ± 0,56 m; p < 0,001) como tras el vasodilatador (2,27 ± 0,46 frente a 2,51 ± 0,54 mm; p < 0,001). No hubo diferencias en la capacidad vasodilatadora de la arteria radial entre los pacientes con y sin vasospasmo (13,0 ± 15,1 frente a 13,4 ± 16,0, respectivamente).
Por otro lado, la presencia de una anomalía anatómica radial se asoció igualmente con la aparición de espasmo radial (p < 0,001). Se han encontrado 37 casos de arterias radiales anómalas, lo que corresponde al 5,8% de la población incluida. Los tipos de anomalías y su porcentaje relativo se describen en la tabla 3. En los pacientes con anomalías anatómicas apareció vasospasmo en 19 casos (51,4%), frente al 18,0% del resto de los pacientes sin variantes anatómicas.
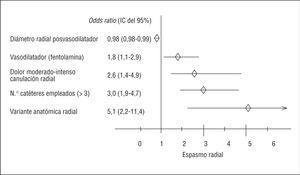
Variables predictoras independientes de la aparición de espasmo radial (fig. 2)
Fig. 2. Predictores independientes de espasmo radial durante el cateterismo cardíaco.
Entre las variables asociadas significativamente con la aparición del vasospasmo radial, el análisis por regresión logística mostró que la anomalía anatómica radial es el factor que se asocia de forma independiente y con más potencia con el espasmo (OR = 5,1; intervalo de confianza [IC] del 95%, 2,2-11,4; p < 0,001).
Las otras variables asociadas independientemente con el espasmo radial fueron: la utilización de más de 3 catéteres durante el procedimiento, el dolor moderado-severo en la canulación radial y la utilización de fentolamina como agente espasmolítico. Por último, el diámetro de la arteria radial posvasodilatador se relacionó de forma independiente e inversa con la aparición de espasmo.
Seguimiento de los pacientes. Consecuencias del espasmo radial presentado en el procedimiento (fig. 3)
Fig. 3. Consecuencias del espasmo radial en el seguimiento (20 ± 18 días posprocedimiento). Sólo el dolor en el antebrazo en los días posteriores al procedimiento fue significativamente superior en los pacientes que habían presentado vasospasmo. No hubo diferencias significativas en las tasas de hematoma y de oclusión radial.
A los 20 ± 18 días tras el procedimiento se realizó una consulta de seguimiento al 94,8% de la población (604 pacientes). De forma mayoritaria (el 88,9% de los casos seguidos) el seguimiento se realizó mediante consulta presencial (anamnesis, exploración física y evaluación con pletismografía y pulsioximetría de la permeabilidad de la arteria radial).
La mayor parte de los pacientes refirió dolor leve o ausencia de dolor en el antebrazo durante el seguimiento (el 93,3% de los 599 pacientes en los que obtuvimos una respuesta). El dolor fue moderado o intenso en 40 pacientes (6,7%). La intensidad del dolor en la zona de punción se relacionó con haber presentado espasmo radial durante el procedimiento (p = 0,003): el 12,4% de los pacientes que presentaron vasospasmo manifestó un dolor moderado o intenso durante el seguimiento, frente a un 5,3% de los casos que no lo presentaron.
Se registró la presencia de hematoma en 64 casos de los 600 pacientes evaluados (10,7%). En todos los casos se trató de hematoma con distribución superficial, con la excepción de un hematoma importante debido a la perforación de la arteria radial durante el procedimiento y que evolucionó satisfactoriamente con tratamiento conservador. No se encontraron diferencias en la presencia de hematoma entre pacientes con y sin vasospasmo (el 10,7 frente al 10,6%, respectivamente).
Por último, se valoró el grado de permeabilidad de la arteria radial en 529 pacientes (el 83,0% de la población incluida). En el 93,4% de los casos, la arteria estaba completamente permeable, en 21 casos (4,0%) se consideró semiocluida y en 14 pacientes (2,6%) estaba ocluida. No hubo asociación significativa entre el espasmo radial y su permeabilidad durante el seguimiento, aunque hubo un mayor porcentaje de casos con radial ocluida en el grupo con vasospasmo (el 4,5 frente al 2,2%). Todos los pacientes con arteria radial ocluida se encontraban asintomáticos, con la excepción de 1 que manifestó claudicación de la mano tras esfuerzos prolongados.
Los pacientes con la arteria radial ocluida fueron revaluados a los 116 ± 47 días del procedimiento (excepto 1 paciente que murió durante el seguimiento). Únicamente en 2 casos la arteria persistía ocluida (el 0,3% de los casos evaluados, los 2 pertenecientes a los pacientes que habían presentado espasmo radial).
DISCUSIÓN
La arteria radial presenta un potencial vasospástico intermedio entre las arterias esplácnicas (hipogástrica y gastroepiploica, con mayor predisposición al espasmo) y las arterias somáticas (arteria mamaria interna). La gran masa muscular en la pared de la arteria radial, superior a la del resto de las arterias, y su alta densidad de receptores alfaadrenérgicos explican su proclividad al espasmo9,10. Aunque la tasa de espasmo radial durante el cateterismo depende de la experiencia del operador13, incluso en los centros más experimentados se describe la aparición de esta complicación en el 15-30% de los procedimientos8. La aparición del vasospasmo radial limita las ventajas de este acceso, ya que el atrapamiento del catéter por la arteria genera dolor al paciente y, por otra parte, dificulta e incluso puede imposibilitar su manipulación. Además, el espasmo radial puede ocasionar otras graves complicaciones, como la perforación del vaso o incluso se ha descrito su sección traumática en el intento de retirar el introductor14.
El espasmo radial en nuestra población
En nuestro estudio, la tasa de vasospasmo fue del 20%. El primer problema que se plantea en un estudio de estas características es la falta de definición clara de espasmo radial durante el cateterismo transradial. Únicamente se ha descrito un método objetivo para cuantificar el grado de espasmo consistente en un mecanismo que mide la fuerza necesaria para retirar un introductor largo de 23 cm de la arteria radial15. Esta forma de determinar el grado de espasmo no es factible en nuestro medio, en el que la tendencia generalizada es la de utilizar introductores radiales más cortos. Por este motivo, optamos por crear una escala propia de espasmo radial en la que se evaluaran sus manifestaciones en la incomodidad para el paciente y en el aumento de la dificultad técnica para el cirujano.
Características de la arteria radial que predicen el vasospasmo
La variable que se asoció de forma más potente con el espasmo radial fue el hecho de que la arteria fuera una variante anatómica de la normalidad, lo que multiplicaba por 5 la probabilidad de espasmo. En nuestra población hemos encontrado un 5,8% de anomalías anatómicas de la arteria radial, una cifra similar a la descrita por otros autores16. La variante anatómica radial más común en nuestra población fue el origen ectópico de la arteria, generalmente en la unión braquio-axilar. Esta gran predisposición de las arterias radiales anómalas a presentar espasmo (en algo más de la mitad de los casos con variantes anatómicas radiales se produjo espasmo) se podría justificar por el mayor grado de manipulación que se requiere para su canulación, aunque tampoco podría descartarse que en la anomalía anatómica también subyaciera una anomalía funcional espasmogénica.
El tamaño de la arteria radial también se asoció de forma independiente con el espasmo. Se ha descrito que, en arterias radiales de pequeño diámetro, la utilización de dispositivos de mayor tamaño se asocia con un mayor daño vascular17. En nuestra población, el diámetro medio radial posvasodilatador fue de 2,46 mm, similar al descrito en otras series, en las que la cuantificación del diámetro intraluminal se hizo mediante ultrasonidos18. El diámetro de la arteria radial fue significativamente menor en los pacientes que presentaron vasospasmo. Esta relación entre un menor tamaño radial y su mayor propensión al espasmo resalta la necesidad de que en la exploración inicial del paciente, tras evaluar el test de Allen, el operador valore también el tamaño de la arteria a través de la calidad del pulso y elija el material acorde con ella.
Variables del procedimiento que se asocian con el espasmo radial
En primer lugar, los procedimientos más complejos y, en concreto, los que cursan con el empleo de más de 3 catéteres (dificultad para el sondaje coronario, intervencionismo percutáneo) se relacionaron con la aparición de espasmo; éste podría ser un argumento para los operadores que consideran que, en previsión de un cateterismo complejo, es más conveniente el abordaje femoral.
La intensidad del dolor que el paciente percibe en el momento inicial de la canulación radial se asoció con el vasospasmo, de tal forma que los pacientes que refirieron un mayor grado de dolor también presentaron una mayor tasa de espasmo. El aumento de catecolaminas circulantes como consecuencia del dolor, o incluso un mayor grado de ansiedad previa, podría justificar el mayor grado de vasospasmo por la estimulación alfaadrenérgica7. Por ello, se debe insistir en la adecuada sedación del paciente antes del procedimiento y en la necesidad de crear una atmósfera de tranquilidad durante el cateterismo.
Por último, la composición del compuesto espasmolítico, y, en concreto, la administración de fentolamina, se asoció también con la aparición del espasmo radial. La fentolamina es una sustancia bloqueadora alfa que es efectiva para prevenir el espasmo radial cuando este vaso se emplea como injerto coronario19. Sin embargo, en nuestra serie ha sido inferior al verapamilo como agente espasmolítico.
Consecuencias del espasmo radial en el seguimiento de los pacientes
El espasmo radial durante el procedimiento tuvo como consecuencia un mayor grado de dolor en la zona de punción en los días siguientes. Una de las ventajas del acceso radial es la ausencia de estructuras nerviosas alrededor de la arteria, lo que reduce la posibilidad de complicaciones neurogénicas. Sin embargo, se ha descrito algún caso de síndrome de dolor crónico regional tras el procedimiento transradial20. En nuestra serie, todos los casos de dolor moderado e intenso estuvieron limitados a la primera-segunda semana tras el procedimiento y solían mostrar una distribución similar al eje radial-braquial, llegando el dolor hasta el codo o incluso al hombro. De forma empírica, los casos con dolor intenso fueron tratados mediante la aplicación tópica de antiinflamatorios no esteroideos.
La oclusión radial, aunque generalmente asintomática, es la complicación más temida del procedimiento transradial. La oclusión radial se ha relacionado con el grado de lesión que presenta la arteria durante el procedimiento17, por lo que el espasmo radial podría asociarse con su posterior oclusión. En nuestra población hemos tenido una tasa de oclusión radial durante el primer mes tras el procedimiento del 2,6%, similar a la de otros estudios21. La tasa de oclusión radial en los pacientes que presentaron espasmo fue superior a la del resto, aunque no encontramos una relación significativa entre el espasmo y la oclusión de la arteria radial. La oclusión radial es un proceso en gran parte reversible18, quizá debido a que su principal motivo es el remodelamiento negativo del vaso tras su estiramiento durante su canulación, quedando la hiperplasia intimal y la trombosis radial como mecanismos secundarios. En nuestra serie, únicamente en 2 pacientes (el 0,3% de la población evaluada) la oclusión radial fue persistente.
Limitaciones
La principal limitación de este trabajo fue la evaluación del espasmo radial mediante un cuestionario propio no validado; sin embargo, pretendimos recoger las distintas manifestaciones que el espasmo radial puede ocasionar durante el procedimiento. El criterio de incluir únicamente a pacientes en los que la canulación radial se consiguiera con éxito y de forma atraumática podría subestimar los casos de espasmo en los que el motivo del fracaso de la punción fuera el propio espasmo; sin embargo, sabemos que, en la mayor pacasos, el fracaso en la punción de la arteria radial se debe a una arteria radial hipoplásica o tortuosa16. Por último, otra limitación es la diferenciación que debía realizarse entre el dolor en la canulación radial y el que pudiera surgir durante el procedimiento por vasospasmo: los operadores fueron cuidadosos en sus preguntas para favorecer esta diferenciación.
CONCLUSIONES
El espasmo radial en el cateterismo cardíaco transradial se produce en 1 de cada 5 pacientes, aunque sólo en un 2% obliga a cambiar de acceso para continuar el procedimiento. Hay características anatómicas de la arteria radial y variables relacionadas con el procedimiento que determinan la aparición del vasospasmo. La arteria radial anómala es el factor que más predispone al vasospasmo. Las arterias radiales de menor diámetro también se asociaron con el espasmo radial. Otras variables que también predisponen al vasospasmo y sobre las que podemos tener una mayor capacidad de actuación son el tipo de vasodilatador empleado como espasmolítico, la intensidad del dolor que experimenta el paciente en la canulación radial y la complejidad del procedimiento. Aparte de la edad, no encontramos ninguna otra variable clínica asociada con el espasmo radial. Las consecuencias del espasmo se reducen a un mayor dolor en el antebrazo en los días siguientes al procedimiento; con una tasa de oclusión radial del 2,6% en el primer mes tras el cateterismo, no encontramos una relación significativa entre el espasmo radial y la posterior oclusión del vaso.
Correspondencia: Dr. R.J. Ruiz-Salmerón.
Departamento de Hemodinámica y Cardiología Intervencionista. Hospital Clínic.
Villarroel, 170. 08036 Barcelona. España.
Correo electrónico: rjruiz@clinic.ub.es